AstraZeneca ، تحت النار لسلامة اللقاحات
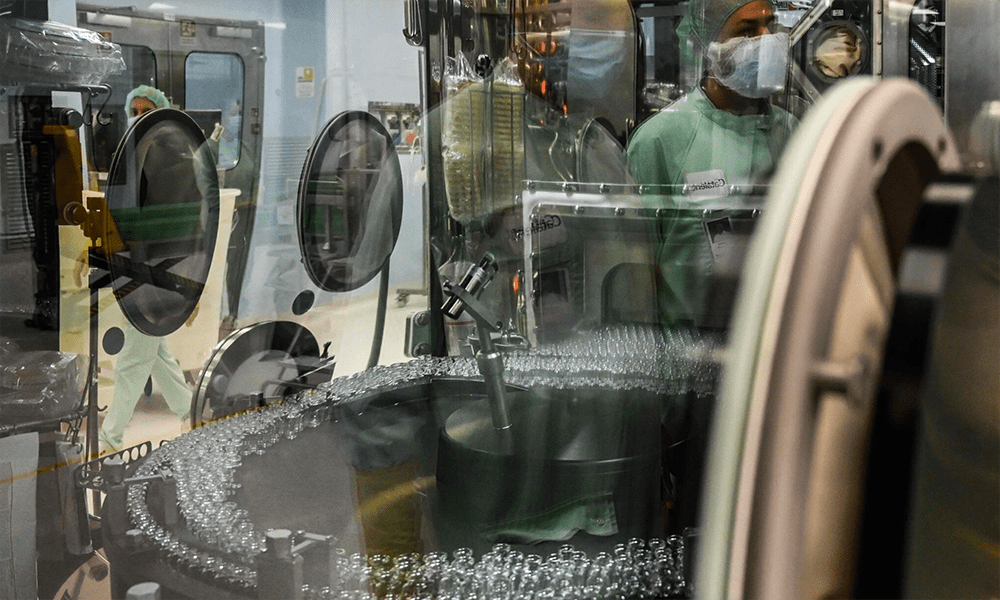
يشعر الخبراء بالقلق من أن الشركة لم تكن شفافة بشأن اثنين من المشاركين الذين أصيبوا بمرض خطير بعد اختبار لقاحها التجريبي.
وجدت استطلاعات الرأي أن الأمريكيين يتوخون الحذر بشكل متزايد بشأن قبول لقاح فيروس كورونا. يشعر العلماء داخل وخارج الحكومة بالقلق من أن المنظمين تحت الضغط قد يطلقون لقاحًا غير مثبت أو غير آمن.
يشعر الخبراء بالقلق بشكل خاص بشأن دراسات لقاح AstraZenec ، التي بدأت في أبريل في بريطانيا ، بسبب رفض الشركة تقديم تفاصيل عن مرض عصبي خطير لدى اثنين من المشاركين ، كلتا المرأتين ، اللتين تلقتا اللقاح التجريبي. دفعت هذه الحالات الشركة إلى التوقف عن الاختبار مرتين ، للمرة الثانية في وقت سابق من هذا الشهر. استؤنفت الدراسات في بريطانيا العظمى والبرازيل والهند وجنوب إفريقيا ، لكنها لا تزال متوقفة في الولايات المتحدة. تلقى حوالي 18.000 شخص حول العالم لقاح AstraZeneca حتى الآن.
يقول مشروع AstraZeneca التجريبي المكون من 111 صفحة والمعروف باسم البروتوكول ، إن هدفه هو لقاح فعال بنسبة 50 ٪ - وهو نفس الحد الذي حددته إدارة الغذاء والدواء في إرشاداتها للقاحات ضد الدواء. فيروس كورونا. لتحديد ما إذا كانت الشركة قد حققت هذا الهدف بيقين إحصائيًا ، يجب أن يكون هناك 150 شخصًا مصابًا بفيروس كورونا المؤكد بين المشاركين الذين تم تطعيمهم أو تلقيهم العلاج الوهمي.
ومع ذلك ، فإن الخطة هي أن لجنة السلامة ستجري تحقيقًا مبكرًا بعد أن كان هناك 75 حالة فقط. إذا كان اللقاح فعالاً بنسبة 50٪ في تلك المرحلة ، فقد يكون من الممكن للشركة إيقاف التجربة مبكرًا والتقدم بطلب للحصول على تصريح حكومي لإطلاق اللقاح للاستخدام الطارئ.
بالسماح بواحد فقط من هذه التحليلات المؤقتة ، تعتبر خطة AstraZeneca أكثر صرامة من التحليلات الأخرى التي تم إصدارها ، بواسطة موديرنا وفايزرقال الدكتور إريك توبول ، خبير الدراسات السريرية في أبحاث سكريبس في سان دييغو ، في مقابلة. تسمح موديرنا بتحليلين من هذا القبيل ، بينما تسمح شركة فايزر بأربعة.
تكمن مشكلة النظر إلى البيانات عدة مرات ، بعد عدد قليل نسبيًا من الحالات ، في أنها تزيد من فرص العثور على جانب من جوانب السلامة والفعالية قد لا يصمد. قد يؤدي إيقاف التجارب مبكرًا أيضًا إلى زيادة خطر فقدان الآثار الجانبية النادرة التي قد تكون مهمة بمجرد إعطاء اللقاح لملايين الأشخاص.
قال الدكتور توبول إن خطة AstraZeneca ، مثل خطة Moderna و Pfizer ، بها ميزة إشكالية: فجميعهم يحسبون حالات Covid-19 الخفيفة نسبيًا عند قياس الفعالية ، مما قد يعيق الجهود المبذولة لتحديد ما إذا كان اللقاح يمنع. مرض معتدل أو شديد.
وقالت ميشيل ميكسيل ، المتحدثة باسم أسترازينيكا ، في بيان إن مثل هذه الخطط لا يتم تقاسمها مع الجمهور عادة "بسبب أهمية الحفاظ على سرية وسلامة المحاكمات".
أصدرت الشركة القليل من التفاصيل حول حالتي المرض الخطير في محاكمتها. تلقى المشارك الأول جرعة من اللقاح قبل الإصابة بالتهاب النخاع الشوكي ، المعروف باسم التهاب النخاع الشوكي ، وفقًا لورقة معلومات المشاركين في لقاح AstraZeneca في يوليو. يمكن أن تسبب الحالة ضعفًا في الذراعين والساقين وشللًا وألمًا ومشاكل في الأمعاء والمثانة.
دعت القضية إلى التوقف في تجارب لقاحات AstraZeneca للسماح بمراجعة السلامة من قبل خبراء مستقلين. قال متحدث باسم الشركة لصحيفة التايمز الأسبوع الماضي أن المتطوع تم تحديده لاحقًا على أنه مصاب بالتصلب المتعدد غير المشخص من قبل ، وأن التجربة استؤنفت بعد ذلك بوقت قصير.
يمكن أن يكون التهاب النخاع المستعرض أحيانًا أول علامة على الإصابة بالتصلب المتعدد ، والذي يتضمن أعراضًا أكثر تعقيدًا. ولكن يمكن أن يحدث التهاب النخاع أيضًا بعد أن يواجه الجسم عاملًا معديًا مثل الفيروس.
وقالت الشركة إنها لم تؤكد التشخيص في الحالة الثانية ، أحد المشاركين الذي مرض بعد الجرعة الثانية من اللقاح. قال شخص مطلع على الوضع ، تحدث إلى التايمز بشرط عدم الكشف عن هويته ، إن مرض المشارك تم تحديده على أنه التهاب النخاع المستعرض. تم تعليق المحاكمة مرة أخرى في 6 سبتمبر / أيلول بعد مرضها.
الحالة نادرة ولكنها خطيرة ، وقال الخبراء إن العثور على حالة واحدة بين آلاف المشاركين في التجربة قد يكون بمثابة دعوة للاستيقاظ. وقالوا إن المزيد من الحالات المؤكدة قد تكون كافية لإيقاف عرض لقاح AstraZeneca تمامًا.
جمعت ورقة حقائق للمشاركين مؤرخة في 11 سبتمبر حول تجربة AstraZeneca في بريطانيا بين حالتي المتطوعين ، مشيرة إلى أنه "من غير المحتمل أن تكون الأمراض مرتبطة باللقاح أو أنه لم يكن هناك دليل كاف للتأكيد على أن الأمراض كانت أو لم تكن مرتبطة باللقاح "، بناءً على مراجعات السلامة. في اليوم التالي ، أعلنت AstraZeneca أنها استأنفت الاختبار في المملكة المتحدة.
لكن إدارة الغذاء والدواء الأمريكية لم تسمح حتى الآن للشركة بإعادة تشغيل التجربة في الولايات المتحدة.
ورفض متحدث باسم إدارة الغذاء والدواء التعليق. وقالت المعاهد الوطنية للصحة في بيان "يبقى أن نرى" ما إذا كان ظهور المرض في المشاركين في التجربة عشوائيًا أم مرتبطًا باللقاح ، مضيفة أن "التوقف للسماح بإجراء مزيد من التقييم يتفق مع الممارسة. اساسي".
قال الدكتور مارك جولدبيرجر ، خبير الأمراض المعدية في شراكة البحث والتطوير العالمية للمضادات الحيوية ومسؤول سابق في إدارة الغذاء والدواء الأمريكية ، إنه وجد الاستئناف السريع للتجارب الخارجية "أمرًا مزعجًا بعض الشيء" ، لا سيما بالنظر إلى نقص تفاصيل عن أعراض المرضى والغموض حول ارتباطهم باللقاح. وقال: "ربما يكون هذا أفضل ما يمكن أن يفعلوه - قد لا يكون من الممكن الحصول على مزيد من اليقين الآن". "إنها علامة استفهام حول ما يحدث.
لم تقم الشركة بإبلاغ الجمهور على الفور بالمشكلات العصبية لكلا المشاركين. كما أنه لم يحذر إدارة الغذاء والدواء على الفور من أنه كان يوقف تجاربه مرة أخرى بعد أن أصيب المتطوع الثاني في المملكة المتحدة بمرض ودعت لجنة سلامة مستقلة إلى تعليق مؤقت ، وفقًا للعديد من الأشخاص الذين يعرفون الموقف. أبلغ الرئيس التنفيذي للشركة المستثمرين بالمشكلات ، لكنه لم يتحدث عنها علنًا حتى تسربت المعلومات وكان ذلك ذكرت من قبل STAT.
قال الدكتور بيتر جاي هوتيز ، عالم الفيروسات في كلية بايلور للطب في هيوستن: "الاتصالات حولها كانت مروعة وغير مقبولة". ليست هذه هي الطريقة التي يجب أن يسمع بها الشعب الأمريكي.
كما انتقد الدكتور هوتز التصريحات التي أدلى بها مسؤولون حكوميون ، بما في ذلك المنظمون في المملكة المتحدة الذين ، على حد قوله ، لم يقدموا سببًا لاستئناف محاكماتهم.
قال الدكتور بول أوفيت ، الأستاذ في جامعة بنسلفانيا وعضو اللجنة الاستشارية للقاحات التابعة لإدارة الغذاء والدواء ، إنه من غير الواضح كيف قررت الشركة - أو حكومة المملكة المتحدة - أن الحالة الثانية لا علاقة لها باللقاح.
وأشار هو وخبراء آخرون إلى أن التهاب النخاع المستعرض نادر الحدوث ، ويتم تشخيصه في حوالي واحد فقط من بين كل 236.000 ألف أمريكي سنويًا. شملت التجربة في بريطانيا العظمى حوالي 8.000 متطوع فقط.
يستخدم اللقاح الذي طورته شركة AstraZeneca ، التي شكلت شراكة مع علماء من جامعة أكسفورد ، فيروسًا يهدف إلى نقل جينات الفيروس التاجي إلى الخلايا البشرية وإطلاق استجابة مناعية تحمي الناس من فيروس كورونا. هذا ما يسمى بالنواقل هو شكل معدل من الفيروسات الغدية التي تسبب نزلات البرد لدى الشمبانزي ، ولكنها كذلك تعتبر آمنة للناس. تتبع العديد من الشركات الأخرى ، بما في ذلك Johnson & Johnson و CanSino ، طرقًا مماثلة تعتمد على الفيروسات الغدية ، على الرغم من وجود أنواع مختلفة من الفيروسات الغدية والمكونات المحددة تختلف من لقاح إلى آخر.
في حين أن المنتجات الأخرى القائمة على الفيروسات الغدية قد حققت بعض النجاح في الماضي ، فقد تم ربطها أيضًا بأحداث ضائرة خطيرة. وكان أشهرها حالة جيسي جيلسنجر البالغة من العمر 1999 عامًا ، والتي توفيت عام XNUMX بعد تلقيها العلاج الجيني من خلال فيروس غدي تسبب في استجابة التهابية قاتلة من جهازه المناعي.
إذا ارتبط أحد الآثار الجانبية الخطيرة بشكل دائم بلقاح AstraZeneca ، فسيحتاج العلماء إلى تحديد ما إذا كان السبب المحفز له يأتي من ناقلات الفيروسات الغدية أو ربما جينات فيروس كورونا التي يحملها ، وهي روابط قد تثير مخاوف بشأن منتجات الشركات الأخرى التي تعتمد عليها. على نفس المكونات.
مصدر: https://www.nytimes.com/2020/09/19/health/astrazeneca-vaccine-safety-blueprints.html

