AstraZeneca, aus Sicherheitsgründen unter Beschuss
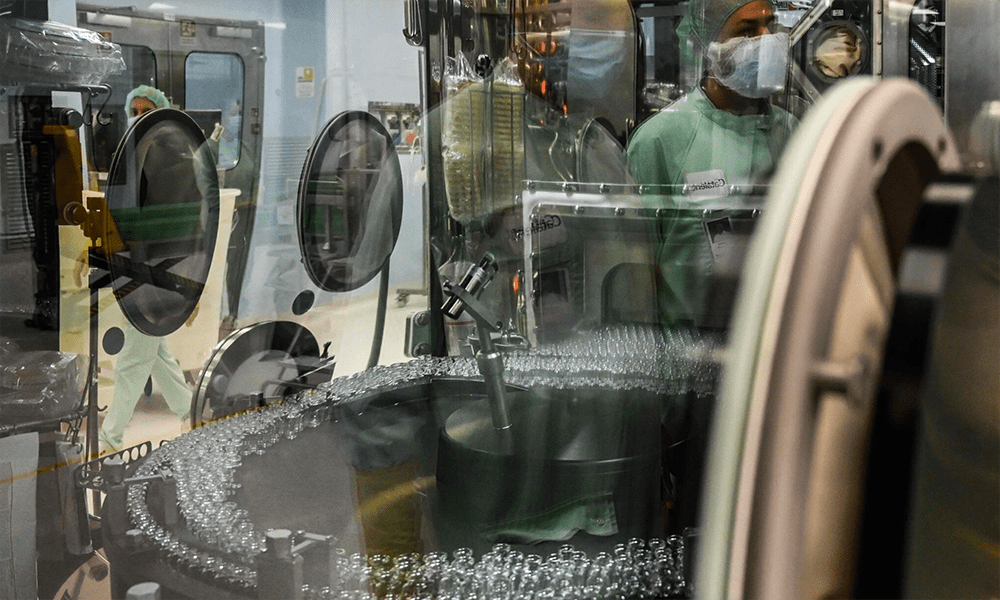
Experten sind besorgt darüber, dass das Unternehmen zwei Teilnehmer, die nach dem Testen seines experimentellen Impfstoffs schwer krank wurden, nicht transparent gemacht hat.
Umfragen haben ergeben, dass die Amerikaner zunehmend vorsichtig sind, einen Coronavirus-Impfstoff zu akzeptieren. Wissenschaftler innerhalb und außerhalb der Regierung befürchten, dass Regulierungsbehörden unter Druck einen unbewiesenen oder unsicheren Impfstoff freisetzen könnten.
Experten sind besonders besorgt über die Impfstoffstudien von AstraZeneca, die im April in Großbritannien begannen, da sich das Unternehmen weigerte, bei zwei Teilnehmern, beide Frauen, die den experimentellen Impfstoff erhielten, Einzelheiten zu schwerwiegenden neurologischen Erkrankungen anzugeben. Diese Fälle veranlassten das Unternehmen, die Tests zweimal einzustellen, das zweite Mal Anfang dieses Monats. Die Studien wurden in Großbritannien, Brasilien, Indien und Südafrika wieder aufgenommen, in den USA werden sie jedoch noch unterbrochen. Weltweit haben bisher rund 18.000 Menschen den AstraZeneca-Impfstoff erhalten.
Das 111-seitige Versuchsprojekt von AstraZeneca, das als Protokoll bekannt ist, besagt, dass das Ziel ein Impfstoff mit einer Wirksamkeit von 50% ist - derselbe Schwellenwert, den die Food and Drug Administration in ihren Richtlinien für Impfstoffe gegen das Medikament festgelegt hat. Coronavirus. Um mit statistischer Sicherheit festzustellen, ob das Unternehmen dieses Ziel erreicht hat, müssen 150 bestätigte Coronavirus-Patienten unter den Teilnehmern sein, die geimpft wurden oder ein Placebo erhalten haben.
Es ist jedoch geplant, dass eine Sicherheitskommission nach nur 75 Fällen eine frühzeitige Untersuchung durchführt. Wenn der Impfstoff zu diesem Zeitpunkt zu 50% wirksam ist, kann das Unternehmen die Studie möglicherweise vorzeitig abbrechen und eine behördliche Genehmigung beantragen, um den Impfstoff für den Notfall freizugeben.
Da nur eine dieser Zwischenanalysen zulässig ist, ist der Plan von AstraZeneca strenger als die anderen, die von veröffentlicht wurden Moderna und PfizerDr. Eric Topol, Experte für klinische Studien bei Scripps Research in San Diego, sagte in einem Interview. Moderna erlaubt zwei solcher Analysen und Pfizer vier.
Das Problem beim zu häufigen Betrachten der Daten nach einer relativ geringen Anzahl von Fällen besteht darin, dass die Wahrscheinlichkeit steigt, einen Aspekt der Sicherheit und Wirksamkeit zu finden, der möglicherweise nicht Bestand hat. Ein vorzeitiger Abbruch der Studien kann auch das Risiko erhöhen, dass seltene Nebenwirkungen fehlen, die nach Verabreichung des Impfstoffs an Millionen von Menschen erheblich sein können.
Dr. Topol sagte, dass AstraZenecas Plan, wie der von Moderna und Pfizer, ein problematisches Merkmal hatte: Sie alle zählen relativ milde Fälle von Covid-19 bei der Messung der Wirksamkeit, was die Bemühungen behindern könnte, festzustellen, ob der Impfstoff verhindert. mittelschwere oder schwere Krankheit.
Solche Pläne werden normalerweise nicht mit der Öffentlichkeit geteilt, "weil es wichtig ist, die Vertraulichkeit und Integrität von Gerichtsverfahren zu wahren", sagte Michele Meixell, ein Sprecher von AstraZeneca, in einer Erklärung.
Das Unternehmen hat in seiner Studie nur wenige Details zu den beiden Fällen schwerer Krankheit veröffentlicht. Der erste Teilnehmer erhielt eine Dosis des Impfstoffs, bevor er eine Entzündung des Rückenmarks entwickelte, die als transversale Myelitis bekannt ist. Dies geht aus einem Teilnehmerinformationsblatt für den AstraZeneca-Impfstoff vom Juli hervor. Der Zustand kann zu Schwäche in Armen und Beinen, Lähmungen, Schmerzen sowie Darm- und Blasenproblemen führen.
Der Fall sah eine Pause in den Impfstoffversuchen von AstraZeneca vor, um eine Sicherheitsüberprüfung durch unabhängige Experten zu ermöglichen. Ein Unternehmenssprecher teilte der Times letzte Woche mit, dass der Freiwillige später entschlossen war, einen zuvor nicht diagnostizierten, impfstoffbedingten Fall von Multipler Sklerose zu haben, und dass die Studie kurz danach wieder aufgenommen wurde.
Transversale Myelitis kann manchmal das erste Anzeichen einer Multiplen Sklerose sein, die komplexere Symptome mit sich bringt. Myelitis allein kann aber auch auftreten, wenn der Körper auf einen Infektionserreger wie ein Virus trifft.
Das Unternehmen sagte, es habe die Diagnose im zweiten Fall nicht bestätigt, einem Teilnehmer, der nach der zweiten Dosis des Impfstoffs krank wurde. Eine mit der Situation vertraute Person, die unter der Bedingung der Anonymität mit der Times sprach, sagte, die Krankheit des Teilnehmers sei als transversale Myelitis identifiziert worden. Der Prozess wurde am 6. September erneut ausgesetzt, nachdem sie krank geworden war.
Die Erkrankung ist selten, aber schwerwiegend, und Experten sagten, dass es ein Weckruf sein könnte, unter Tausenden von Studienteilnehmern auch nur einen Fall zu finden. Weitere bestätigte Fälle könnten ausreichen, um das Impfangebot von AstraZeneca insgesamt einzustellen.
In einem Teilnehmerdatenblatt vom 11. September über die AstraZeneca-Studie in Großbritannien wurden die Fälle der beiden Freiwilligen zusammengefasst, in dem festgestellt wurde, dass die Krankheiten "wahrscheinlich nicht mit dem Impfstoff in Verbindung gebracht werden oder es nicht genügend Beweise gibt, um sicher zu sein, dass es sich um Krankheiten handelt." oder waren nicht mit dem Impfstoff verwandt ", basierend auf Sicherheitsüberprüfungen. Am nächsten Tag gab AstraZeneca bekannt, dass die Tests in Großbritannien wieder aufgenommen wurden.
Bisher hat die FDA dem Unternehmen jedoch nicht gestattet, die Studie in den USA erneut zu starten.
Ein FDA-Sprecher lehnte eine Stellungnahme ab. Die National Institutes of Health sagten in einer Erklärung, dass "es abzuwarten bleibt", ob der Ausbruch der Krankheit bei den Studienteilnehmern zufällig oder impfstoffbedingt war, und fügten hinzu, dass "eine Pause, um eine weitere Bewertung zu ermöglichen, mit der Praxis vereinbar ist. Standard".
Dr. Mark Goldberger, Experte für Infektionskrankheiten bei der Global Antibiotic Research and Development Partnership und ehemaliger FDA-Beamter, sagte, er empfinde die rasche Wiederaufnahme von Studien in Übersee als "ein wenig beunruhigend", insbesondere angesichts des Mangels an von Details über die Symptome der Patienten und die Unklarheit über ihre Verbindung zum Impfstoff. "Vielleicht ist dies das Beste, was sie tun können - es ist derzeit möglicherweise nicht möglich, mehr Sicherheit zu erlangen", sagte er. "Es ist ein Fragezeichen darüber, was los ist.
Das Unternehmen informierte die Öffentlichkeit nicht sofort über die neurologischen Probleme beider Teilnehmer. Er warnte die FDA auch nicht sofort, dass er seine Experimente erneut pausierte, nachdem der zweite britische Freiwillige eine Krankheit entwickelt hatte und ein unabhängiges Sicherheitskomitee eine vorübergehende Suspendierung forderte, so mehrere Personen, die die Situation kannten. Der CEO des Unternehmens informierte die Anleger über die Probleme, sprach jedoch erst öffentlich darüber, als die Informationen durchgesickert waren und waren von der STAT gemeldet.
"Die Kommunikation war schrecklich und inakzeptabel", sagte Dr. Peter Jay Hotez, Virologe am Baylor College of Medicine in Houston. "So sollte das amerikanische Volk nicht davon hören."
Dr. Hotez kritisierte auch Aussagen von Regierungsbeamten, einschließlich britischer Aufsichtsbehörden, die, wie er sagte, keine Begründung für die Wiederaufnahme ihrer Prozesse lieferten.
Dr. Paul Offit, Professor an der University of Pennsylvania und Mitglied des Impfstoffbeirats der FDA, sagte, es sei unklar, wie das Unternehmen - oder die britische Regierung - feststellte, dass der zweite Fall nicht mit dem Impfstoff zusammenhängt.
Er und andere Experten stellten fest, dass transversale Myelitis selten ist und nur bei etwa einem von 236.000 Amerikanern pro Jahr diagnostiziert wird. An dem Prozess in Großbritannien waren nur rund 8.000 Freiwillige beteiligt.
Der von AstraZeneca entwickelte Impfstoff, der eine Partnerschaft mit Wissenschaftlern der Universität Oxford geschlossen hat, verwendet ein Virus, das Coronavirus-Gene in menschliche Zellen transportieren und eine Immunantwort auslösen soll, die Menschen vor dem Coronavirus schützt. Dieser sogenannte Vektor ist eine modifizierte Form des Adenovirus, die bei Schimpansen Erkältungen verursacht, dies ist jedoch der Fall als sicher für Menschen. Mehrere andere Unternehmen, darunter Johnson & Johnson und CanSino, verfolgen ähnliche Ansätze auf der Basis von Adenoviren, obwohl es verschiedene Arten von Adenoviren gibt und die spezifischen Inhaltsstoffe von Impfstoff zu Impfstoff unterschiedlich sind.
Während andere Produkte auf Adenovirus-Basis in der Vergangenheit einige Erfolge erzielt haben, wurden sie auch mit schwerwiegenden unerwünschten Ereignissen in Verbindung gebracht. Am bekanntesten war der Fall des 1999-jährigen Jesse Gelsinger, der XNUMX starb, nachdem er eine Gentherapie durch ein Adenovirus erhalten hatte, das eine tödliche Entzündungsreaktion seines Immunsystems auslöste.
Wenn eine schwerwiegende Nebenwirkung dauerhaft mit dem Impfstoff von AstraZeneca verbunden wäre, müssten Wissenschaftler feststellen, ob sein Auslöser vom Adenovirus-Vektor oder möglicherweise von den darin enthaltenen Coronavirus-Genen herrührt. Diese Zusammenhänge könnten Bedenken hinsichtlich der Produkte anderer Unternehmen aufkommen lassen, die darauf angewiesen sind. auf den gleichen Komponenten.
Quelle: https://www.nytimes.com/2020/09/19/health/astrazeneca-vaccine-safety-blueprints.html

