Bewertung der Wirksamkeit und Effizienz von Influenza-Impfstoffen bei gesunden Kindern: systematische Überprüfung

The Lancet
T. Jefferson, S. Smith, V. Demicheli, A. Harnden, A. Rivetti, C. Di Pietrantonj
2005
Abstrakt
Hintergrund Wir wollten den Nachweis der Wirksamkeit und Effizienz von abgeschwächten und inaktivierten Influenza-Lebendimpfstoffen bei Kindern bis zu 16 Jahren evaluieren.
Methoden Wir haben die Cochrane Library, MEDLINE, EMBASE Biological Abstracts und den Science Citation Index seit Juni 2004 in einer beliebigen Sprache überprüft und uns an die entsprechenden Impfstoffhersteller und Autoren der Studie gewandt, um zusätzliche Daten zu ermitteln. Wir haben randomisierte Fälle, Kohorten- und Kontrollfälle eingeschlossen, in denen die Wirksamkeit von Influenza-Impfstoffen (Verringerung der im Labor bestätigten Fälle), die Wirksamkeit von Impfstoffen gegen Influenza-ähnliche Krankheiten (Verringerung der symptomatischen Fälle) oder beides verglichen wurden , mit Placebo oder ohne Intervention. Wir analysierten die folgenden Ergebnisse: Grippe, grippeähnliche Krankheit, Krankenhausaufenthalte, Schulabwesenheiten, Komplikationen und sekundäre Übertragung.
Ergebnisse 14 randomisierte kontrollierte Studien, acht Kohortenstudien, eine Fall-Kontroll-Studie und eine randomisierte kontrollierte Studie zur Verwendung von intraepidemischen Impfstoffen wurden eingeschlossen. Lebendimpfstoffe gegen abgeschwächte Influenza sind im Vergleich zu Placebo oder Immunisierung bei Kindern über 79 Jahren zu 38% wirksam und zu 2% wirksam. Inaktivierte Impfstoffe hatten eine geringere Wirksamkeit (65%) als attenuierte Lebendimpfstoffe und hatten bei Kindern im Alter von 2 Jahren oder weniger ähnliche Auswirkungen auf das Placebo. Die Wirksamkeit der inaktivierten Impfstoffe betrug bei Kindern über 28 Jahren etwa 2%.
Impfstoffe waren wirksam bei der Reduzierung von langen Schulabwesenheiten (relatives Risiko 0-14 [95% CI 0 · 07-0 · 27]). Studien, in denen die Auswirkungen von Impfstoffen auf Sekundärfälle, Erkrankungen der unteren Atemwege, akute Mittelohrentzündung und Krankenhausaufenthalt untersucht wurden, wiesen keinen Unterschied zur Placebo- oder Standardbehandlung auf, es fehlte jedoch statistische Aussagekraft.
Interpretation Influenza-Impfstoffe (insbesondere attenuierte Lebendimpfstoffe mit zwei Dosen) sind bei Kindern über 2 Jahren wirksam. Die Wirksamkeit und Wirksamkeit der Impfstoffe ist sehr unterschiedlich. Nur zwei kleine Studien untersuchten die Auswirkungen von Grippeimpfstoffen auf die Krankenhauseinweisung, und keine Studien untersuchten die Verringerung der Sterblichkeit, schwerwiegende Komplikationen und die Übertragung der Grippe durch die Bevölkerung.
Wenn eine Grippeimpfung bei Kindern im Rahmen der öffentlichen Gesundheitspolitik empfohlen werden soll, müssen dringend groß angelegte Studien durchgeführt werden, in denen diese wichtigen Ergebnisse bewertet und direkte Impfstoffvergleiche durchgeführt werden.
Einführung
Die Bemühungen zur Verhinderung der jährlichen Ausbreitung der Influenza konzentrierten sich auf den Einsatz von Impfstoffen. Bisher richteten sich Impf- und Berichterstattungskampagnen an Personen, die 65 Jahre oder älter sind. In einer nicht-pandemischen Situation besteht die Wahl der Präventionsstrategie in der Immunisierung bestimmter Bevölkerungsgruppen, z. B. Kinder, ältere Menschen, chronisch Kranke, Gesundheitspersonal oder der gesamten Bevölkerung.
Der Beratende Ausschuss der American Academy of Paediatrics und der US-amerikanischen Zentren für Krankheitskontrolle und Prävention für Impfpraktiken1 (Beratender Ausschuss für Impfungen der US-amerikanischen Zentren für die Kontrolle und Prävention von Krankheiten) haben empfohlen, die Impfung von Kindern im Alter von 6 bis 23 Monaten gegen die Grippe als Maßnahme für die öffentliche Gesundheit ab der Grippesaison einzuführen 2004-05. Erklärung des Beratenden Ausschusses für Impfpraktiken vom Mai 2004 mit dem Titel abwehr und Kontrolle der Influenza 2 (Prävention und Bekämpfung der Grippe) empfiehlt außerdem, dass Personen im engen Kontakt mit Säuglingen im Alter zwischen 0 und 23 Monaten immunisiert werden.
In Kanada das National Advisory Committee on Immunization3 (National Advisory Committee on Immunization) folgte im Februar 2004. Die Hauptthemen für die Ausweitung der Immunisierung auf gesunde Kinder im Alter zwischen 6 und 23 Monaten4-6 und diejenigen, die die Schule besuchen6,7 umfassen die Reduzierung von: der Anzahl der Patienten mit Influenza; die Anzahl der Überaufnahmen; die Sterblichkeit älterer Menschen in Familien mit Kindern; Gesundheitskontakte (z. B. Hausärzte); die Anzahl der Antibiotika-Rezepte; und Fehlzeiten für Kinder und Mitbewohner.
Der logische Entscheidungsprozess zur Prävention von Influenza wird durch das Fehlen zuverlässiger Vorhersagen über die Wirkung des Virus und durch die Unsicherheiten über die Wirkung von Impfstoffen in verschiedenen Altersgruppen erschwert.
In einem Cochrane-Review von Influenza-Impfstoffen bei gesunden Erwachsenen 8Es wurde ein merklicher Unterschied zwischen der Wirksamkeit gegen Influenza (Verringerung der im Labor bestätigten Fälle) und der Wirksamkeit gegen Influenza-ähnliche Erkrankungen (Verringerung der symptomatischen Fälle) von Impfstoffen beobachtet. Eine genaue Bewertung der Wirksamkeit und Effizienz von Influenza-Impfstoffen ist unerlässlich, um eine begründete Wahl zwischen alternativen Strategien zu ermöglichen.
Ziel war es, vergleichende Studien zu identifizieren und auszuwerten, die die Wirksamkeit und Effizienz von Influenza-Impfstoffen bei gesunden Kindern unter 16 Jahren bewerten.
Unser Artikel ist Teil eines bevorstehenden größeren Cochrane-Reviews, das Impfsicherheitstests umfasst.9
Methoden und Forschung
Um Studienberichte und systematische Reviews zu identifizieren, haben wir bis Ende Mai 2004 die folgenden elektronischen Datenbanken durchsucht: die Cochrane Library, einschließlich der Cochrane Database of Systematic Reviews, der NHS Database of Abstracts of Reviews of Effectiveness und des Cochrane Central Register kontrollierter Studien (CENTRAL); MEDLINE (OVID, ab Januar 1966); EMBASE (Dialog, 1974–79; SilverPlatter, 1980); Biologische Abstracts (SilverPlatter, ab 1969); und Science Citation Index (Web of Science, von 1974).
Wir haben in jeder Sprache geforscht.
Die Details der Suchstrategie finden Sie im Webanhang 1 (http://image.thelancet.com/extras/04art9306webappendix1.pdf).
Um zusätzliche veröffentlichte und unveröffentlichte Studien zu identifizieren, haben wir den wissenschaftlichen Zitierindex durchsucht, um Artikel zu identifizieren, die relevante Studien zitieren. Wir haben diese Studien auch in PubMed aufgenommen und die Funktion "Verwandte Artikel" verwendet. Wir haben die Bibliographien aller relevanten Artikel ausgewertet und alle Bewertungen für weitere Studien veröffentlicht. Zur Klärung haben wir uns an die Impfstoffhersteller selbst oder an die entsprechenden Autoren der Studie gewandt.
Auswahl
Wir haben randomisierte klinische Studien, Kohortenstudien und Fall-Kontroll-Studien ausgewählt (Web-Anhang 2; http://image.thelancet.com/extras/04art9306webappendix2.pdf) zur Bewertung der Immunisierung von Kindern im Alter von 16 Jahren und jünger in einer beliebigen geografischen Position mit einem Grippeimpfstoff, der unabhängig, in einer beliebigen Dosis, Zubereitung oder einem beliebigen Zeitplan im Vergleich zu Placebo oder ohne Intervention verabreicht wird.
Wir haben beschlossen, Belege aus nicht randomisierten Vergleichsstudien aufzunehmen, um die Relevanz der Überprüfung zu verbessern.
Bei der Auswahl der Studien berücksichtigten wir die folgenden primären Zielgrößen: präventive Wirksamkeit und Effizienz; Fälle von Influenza, die durch Virusisolierung, serologische Unterstützung, jede andere Art von Labortest zur Identifizierung von Viren (Fälle von Influenza) oder eine Kombination davon bestätigt wurden; grippeähnliche Krankheitsfälle innerhalb eines Jahres nach Impfung; Krankenhausaufenthalte wegen einer grippeähnlichen Krankheit oder Grippe; Todesfälle (aufgrund einer grippeähnlichen Krankheit oder Grippe); und alle anderen direkten oder indirekten Indikatoren für die Auswirkung der Krankheit. Wir haben die serologischen Outcome-Daten nicht berücksichtigt, da unser Ziel darin bestand, die Auswirkungen der Impfung auf die öffentliche Gesundheit zu bewerten.
Datenextraktion und Bewertung der Validität der Studie
Zwei von uns (SS und AR) wendeten die Einschlusskriterien unabhängig voneinander auf alle identifizierten und abgerufenen Gegenstände an und extrahierten dann Daten aus den eingeschlossenen Studien zu den Standardformen des Cochrane Vaccines Field. Das Verfahren wurde von TJ und VD überwacht und vermittelt.
Wir bewerteten die methodische Qualität für randomisierte kontrollierte Studien mit Kriterien aus dem Cochrane Reviewer-Handbuch.10 Wir bewerteten Studien nach Randomisierung, Sequenzgenerierung und Verdeckung der Zuordnung, verblindeten Studien und nachfolgenden Studien. Wir haben die Qualität der nicht randomisierten Studien in Bezug auf das Vorhandensein möglicher Störfaktoren bewertet. Wir verwendeten die Newcastle-Ottawa-Treppe, um die Studien auszuwerten.11
Aufgrund des Mangels an empirischen Belegen für die Auswirkung der methodischen Qualität auf die Ergebnisse nicht randomisierter Studien verwendeten wir die Qualität in der Analysephase als Mittel zur Interpretation der Ergebnisse durch eine schrittweise Sensitivitätsanalyse. Ausführliche Informationen zur Qualitätsbewertung erhalten Sie beim jeweiligen Autor.
Wir haben die extrahierten Daten in die Cochrane RevMan-Software (Version 4.2, Cochrane Collaboration, Oxford, UK) eingegeben. Die Aggregation der Daten hing von der Sensitivität und Homogenität der verwendeten Definitionen von Exposition, Populationen und Ergebnissen ab. Wenn die Studien homogen waren, haben wir für jede Projektkategorie eine Metaanalyse durchgeführt. Wir haben die Effizienz- und Effektivitätsschätzungen als relatives Risiko mit 95% CIs zusammengefasst. Die Wirksamkeit des absoluten Impfstoffs wurde mit 1 abzüglich des relativen Risikos berechnet und als Prozentsatz ausgedrückt.
Wir haben eine schrittweise sensorische Analyse begonnen, indem wir die in der ehemaligen Sowjetunion durchgeführten Studien von unserer Metaanalyse ausgeschlossen haben. Wir führten auch eine Untergruppenanalyse durch, wenn Daten nach Art des verabreichten Impfstoffs, Alter der Personen und Spezifität der Definitionen der Ergebnisse verfügbar waren.
Die Altersschichtung (≤2 Jahre, ≤6 Jahre und> 6 Jahre) gibt die häufigste Schichtung an, über die in den eingeschlossenen Studien berichtet wurde. Um den Effekt auf die statistische Heterogenität zu bewerten, haben wir I berechnet2 für jede aggregierte Schätzung.12 Diese Statistik kann als Anteil der Gesamtabweichung zwischen den Schätzungen des Effekts interpretiert werden, der eher auf Heterogenität als auf Stichprobenfehler zurückzuführen ist und von der Anzahl der Studien an sich unabhängig ist. Wenn ich2 weniger als 30% beträgt, gibt es wenig Bedenken hinsichtlich der statistischen Heterogenität.12-14 Wir haben Zufallseffektmodelle verwendet, um die Varianz der Studie in unseren Ergebnissen zu erklären.15
Rolle der Finanzierungsquelle
Der Sponsor hatte keinerlei Einfluss auf das Studiendesign, die Datenerfassung, die Datenanalyse, die Dateninterpretation oder das Verfassen von Berichten. Der Autor hatte uneingeschränkten Zugriff auf alle Studiendaten und war letztendlich für die Entscheidung verantwortlich, diese zur Veröffentlichung einzureichen.
Ergebnisse
Aus den 1204 von unserer Forschung identifizierten Titeln haben wir 125 Studienberichte ausgewählt und abgerufen, die die Einschlusskriterien erfüllen könnten (Abbildung 1). 100 Berichte wurden ausgeschlossen. Der häufigste Grund für den Ausschluss war das Fehlen unabhängiger Kontrollen (n = 29) und eines nicht vergleichenden Designs (n = 15). Eine vollständige Liste mit Ausschlussgründen ist auf Anfrage beim Autor erhältlich.
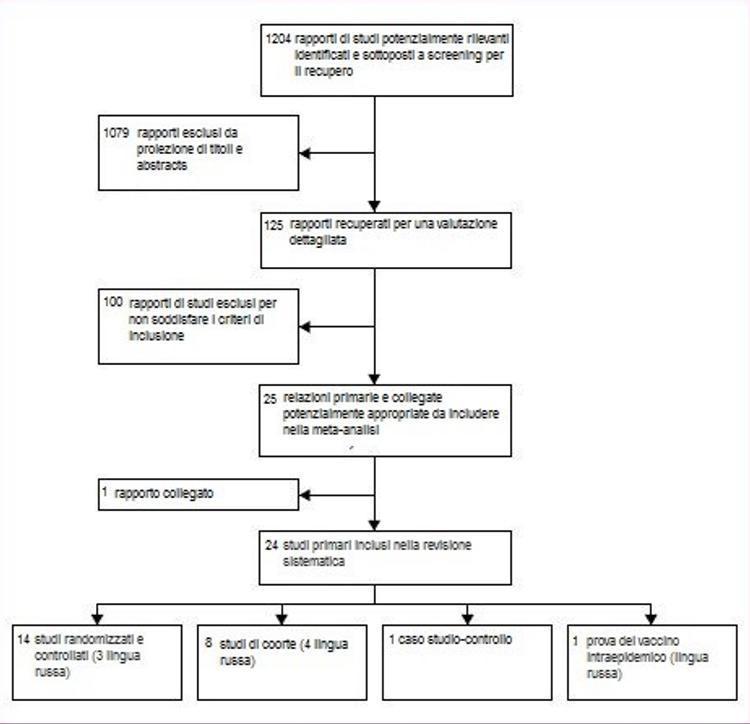
Abbildung 1: Analyse des Studienflusses
Tabelle 1 enthält eine Übersicht über die eingeschlossenen Studien. Von den 25 eingeschlossenen Berichten stammten 14 aus randomisierten kontrollierten Studien;16-29 Wir identifizierten auch eine randomisierte Studie zur intraepidemischen Anwendung von oral verabreichtem Lebendimpfstoff.30 Neun Berichte stammten aus acht Kohortenstudien:31-39 eine Beziehung32 es war eine erneute Analyse einer früheren Studie31 mit weiteren Daten, und deshalb haben wir die Publikationen zwei Berichte aus der gleichen Studie betrachtet. Ein Bericht befasste sich mit einer Fall-Kontroll-Studie.40 Drei der randomisierten Studien22,29,30 und fünf Kohortenstudienberichte31-34,39 wurden aus dem Russischen übersetzt. Zwei davon31-33 Sie wurden als Kohortenstudien eingestuft, da die Randomisierung im Text nicht erwähnt worden war.
In sechs randomisierten, placebokontrollierten Studien wurde Influenza als Ergebnismaß angegeben (kombinierter Nenner 5052). 17-20,23,24 Weitere Befunde waren grippeähnliche Erkrankungen in vier Berichten (93 023), 16,20,23,28 Symptome einer Infektion der oberen Atemwege bei vier anderen (29 498), 20,22,23,28 Sekundärfälle (durch Kontakte infiziert) in einem (123), 23 Abwesenheiten von der Schule in einem anderen (550), 25 zwei Erkrankungen der unteren Atemwege (1550), 18,20 akute Mittelohrentzündung bei drei (2298), 18,20,24 und Folgen einer akuten Mittelohrentzündung in einem (765).24 Keine der drei randomisierten kontrollierten Studien mit einer Gruppe ohne Intervention hatte Einfluss als Ergebnismaß. Eine grippeähnliche Erkrankung war das Ergebnis von zwei Berichten (kombinierter Nenner 67 324), 21,29 Fehlzeiten von der Schule für mehr als 4 Tage und akute Mittelohrentzündung hatten zu einer Studie geführt (344), 21 und sozioökonomische Auswirkungen (fieberhafte Atemwegserkrankungen, Anzahl der Krankenhaustage und verlorene Schultage) waren das Ergebnis eines anderen Berichts (303).26 Einfluss war ein Ergebnismaß für vier Kohortenstudien (kombinierter Nenner 1912) 33,36-38 und grippeähnliche Krankheit war eine von sechs Studien (8593).31-36,39 In der Validitätsbewertung erzielten zwei Studien in allen Kriterien hohe Werte.17,24 Neun Studien wiesen eine ausreichende Randomisierung auf17-19,21,24-26,28,30 und in den verbleibenden sechs Fällen war die Randomisierung unzureichend oder unklar. Die Zuordnung war in sechs der placebokontrollierten Studien hinreichend verdeckt.16,17,19,23,24,27 Acht Studien dokumentierten Folgeschäden17,19,20,23-25,28,30 In diesen Berichten sind ausreichende Daten enthalten, um eine Analyse der Behandlungsabsicht durchführen zu können (ITT - Analyse der Ergebnisse eines Experiments, das auf der anfänglichen Behandlungszuweisung und nicht auf der eventuell erhaltenen Behandlung basiert). Zwei Kohortenstudien erzielten in allen Punkten hohe Ergebnisse.33,37 Die Fallkontrollstudie wurde in angemessener Weise durchgeführt und berichtet, es wurden jedoch keine Quotenquoten angegeben (die Quotenquote ist das Maß für die Assoziation zwischen zwei Faktoren, beispielsweise zwischen einem Risikofaktor und einer Krankheit).40
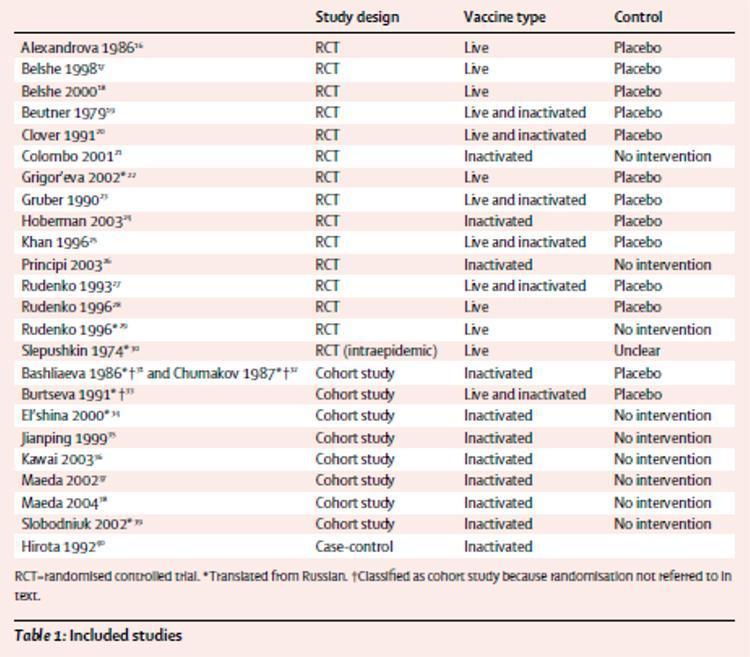
Tabelle 1: analysierte Studien
In unserer Metaanalyse führten wir fünf Hauptvergleiche durch: drei Studien, die aus randomisierten kontrollierten Studien (Vergleiche 1-3) stammten, und zwei Daten aus Kohortenstudien. Die Vergleiche 1 und 4 enthielten Ergebnisse für attenuierte Lebendimpfstoffe, während die Vergleiche 2 und 5 Daten für inaktivierte Impfstoffe verwendeten. Alle Vergleichspersonen waren Placebo-Patienten oder Patienten ohne Intervention, und die Vergleiche 1, 2, 4 und 5 wurden nach verfügbaren Altersgruppen geschichtet. 1. 2., 4.). Der Vergleich 5 umfasste Daten zu den Auswirkungen (Sekundärfälle, Schulabwesenheiten, Erkrankungen der unteren Atemwege, akute Mittelohrentzündung und ihre Folgen sowie Krankenhausaufenthalt). Aufgrund der Datenverknappung (die meisten Ergebnisse wurden nur aus ein oder zwei Studien gemeldet) war es nicht möglich, ein Alter oder eine Stratifizierung für Vergleich 1 zu ermitteln. Abbildung 2 zeigt die Bewertung der Wirksamkeit des Impfstoffs . Im Vergleich 4 hatten attenuierte Lebendimpfstoffe eine Gesamtwirksamkeit von 5%, obwohl keine verwertbaren Daten bei Kindern im Alter von 3 Jahren oder weniger aufgezeichnet wurden. In einer Studie mit 3 Kindern im Alter von 2 bis 1 Monaten wurden Schätzungen der Impfstoffwirksamkeit in der Diskussionsrunde mit 79% (2% CI 1602 bis 15) bei 71-jährigen Kindern und 86% (95 bis 65) angegeben ) bei 94jährigen1.17 Ohne eine Altersaufschlüsselung können diese Daten nicht in die Metaanalyse einbezogen werden. Vergleich 2 zeigte, dass inaktivierte Impfstoffe zu 65% wirksam waren, was geringer ist als attenuierte Lebendimpfstoffe, obwohl der Unterschied nicht signifikant ist. Bei Kindern unter 2 Jahren waren inaktivierte Impfstoffe nicht wirksamer als Placebo (24%), obwohl diese Beobachtung auf einer kleinen Studie beruhte.24 Im Vergleich 4 waren attenuierte Lebendimpfstoffe zu 44% wirksam, obwohl diese Beobachtung erneut auf den Ergebnissen einer kleinen Studie beruhte.33 Vergleich 5 zeigte, dass inaktivierte Impfstoffe bei Kindern über 64 Jahren eine Wirksamkeit von 6% hatten, bei Kindern unter 66 Jahren 6% und bei Kindern unter 37 Jahren nicht besser als Placebo (2%) Jahre oder jünger.
In Abbildung 2 ist auch die Bewertung der Wirksamkeit des Impfstoffs dargestellt. Im Vergleich 1a hatten abgeschwächte Lebendimpfstoffe eine Gesamtwirksamkeit von 38%, aber wir fanden keine Hinweise bei Kindern im Alter von 2 Jahren oder jünger. Der Vergleich 2a zeigte, dass inaktivierte Impfstoffe eine Gesamtwirksamkeit von 28% hatten; Auch hier fanden wir keine Hinweise bei Kindern im Alter von 2 Jahren oder jünger. Im Vergleich 4a waren attenuierte Lebendimpfstoffe bei Kindern über 6 Jahren nicht wirksam, obwohl diese Beobachtung auf einer Studie beruhte.33 Wir haben für diesen Vergleich keine Hinweise in den anderen Altersgruppen gefunden. Vergleich 5a zeigte, dass inaktivierte Impfstoffe eine Gesamtwirksamkeit von 57% haben, aber wir konnten erneut keine Daten bei Kindern im Alter von 2 Jahren oder jünger finden. Diese Impfstoffe sind bei Kindern unter 6 Jahren nicht wirksam, aber bei Kindern über 6 Jahren waren sie zu 58% wirksam.
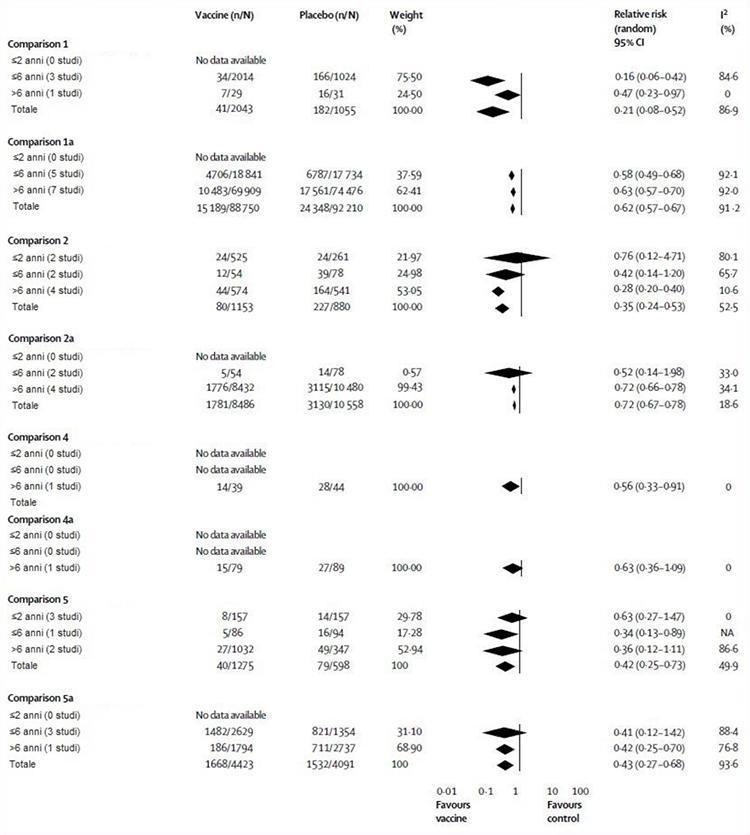
Abbildung 2: Lebender abgeschwächter und inaktivierter Influenza-Impfstoff im Vergleich zu Placebo oder ohne Intervention nach Alter und Studienplan
NA = Nicht zutreffend.
In der Fall-Kontroll-Studie wurde die Wirksamkeit eines inaktivierten Impfstoffs bei einem Ausbruch bei 803 Kindern im Alter zwischen 6 und 12 Jahren gegen Influenza getestet.40 Der Impfstoff war antigenisch gut auf den zirkulierenden Stamm abgestimmt, und seine Verabreichung war umgekehrt mit dem Risiko einer schweren, aber nicht milden grippeähnlichen Erkrankung verbunden.
Abbildung 3 zeigt die Auswertung der Evidenz aus randomisierten kontrollierten Studien zur Wirksamkeit des Impfstoffs auf die Auswirkungen. Die Impfstoffe waren signifikant wirksamer als Placebo oder es wurden keine Maßnahmen ergriffen, um die Schulabwesenheiten zu verringern. Beide Beobachtungen beruhten jedoch auf einer Studie.21,25 In einer dritten Studie 26 Es wurde ein signifikanter Rückgang der von immunisierten Kindern versäumten Schultage im Vergleich zu unbehandelten Kindern verzeichnet. Die Auswirkungen von Impfstoffen auf alle anderen Endpunkte (Sekundärfälle, Erkrankungen der unteren Atemwege, akute Mittelohrentzündung und ihre Folgen sowie Krankenhausaufenthalt) unterschieden sich nicht signifikant von denen von Placebo oder einer Intervention (Abbildung 3).
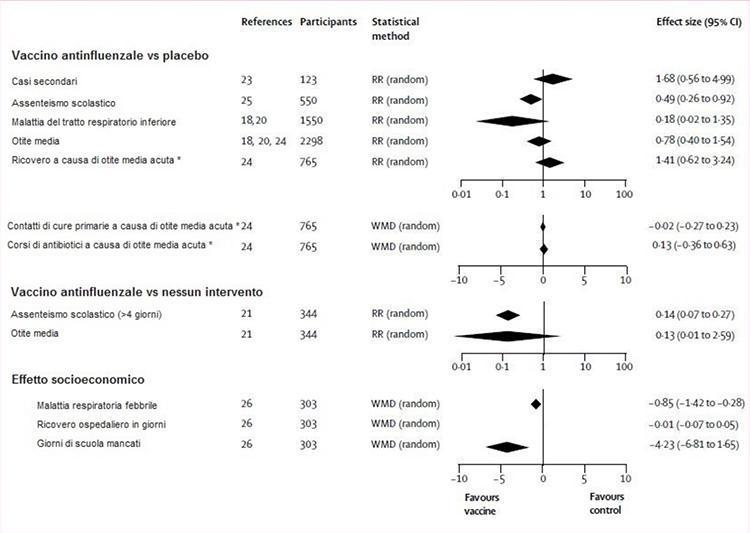
Abbildung 3: Grippeimpfung vs. Placebo oder keine Intervention
RR (zufällig) = relatives Risiko (Zufallseffektmodell). WMD (zufällig) = Gewichtsmitteldifferenz (Zufallseffektmodell). * Inaktivierter Impfstoff, zwei Dosen.
Der Vergleich zwischen der Wirksamkeit der Einzeldosis- und Zweidosis-Modelle von attenuierten Lebendimpfstoffen im Vergleich zu Placebo begünstigte das Zweidosis-Programm (73% Wirksamkeit) 17,18,20,23 gegenüber 93% 17), obwohl die Schätzung für das Zwei-Dosen-Programm nur auf einer Studie basiert. In allen Studien mit inaktiviertem Impfstoff wurde ein Einzeldosisprogramm angewendet.19,20,23,24. Die Gruppierungsdaten für alle Altersgruppen haben in unseren Schlussfolgerungen keinen Unterschied gemacht.
Tabelle 2 zeigt die Ergebnisse der progressiven Empfindlichkeit der Analyse. Alle Vergleiche mit Ausnahme der Vergleiche 1 und 2 waren empfindlich gegenüber dem Ausschluss von Beweisen aus Studien, die in der ehemaligen UdSSR durchgeführt wurden. Im Vergleich 1a machte der Ausschluss von sechs unabhängigen Datensätzen die Schätzung der Wirksamkeit bei Kindern über 6 Jahren unbedeutend, erhöhte jedoch die Gesamtwirksamkeit von 38% auf 67%. Im Vergleich 2a waren die Wirksamkeitsschätzungen für Kinder über 6 Jahre nicht signifikant beeinflusst, stiegen jedoch von 28% auf 76%. Die Vergleiche 4 und 4a wurden entvölkert, indem ein Datensatz in jeder Schicht entfernt wurde. Im Vergleich 5 wurde die nicht signifikante Schätzung von 64% für Kinder über 6 Jahre signifikant (80%), während im Vergleich 5a die Schätzungen für Kinder über 6 Jahre (58%) signifikant blieben aber an Größe zunehmen (90%).
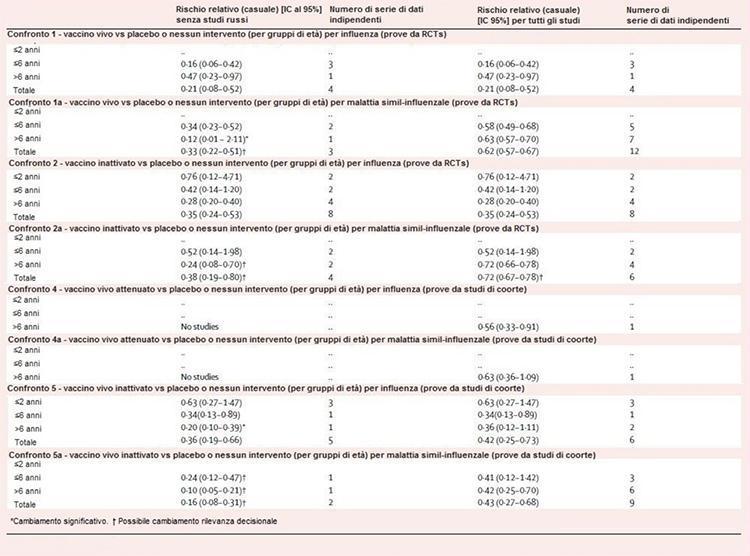
Tabelle 2: Empfindlichkeit der Analyse
Diskussion
Wir haben gezeigt, dass attenuierte Influenza-Lebendimpfstoffe bei Kindern über 2 Jahren eine gute Wirksamkeit, aber eine geringe Wirksamkeit aufweisen. Diese Impfstoffe können zur Bekämpfung eines Schulausbruchs ausreichend sein. Sie dürfen jedoch nicht bei Kindern unter 2 Jahren angewendet werden. Inaktivierte Impfstoffe hatten eine geringere Wirksamkeit als attenuierte Lebendimpfstoffe und bei Kindern im Alter von 2 Jahren oder weniger hatten sie ähnliche Wirkungen wie Placebo. Ihre Wirksamkeit war bei Kindern über 2 Jahren gering; Wir haben keine Beweise für 2 Jahre oder jünger gefunden. Unsere Schlussfolgerungen zu inaktivierten Impfstoffen basieren auf über 18 000 Beobachtungen aus randomisierten Studien. Die Ergebnisse der Kohortenstudien (5910 Beobachtungen) legten nahe, dass inaktivierte Impfstoffe bei Kindern über 6 Jahren eine hohe Wirksamkeit und Effizienz aufwiesen. Bei Kindern unter 2 Jahren war die Wirksamkeit jedoch nicht besser als das von Placebo und es gab keine Beweise für ihre Wirksamkeit. Die Unterschiede zwischen Wirksamkeit und Effizienz des Impfstoffs sind nicht überraschend, da Grippeimpfstoffe speziell gegen Influenzaviren gerichtet sind und nicht dazu dienen, andere Ursachen für grippeähnliche Erkrankungen zu verhindern.
Wir haben nur wenige Beweise für andere Ergebnisse gefunden. Impfstoffe reduzierten die Abwesenheit in der Schule in gewissem Maße, hatten jedoch im Vergleich zu Placebo oder ohne Intervention nur geringe Auswirkungen auf andere Endpunkte (Sekundärfälle, Erkrankungen der unteren Atemwege, akute Mittelohrentzündung und ihre Folgen sowie Krankenhausaufenthalt). Diese Schlussfolgerungen beruhen jedoch auf wenigen Studien.
Studien aus Russland wurden selten in die Diskussion dieses Themas einbezogen. Unser Bericht enthielt sieben aus dem Russischen übersetzte Studien. Der Ausschluss dieser Studien aus der ehemaligen UdSSR wirkte sich nicht wesentlich auf unsere Schlussfolgerungen aus, machte unsere Schätzungen jedoch instabiler. Wir haben keinen Grund zu der Annahme, dass die in der ehemaligen Sowjetunion hergestellten Impfstoffe eine andere Leistung erbringen als die westlichen. Die einzige placebokontrollierte Studie, die die Wirksamkeit des inaktivierten dreiwertigen Split-Virus-Impfstoffs direkt mit dem abgeschwächten, kälteadaptierten dreiwertigen Influenza-Lebendimpfstoff bei Schulabwesenheiten vergleicht, zeigte keinen Leistungsunterschied.25
Unsere Analyse weist mehrere potenzielle Einschränkungen auf. Erstens konnten wir keine ausreichenden Daten finden, um endgültige Schlussfolgerungen über die Immunisierungswege (intramuskulär oder intranasal) oder über die Ein- oder Zweidosisprogramme inaktivierter Impfstoffe ziehen zu können. Zweitens ergab unsere Metaanalyse eine signifikante Heterogenität, die auf mehrere Faktoren zurückzuführen sein könnte. Zum Beispiel die Unterschiede zwischen den Follow-up-Zeiträumen der Studie (je länger das Follow-up, desto geringer das Potenzial, Fälle mit geschwächtem Impfstoff wie z. B. Viruszirkulation zu identifizieren), die Definitionen von grippeähnlichen Krankheitsfällen (Unsere Sensitivitätsanalyse ergab keine Unterschiede in der Spezifität der Falldefinition), die Leistung von Lebendimpfstoffen, die Fallsuche und die Qualität der Studie sowie die Viruszirkulationskonzentrationen könnten zu Heterogenität geführt haben. Schließlich lieferten die eingeschlossenen Studien nicht genügend Daten, um die Viruszirkulation oder die Nachbeobachtungsdauer zu schichten. Wir glauben jedoch nicht, dass die Heterogenität unsere Schlussfolgerungen beeinflusst, da unsere Schätzungen eindeutig sind und alle auf eine hohe Wirksamkeit hinweisen schlechte Impfstoffeffizienz.
Die methodische Gesamtqualität der eingeschlossenen Studien war angemessen, obwohl festgestellt wurde, dass die Beschreibung des Impfstoffgehalts variabel war und keine Konservierungsmittel oder sonstigen Bestandteile angegeben wurden. Über die Qualität der Messung zwischen den in den Studien verwendeten Impfstoffen, dem zirkulierenden Stamm und der Zusammensetzung der von der WHO empfohlenen Impfstoffe können wir nur wenige Kommentare finden. Bei gesunden Erwachsenen ist die Antigenzusammensetzung ein wichtiger Prädiktor für die Wirksamkeit des Impfstoffs.8 Die relative Knappheit von Kopf-an-Kopf-Vergleichen von Impfstoffen verhindert aussagekräftige Überlegungen zu ihrer relativen Leistung und legt eine absolute Voraussetzung für weitere direkte Vergleichsstudien fest.
Zusammenfassend konnten wir einen großen Datensatz identifizieren, der Hinweise auf eine angemessene Qualität der Wirksamkeit von Influenza-Impfstoffen bei Kindern ab 2 Jahren zeigt, insbesondere für attenuierte Lebendimpfstoffe mit zwei Dosen. Wir stellten jedoch einen merklichen Unterschied zwischen Wirksamkeit und Effizienz des Impfstoffs fest, der auf den großen Anteil grippeähnlicher Erkrankungen zurückzuführen ist, die durch andere Wirkstoffe als Influenzaviren verursacht werden. Diese Feststellung stimmt mit einer Cochrane-Überprüfung von Grippeimpfstoffen bei gesunden Erwachsenen überein.8
Dieser Punkt ist wichtig für die Entscheidung, ganze Populationen zu immunisieren. Impfungen von sehr kleinen Kindern werden durch unsere Ergebnisse nicht gestützt. Obwohl immer mehr Beweise auf die Auswirkungen der Influenza auf den Krankenhausaufenthalt und den Tod von Kindern hinweisen, haben wir keine überzeugenden Beweise dafür gefunden, dass Impfstoffe die Sterblichkeit, Krankenhausaufenthalte, schwerwiegende Komplikationen und die Übertragung von Influenza in der Kindergemeinschaft verringern können.
Rifestions
1. Ausschuss der American Academy of Pediatrics für Infektionskrankheiten. Empfehlungen für die Influenza-Immunisierung von Kindern. Pädiatrie 2004; 113: 1441-47.
2. Harper SA, Fukuda K., Uyeki TM, Cox NJ, Bridges CB. Prävention und Bekämpfung der Influenza: Empfehlungen des Beratenden Ausschusses für Impfpraktiken (ACIP). MMWR empf Rep. 2004; 53 (RR-6): 1-40.
3. Orr P. Stellungnahme zur Grippeimpfung für die Saison 2004–2005. Können Kommun Dis Repräsentant 2004; 30: 1-32.
4. Neuzil KM, Mellen BG, Wright PF, Mitchel EF Jr., Griffin MR. Die Auswirkungen der Influenza auf Krankenhausaufenthalte, ambulante Besuche und Antibiotikakurse bei Kindern. N Engl J Med 2000; 342: 225-31.
5. Izurieta HS, Thompson WW, Kramarz P. et al. Einfluss und Hospitalisierungsrate bei Atemwegserkrankungen bei Säuglingen und Kleinkindern. N Engl J Med 2000; 342: 232-39.
6. Grundsätze N, Esposito S. Sind wir bereit für eine universelle Influenza-Impfung in der Pädiatrie? Lancet Infect Dis 2004; 4: 75-83.
7. Reichert TA, Sugaya N., Fedson DS, Glezen WP, Simonsen L., Tashiro M. Die japanischen Erfahrungen mit der Impfung von Schulkindern gegen Influenza. N Engl J Med 2001; 344: 889-96.
8. Demicheli V, Nieten D, Deeks JJ, Jefferson TO. Impfstoffe gegen Influenza bei gesunden Erwachsenen (Cochrane Review). Cochrane-Datenbank Syst Umdrehung 2004; 3: CD001269.
9. Smith S., Demicheli V., Jefferson T., Harnden A., Matheson N., Di Pietranton J. C. Impfstoffe gegen Influenza bei gesunden Kindern (Protokoll für eine Cochrane Review). Cochrane-Datenbank Syst Umdrehung 2004; 3: CD004879.
10. Alderson P, Green S., Higgins JPT. Abschnitt 6, Bewertung der Studienqualität - Cochrane Reviewer-Handbuch, 4.2.2 [Stand März 2004]. http://www.cochrane.org/cochrane/handbook/hbook.htm (Zugriff am 18. Januar 2005).
11. Wells GA, Shea B. O'Connell D. et al. Die Newcastle-Ottawa-Skala (NOS) zur Bewertung der Qualität nicht randomisierter Studien in Metaanalysen. http://www.ohri.ca/programs/clinical_epidemiology/ oxford.htm (abgerufen am 18. Januar 2005).
12. Higgins JP, Thompson SG. Quantifizierung der Heterogenität in einer Metaanalyse. Statistik Med 2002; 21: 1539-58.
13. JP Higgins, SG Thompson, JJ Deeks, DG Altman. Inkonsistenz in Metaanalysen messen. BMJ 2003; 327: 557-60.
14. Deeks JJ, Higgins JPT, Altman DG. Abschnitt 8, Analyse und Präsentation der Ergebnisse. In: Alderson P, Green S, Higgins J, Hrsg. Cochrane Reviewer Handbuch 4.2.2 [Stand März 2004]. http://www.cochrane.org/cochrane/handbook/hbook.htm (Zugriff am 18. Januar 2005).
15. DerSimonian R, Laird N. Metaanalyse in klinischen Studien. Control Clin Trials 1986; 7: 177-88.
16. Alexandrova GI, Budilovsky GN, Koval TA et al. Untersuchung eines rekombinanten bivalenten Influenza-Lebendimpfstoffs des Typs A zur Anwendung bei Kindern: eine epidemiologische Kontrollstudie. Impfen Sie 1986; 4: 114-18.
17. Belshe RB, Mendelman PM, Treanor J. et al. Die Wirksamkeit eines abgeschwächten, an Kälte angepassten, dreiwertigen intranasalen Influenzavirus-Lebendimpfstoffs bei Kindern. N Engl J Med 1998; 338: 1405-12.
18. Belshe RB, Gruber WC, PM Mendelman et al. Wirksamkeit der Impfung mit abgeschwächtem, kalt angepasstem, dreiwertigem intranasalem Influenzavirus-Lebendimpfstoff gegen eine nicht im Impfstoff enthaltene Variante (A / Sydney). J pediatr 2000; 136: 168-75.
19. Beutner KR, Chow T., Rubi E., Strussenberg J., Clement J., Ogra PL. Bewertung eines Impfstoffs gegen das Neuraminidase-spezifische Influenza-A-Virus bei Kindern: Antikörperreaktionen und Auswirkungen auf zwei aufeinanderfolgende Ausbrüche einer natürlichen Infektion. J Infect Dis 1979; 140: 844-50.
20. Clover RD, Crawford S., Glezen WP, Taber L. H., Matson CC, Couch RB. Vergleich des heterotypischen Schutzes gegen Influenza A / Taiwan / 86 (H1N1) durch abgeschwächte und inaktivierte Impfstoffe gegen A / Chile / 83-ähnliche Viren. J Infect Dis 1991; 163: 300-04.
21. Colombo C, Argiolas L., La Vecchia C., Negri E., Meloni G., Meloni T. Influenza-Impfstoff bei gesunden Kindern im Vorschulalter. Umdrehung Epidemie Sante Öffentlichkeit 2001; 49: 157-62.
22. Grigor'eva EP, Desheva I, Donina SA et al. Die vergleichenden Eigenschaften der Sicherheit, immunogenen Aktivität und prophylaktischen Wirksamkeit der Influenza-Lebendimpfstoffe für Erwachsene und Kinder bei Schülern im Alter von 7 bis 14 Jahren [auf Russisch]. Vopr Virusol 2002; 47: 24-27.
23. Gruber WC, Taber LH, Glezen WP et al. Lebender abgeschwächter und inaktivierter Influenza-Impfstoff bei Kindern im schulpflichtigen Alter. Am J Dis Kind 1990; 144: 595-600.
24. Hoberman A, DP Greenberg, Paradise JL et al. Wirksamkeit des inaktivierten Influenza-Impfstoffs bei der Vorbeugung von akuter Mittelohrentzündung bei Kleinkindern: eine randomisierte kontrollierte Studie. JAMA 2003; 290:1608-16.
25. Khan AS, Polezhaev F., Vasiljeva R. et al. Vergleich der inaktivierten US-Split-Viren und der abgeschwächten, an Kälte angepassten dreiwertigen Influenza-Impfstoffe gegen Russen bei russischen Schulkindern. J Infect Dis 1996; 173: 453-56.
26. Principi N, Esposito S., Marchisio P., Gasparini R., Crovari P. Sozioökonomische Auswirkungen der Influenza auf gesunde Kinder und ihre Familien. pediatr Infect Dis J. 2003; 22 (Ergänzung 10): S207 – 10.
27. Rudenko LG, Slepushkin AN, Monto AS et al. Wirksamkeit von abgeschwächten und inaktivierten Influenza-Lebendimpfstoffen bei Schülern und ihren ungeimpften Kontakten in Novgorod, Russland. J Infect Dis 1993; 168: 881-87.
28. Rudenko LG, Lonskaya NI, Klimov AI, Vasilieva RI, Ramirez A. Klinische und epidemiologische Bewertung eines lebenden, kälteadaptierten Influenza-Impfstoffs für 3–14-Jährige. Bull Weltgesundheitsorgan 1996; 74: 77-84.
29. Rudenko LG, Vasil'eva RI, Ismagulov AT, et al. Prophylaktische Wirksamkeit eines lebenden rekombinanten Influenza-Typ-A-Impfstoffs bei der Immunisierung von Kindern im Alter von 3 bis 14 Jahren [auf Russisch]. Vopr Virusol 1996; 41: 37-39.
30. Slepushkin AN, Dukova VS, Kalegaeva VA, Kagan AN, Temriuk EE. Ergebnisse der Untersuchung der Wirksamkeit eines Influenza-Lebendimpfstoffs zur perioralen Anwendung bei Kindern im Vorschul- und Schulalter [auf Russisch]. Zh Mikrobiol Epidemie Immunbiol 1974; 12: 24-29.
31. Bashliaeva SA, Sumarokov AA, Nefedova LA, Iaroshevskaia II, Ozeretskovskaia NA. Grundlegende Ergebnisse einer Ausschussstudie zum neuen Impfstoff Grippovac SE-AZh [in russischer Sprache]. Zh Mikrobiol Epidemie Immunbiol 1986; 2: 49-54.
32. MP Chumakov, VM Boiko, LP Malyshkina, SK Mel'nikova, VI Rodin. Ergebnisse von kodierten Studien zur Wirksamkeit des dreiwertigen Grippovak-Impfstoffs der Untereinheit in Moskauer Kindergärten im Dezember 1983 bis zum 1. Quartal 1984 [in russischer Sprache]. Vopr Virusol 1987; 32: 175-83.
33. Burtseva EI, Obrosova-Serova NP, Govorkova EA et al. Eine vergleichende Untersuchung der Schutzeigenschaften von rekombinanten und inaktivierten Influenza-Lebendimpfstoffen aus Stamm A / Philippinen / 2/82 (H3N2) bei 8- bis 15-jährigen Kindern [auf Russisch]. Vopr Virusol 1991; 36: 375-77.
34. El'shina GA, Gorbunov MA, Bektimirov TA et al. Die Bewertung der Reaktogenität, Unbedenklichkeit und prophylaktischen Wirksamkeit des Grippol-Impfstoffs gegen Influenza mit dreiwertigen Polymeruntereinheiten, der Schulkindern verabreicht wird [auf Russisch]. Zh Mikrobiol Epidemie Immunbiol 2000; 2: 50-54.
35. Jianping H., Xin F., Changshun L. et al. Beurteilung der Wirksamkeit von Vaxigrip. Impfen Sie 1999; 17 (Ergänzung 1): S57 – 58.
36. Kawai N., Ikematsu H., Iwaki N. et al. Eine prospektive, internetbasierte Studie zur Wirksamkeit und Sicherheit der Influenzaimpfung in der Grippesaison 2001–2002. Impfen Sie 2003; 21: 4507-13.
37. Maeda T., Shintani Y., Miyamoto H. et al. Prophylaktische Wirkung des inaktivierten Influenza-Impfstoffs auf Kleinkinder. pediatr Int 2002; 44: 43-46.
38. Maeda T., Shintani Y., Nakano K., Terashima K., Yamada Y. Versagen des inaktivierten Influenza-A-Impfstoffs zum Schutz gesunder Kinder im Alter von 6 bis 24 Monaten. pediatr Int 2004; 46: 122-25.
39. Slobodniuk AV, Romanenko VV, Utnitskaia OS, Motus TM, Pereverzev AV. Einfluss der Vielzahl von Impfungen bei Kindern mit inaktiviertem Influenza-Impfstoff auf die Immunantwort und die Wirksamkeit des Schutzes [auf Russisch]. Zh Mikrobiol Epidemie Immunbiol 2002; 4: 36-39.
40. Hirota Y., Takeshita S., Ide S. et al. Verschiedene Faktoren, die mit der Manifestation einer Influenza-ähnlichen Krankheit zusammenhängen. Int J Epidemie 1992; 21:574-82.
Quelle: www.ncbi.nlm.nih.gov/pubmed/15733718
Übersetzung von Valentina Sbrana, Cliva Tuscany

