AstraZeneca, sous le feu de la sécurité des vaccins
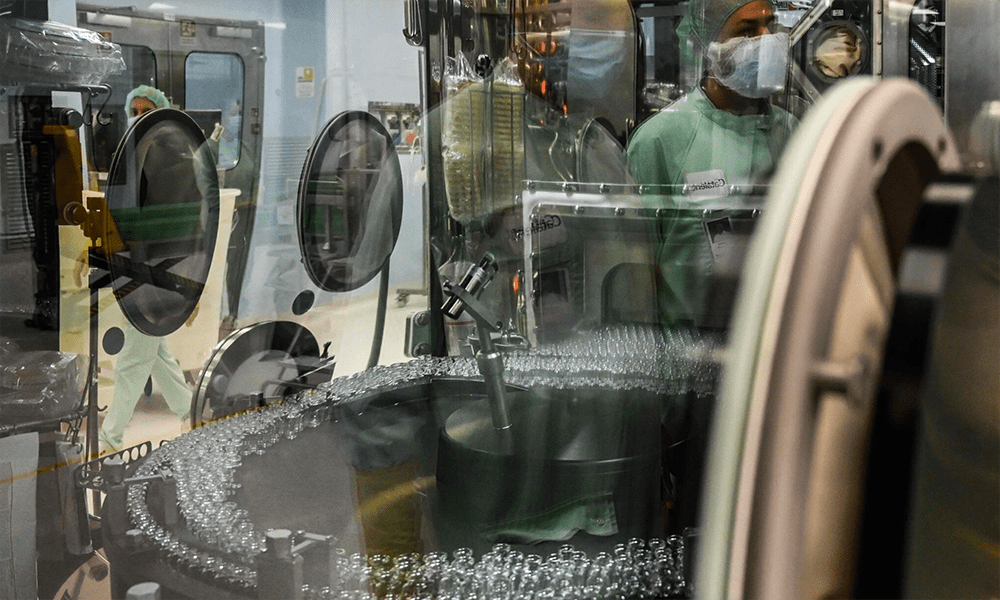
Les experts craignent que l'entreprise n'ait pas fait preuve de transparence au sujet de deux participants qui sont tombés gravement malades après avoir testé son vaccin expérimental.
Les sondages révèlent que les Américains sont de plus en plus prudents quant à l'acceptation d'un vaccin contre le coronavirus. Les scientifiques à l'intérieur et à l'extérieur du gouvernement craignent que les régulateurs sous pression puissent libérer un vaccin non prouvé ou dangereux.
Les experts sont particulièrement préoccupés par les études vaccinales d'AstraZeneca, qui ont débuté en avril en Grande-Bretagne, en raison du refus de la société de fournir des détails sur une maladie neurologique grave chez deux participants, tous deux des femmes, qui ont reçu le vaccin expérimental. Ces cas ont incité l'entreprise à interrompre les procès à deux reprises, la deuxième fois plus tôt ce mois-ci. Les études ont repris en Grande-Bretagne, au Brésil, en Inde et en Afrique du Sud, mais sont toujours en pause aux États-Unis. À ce jour, environ 18.000 XNUMX personnes dans le monde ont reçu le vaccin AstraZeneca.
Le projet d'essai de 111 pages d'AstraZeneca, connu sous le nom de protocole, indique que sa cible est un vaccin avec une efficacité de 50% - le même seuil que la Food and Drug Administration a fixé dans ses lignes directrices pour les vaccins contre le médicament. coronavirus. Pour déterminer avec une certitude statistique si l'entreprise a atteint cet objectif, il faudra 150 patients confirmés de coronavirus parmi les participants qui ont été vaccinés ou ont reçu un placebo.
Cependant, le plan est qu'une commission de sécurité mènera une enquête précoce après qu'il n'y ait eu que 75 cas. Si le vaccin est efficace à 50% à ce stade, il peut être possible pour la société d'arrêter l'essai prématurément et de demander l'autorisation du gouvernement de libérer le vaccin pour une utilisation d'urgence.
En n'autorisant qu'une seule de ces analyses intermédiaires, le plan d'AstraZeneca est plus rigoureux que les autres qui ont été publiés, par Moderna et PfizerLe Dr Eric Topol, un expert en études cliniques chez Scripps Research à San Diego, a déclaré dans une interview. Moderna autorise deux analyses de ce type et Pfizer quatre.
Le problème avec l'examen des données trop souvent, après un nombre relativement petit de cas, est que cela augmente les chances de trouver un aspect de la sécurité et de l'efficacité qui peut ne pas tenir. L'arrêt précoce des essais peut également augmenter le risque de manquer des effets secondaires rares qui pourraient être importants une fois le vaccin administré à des millions de personnes.
Le Dr Topol a déclaré que le plan d'AstraZeneca, comme ceux de Moderna et Pfizer, avait une caractéristique problématique: ils comptent tous des cas relativement bénins de Covid-19 lors de la mesure de l'efficacité, ce qui peut entraver les efforts visant à déterminer si le vaccin prévient. maladie modérée ou grave.
Ces plans ne sont généralement pas partagés avec le public "en raison de l'importance de maintenir la confidentialité et l'intégrité des procès", a déclaré Michele Meixell, un porte-parole d'AstraZeneca, dans un communiqué.
La société a publié quelques détails sur les deux cas de maladie grave lors de son procès. Le premier participant a reçu une dose du vaccin avant de développer une inflammation de la moelle épinière, connue sous le nom de myélite transverse, selon une fiche d'information du participant pour le vaccin AstraZeneca de juillet. La maladie peut causer une faiblesse des bras et des jambes, une paralysie, des douleurs et des problèmes intestinaux et vésicaux.
L'affaire a appelé à une pause dans les essais de vaccins d'AstraZeneca pour permettre un examen de l'innocuité par des experts indépendants. Un porte-parole de la société a déclaré au Times la semaine dernière que le volontaire avait par la suite été déterminé à avoir un cas de sclérose en plaques lié au vaccin, non diagnostiqué auparavant, et que l'essai avait repris peu de temps après.
La myélite transversale peut parfois être le premier signe de sclérose en plaques, impliquant des symptômes plus complexes. Mais la myélite seule peut également survenir après que le corps rencontre un agent infectieux tel qu'un virus.
La société a déclaré qu'elle n'avait pas confirmé le diagnostic dans le deuxième cas, un participant tombé malade après la deuxième dose du vaccin. Une personne familière avec la situation, qui s'est entretenue avec le Times sous couvert d'anonymat, a déclaré que la maladie du participant avait été identifiée comme une myélite transverse. Le procès a de nouveau été suspendu le 6 septembre après qu'elle soit tombée malade.
La condition est rare, mais grave, et les experts ont déclaré que trouver ne serait-ce qu'un cas parmi des milliers de participants à l'essai pourrait être un réveil. Des cas plus confirmés, ont-ils déclaré, pourraient suffire à arrêter complètement l'offre de vaccins d'AstraZeneca.
Une fiche d'information du participant datée du 11 septembre sur l'essai d'AstraZeneca en Grande-Bretagne combinait les cas des deux volontaires, indiquant que les maladies n'étaient "probablement pas associées au vaccin ou qu'il n'y avait pas suffisamment de preuves pour dire avec certitude que les maladies étaient ou n'étaient pas liés au vaccin », d'après les examens de l'innocuité. Le lendemain, AstraZeneca a annoncé qu'elle avait repris les tests au Royaume-Uni.
Mais la FDA n'a jusqu'à présent pas autorisé l'entreprise à relancer l'essai aux États-Unis.
Un porte-parole de la FDA a refusé de commenter. Les National Institutes of Health ont déclaré dans un communiqué qu '"il reste à voir" si l'apparition de la maladie chez les participants à l'essai était aléatoire ou liée au vaccin, ajoutant que "une pause pour permettre une évaluation plus approfondie est conforme à la pratique. la norme".
Le Dr Mark Goldberger, expert en maladies infectieuses au Global Antibiotic Research and Development Partnership et ancien fonctionnaire de la FDA, a déclaré qu'il trouvait la reprise rapide des essais à l'étranger "un peu dérangeante", en particulier compte tenu du manque de des détails sur les symptômes des patients et l'ambiguïté quant à leur lien avec le vaccin. "C'est peut-être le mieux qu'ils puissent faire - il n'est peut-être pas possible d'obtenir plus de certitude pour le moment", a-t-il déclaré. «C'est un point d'interrogation sur ce qui se passe.
L'entreprise n'a pas immédiatement informé le public des problèmes neurologiques des deux participants. Il n'a pas non plus immédiatement averti la FDA qu'il mettait de nouveau en pause ses expériences après que le deuxième volontaire britannique eut développé une maladie et un comité de sécurité indépendant a appelé à une suspension temporaire, selon plusieurs personnes qui connaissaient la situation. Le PDG de la société a informé les investisseurs des problèmes, mais n'en a pas parlé publiquement tant que l'information n'a pas été divulguée. rapporté par la STAT.
«La communication autour de lui a été horrible et inacceptable», a déclaré le Dr Peter Jay Hotez, virologue au Baylor College of Medicine à Houston. "Ce n'est pas ainsi que le peuple américain devrait en entendre parler."
Le Dr Hotez a également critiqué les déclarations faites par des responsables gouvernementaux, y compris des régulateurs britanniques qui, a-t-il déclaré, n'ont pas fourni de justification pour la reprise de leurs essais.
Le Dr Paul Offit, professeur à l'Université de Pennsylvanie et membre du comité consultatif des vaccins de la FDA, a déclaré que l'on ne savait pas comment la société - ou le gouvernement britannique - avait déterminé que le deuxième cas n'était pas lié au vaccin.
Lui et d'autres experts ont noté que la myélite transverse est rare, diagnostiquée chez seulement environ un Américain sur 236.000 8.000 par an. Le procès en Grande-Bretagne n'a impliqué que XNUMX XNUMX volontaires environ.
Le vaccin développé par AstraZeneca, qui a formé un partenariat avec des scientifiques de l'Université d'Oxford, utilise un virus destiné à transporter des gènes de coronavirus dans les cellules humaines et à déclencher une réponse immunitaire qui protégera les personnes contre le coronavirus. Ce soi-disant vecteur est une forme modifiée d'adénovirus qui provoque le rhume chez les chimpanzés, mais il est considéré comme sûr pour les personnes. Plusieurs autres sociétés, dont Johnson & Johnson et CanSino, poursuivent des approches similaires basées sur les adénovirus, bien qu'il existe différents types d'adénovirus et que les ingrédients spécifiques diffèrent d'un vaccin à l'autre.
Alors que d'autres produits à base d'adénovirus ont connu un certain succès dans le passé, ils ont également été associés à des événements indésirables graves. Le plus célèbre a été le cas de Jesse Gelsinger, 1999 ans, décédé en XNUMX après avoir reçu une thérapie génique par un adénovirus qui a déclenché une réponse inflammatoire mortelle de son système immunitaire.
Si un effet secondaire grave était lié en permanence au vaccin d'AstraZeneca, les scientifiques devraient déterminer si sa cause de déclenchement provient du vecteur adénovirus ou peut-être des gènes de coronavirus qu'il porte, des connexions qui pourraient soulever des inquiétudes concernant les produits d'autres entreprises qui en dépendent. sur les mêmes composants.
source: https://www.nytimes.com/2020/09/19/health/astrazeneca-vaccine-safety-blueprints.html

