Pierwsza recenzowana publikacja na temat szczepionek MMRV (Priorix Tetra)

Wreszcie jesteśmy - po prawie dwóch latach - publikowana jest pierwsza recenzowana publikacja naszych analiz, a wiele innych zostanie opublikowanych.
Celem tego artykułu jest podsumowanie następujących kwestii: co zostało opublikowane, jaka jest jego ważność i dlaczego jest ważne dla naszego dochodzenia w sprawie szczepionek. Wszystkie te argumenty zostaną potraktowane w sposób potoczny i nietechniczny na pierwszych stronach, natomiast od strony 3 zostaną przeprowadzone badania techniczne, aby umożliwić specjalistom z tego sektora samodzielną ocenę artykułu.
Artykuł opublikowany na temat „F1000 Research”1 jest wynikiem wstępnego badania przeprowadzonego przez jedno z laboratoriów, które Stowarzyszenie Corvelva wyznaczyło do przeprowadzenia analiz. Przypominamy - ponieważ od początku tej pracy minęły ponad dwa lata, a do pierwszych dodano wiele innych wyników - pierwszym poważnym problemem, który musieliśmy zbadać, była nienormalna ilość ludzkiego DNA znaleziona w analizowanych szczepionkach.
Wstępne analizy wykazały, że obie analizowane czterowartościowe szczepionki MMRV zawierały od 1 do 2.7 mikrograma / fiolkę (jak opublikowano w niniejszym artykule) i postanowiliśmy publicznie i natychmiast przedstawić takie wyniki, ponieważ po prostu nie oczekiwano, że taka ilość DNA może być obecny w szczepionce.
Oprócz rozważań i wniosków wyciągniętych z badania, które są ściśle techniczne, a zatem zrozumiałe tylko dla tych, którzy pracują w dziedzinie badań metagenomicznych, na wykresach widać, że dwie próbki szczepionki zawierają wysoki odsetek odczytów ludzkiego DNA w dodatku do tych oczekiwanych z genomu wirusa ospy wietrznej (ludzki wirus alfa-herpes 3), jedyny wykrywalny spośród czterech, jako analiza typu DNA o sekwencji, została przedstawiona w artykule.
Chcielibyśmy jednak zaznaczyć, że ilości DNA, które zostały znalezione i potwierdzone przez ta sama metoda, która jest teraz zatwierdzona tutaj były jeszcze wyższe: do 3.7 mikrograma na fiolkę, co prowadzi do znacznej różnicy między partiami. W rzeczywistości w naszym raporcie wydanym 22 grudnia 2018 r2 wyniki uzyskane z analizy różnych partii niż te omówione w niniejszym artykule zostały zgłoszone, a następnie potwierdzone przez analizę międzylaboratoryjną, która jest wciąż w trakcie publikacji.
W związku z tym niniejszą publikację należy uznać za szczególnie interesującą, ponieważ weryfikuje ona zastosowaną metodę, stanowi ważny punkt dyskusji na temat „rodzaju” przeprowadzonej analizy, i w konsekwencji w ostateczny sposób potwierdza wszystkie badania, które zostały następnie przeprowadzone metodą NGS: dogłębna analiza rodzaju materiału genetycznego, obecność wirusów przypadkowych, wielki brak atenuowanych wirusów, które powinny być obecne oraz ilość ludzkiego DNA, która była całkowicie poza kontrolą (również dlatego, że bardzo różni się od próbki do próbki) , zmutowana populacja, fagi, DNA z innych gatunków i tak dalej. Można znaleźć aWyniki podsumowane na naszej stronie internetowej3.
Wszystko, co potępiliśmy w ostatnich latach, z biologicznego punktu widzenia, dokładnego raportowania wyników organom kontrolnym, nabiera bardziej istotnej konotacji naukowej (nawet jeśli, powtórzmy to jeszcze raz, nie były to wzajemne oceny martw się, ale przedstawione dane, bardzo poważne pod względem treści i ich możliwych konsekwencji dla zdrowia ludzi). Jednak teraz, gdy opublikowano tę metodę, będziemy żądać odpowiedzi, których jeszcze nie otrzymaliśmy.
Wyniki te bez wątpienia potwierdzają obecność DNA płodu w szczepionkach Priorix tetra, w różnych ilościach między partiami, co wskazuje na słabą kontrolę jakości tych produktów farmaceutycznych.
Przypominamy również raport na temat całego sekwencjonowania genomu MRC-5 opublikowany na stronie internetowej Corvelva 27 września 2019 r.4 pokazujące głęboką modyfikację tego DNA nawet w genach związanych z rozwojem chorób nowotworowych (te dane również wkrótce zostaną opublikowane). Zanieczyszczające DNA płodu występujące we wszystkich analizowanych próbkach w zmiennych (tj. Niekontrolowanych) ilościach jest do 300 razy wyższe niż limit nałożony przez EMA dla rakotwórczego DNA (10 ng / dawkę, co odpowiada DNA zawartemu w około 1000 komórek nowotworowych, na podstawie obliczeń statystycznych, podczas gdy ostrożny limit wynosi 100 pg / dawkę), limit, który należy koniecznie zastosować również do DNA płodu, który nieuchronnie zanieczyszcza szczepionkę Priorix Tetra.
W rezultacie szczepionkę tę należy uznać za wadliwą i potencjalnie niebezpieczną dla zdrowia ludzkiego, w szczególności dla populacji pediatrycznej, która jest znacznie bardziej podatna na uszkodzenia genetyczne i autoimmunologiczne z powodu niedojrzałości układów odpornościowych.
Zgodnie z przewidywaniami, następna część artykułu jest bardziej „techniczna” i trudna do zrozumienia dla osób niebędących ekspertami, dlatego postanowiliśmy, nawet ze względu na przejrzystość, dołączyć do tego dokumentu również „Dokumentacja EMA - Dokumentacja NGS Dyskusja na temat wyników badania jakości szczepionki”, Musieliśmy ekstrapolować tylko tę część, która mogła zostać opublikowana, tj. 50 stron dokumentacji w porównaniu do 200 stron NGS, ponieważ większość informacji zawartych i zarejestrowanych w organach regulacyjnych musi pozostać poufna. Surowe prawo nauki nakazuje, aby część informacji mogła zostać opublikowana w czasopiśmie tylko wtedy, gdy jest oryginalna, a ponieważ trwają inne prace, nie chcemy ryzykować.
Dokumentacja EMA - NGS Dyskusja na temat wyników badania jakości szczepionki ". - https://bit.ly/342XKi7
Wreszcie, aby uniknąć nieporozumień, chcielibyśmy podkreślić część „Deklaracji finansowej” z wyżej wymienionej publikacji:
„Sekwencjonowanie metagenomiczne B1 i B2 zostało sfinansowane przez Corvelva (stowarzyszenie non-profit, Veneto, Włochy) na podstawie umowy o świadczenie usług z laboratorium. Żadne inne wsparcie nie było zaangażowane we wspieranie prac. Fundatorzy nie odgrywali żadnej roli w projektowaniu badanie, gromadzenie i analiza danych, decyzja o publikacji lub przygotowanie manuskryptu ”
W załączeniu:
- Publikacja - Czy mnie kochasz? Wpływ zmniejszenia zasięgu na badania sekwencjonowania strzelby metagenomowej
- CORVELVA thread NGS-EMA-pol
- Pierwsza recenzowana publikacja na temat szczepionek MMRV (Priorix Tetra)
W artykule „Czy mnie kochasz? Wpływ zmniejszenia zasięgu na badania sekwencjonowania strzelby metagenomowej ”
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
Autorzy zajmują się techniczno-metodologicznym pytaniem, czy możliwe jest zastosowanie masowo równoległego podejścia metagenomicznego o niskim zasięgu odczytu do scharakteryzowania złożonych matryc biologicznych. Szacunki dotyczące różnorodności, liczebności gatunków i zdolności do rekonstrukcji metagenomu de novo pod względem długości i kompletności są obliczane, aby zrozumieć, jak bardzo spadek głębokości sekwencjonowania, zmieniany przez losowe odczyty sekwencjonowania podpróbkowania, może wpływać na ostateczne wyniki. Wyniki pokazują, że wskaźniki różnorodności złożonych społeczności prokariotycznych, eukariotycznych i wirusowych można dokładnie oszacować przy 500,000 1,000,000 odczytów lub mniej, chociaż szczególnie złożone próbki mogą wymagać 1,000,000 XNUMX XNUMX odczytów. Przeciwnie, projekt obejmujący rekonstrukcję metagenomu i genów zawiera wymaga ponad XNUMX XNUMX XNUMX odczytów.
Wśród różnych, bardzo różniących się od siebie, złożonych matryc poddanych masowej analizie metagenomicznej, uwzględniono dwa leki biologiczne, mianowicie dwie różne partie żywej atenuowanej szczepionki MPRV stosowanej do immunizacji przeciwko odrze, śwince, różyczce i ospie wietrznej u dzieci. DNA zostało wyodrębnione ze szczepionek, biblioteki genomowe zbudowano przy użyciu standardowych komercyjnych protokołów i przeprowadzono masowe sekwencjonowanie z wykorzystaniem technologii Illumina.
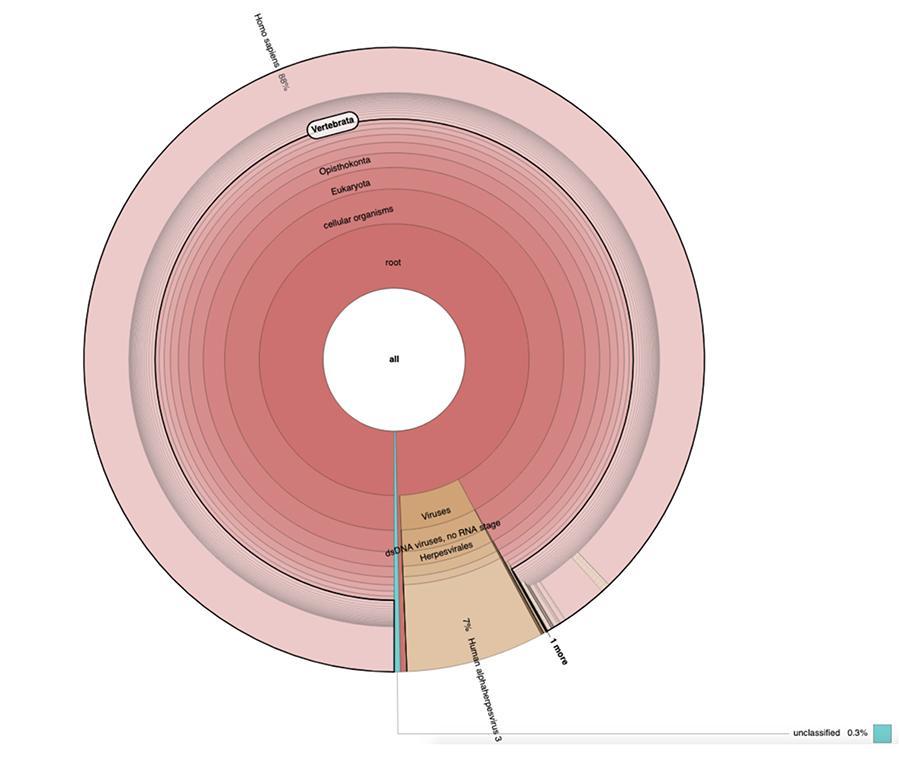
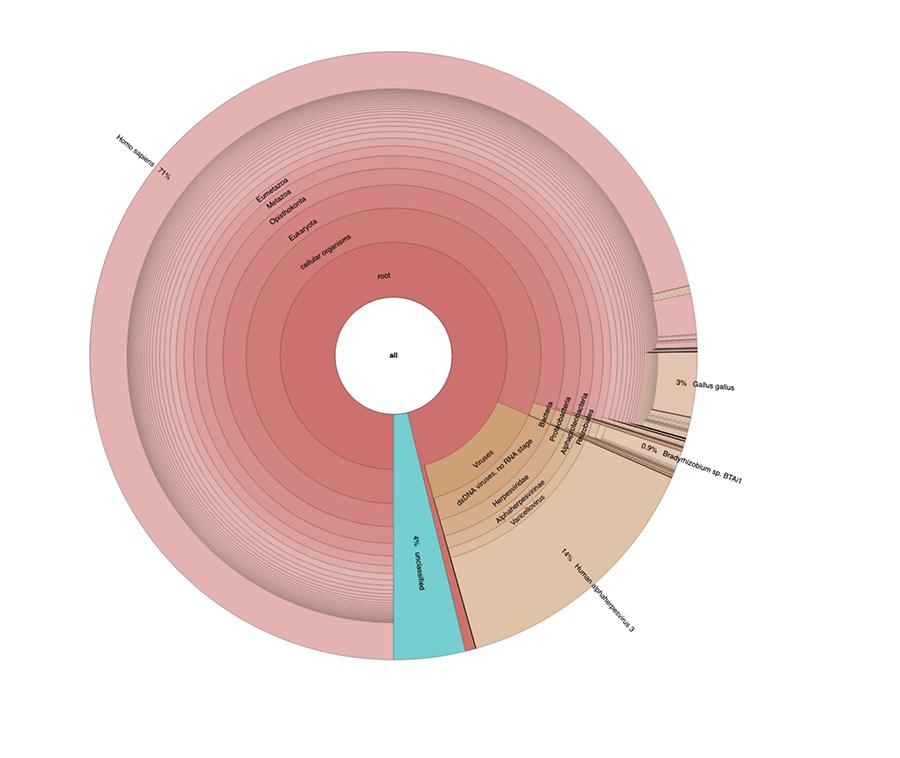
Oprócz rozważań i wniosków wyciągniętych z pracy, które są ściśle techniczne, a zatem zrozumiałe tylko dla tych, którzy prowadzą badania w dziedzinie metagenomiki, co zaobserwowano na wykresach kołowych zawartych w „danych rozszerzonych” (https://osf.io/wq395/ próbki B1 i B2) są takie, że stwierdzono, że dwie próbki szczepionki zawierają wysoki odsetek odczytów ludzkiego DNA oprócz tych oczekiwanych na podstawie genomu wirusa ospy wietrznej (człowiek alfaherpes wirus 3), jedyny wykrywalny wśród czterech, ponieważ w artykule przedstawiono analizę typu sekwencji DNA.
71% odczytów w jednej partii i 88% w drugiej jest pochodzenia ludzkiego, prawdopodobnie pochodzącego z linii komórkowej płodu MRC-5 (pamiętaj, że późniejsza analiza potwierdziła, że linia to MRC5), w której żyją atenuowane wirusy różyczki i ospy wietrznej uprawiane podczas przygotowywania szczepionki. Ponadto, jak to miało miejsce w różnych partiach tej samej szczepionki MPRV testowanej przez Corvelva w latach 2017-2019, ilość ekstrahowanego DNA jest rzędu mikrograma.
W partiach szczepionek testowanych przy użyciu tych samych protokołów i technologii opisanych w materiałach i metodach wyrobu wykryte ilości wahały się od 1 do prawie 3 mikrogramów na fiolkę, przy czym ilości różniły się między partiami, ale zawsze były znaczące.
W raporcie opublikowanym przez Corvelva w dniu 22.12.2018 5, następujące wyniki zostały zgłoszone dla kolejnych partii analizowanych po tych omówionych w artykule, później potwierdzonych przez analizę międzylaboratoryjną wciąż w trakcie publikacji.
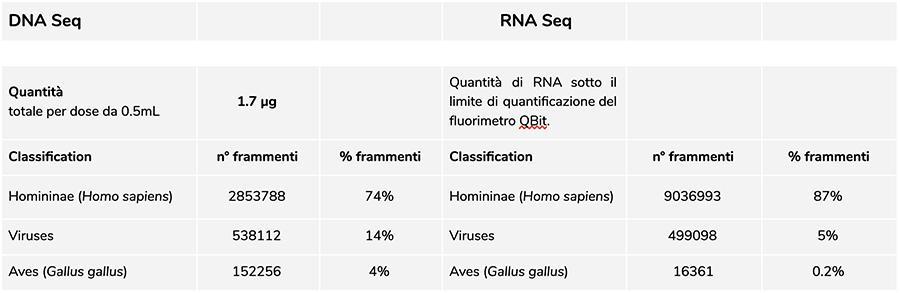
Priorix Tetra lot. A71CB205A (czerwiec 2018 r.) - Analiza DNA
Priorix Tetra lot. A71CB256A (grudzień 2018 r.) - Analiza DNA
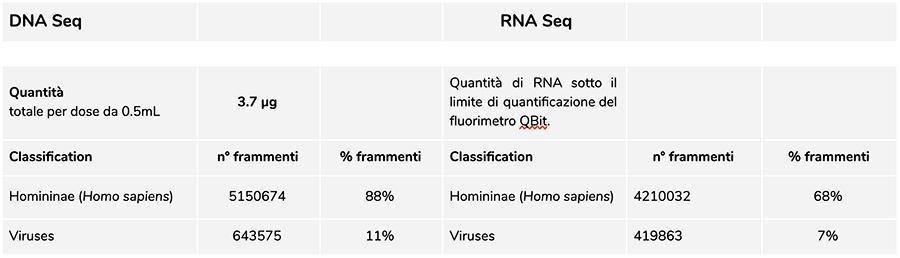
Analiza DNA
Pomiar stężenia DNA za pomocą fluorometru QuBit wykazał, że partia A71CB205A zawiera łącznie 1.7 µg gDNA na dawkę 0.5 ml, obliczoną w następujący sposób: 9.41 ng / µl (stężenie określone w QuBit) x 45 (końcowa objętość zawiesiny DNA po ekstrakcji wyrażona w mikrolitrach) x 4 (objętość początkowa poddana procedurze ekstrakcji wynosi ¼ objętości dawki zawartej w całej fiolce 0.5 ml).
Pomiar DNA stężenie fluorometrem QuBit wykazało, że A71CB256A dużo zawiera sumę gDNA 3.7 µg na dawkę 0.5 ml, obliczone w następujący sposób: 40.8 ng / µl (stężenie określone w QuBit) x 55 (końcowa objętość DNA w zawiesinie po ekstrakcji wyrażona w mikrolitrach) x 5/3 (objętość początkowa poddana procedurze ekstrakcji wynosi 300 µl na 500 µl zawiesiny ).
Ludzki DNA znaleziony w tej partii ma około 8 do 1 w stosunku do DNA ospy wietrznej (patrz następujące wyniki klasyfikacji fragmentów sekwencji DNA, które pokazują, że 88% wszystkich zsekwencjonowanych fragmentów DNA jest pochodzenia ludzkiego, a 11% to genomu wirusa ospy wietrznej).
Biorąc pod uwagę, że NGS jest technologią ilościową, fluorymetryczna kwantyfikacja całkowitego DNA ekstrahowanego ze szczepionki (np. Partia A71CB256A = 3.7 mikrograma na dawkę), w połączeniu z rozważeniem względnej kwantyfikacji dokonanej powyżej (8: 1), pozwala nam powiedzieć, że człowiek DNA może wynosić około 2.9 mikrograma na dawkę, w porównaniu do około 740 nanogramów DNA ospy wietrznej. Jest również prawdopodobne, że co najmniej jedna część DNA o wysokiej masie cząsteczkowej widoczna na żelu może być ludzkim DNA o wysokiej masie cząsteczkowej.
Analiza RNA
Ilość RNA zawarty w fiolce ze szczepionką partia A71CB256A okazała się w przybliżeniu 200ng.
RIN równy 8 oznacza an doskonała jakość RNA i nienaruszony eukariotyczny RNA, ponieważ obecne są zarówno piki 18S, jak i 28S typowe dla eukariotycznego RNA.
Odpowiedzi na nasze pytania przekazywane z czasem organom regulacyjnym są niezwykle ważne. Obecnie agencje nie odpowiedziały jeszcze na pytania dotyczące wyników pełnych analiz dostarczonych do EMA i AIFA.
Wyciąg z odpowiedzi udzielonej przez EMA na nasze pytanie dotyczące bezpieczeństwa pozostałości MRC-5 w szczepionce Priorix® tetra (numer referencyjny na żądanie EMA - 43967 3 sierpnia 2018 r.) - „Na podstawie opublikowanych informacji Priorix® Tetra zawiera szczepy wirusowe wytwarzane osobno w komórkach zarodka kurzego (świnka i odra) lub w ludzkich komórkach diploidalnych MRC-5 (różyczka i ospa wietrzna). Linie komórkowe stosowane w Priorix® Tetra obejmują ludzkie diploidalne linie komórkowe, które nie mogą w sposób ciągły dzielić. Należy pamiętać, że zgodnie z Farmakopeą Europejską: diploidalne linie komórkowe MRC-5 nie są rakotwórcze, co potwierdzają dziesięciolecia użytkowania i kontroli, a zatem nie ma zastosowania maksymalny limit DNA komórek MRC-5 ”
Na dzień dzisiejszy nie przedstawiono dowodów (ani w postaci certyfikatów analizy jakości produktu, ani referencyjnej literatury naukowej dla EMA) na te kontrole, które gwarantowałyby, że nie należy stosować maksymalnego limitu.
W wytycznych FDA „Wytyczne dla przemysłu: charakterystyka i kwalifikacja substratów komórkowych i innych materiałów biologicznych stosowanych w produkcji szczepionek wirusowych do wskazań chorób zakaźnych”6 stwierdzono, że:
- szczep komórek diploidalnych powinien zawsze pozostać diploidalny. Jeżeli te cechy nie są stabilne, konieczne jest wykazanie, że niestabilność nie wpływa negatywnie na produkcję lub zgodność produktu.
- w przypadku powszechnie stosowanych szczepów ludzkich komórek diploidalnych, takich jak komórki MRC-5 i WI-38, pomiar resztkowego DNA może nie być konieczny, ponieważ nie uważamy resztkowego DNA tych ludzkich diploidalnych komórek za zagrożenie dla bezpieczeństwa
- resztkowe DNA powinno być ograniczone dla nienowotworowych komórek ciągłych, takich jak komórki TRUE z małą liczbą pasaży, mniejszą niż 10 ng / dawkę do zaszczepienia pozajelitowego zgodnie z zaleceniami WHO
I wytyczna WHO „Załącznik 3 - Zalecenia dotyczące oceny kultur komórek zwierzęcych jako substratów do produkcji leków biologicznych i charakteryzacji banków komórek. Zastąpienie załącznika 1 do serii raportów technicznych WHO, n. 878 ”dodaje: (...) zgromadzono znaczne doświadczenie w zakresie cytogenetyki WI-38 i MRC-5 od lat 1960 Aby wesprzeć to doświadczenie, wymieniono następujące artykuły:
- Jacobs JP. Zaktualizowano wyniki kariologii szczepów komórkowych WI-38, MRC-5 i MRC-9. Developments in Biological Standization, 1976, 37: 155–156.
- Jacobs JP. i in. Wytyczne dotyczące dopuszczalności, zarządzania i testowania seryjnie namnażanych ludzkich komórek diploidalnych do produkcji żywych szczepionek wirusowych do stosowania u ludzi. Journal of Biological Standization, 1981, 9: 331–342.
- Petricciani JC i in. Standardy kariologiczne dla diploidalnej linii komórkowej rezus DBS-FRhL-2. Journal of Biological Standization, 1976, 4: 43–49.
- Schollmayer i in. Analiza wysokiej rozdzielczości i różnicowa kondensacja w ludzkich chromosomach z pasmem RBA. Human Genetics, 1981, 59: 187–193.
- Rønne M. Przygotowanie preparatów chromosomowych i techniki pasmowania w wysokiej rozdzielczości: przegląd. Journal of Dairy Science, 1989, 72: 1363–1377.
Można wyraźnie zaobserwować, że literatura referencyjna, która utrzymuje, że diploidalne komórki użyte do produkcji szczepionek są bezpieczne z punktu widzenia stabilności genetycznej, jest przestarzały, Już 40 lat temu znaleziono pierwsze anomalie genetyczne, uważane za nieistotne dla bezpieczeństwa szczepionek, i na podstawie tego, co podano w wytycznych WHO, od tego czasu nie wprowadzono żadnych aktualizacji nowych technologii sekwencjonowania, w szczególności w NGS, co jest ponadto ekonomiczny i szybki, w konsekwencji w podawanych szczepionkach od dziesięcioleci agencje dopuszczają obecność coraz bardziej genetycznie zmodyfikowanego DNA w niekontrolowanych ilościach. Na ten temat zob. Raport na temat sekwencjonowania całego genomu MRC-5 opublikowany na stronie internetowej Corvelva w dniu 27.09.2019, w którym głęboka modyfikacja tego DNA jest również widoczna w genach związanych z rozwojem patologii nowotworów. (dane są publikowane)
Poniżej znajduje się wyciąg z listu dr T. Deishera - światowego eksperta w dziedzinie wykorzystania komórek macierzystych do celów terapeutycznych i terapii genowej - który podkreśla obawy związane z ryzykiem związanym ze stosowaniem szczepionek zanieczyszczonych pozostałościami ludzkich komórek płodowych :
Dr T. DEISHER (list do gubernatorów - 8 kwietnia 2019 r.) - (...) wstrzyknięcie naszym dzieciom skażenia DNA płodu ludzkiego niesie ryzyko wywołania dwóch skonsolidowanych patologii:
- mutageneza insercyjna: ludzkie DNA płodu jest włączone do DNA dziecka powodującego mutacje. Terapia genowa z zastosowaniem homologicznej rekombinacji małych fragmentów wykazała, że ilości tak małe jak 1.9 ng / ml fragmentów DNA powodują wstawienie komórek macierzystych do genomu u 100% wstrzykniętych myszy. Poziomy fragmentów DNA ludzkiego płodu u naszych dzieci po szczepieniu szczepionkami MMR, VARIVAX (ospa wietrzna) lub wirusowym zapaleniem wątroby typu A osiągają poziomy powyżej 1.9 ng / ml.
- choroby autoimmunologiczne: ludzki DNA płodu stymuluje reakcję układu odpornościowego na atak ciała dziecka.
Nasze wyniki znacznie wzmacniają obserwacje eksperymentalne dr Deishera, przede wszystkim fakt, że zanieczyszczające płodowe DNA obecne we wszystkich próbkach analizowanych w różnych ilościach (a zatem niekontrolowane) jest do 300 razy wyższy niż limit nałożony przez EMA dla rakotwórczego DNA (10 ng / dawkę, odpowiadającą DNA zawartemu w około 1000 komórek rakowych, uzyskanym na podstawie obliczeń statystycznych, podczas gdy limit ostrożnościowy wynosi 100 pg / dawkę) limit, który koniecznie należy zastosować także do DNA płodu, który nieuchronnie zanieczyszcza Priorix® Tetra.
Dlatego szczepionkę należy uznać za wadliwą i potencjalnie niebezpieczną dla zdrowia ludzkiego, w szczególności w populacji pediatrycznej, która jest znacznie bardziej podatna na uszkodzenia genetyczne i autoimmunologiczne z powodu niedojrzałości w systemach naprawczych.
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.corvelva.it/speciale-corvelva/vaccinegate.html
https://www.corvelva.it/speciale-corvelva/vaccinegate-en.html - https://www.corvelva.it/speciale-corvelva/vaccinegate/sequenziamento-del-genoma-completo-di-mrc-5-contenuto-in-priorix-tetra.html
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.federalregister.gov/documents/2010/03/04/2010-4553/guidance-for-industry-characterization-and-qualification-of-cell-substrates-and-other-biological

