Итоговый технический отчет - Анализ молекулярного профиля вакцин

Предисловие
Прежде всего, мы хотели бы поблагодарить очень полезные комментарии, предоставленные теми, кто просматривал результаты анализов, проведенных в контексте научных исследований, касающихся продуктов Priorix tetra и Infanrix Hexa. Выявленные критические проблемы были на самом деле очень полезны для добавления научно-технических интеграций, способных прояснить проделанную работу. Мы считаем, что только благодаря здоровому общению научных взглядов можно сделать выводы о полученных данных, которые могут быть полезны для всего научного сообщества и людей, которые к нему обращаются.
1. Состояние техники
Предварительные исследования (скрининг, не подлежащий подтверждению) биомолекулярного, метаболического и протеомного профиля, выполненные на продуктах Priorix Tetra и Infanrix Hexa, позволили получить композиционную картину, обобщенную в следующих пунктах:
- Наличие различных аналитических сигналов, которые нельзя связать с известными соединениями при поиске в базах данных Metlin 1-2 и KEGG 3, Поэтому возникла картина, связанная со значительной сложностью в составе коммерческих продуктов.
- Присутствие необъявленных белков в листовке в продукте Priorix Tetra. Последнее потенциально может быть связано с остатками от производственного процесса
- Не обнаружены антигены, заявленные внутри продукта Infanrix Hexa. Техника анализа состояла из ферментативного расщепления трипсином, связанного с методами масс-спектрометрии. 4-5
Эти данные вызвали несколько комментариев, особенно в отношении пункта C - Обнаружение белков на самом деле осуществляется с использованием стандартного подхода, признанного на международном уровне в течение более 10 лет 4переваривание через фермент трипсина 4, Полученные таким образом пептиды разделяют хроматографически и анализируют с помощью масс-спектрометрии. 4-5, Основное наблюдение было присуще тому факту, что адъювантные соединения на основе алюминия присутствуют в вакцинах, которые потенциально могут ингибировать ферментативный процесс пищеварения.
Полученные впоследствии данные позволили дать существенные разъяснения, особенно в отношении спора, указанного в пункте с.
2. Новые идеи и анализы
2.1 Дополнительная информация об анализе продукта Infanrix Hexa
Прежде чем приступить к иллюстрации новых полученных данных о вакцинах Hexyon и Gardasil 9, необходимо ответить на вопрос, связанный с сомнением в отношении ингибирования протеолитической активности трипсина, вызванного присутствием адъювантов на основе алюминия. в вакцине Infanrix Hexa. В связи с этим необходимо указать, что в триптическом пищеварении всегда присутствует элемент управления пищеварением. Фактически, трипсин, используемый для осуществления пищеварения, хотя и сконструирован с целью предотвращения автолиза, имеет небольшой процент последнего, что в случае ферментативной активности приводит к получению фрагмента, имеющего m / z 842, и следующей пептидной последовательности : VATVSLPR. Этот фрагмент был фактически обнаружен внутри триптического расщепления продукта Infanrix Hexa, что подтверждается хроматограммой ионной экстракции (рис. 1).
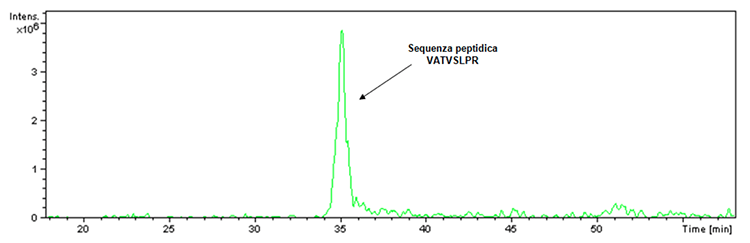
Фигура 1: Хроматограмма ионной экстракции, связанная с отношением ионов при m / z 842, обнаруженным в образце, относящемся к партии продукта Infanrix Hexa (номер партии A21CD072D).
Кроме того, выполняется внешняя проверка путем переваривания гемоглобина, чтобы дополнительно проверить качество использованной партии трипсина. Гемоглобин, анализируемый в разделе анализа, в котором отслеживался продукт, был признан со значительным статистическим баллом (loge <-100). Эти данные позволили подтвердить факт наличия активности фермента.
2.2 Новые анализы, связанные с продуктами Hexyon и Gardasil
Анализ продуктов Hexyon и Gardasil 9 привел к обнаружению сложных молекулярных профилей. В этом случае, однако, было обнаружено присутствие большинства антигенов, указанных в листовке. Они были обнаружены с помощью триптического расщепления и в присутствии адъювантов. Этот факт дополнительно подтверждает доказательства того, что реакция расщепления трипсином не ингибируется в присутствии адъювантов.
В случае вакцин Hexyon и Gardasil 9 сложность молекулярного профиля в основном объяснялась присутствием многочисленных видов с низким молекулярным весом, которые нельзя идентифицировать с помощью справочных баз данных Metlin. 1-2 и KEGG 3.
3. Выводы и заключительные соображения
Проведенные анализы позволили сделать следующий вывод:
- Молекулярный профиль анализируемых вакцин, как правило, сложен и в значительной степени неизвестен.
- Существуют белковые загрязнения, не указанные в листовке, состав которых варьируется.
- В нескольких случаях заявленные в листовке антигены не были обнаружены. Этот факт можно объяснить несколькими факторами. Среди последних можно рассмотреть чувствительность используемого метода. Однако мы считаем, что можем исключить явление торможения пищеварения из-за присутствия адъювантов в составе вакцины. Фактически, ферментативная активность подтверждается главным образом присутствием фрагментов триптического автолиза внутри растворов расщепленных вакцин (внутренний контроль).
4. Будущие исследования
Дальнейшие исследования будут проводиться в рамках исследований и разработок, направленных на изучение следующих аспектов:
- макромолекулярная композиция, связанная с твердыми остатками, присутствующими в вакцинах (анализ MALDI TOF MS); 5
- оценка концентрации металлов, присутствующих в продуктах.
- Второй уровень анализа для подтверждения наличия токсических соединений, обнаруженных на этапе скрининга. Поэтому их концентрация будет зависеть от их токсичности на основании того, что указано в международных паспортах безопасности. Анализы второго уровня будут проводиться в соответствии с европейской директивой ЕС 2002/657 / EC, полезной для гарантии высоких стандартов качества в секторе масс-спектрометрии. 6
в вере
д.сса лоретта болган
5. Библиографические ссылки
- Аутенхан Р, Чо К, Уритбоунтай В, Чжу З, Патти Дж, Сиуздак Г (сентябрь 2012). «Ускоренный рабочий процесс для нецелевой метаболомики с использованием базы данных METLIN». Природная биотехнология. 30: 826–828. DOI: 10.1038 / nbt.2348. PMC 3666346. PMID 22965049.
- Смит CA, I'Maille G, Want EJ, Цинь C, Trauger SA, Брэндон TR, Custodio DE, Абагьян R, Siuzdak G (декабрь 2005). "МЕТЛИН: база данных масс-спектра метаболитов" (PDF). Ther Drug Monit. 27 (6): 747–51. DOI: 10.1097 / 01.ftd.0000179845.53213.39. PMID 16404815.
- Канехиса М (2013). «Химическая и геномная эволюция ферментативно-катализируемых реакционных сетей». FEBS Lett. 587 (17): 2731–7.
- Кристони С, Бернарди Л.Р. «Биоинформатика в масс-спектрометрическом анализе данных для протеомных исследований». Эксперт Рев Протеомика. 2004 Dec; 1 (4): 469-83.
- Кристони С., Бернарди Л. Р.. «Разработка новых методик масс-спектрометрического исследования биоорганических макромолекул». Mass Spectrom Rev.2003 ноябрь-декабрь; 22 (6): 369-406.
- Кристони С, Дуси Дж, Брамбилла П, Альбини А, Конти М, Брамбилла М, Бруно А, Ди Гаудио Ф, Ферлин Л, Таццари В, Менгоцци С, Барера С, Сиалер С, Тренти Т, Канту М, Росси Бернарди Л, Нунан Д.М. «SANIST: оптимизация технологии идентификации соединений на основе директивы Европейского Союза с применением в криминалистической, фармацевтической и пищевой анализах». J. Mass Spectrom. 2017 январь; 52 (1): 16-21. doi: 10.1002 / jms.3895.
Скачать: CORVELVA-Report-техника-Finale.pdf

