Обязанности вакцин от Covid-19: 20 научных фактов, бросающих вызов гипотезам

ГИПОТЕЗА: Вакцины против COVID-19 значительно сокращают распространение COVID-19, поэтому высокие показатели всеобщей вакцинации предотвратят вспышки и положат конец пандемии. |
СДЕЛАНО #1: исследование вспышки COVID-19 в июле 2021 года, опубликованное в Eurosurveillance, показало, что «Все передачи между пациентами и персоналом происходили между лицами в масках и вакцинированными, как это произошло во время вспышки в Финляндии».. Авторы утверждают, что исследование «оспаривает гипотезу о том, что высокие универсальные показатели вакцинации приводят к коллективному иммунитету и предотвращают вспышки COVID-19»..1
СДЕЛАНО #2: Исследование Центров по контролю и профилактике заболеваний, посвященное другой вспышке COVID-19 в июле 2021 года, показало, что 74 процента заболевших были полностью вакцинированы.2
СДЕЛАНО #3: Гарвардское исследование, в ходе которого были проанализированы случаи заболевания COVID-19 в 68 странах и 2.947 округах США, не выявило "отсутствие существенных признаков снижения числа случаев COVID-19 при наличии более высокого процента полностью вакцинированного населения».3
ГИПОТЕЗА: Вакцины против COVID-19 предотвращают смерть от COVID-19 |
СДЕЛАНО #4: В клинических испытаниях приняли участие десятки тысяч субъектов, и это единственные испытания, включающие контрольную группу и в которых все субъекты находились под наблюдением и тестировались на COVID-19 независимо от статуса вакцинации. Однако в этих исследованиях не было обнаружено достаточного количества смертей от COVID-19, чтобы измерить значительную разницу в смертности между вакцинированными и невакцинированными пациентами.4-7 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) заявляет, что: «Для подтверждения эффективности вакцины против смертности потребуется больше людей с высоким риском заражения COVID-19 и более высокими показателями заболеваемости»..4-7
СДЕЛАНО #5: Исследование вспышки COVID-19 в июле 2021 года, опубликованное в Eurosurveillance, показало, что 100% серьезных, критических и смертельных случаев COVID-19 произошли у вакцинированных лиц.1
СДЕЛАНО #6: Данные CDC показывают, что массовая вакцинация вакциной против COVID-19 не оказала заметного влияния на уровень смертности от COVID-19 в США. За девять месяцев, предшествовавших введению массовой вакцинации (с апреля 2020 г. по декабрь 2020 г.), от COVID-356.000 умерло около 19 39.500 человек, или 0,120 1.000 смертей в месяц — коэффициент смертности 2021 на 2021 человек. За девять месяцев после введения массовой вакцинации (с января 342.000 г. по сентябрь 19 г.) от COVID-38.000 умерло 0,115 1.000 человек или 2021 2022 смертей в месяц — коэффициент смертности 249.000 на 19 человек. В последующие пять месяцев (с октября 49.800 г. по февраль 0,151 г.) было зарегистрировано еще 1.000 XNUMX смертей от COVID-XNUMX, или XNUMX XNUMX смертей в месяц, при коэффициенте смертности XNUMX на XNUMX человек.7
ГИПОТЕЗА: Для детей инъекция вакцины против COVID-19 безопаснее, чем заражение SARS-CoV-2. |
СДЕЛАНО #7: В клиническом исследовании Pfizer не было случаев тяжелого течения COVID-19 у детей, не получавших вакцину.8-9 Напротив, у детей в возрасте 5 лет и старше клиническое исследование вакцины против COVID-19, проведенное компанией Pfizer, показало, что вакцина вызывает тяжелые (3-я степень) системные реакции, которые включают лихорадку выше 39°C, рвоту, требующую гидратации для внутривенного введения, 24- часовая диарея и сильная усталость, сильная головная боль, сильная боль в мышцах или сильная боль в суставах, которые мешают повседневной деятельности.9-12
СДЕЛАНО #8: В клиническом исследовании от 1 из 59 до 1 из 143 вакцинированных детей в возрасте от 5 до 11 лет наблюдались тяжелые системные реакции в течение семи дней после введения второй дозы. В вакцинированной группе на каждые 3 несерьезных случаев COVID-8 в непривитой группе приходилось от 10 до 19 случаев серьезных системных реакций.9
СДЕЛАНО #9: В клиническом исследовании у 1 из 9 вакцинированных подростков в возрасте от 12 до 15 лет в течение семи дней после получения второй дозы наблюдались тяжелые системные реакции. Тяжелые системные реакции, наблюдаемые в вакцинированной группе, были в 7 раз выше, чем несерьезные случаи COVID-19 в непривитой группе.10-12
СДЕЛАНО #10: Клиническое исследование также показало, что у 1 из примерно 1.100 вакцинированных детей в возрасте от 12 до 15 лет после введения первой дозы наблюдалась системная реакция 4 степени (лихорадка выше 39 °C), которая потребовала посещения отделения неотложной помощи и выхода из исследования.10-13
ГИПОТЕЗА: Клинические испытания вакцины против COVID-19 были достаточно масштабными, чтобы продемонстрировать ее безопасность для детей.
|
ФАКТ №11: Клиническое исследование Pfizer не имело достаточной статистической мощности, чтобы продемонстрировать, что вакцина безопасна для детей в возрасте до 18 лет, поскольку в исследование не было включено достаточное количество субъектов для установления безопасности (т. возраст 2.600 и 5 лет).9-14 Для сравнения, известно, что случаи смерти детей от COVID-19 редки. По состоянию на 3 ноября 2021 года вероятность того, что 17-летний или моложе заразится SARS-CoV-2 и умрет от COVID-19, составляла 1 к 126.000 0,0008 или XNUMX%.15
Клинические испытания вакцины против COVID-19 недостаточны для демонстрации безопасности у детей.
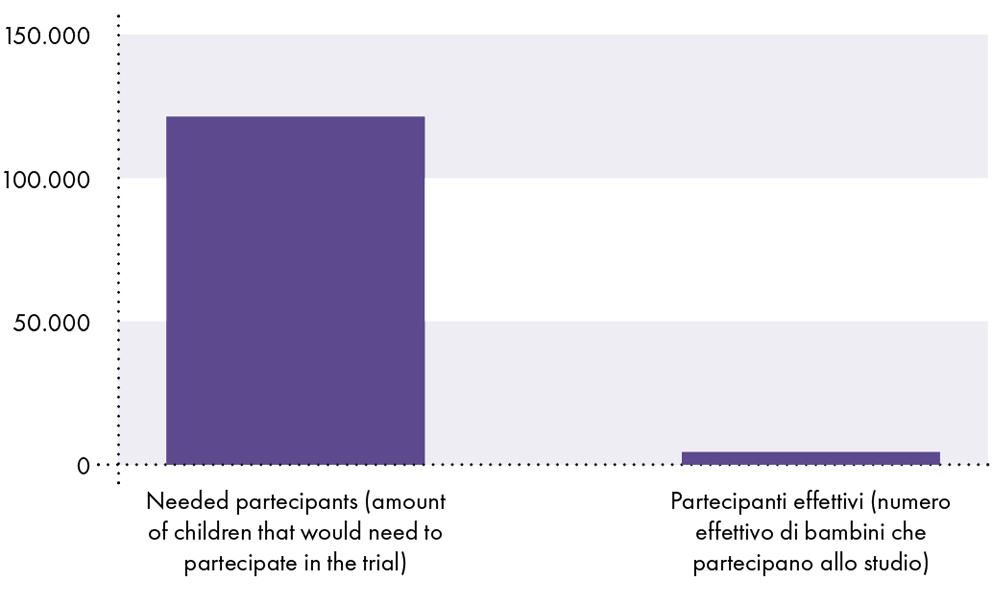
Поскольку вероятность того, что ребенок заразится SARS-CoV-2 и умрет от COVID-19, составляет 0,0008% или 1 из 126.000 126.000, для выявления смерти от COVID-19 необходимо как минимум 126.000 19 детей. Поэтому в клиническом испытании должно быть задействовано не менее 2.600 XNUMX вакцинированных участников, чтобы сравнить риск смерти от COVID-XNUMX с риском смерти от вакцин. Однако в клиническом исследовании приняли участие лишь около XNUMX вакцинированных детей.
ГИПОТЕЗА: Известно, что вакцины против COVID-19 не имеют долгосрочных побочных эффектов.
|
ФАКТ № 12: Поскольку все участники клинических испытаний наблюдались только в течение двух-шести месяцев, долгосрочная безопасность вакцин против COVID-19 для любой возрастной группы неизвестна. По данным FDA, в настоящее время недостаточно данных, чтобы делать выводы о безопасности вакцин Pfizer, Moderna и Johnson & Johnson для таких групп населения, как беременные и кормящие люди, а также лица с ослабленным иммунитетом.4-8-16 Для Pfizer вакцина «не оценивалась способность вызывать канцерогенность, генотоксичность или нарушение мужской фертильности»..17
ФАКТ №13: В отчетах о надзоре за безопасностью указаны серьезные риски миокардита и перикардита у лиц в возрасте до 40 лет в течение семи дней после вакцинации. У мальчиков в возрасте 16 или 17 лет FDA сообщило о повышенном риске миокардита или перикардита 1 на 5.000 после второй дозы вакцины Pfizer COVID-19.18 И у мальчиков в возрасте от 12 до 17 лет, снова после второй дозы. дозу вакцины Pfizer против COVID-19, исследование в Гонконге выявило повышенный риск миокардита или перикардита 1 на 2.700.19
ГИПОТЕЗА: Бустеры решат проблему падения вакцинного иммунитета.
|
ФАКТ № 14: Клинические исследования показали, что иммунитет к вакцине значительно снижается за короткий период времени. Например, эффективность вакцины Pfizer снизилась с 8% до 18% всего за шесть месяцев, а эффективность вакцины Johnson & Johnson снизилась с 25% до 29% всего за шесть месяцев.20-21 Кроме того, эффективность, измеренная в клинических испытаниях, была направлена против исходного штамма Ухань, а не против новых вариантов.
ФАКТ №15: В ходе клинических испытаний третья доза вакцины Pfizer или Moderna или вторая доза вакцины Johnson & Johnson не оценивалась на предмет эффективности против болезни, а скорее наблюдалось количество антител у небольшого числа вакцинированных субъектов всего в течение одного месяца.18-21-22
ГИПОТЕЗА: Не существует известных эффективных способов лечения или профилактики COVID-19, за исключением вакцин.
|
ФАКТ №16Лечение COVID-19 значительно улучшилось с начала пандемии в начале 2020 года, что привело к повышению показателей выживаемости среди госпитализированных пациентов.23-24 Фактически, для людей, которые не живут в доме престарелых, общая выживаемость при COVID-19 составляет 99,8% в США и 99,999% для детей в частности.25-26
ФАКТ №17: Сотни исследований изучали эффективность различных методов лечения, наиболее изученными из которых являются ивермектин, витамин D, гидроксихлорохин (HCQ) и моноклональные антитела.27-30 Эти методы лечения также могут быть полезны для профилактики (т. е. доконтактной или постконтактной профилактики симптоматических инфекций COVID-19).31-35
ГИПОТЕЗА: Людям, которые ранее были инфицированы SARS-CoV-2, необходимо пройти вакцинацию, поскольку естественный иммунитет недостаточен. |
ФАКТ №18Показано, что предыдущая инфекция SARS-CoV-2 более эффективна для предотвращения инфекции SARS-CoV-2, чем вакцины против COVID-19. Клинические испытания вакцины против COVID-19, проводимые Johnson & Johnson, включали более 2.000 человек, заразившихся SARS-CoV-2 до начала исследования. В исследовании, в котором последовательно тестировались непривитые и привитые люди, была зарегистрирована заболеваемость COVID-19 в непривитой группе по крайней мере через 28 дней после вакцинации других субъектов исследования. Заболеваемость COVID-19 в невакцинированной группе с предшествующей инфекцией SARS-CoV-2 составила 0,1% (2/2.021), в то время как заболеваемость COVID-19 у привитых составила 0,59% (113/19.306). Эти данные свидетельствуют о том, что случаи заболевания COVID-19 у вакцинированных лиц в 6 раз выше, чем у невакцинированных субъектов, ранее инфицированных SARS-CoV-2.36
ФАКТ №19Данные клинического исследования Johnson & Johnson также показывают, что невакцинированный человек, ранее инфицированный SARS-CoV-2, имеет 99,9% шансов на защиту от новой инфекции. Следует отметить, что по состоянию на 1 июля 2021 года в США зарегистрировано 177,4 млн случаев заражения SARS-CoV-2, что составляет 53,8% населения США.26-36
ГИПОТЕЗА: Было показано, что обязательные вакцины создают более безопасную среду. |
ФАКТ №20: Заражение и передача SARS-CoV-2 происходят с высокой частотой среди полностью вакцинированных групп населения, и значительный процент тяжелых, критических и смертельных случаев COVID-19 приходится на полностью вакцинированных лиц. Данные CDC показывают, что массовая вакцинация вакцинами против COVID-19 не оказала заметного влияния на смертность от COVID-19 в Соединенных Штатах. Кроме того, данные краткосрочных клинических испытаний показывают, что от 1 из 6 до 1 из 9 человек в возрасте от 12 до 55 лет, получающих вакцину против COVID-19 на основе мРНК, страдают тяжелыми системными реакциями (степень 3) и отсутствием долгосрочной безопасности. были проведены исследования.13-37 Таким образом, научные данные показывают, что принудительная вакцинация не может создать более безопасную среду.
Ссылки
- Шитрит П., Цукерман Н.С., Мор О., Готтесман Б.С., Чауэрс М. Внутрибольничная вспышка, вызванная дельта-вариантом SARS-CoV-2 среди высоковакцинированного населения, Израиль, июль 2021 г. Euro Surveill. 2021 Сен, 26 (39). https://pubmed.ncbi.nlm.nih.gov/34596015/.
- Браун К.М., Восток Дж., Джонсон Х., Бернс М., Гарпюр Р., Сами С., Сабо Р.Т., Холл Н., Форман А., Шуберт П.Л., Галлахер Г.Р., Финк Т., Мэдофф Л.С., Габриэль С.Б., Макиннис Б., Парк Диджей, Сиддл К.Дж. , Харик В., Арвидсон Д., Брок-Фишер Т., Данн М., Кернс А., Лэйни А.С. Вспышка инфекций SARS-CoV-2, в том числе инфекций, вызываемых вакциной против COVID-19, связанных с массовыми публичными собраниями — округ Барнстейбл, штат Массачусетс, июль 2021 г. MMWR Morb Mortal Wkly Rep. 2021 Aug 6; 70 (31): 1059-62. https://www.cdc.gov/mmwr/volumes/70/wr/mm7031e2.htm?s_cid=mm7031e2_w.
- Субраманиан С.В., Кумар А. Рост заболеваемости COVID-19 не связан с уровнем вакцинации в 68 странах и 2947 округах США. Евр J Эпидемиол. 2021, 30 сентября: 1–4. https://pubmed.ncbi.nlm.nih.gov/34591202/.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: Современная вакцина против COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 17 декабря 2020 г. https://www.fda.gov/media/144434/download.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: вакцина Janssen Ad26.COV2.S для профилактики COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 26 февраля 2021 г. Таблица 22. Эффективность вакцины при первом появлении среднетяжелого/тяжелого/критического и тяжелого/критического COVID-19, включая нецентрально подтвержденные случаи с началом не менее 14 или не менее 28 лет дней после вакцинации, по странам-участницам, по протоколу, исследование 3001; 37. https://www.fda.gov/media/146217/download.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: вакцина Pfizer-BioNTech против COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 10 декабря 2020 г. https://www.fda.gov/media/144245/download.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Трекер данных COVID: тенденции количества случаев COVID-19 и смертей в США, о которых сообщается в CDC, по штатам/территориям; [цитировано 2022 апреля 2 г.]. https://covid.cdc.gov/covid-data-tracker/#trends_totaldeaths.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Центр оценки и исследований биологических препаратов (CBER), Управление исследований и анализа вакцин (OVRR). Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Поправка к разрешению на использование в чрезвычайных ситуациях (EUA) для неутвержденного продукта: обзорный меморандум; 2021 9 апр: 23, 39. https://www.fda.gov/media/148542/download.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: запрос на внесение поправок в EUA в отношении вакцины Pfizer-BioNTech против COVID-19 для детей в возрасте от 5 до 11 лет. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 26 октября 2021 г. https://www.fda.gov/media/153447/download.
- Уоллес М. Классификация рекомендаций, оценка, разработка и оценка (GRADE): вакцина Pfizer-BioNTech против COVID-19. Рабочая группа по вакцинам против COVID-19 Консультативного комитета по практике иммунизации (ACIP). Центры по контролю и профилактике заболеваний. 2021 12 мая: 24, 25. https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-05-12/03-COVID-Wallace-508.pdf.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Классификация рекомендаций, оценка, разработка и оценка (GRADE): вакцина Pfizer-BioNTech COVID-19 для лиц в возрасте 12–15 лет; [цитировано 2021 мая 14 г.]. https://www.cdc.gov/vaccines/acip/recs/grade/covid-19-pfizer-biontech-vaccine-12-15-years.html#table03d.
- Пфайзер. Нью-Йорк (Нью-Йорк): Информационный бюллетень Pfizer Inc. для поставщиков медицинских услуг, проводящих вакцинацию (поставщики вакцин); пересмотрено 2022 января 3 г. Таблица 11: эффективность вакцины — первое появление COVID-19 через 7 дней после дозы 2: без признаков инфекции и с признаками инфекции или без них до 7 дней после дозы 2 — слепой плацебо-контролируемый период наблюдения , подростки от 12 до 15 лет оцениваемой эффективности (7 дней) населения; 48. https://www.fda.gov/media/153713/download.
- Врачи за информированное согласие. Вакцина Pfizer против COVID-19: краткосрочные данные об эффективности и безопасности. декабрь 2021 г. https://www.physiciansforinformedconsent.org/COVID-19-vaccines.
- Пфайзер. Нью-Йорк (Нью-Йорк): Информационный бюллетень Pfizer Inc. для поставщиков медицинских услуг, проводящих вакцинацию (поставщики вакцин); исправлено 2022 3 января: 48. https://www.fda.gov/media/153713/download.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Еженедельные обновления по отдельным демографическим и географическим характеристикам: предварительные данные о смертности от коронавирусной болезни (COVID-19); [цитировано 2021 ноября 3 г.]. https://www.cdc.gov/nchs/nvss/vsrr/covid_weekly/index.htm#AgeAndSex.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: вакцина Janssen Ad26.COV2.S для профилактики COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 26 февраля 2021 г. https://www.fda.gov/media/146217/download.
- Пфайзер. Нью-Йорк (Нью-Йорк): Pfizer Inc. Comirnaty (вакцина против COVID-19, мРНК), суспензия для инъекций, для внутримышечного введения; пересмотрено 2021 дек. https://www.fda.gov/media/151707/download.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Справочный документ FDA: Заявка на лицензирование бустерной дозы для Comirnaty (вакцина против COVID-19, мРНК). Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 17 сентября 2021 г. https://www.fda.gov/media/152176/download.
- Chua GT, Kwan MYW, Chui CSL, Smith RD, Cheung EC, Tian T, Leung MTY, Tsao SSL, Kan E, Ng WKC, Man Chan VC, Tai SM, Yu TC, Lee KP, Wong JSC, Lin YK, Shek CC, Leung ASY, Chow CK, Li KW, Ma J, Fung WY, Lee D, Ng MY, Wong WHS, Tsang HW, Kwok J, Leung D, Chung KL, Chow CB, Chan GCF, Leung WH, To KKW, Yuen KY, Lau YL, Wong ICK, Ip P. Эпидемиология острого миокардита/перикардита у подростков Гонконга после вакцинации Comirnaty. Клин Инфекция Дис. 2021, 28 ноября: ciab989. https://pubmed.ncbi.nlm.nih.gov/34849657.
- Томас С.Дж., Морейра Э.Д.-младший, Китчин Н., Абсалон Дж., Гуртман А., Локхарт С., Перес Дж.Л., Перес Марк Г., Полак Ф.П., Зербини С., Бейли Р., Суонсон К.А., Сюй Х., Ройчоудхури С., Кури К., Бугермух С., Kalina WV, Cooper D, Frenck RW Jr, Hammitt LL, Türeci Ö, Nell H, Schaefer A, Ünal S, Yang Q, Liberator P, Tresnan DB, Mather S, Dormitzer PR, Şahin U, Gruber WC, Jansen KU; C4591001 Группа клинических испытаний. Безопасность и эффективность мРНК-вакцины BNT162b2 covid-19 в течение 6 месяцев. N Engl J Med., 2021 ноября 4 г., 385 (19): 1761-73. https://pubmed.ncbi.nlm.nih.gov/34525277.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: запрос на внесение поправок в EUA для бустерной дозы вакцины Janssen против COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 15 октября 2021 г. 21, 39. https://www.fda.gov/media/153037/download.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: запрос на внесение поправок в EUA для бустерной дозы вакцины Moderna COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 14 октября 2021 г. https://www.fda.gov/media/152991/download.
- Хорвиц Л.И., Джонс С.А., Серфолио Р.Дж., Франсуа Ф., Греко Дж., Руди Б., Петрилли К.М. Тенденции в показателях смертности от COVID-19 с поправкой на риск. J Hosp Med., 2021, февраль, 16 (2): 90-2. https://www.journalofhospitalmedicine.com/jhospmed/article/230561/hospital-medicine/trends-covid-19-risk-adjusted-mortality-rates.
- Деннис Дж.М., Макговерн А.П., Фоллмер С.Дж., Матин Б.А. Повышение выживаемости пациентов интенсивной терапии с коронавирусной болезнью 2019 г. в Англии: национальное когортное исследование, март-июнь 2020 г. Crit Care Med., 2021, 1 февраля, 49 (2): 209-14. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7803441/.
- Иоаннидис, JPA. Согласование оценок глобального распространения и смертности от COVID-19: обзор систематических оценок. Евро Джей Клин Инвест. 2021; 51: e13554. https://onlinelibrary.wiley.com/doi/epdf/10.1111/eci.13554.
- Врачи за информированное согласие. COVID-19 - Информационное заявление о заболевании (DIS). август 2021 г. https://physiciansforinformedconsent.org/covid-19/.
- C19early.com. Раннее лечение COVID-19: анализ 1,298 исследований в режиме реального времени; [цитировано 2022 января 11 г.]. https://c19early.com/.
- Регенерон. Тэрритаун, (Нью-Йорк): Regeneron Pharmaceuticals, Inc. Информационный бюллетень для поставщиков медицинских услуг: разрешение на использование в экстренных случаях (EUA) REGEN-COV (казиривимаб и имдевимаб); пересмотрено 2021 дек. https://www.regeneron.com/downloads/treatment-covid19-eua-fact-sheet-for-hcp.pdf.
- Лилли. Индианаполис (Индиана): Эли Лилли и компания. Нейтрализующие антитела к COVID-19; [цитировано 2022 февраля 9 г.]. https://www.lilly.com/news/media/media-kits/bamlanivimab-covid19.
- ГСК. Лондон (Великобритания): GlaxoSmithKline plc. GSK и Vir Biotechnology объявляют о соглашении с правительством США о закупке дополнительных запасов сотровимаба, разрешенного для раннего лечения COVID-19; 2022 января 11 г. [цитировано 2022 февраля 9 г.]. https://www.gsk.com/en-gb/media/press-releases/gsk-and-vir-biotechnology-announce-united-states-government-agreement-to-purchase-additional-supply-of-sotrovimab.
- C19early.com. Исследования COVID-19: ивермектин; [цитировано 2022 февраля 12 г.]. https://c19ivermectin.com.
- Брайант А., Лори Т.А., Доусуэлл Т., Фордхэм Э.Дж., Митчелл С., Хилл С.Р., Тэм Т.С. Ивермектин для профилактики и лечения инфекции COVID-19: систематический обзор, метаанализ и последовательный анализ испытаний для информирования клинических руководств. Am J Ther. 2021 июня 21 г., 28 (4): e434-60. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8248252/.
- C19early.com. Исследования COVID-19: витамин D; [цитировано 2022 февраля 12 г.]. https://c19vitamind.com.
- Илие П.С., Стефанеску С., Смит Л. Роль витамина D в профилактике коронавирусной инфекции 2019 года и смертности. Aging Clin Exp Res., июль 2020 г., 32 (7): 1195-8. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7202265/.
- C19early.com. HCQ для COVID-19: метаанализ 303 исследований в реальном времени; [цитировано 2022 января 10 г.]. https://hcqmeta.com.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Консультативный комитет по вакцинам и сопутствующим биологическим продуктам. Информационный документ FDA: вакцина Janssen Ad26.COV2.S для профилактики COVID-19. Заседание Консультативного комитета по вакцинам и родственным биологическим продуктам: 26 февраля 2021 г. вакцинация по исходному статусу SARS-CoV-14 в соответствии с набором протоколов; 19. https://www.fda.gov/media/146217/download.
- Эль Сахли Х.М., Баден Л.Р., Эссинк Б., Доблеки-Льюис С., Мартин Дж.М., Андерсон Э.Дж., Кэмпбелл Т.Б., Кларк Дж., Джексон Л.А., Фихтенбаум С.Дж., Зервос М., Рэнкин Б., Эдер Ф., Фельдман Г., Кеннелли С., Хан- Конрад Л., Левин М., Нойзил К.М., Кори Л., Гилберт П., Джейнс Х., Фоллманн Д., Марович М., Полаковски Л., Маскола Дж.Р., Леджервуд Дж.Е., Грэм Б.С., Август А., Clouting H, Дэн В., Хан С., Лиав Б. , Манзо Д., Пайон Р., Шёдель Ф., Томассини Дж. Э., Чжоу Х., Миллер Дж.; Исследовательская группа COVE. Эффективность вакцины мРНК-1273 SARS-CoV-2 по завершении слепой фазы. N Engl J Med., 2021 ноября 4 г., 385 (19): 1774-85. Приложение; 36-7. https://www.nejm.org/doi/suppl/10.1056/NEJMoa2113017/suppl_file/nejmoa2113017_appendix.pdf.
Статью перевел Врачи за осознанное согласие

