Может ли вакцина против столбняка вызвать травму и/или смерть?

В следующей статье делается попытка пролить свет на огромный мир побочных реакций, с особым вниманием к реакции против столбняка, но мы настоятельно рекомендуем вам прочитать все основные моменты, указанные ниже, чтобы понять другие связанные с этим вопросы, такие как проблема множественных вакцин. , гиперчувствительность к одному или нескольким компонентам вакцины, проблема СВДС и проблема адъювантов. Большинство вакцин на рынке производятся для коммерческих целей, часто в нескольких составах, и это делает тему вреда от вакцин намного шире.
Проблема множественных вакцин (нажмите, чтобы открыть)
Проблема множественных вакцин

Текущие календари прививок, особенно для детского возраста, предусматривают введение нескольких антигенов и вакцин за один сеанс, что способствует комфорту в ущерб безопасности. Для того, чтобы иметь возможность произнести конкретную речь о безопасности вакцин, мы обязательно должны учитывать сложность явления, советуя всем читателям адекватно осведомляться обо всех аспектах вакцинации, плюсах и минусах.
Доктор Рассел Блейлок, клинический доцент нейрохирургии в Медицинском центре Университета Миссисипи, много лет изучал «токсическую синергию» и смог наблюдать, что когда два слаботоксичных пестицида, ни один из которых не способен вызвать синдром Паркинсона у экспериментальных животных, сочетаются друг с другом, могут вызвать заболевание даже быстро, и сравнивает это явление с явлением, когда несколько вакцин вводятся одновременно: «Прививки, если их слишком много и слишком близко друг к другу, ведут себя как хроническое заболевание».(A). Другие Два исследования подтвердили, что внезапная младенческая смерть может наступить после однократного введения нескольких вакцин.(до н.э)
Исследование, опубликованное в журнале Human and Experimental Toxicology, показало, что страны, которые назначают больше вакцин детям, как правило, имеют более высокий уровень младенческой смертности.(D) Например, в США, где дети получают 26 вакцин, умирает более 6 детей на 1000 живорождений, а в Швеции и Японии, где вводится 12 педиатрических вакцин, на каждую 3 живорождений приходится 1000 смерти. В вышеупомянутом исследовании также рассматривается связь между вакцинами и СВДС.
Из швейцарского исследования, опубликованного в 2005 году в Европейском журнале педиатрии.(Е) получается, что, что касается воздействия на недоношенных детей, частота повторного или усиленного апноэ и брадикардии после введения шестивалентных вакцин составляет 13%. В том же году в том же журнале было опубликовано немецкое исследование, в котором изучалась внезапная смерть младенцев после шестивалентного отравления. Авторы пишут: «Эти результаты, основанные на спонтанных сообщениях, не доказывают причинно-следственной связи между вакцинацией и внезапной младенческой смертью, но представляют собой сигнал относительно одного из двух имеющихся шестивалентников; сигнал, который должен привести к усилению эпиднадзора за внезапными младенческими смертями после вакцинации».(F)
В 2006 году она была опубликована в медицинском журнале Vaccine.(Г) письмо от группы исследователей из Мюнхенского университета, в котором сообщается о «шести случаях внезапной детской смерти после шестивалентной вакцинации. Все найдены мертвыми без объяснения причин через 1-2 дня после вакцинации». Они были классифицированы как типичные случаи внезапной детской смерти, но аутооптическая верификация выявила нейропатологические и гистологические отклонения, и у всех детей наблюдался значительный отек головного мозга, что делало их исключением по сравнению с другими случаями СВДС.синдром внезапной детской смерти). Исследователи писали, что «До введения шестивалентной вакцины (в 1994-2000 годах) мы наблюдали случай внезапной младенческой смерти только у одного из 198 детей, который умер вскоре после прививки АКДС. Но в период с 2001 по 2004 год они выявили пять подобных случаев из 74 случаев СВДС. Это будет означать тринадцатикратное увеличение».
Также в 2006 г. в архиве Вирхова.(H), группа из Института патологии Миланского университета написала: «Эксперты Европейского агентства по оценке медицинских продуктов проанализировали возможность того, что между шестивалентными вакцинами и некоторыми случаями смерти может быть связь. В число участников входили патологоанатомы с опытом работы с вакцинами и синдромом внезапной детской смерти, проводившие вскрытия, но, насколько нам известно, исследованию ствола мозга и кровяного сердца на серийных срезах уделялось мало внимания и не было возможности установить триггерную роль вакцины от этих смертей. Здесь мы сообщаем о случае внезапной смерти 3-месячной девочки после шестивалентной вакцинации. При исследовании ствола головного мозга на серийных срезах выявлена двусторонняя гипоплазия аркуатных ядер. Проводящая система сердца имела стойкую фетальную дисперсию и дистрофию. Этот случай предлагает уникальное понимание возможной роли шестивалентной вакцины в летальных последствиях для уязвимого ребенка. В любом случае внезапной и неожиданной смерти, наступившей вскоре после рождения или в раннем детстве, особенно после вакцинации, всегда следует проводить полное вскрытие в соответствии с рекомендациями.
Ссылки
- Блейлок Р., «Прививки: скрытые опасности», Отчет о состоянии здоровья Блейлока, май 2004 г., стр. 1–9.
- Оттавиани Г. и др., «Синдром внезапной детской смерти (СВДС) вскоре после шестивалентной вакцинации: еще одна патология при подозрении на СВДС?», Вирхов Архив., 2006, 448, с. 100-104.
- Зинка Б. и др., «Необъяснимые случаи внезапной детской смерти вскоре после шестивалентной вакцинации», Вакцина, июль 2006 г., 24 (31-32), стр. 5779-5780.
- Миллер Н.З. и др.1. , "Показатели младенческой смертности регрессировали в зависимости от количества рутинно вводимых доз вакцины: есть ли биохимическая или синергетическая токсичность?», Hum. Exp. Toxicol., May 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Проблема с алюминием (нажмите, чтобы открыть)
Алюминий в вакцинах: что нужно знать родителям

1. Что такое алюминий?
Алюминий — легкий металл серебристо-белого цвета, ковкий и прочный. Эти качества делают его полезным во многих отраслях и продуктах, включая машины, строительство, склады, посуду, кухонную утварь, текстиль, красители и косметику. Алюминий также является самым распространенным металлом в земной коре, и практически весь алюминий в окружающей среде содержится в почве. Однако в естественных условиях алюминий не содержится в значительных количествах в живых организмах (таких как растения и животные) и не имеет известной биологической функции. За последнее столетие использование алюминия в некоторых продуктах привело к увеличению воздействия на человека. Основными источниками воздействия являются продукты, содержащие алюминий (например, разрыхлители, полуфабрикаты, детские смеси и т. д.), медицинские продукты (например, антиперспиранты, антациды и т. д.), инъекции от аллергии и вакцины.1-3
2. Почему алюминий присутствует в вакцинах?
В некоторых вакцинах в качестве адъювантов используются соединения алюминия (гидроксид алюминия и фосфат алюминия), которые являются ингредиентами, усиливающими иммунный ответ на антиген (чужеродное вещество).4-5 Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) заявляет, что если некоторые вакцины не будут содержать алюминий, иммунный ответ, который они вызывают, может снизиться.6
3. Какие вакцины содержат алюминий?
Следующие вакцины содержат алюминий и вводятся младенцам, детям и подросткам (рис. 1):
- Гепатит В (HepB)
- шестивалентный
- Дифтерия, столбняк и коклюш (DTaP и Tdap)
- Haemophilus influenzae типа b (PedvaxHIB)
- Пневмококк (ЦВС)
- Гепатит А (HepA)
- Вирус папилломы человека (ВПЧ)
- Менингококк В (MenB)
Рисунок 1: До 18 доз вакцин, содержащих алюминий, вводят от рождения до 22 лет.7-8
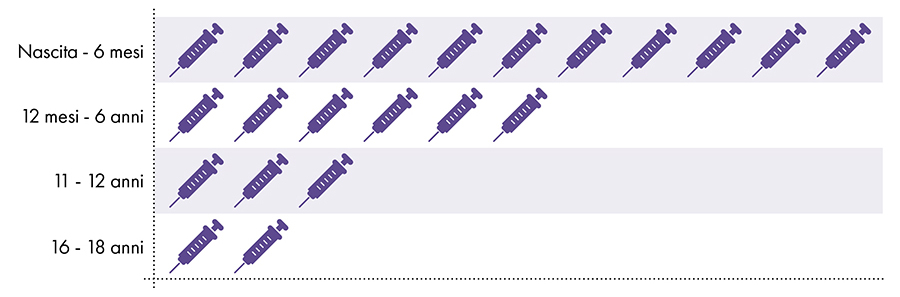
4. Безопасно ли воздействие алюминия?
FDA считает алюминий общепризнанным безопасным (GRAS) с 1975 года.9 Однако до 1990 года не существовало технологий для точного определения небольших количеств алюминия, вводимых субъектам в научных исследованиях.10 Следовательно, количество алюминия, которое могло абсорбироваться до появления побочных эффектов, было неизвестно.
С 1990-х годов благодаря техническим достижениям было замечено, что небольшие количества алюминия, остающиеся в организме человека, нарушают ряд клеточных и метаболических процессов в нервной системе и тканях других частей тела.1-10-11 Наибольшие негативные эффекты алюминия наблюдаются в нервной системе и варьируются от нарушения двигательных навыков до энцефалопатии (изменение психического статуса, изменения личности, трудности мышления, потеря памяти, судороги, кома и др.).2-12
Министерство здравоохранения и социальных служб США (HHS) признает алюминий известным нейротоксином.2 Кроме того, FDA предупредило о рисках токсичности алюминия у младенцев и детей.13
ФЕДЕРАЛЬНЫЙ РЕГИСТР: Ежедневная газета правительства США.«Даже доношенные дети с нормальной функцией почек могут подвергаться риску из-за быстрого роста и незрелости мозга и скелета, а также незрелости гематоэнцефалического барьера. скорости клубочковой фильтрации, чем у взрослых, что влияет на их функцию почек.Агентство опасается, что маленькие дети и люди с незрелой функцией почек подвергаются повышенному риску воздействия алюминия». |
5. Насколько пероральный алюминий небезопасен?
В 2008 году Агентство по регистрации токсических веществ и заболеваний (ATSDR), подразделение HHS, использовало исследования нейротоксического действия алюминия, чтобы определить, что не более 1 миллиграмма (1.000 микрограммов) алюминия на килограмм веса тела в день для избежать негативного воздействия алюминия.2
6. Какое количество введенного алюминия небезопасно?
Чтобы определить количество алюминия, которое можно безопасно вводить инъекционно, необходимо преобразовать пероральный предел алюминия ATSDR. Предел ATSDR для перорального алюминия (1.000 мкг алюминия на килограмм массы тела в день) основан на 0,1% перорального алюминия, который всасывается в кровоток, поскольку пищеварительный тракт блокирует почти весь пероральный алюминий.2 Напротив, алюминий, введенный внутримышечно, не проходит через желудочно-кишечный тракт, и 100% алюминия со временем может всосаться в кровоток (т. е. доля абсорбированного алюминия в 1.000 раз выше). Чтобы учесть эти различные количества абсорбции, предел алюминия для перорального приема в ATSDR необходимо разделить на 1000. Это преобразование приводит к полученному из ATSDR пределу алюминия в крови, равному 1 мкг алюминия (0,1% от 1.000 мкг) на килограмм массы тела. в день. Следовательно, чтобы избежать нейротоксического действия алюминия, ежедневно в кровоток должно поступать не более 1 мкг алюминия на килограмм массы тела. На рисунке 3 показан предельный уровень алюминия в крови, полученный с помощью ATSDR, для младенцев разного возраста в зависимости от их веса.
7. Сколько алюминия содержится в вакцинах?
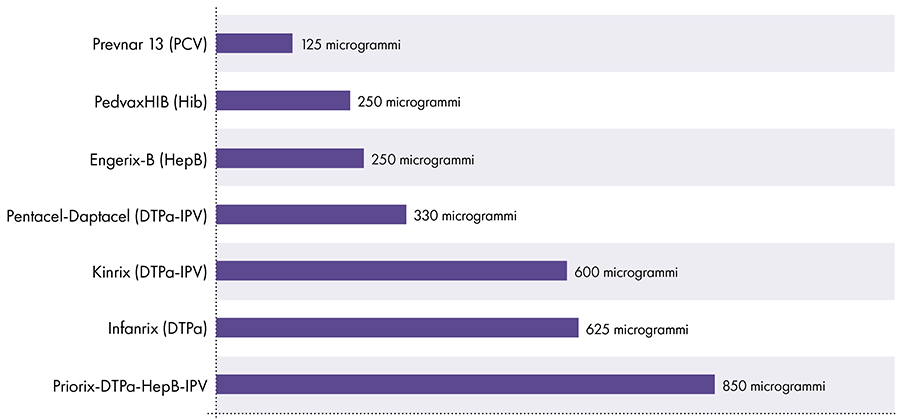
Количество алюминия в вакцинах варьируется.16 В 1968 году федеральное правительство США установило предел содержания алюминия в вакцинах на уровне 850 мкг на дозу, исходя из количества алюминия, необходимого для обеспечения эффективности некоторых вакцин.6-17 Следовательно, количество алюминия в алюминийсодержащих детских вакцинах колеблется от 125 до 850 мкг на дозу. На рис. 4 показано содержание алюминия в одной дозе различных вакцин, вводимых детям.
8. Проводились ли какие-либо исследования по сравнению количества алюминия в вакцинах с пределом, установленным Агентством по регистрации токсичных веществ и заболеваний (ATSDR)?
В 2011 году было опубликовано исследование, целью которого было сравнить количество алюминия в вакцинах с пределом кровотока, установленным ATSDR.18 Однако это исследование неправильно основывало свои расчеты на 0,78% перорального поступления алюминия в кровоток, а не на значении 0,1%, используемом в расчетах ATSDR.19-20 В результате исследование 2011 года выдвинуло гипотезу о том, что почти в 8 раз (0,78% / 0,1%) алюминий может безопасно попасть в кровоток, и это привело к неверному выводу.
9. Безопасно ли воздействие алюминия из вакцин?
Вакцины вводят внутримышечно, и скорость, с которой алюминий из вакцин мигрирует из мышц человека в кровоток, неизвестна. Исследования на животных показывают, что попадание алюминия из вакцин в кровоток может занять от пары месяцев до более года из-за множества переменных.21-23 Поскольку кумулятивное воздействие алюминия из вакцин у детей в возрасте до одного года превышает дневной лимит, установленный ATSDR, на несколько сотен (рис. 3 и 4), предел все равно будет превышен, если алюминий из вакцин попадет в кровоток в течение курса лечения. около года. Кроме того, некоторые исследования показали, что алюминий из вакцин поглощается иммунными клетками и достигает частей тела, удаленных от места инъекции, включая мозг.24
Степень неблагоприятного воздействия алюминия в вакцинах неизвестна, поскольку исследования безопасности не проводились, сравнивая население, вакцинированное алюминийсодержащими вакцинами, с населением, не вакцинированным такими вакцинами.
Алюминиевое ограничение кровотока, полученное из ATSDR2-14-15
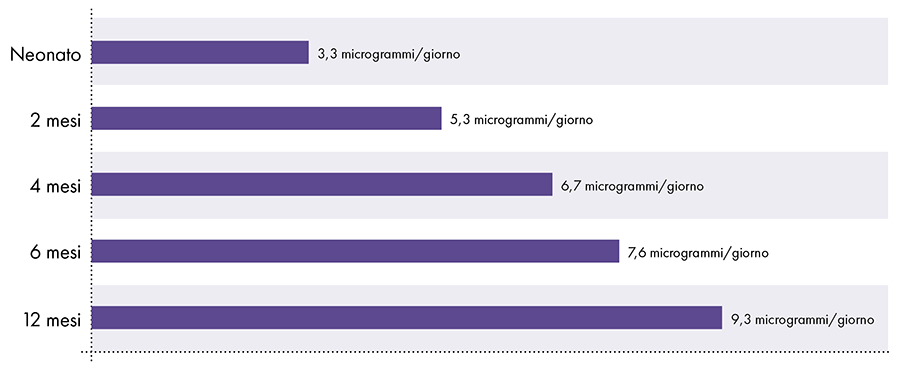 Рисунок 3: На этом графике показано предельное содержание алюминия для детей разного возраста, полученное из Реестра токсичных веществ и заболеваний, подразделения Министерства здравоохранения и социальных служб США. Ограничение указывает на то, что не более 1 микрограмма алюминия на килограмм веса тела должно ежедневно попадать в кровоток, чтобы избежать нейротоксического действия алюминия.
Рисунок 3: На этом графике показано предельное содержание алюминия для детей разного возраста, полученное из Реестра токсичных веществ и заболеваний, подразделения Министерства здравоохранения и социальных служб США. Ограничение указывает на то, что не более 1 микрограмма алюминия на килограмм веса тела должно ежедневно попадать в кровоток, чтобы избежать нейротоксического действия алюминия.
Количество алюминия в вакцинах
Ссылки
- Американская академия педиатрии, Комитет по питанию. Токсичность алюминия у младенцев и детей. Педиатрия. 1996 март; 97 (3): 413.
- Агентство регистрации токсичных веществ и заболеваний (ATSDR). Токсикологический профиль алюминия. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США; 2008.3, 13-24, 145, 171-7, 208.
- Йокель РА. Алюминий в продуктах питания — природа и вклад пищевых добавок. В: Эль-Самраги Й, редактор. Пищевая добавка. Риека (Хорватия): InTech; 2012. 203-28.
- Маррак П., Макки А.С., Манкс М.В. К пониманию адъювантного действия алюминия. Нат Рев Иммунол. 2009 апр; 9 (4): 287.
- Волк В.К., Банни В.Е. Иммунизация дифтерии жидким анатоксином и квасцовым анатоксином. Am J Общественное здравоохранение Здоровье наций. 1942 июль, 32 (7): 690-9.
- Бэйлор Н.В., Иган В., Ричман П. Соли алюминия в вакцинах — точка зрения США. вакцина. 2002 г., 31 мая, 20 Приложение 3: S18-22.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Silver Spring (MD): Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Вакцины, лицензированные для использования в США; [обновлено 2018 февраля 14 г .; цитируется 2018 февраля 27 г.]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Рекомендуемый график прививок для детей и подростков в возрасте 18 лет и младше, США, 2018 г. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Silver Spring (MD): Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. SCOGS (Специальный комитет по веществам GRAS); [цитировано 2018 августа 16 г.]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Священник Н.Д. Биологическое поведение и биодоступность алюминия у человека с особой ссылкой на исследования с использованием алюминия-26 в качестве индикатора: обзор и обновление исследования. J Мониторинг окружающей среды. 2004, 6: 376,392.
- Пул Р.Л., Пьерони К.П., Гаскари С., Диксон Т.К., Парк К.Т., Кернер Дж.А. Алюминий в педиатрических продуктах для парентерального питания: измеренное содержание в сравнении с указанным на этикетке. J Pediatr Pharmacol Ther. 2011, 16 (2): 92-7.
- Седман А. Токсичность алюминия в детском возрасте. Педиатр Нефрол. 1992 июль, 6 (4): 383-93.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Министерство здравоохранения и социальных служб. Правила и положения. Реестр ФРС. 2003 июнь; 68 (100): 34286.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Национальный центр медицинской статистики: Таблица данных для мальчиков, диаграмм роста и веса по возрасту; [цитировано 2019 апреля 2 г.]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Центры по контролю и профилактике заболеваний. Вашингтон, округ Колумбия: Министерство здравоохранения и социальных служб США. Национальный центр статистики здравоохранения: Таблица данных для диаграмм роста и веса девочек по возрасту; [цитировано 2019 апреля 2 г.]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, Министерство здравоохранения и социальных служб. Пересмотр требований к составным материалам. Окончательное правило. Реестр ФРС. 2011 13 апреля, 76 (71): 20513-8.
- Управление Федерального реестра, Национальная служба архивов и документации, Управление общих служб. Правила и положения. Реестр ФРС. 1968 г., январь; 33 (6): 369.
- Миткус Р.Дж., Кинг Д.Б., Хесс М.А., Форши Р.А., Вальдерхауг М.О. Обновленная фармакокинетика алюминия после воздействия на младенцев через диету и вакцинацию. вакцина. 2011 28 ноября, 29 (51): 9538-43.
- Миллер С., Врачи за информированное согласие. Опечатка в «Обновленной фармакокинетике алюминия после воздействия на младенцев через диету и вакцинацию». В: ResearchGate. Берлин (Германия): ResearchGate GmbH; 2020 марта 6 г. [цитировано 2020 марта 6 г.]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Врачи за информированное согласие. Ньюпорт-Бич (Калифорния): Врачи за информированное согласие. Опечатка в «Обновленной фармакокинетике алюминия после воздействия на младенцев через диету и вакцинацию»; [цитировано 2020 марта 6 г.]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Абсорбция алюминийсодержащих вакцинных адъювантов in vivo с использованием 26Al. Вакцина 1997, август-сентябрь, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Анализ алюминия и оценка местной реакции в несколько моментов времени после внутримышечного введения вакцин, содержащих алюминий, у обезьян Cynomolgus. вакцина. 2005 3 февраля, 23 (11): 1359-67.
- Вайссер К., Гён Т., Одуро Д.Д., Вангорш Г., Ханшманн К.О., Келлер-Станиславски Б. Алюминий в плазме и тканях после внутримышечной инъекции адъювантных человеческих вакцин крысам. Арх Токсикол. 2019 окт; 93 (10): 2787-96.
- Массон Д.Д., Крепо Г., Отье Ф.Дж., Эксли С., Герарди Р.К. Критический анализ эталонных исследований токсикокинетики адъювантов на основе алюминия. Дж. Инорг Биохим. 2018 Апрель; 181: 87-95.
Статью перевел Врачи за осознанное согласие
Во многих опубликованных исследованиях сообщалось о серьезных побочных реакциях после вакцинации столбнячным анатоксином. Побочные эффекты включают анафилаксию,(1-2) плечевой неврит,(3) буллезный пемфигоид(4-5-6) синдром Гийена-Барре (СГБ),(7-8) острый рассеянный энцефаломиелит (ОРЭМ),(9) многоформная эритема,(10-11-12) миокардит,(13-14-15-16-17) артрит,(18-19) неврит зрительного нерва,(20-21) и другие аутоиммунные заболевания.(22-23)
Нежелательные эффекты, о которых сообщалось после вакцинации против столбняка, были собраны немецким автором.(24) и Системой мониторинга нежелательных явлений после иммунизации(25) и могут быть разделены на две группы: местные побочные эффекты и системные побочные эффекты.
Можно сказать, что эти эффекты зависят от различных факторов:
- возраст реципиента вакцины;
- физиологические и патологические состояния реципиента вакцины;
- количество принятых доз вакцины;
- количество введенного столбнячного токсина;
- наличие других бактериальных и/или вирусных антигенов, связанных со столбнячным токсином;
- наличие адъювантов или других сопутствующих токсичных веществ.
Считается, что нежелательные эффекты, вызванные первым введением противостолбнячной вакцины, накладываются на те, которые могут возникнуть при бустерных дозах, и при слишком частом введении создают состояние гипериммунизации, что значительно увеличивает риск повреждения вакцины, и по этой причине многие исследования ученые рекомендуют не вводить бустеры этой вакцины с интервалом менее 10 лет.(26) К этому следует добавить, что детский столбнячный анатоксин, содержащийся в комбинированных вакцинах, выше, чем тот, который используется для взрослых, потому что из-за незрелости иммунитета новорожденного необходимо чрезмерно стимулировать для получения адекватного ответа антител.
Наиболее распространенные и обычно более легкие и преходящие местные побочные эффекты прививки от столбняка(32) они обусловлены особой повышенной чувствительностью к столбнячному токсину и представлены: болью (50-85% случаев), покраснением, уплотнением и отеком (25-30% случаев) вплоть до абсцесса.(27) В некоторых случаях местные реакции были особенно серьезными, например, при синдроме Лайелла (или синдроме ошпаренной кожи), смертность от которого составляет 50% у взрослых и 25% у детей.(28)
Все местные побочные эффекты более часты, если вакцину вводят подкожно, а не внутримышечно. Эти эффекты усиливаются с увеличением количества инокулированного столбнячного токсина.(29) и это происходит особенно у субъектов, которым сделали несколько и частых инъекций противостолбнячной вакцины.(30-27)
Исследование 2017 года показывает, что среди детей с обширным отеком конечностей после введения четвертой дозы вакцины против дифтерии-столбняка-ацеллюлярного коклюша рецидивы местной реакции были особенно частыми после введения пятой дозы вакцины (78% привитых).(31)
Побочные эффекты также усиливаются, если противостолбнячную вакцину комбинируют с другими вакцинами, а не используют отдельно.(32)
В 1994 г. Институт медицины США (IOM) сообщил, что существуют убедительные научные доказательства того, что вакцины против столбняка, DT и Td могут вызывать синдром Гийена-Барре (СГБ), включая смерть, неврит плечевого сустава и смерть от анафилаксии (шока). ).(33) МОМ также признала, что существует индивидуальная восприимчивость к реакциям на вакцины по генетическим, биологическим и экологическим причинам, но поставщики вакцин не могут точно предсказать, у кого возникнут осложнения, травмы или смерть до введения вакцины из-за вакцинации.(34)
В 2017 году исследователи из Гвинеи-Бисау сравнили показатели смертности младенцев, привитых от дифтерии, столбняка и цельноклеточного коклюша (АКДС) в возрасте от 3 до 5 месяцев, с смертностью младенцев, еще не привитых вакциной АКДС. Смертность от этой причины была значительно выше среди младенцев, вакцинированных АКДС, чем среди тех, кто еще не был вакцинирован. Исследователи также отметили, что, если пероральная вакцина против полиомиелита (ОПВ) вводилась одновременно с вакциной АКДС, показатели смертности от всех причин снижались, но все равно оставались значительно выше, чем у непривитых детей.(35)
Важным местным нежелательным эффектом, который с относительной частотой можно обнаружить у взрослых, является невропатия плечевого сплетения,(36) если прививка проводится в руку и появляется через несколько дней или недель после вакцинации(37). Эта невропатия характеризуется мышечной болью, слабостью и атрофией мышц. В дополнение к невропатиям, локализованным в области, где была привита вакцина, в литературе мы также находим различные другие сообщения о локализованных невропатиях, вызванных введением противостолбнячного препарата.(38-39) например, вовлечение различных черепно-мозговых нервов(40-41) или глазные нервы(42) или возвратный гортанный нерв.(43)
Наиболее распространенные системные эффекты прививки от столбняка(32) можно разделить на:
- неспецифические эффекты, такие как лихорадка, головная боль (что является довольно частым побочным эффектом после вакцинации), миалгии, крапивница, тошнота, рвота,(44) астения, анорексия, раздражительность, сонливость,
- специфические эффекты, такие как анафилактический шок, генерализованная невропатия, интенсивные боли в животе с диареей, различные воспалительные формы, даже тяжелые, а в некоторых редких случаях даже смерть.
Среди всех наиболее распространенных и многочисленных системных эффектов мы находим неврологические повреждения.(45) и среди них на первое место, безусловно, следует поставить полиневропатию, поражающую периферическую нервную систему, которая встречается чаще, чем поражение центральной нервной системы, и может появиться как после первой дозы вакцины, так и после третьей.(46) Полиневропатия обычно возникает в течение от нескольких минут до нескольких часов (в случае острых аллергических реакций) или в течение 12-48 часов (в случае отсроченных аллергических реакций) или самое большее в течение 4-14 дней после прививки (в случае неврит).(47) Полинейропатия может поражать несколько нервов или большие участки тела вплоть до поражения продолговатого мозга и коры головного мозга и может быть вызвана только противостолбнячной вакциной.(48) или от введения других вакцин в сочетании с вакциной против столбняка.(36-49)
Среди различных форм полинейропатии сообщалось о следующих: демиелинизирующая полинейропатия;(50) асимметричная полинейропатия; полирадикулоневрит с парезом мочевого пузыря и прямой кишки;(51) скарлатиноподобная сыпь,(40) острые уртикарные реакции,(44) паралич дыхательных нервов (паралич Ландри), который также может привести к летальному исходу;(52-53) тетанические судороги;(44) поперечный миелит;(54) синдром Гийена-Барре;(55-56) периферическая моторная афазия;(57) и смерть.(28)
Ссылки (нажмите, чтобы открыть)
- Майорга С., Торрес М.Дж., Корсо Дж.Л. и др. Непосредственная аллергия на вакцину против столбняка: определение антител иммуноглобулина Е и иммуноглобулина G к аллергенным белкам. Энн Аллергия Астма Иммунол. 2003 Feb;90(2):238-43.
- Мартин-Муньос М.Ф., Перейра М.Дж., Посадас С. и др. Анафилактическая реакция на дифтерийно-столбнячную вакцину у ребенка: определение специфических IgE/IgG и исследования перекрестной реактивности. Вакцины. 2002 Sep 10;20(27-28):3409-12.
- Хамати-Хаддад А., Фенихель Г.М. Плечевой неврит после плановой детской иммунизации против дифтерии, столбняка и коклюша (АКДС): отчет о двух случаях и обзор литературы. Педиатрия. 1997 Apr;99(4):602-3.
- Фурнье Б., Декамп В., Бускарат Ф. и др. Буллезный пемфигоид, вызванный вакцинацией. Br J Dermatol. 1996 Jul;135(1):153-4.
- Веннинг В.А., Войнаровска Ф. Индуцированный буйный пемфигоид. Br J Dermatol. 1995 May;132(5):831-2.
- Сезин Т., Эгози Э., Хиллу В. и др. Анти-ламинин-332 пемфигоид слизистых оболочек, развивающийся после прививки от столбняка дифтерии. ДЖАМА Дерматол. 2013 Jul;149(7):858-62.
- Бакши Р., Грейвс М.С. Синдром Гийена-Барре после комбинированной вакцинации столбнячно-дифтерийным анатоксином. J Neurol Sci. 1997 Apr 15;147(2):201-2.
- Ньютон Н. мл., Джанати А. Синдром Гийена-Барре после вакцинации очищенным столбнячным анатоксином. Южный Мед Дж. 1987 Aug;80(8):1053-4.
- Хамидон ББ, Рэймонд АА. Острый диссеминированный энцефаломиелит (ОРЭМ), проявляющийся судорогами, вторичными по отношению к вакцинации против столбнячного токсина. Med J Малайзия. 2003 Dec;58(5):780-2.
- Гриффит Р.Д., Миллер О.Ф. III Многоформная эритема после прививки дифтерийным и столбнячным анатоксином. J Am Acad Дерматол. 1988 Oct;19(4):758-9.
- Фредериксен М.С., Брено Э., Триер Дж. Многоформная малая эритема после прививки педиатрическими вакцинами. Сканд Джей Инфекция Дис. 2004;36(2):154-5.
- Каур С., Ханда С. Многоформная эритема после вакцинации у младенца. Индийский J Dermatol Venereol Leprol. 2008 May-Jun;74(3):251-3.
- Кумар В., Сидху Н., Рой С., Гаурав К. Миокардит после вакцинации против дифтерии, цельноклеточного коклюша и столбнячного анатоксина у новорожденного. Энн Педиатр Кардиол. 2018 May-Aug;11(2):224-226
- Ямамото Х., Хашимото Т., Охта-Ого К. и др. Случай подтвержденного биопсией эозинофильного миокардита, связанного с иммунизацией столбнячным анатоксином. Сердечно-сосудистый патол. 2018 ноябрь - декабрь; 37:54-57
- Ву С.Дж., Сун С., Ли Дж.И. и др.. Острый молниеносный миокардит после прививки от дифтерии, полиомиелита и столбняка. Азиатская сердечно-сосудистая грудная клетка Ann. 2006 Dec;14(6):e111-2.
- Дилбер Э., Карагоз Т., Айтемир К. и др. Острый миокардит, связанный с вакцинацией против столбняка. Mayo Clin Proc. 2003 Nov;78(11):1431-3.
- Амсель С.Г., Ханукоглу А., Фрид Д., Воливович М. Миокардит после тройной иммунизации. Арка Дис Дитя, Апрель 1986; 61 (4): 403–405.
- Джавад А.С., Скотт Д.Г. Иммунизация вызывает ревматоидный артрит? Энн Реум Дис. 1989 г., февраль; 48(2):174.
- Каул А., Адлер М., Алокайли Ф., Джавад А. Рецидив реактивного артрита после бустерной дозы столбнячного анатоксина Энн Реум Дис. 2002 г., февраль; 61(2):185.
- О'Брайен П., Вонг RW Неврит зрительного нерва после комбинированной вакцинации против дифтерии, столбняка, коклюша и инактивированного полиовируса: клинический случай. J Med Case Rep. 2018 Nov 30;12(1):356
- Кабрера-Македа Дж. М., Эрнандес-Кларес Р., Байдес-Герреро А. Е. и соавт. Неврит зрительного нерва при беременности после вакцинации Tdap: отчет о двух случаях. Клин Нейрол Нейрохирург. 2017 Сентябрь; 160: 116-118.
- Рурман-Шахар Н., Торрес-Руис Дж., Ротман-Пикельни П., Леви Ю. Аутоиммунная реакция после вакцинации против столбняка - описание четырех случаев и обзор литературы. Иммунол Рез. 2017 Feb;65(1):157-163.
- Шенфельд Ю., Арон-Маор А. Вакцинация и аутоиммунитет-«вакциноз»: опасная связь? J Аутоиммунный. 2000 Feb;14(1):1-10.
- Побочные эффекты наркотиков Ежегодник. Том 12. (Эльзевир, 988).
- Побочные эффекты наркотиков Ежегодник. Том 13. (Эльзевир, 1989).
- Адебар, Г. [Смерть от шока при первой профилактической подкожной инъекции противостолбнячной сыворотки]. Дтч. Z. Gesamte Gerichtl. Медицина 41, 405-8 (1952).
- Побочные действия препаратов ежегодно. Том 11. (Эльзевир, 1987).
- Frank, K.-H. Todliche Imptcomplikationen (Lyell-Syndrom) nach Tetatoxoid. Dt Gesundh.wes. 29, 1430-4 (1974).
- Релихан М. Реакции на столбнячный анатоксин. J. Jr. Med Assoc. 62, 430-4 (1969).
- Левин Л., Ипсен Дж. и МакКомб Дж. Иммунизация взрослых. Подготовка и оценка комбинированных жидких анатоксинов столбняка и дифтерии для взрослых. Ам. Дж. Хиг. 73, 20 (1961).
- Зафак, Дж. Г. и соавт. Риск повторения нежелательных явлений после иммунизации: систематический обзор. Педиатрия 140, (2017).
- Cody, CL, Baraff, LJ, Cherry, JD, Marcy, SM & Manclark, CR Природа и частота побочных реакций, связанных с иммунизацией АКДС и DT у младенцев и детей. Педиатрия 68, 650-60 (1981).
- Комитет Института Медицины, чтобы Рассмотреть Побочные эффекты Вакцин. Побочные эффекты вакцин: доказательства и причинно-следственная связь. (Оценка биологических механизмов нежелательных явлений: повышенная восприимчивость). Вашингтон, округ Колумбия.: Пресса национальных академий. 1994. Глава 5 Дифтерийный и столбнячный анатоксины 67 - 117 с.
- Комитет Института Медицины, чтобы Рассмотреть Побочные эффекты Вакцин. Побочные эффекты вакцин: доказательства и причинно-следственная связь. (Оценка биологических механизмов нежелательных явлений: повышенная восприимчивость). Вашингтон, округ Колумбия.: Пресса национальных академий. 2012
- Могенсен С.В., Андерсен А., Родригес А. и соавт. Внедрение дифтерийно-столбнячно-коклюшной и оральной вакцины против полиомиелита среди младенцев в городской африканской общине: естественный эксперимент. ЭБиоМедицина. 2017 март; 17: 192-198.
- Tsairis, P., Dyck, PJ & Mulder, DW Естественная история невропатии плечевого сплетения. Отчет о 99 пациентах. Arch. Нейро/. 27, 09-17 (1972).
- Блюмштейн, Г. И. и Крайтен, Х. Периферическая невропатия после введения столбнячного анатоксина. ЯМА 198, I 030-1 (1966)
- Герсбах П. и Варидель Д. Паралич после профилактики столбняка. Швейцария. Медицинский работник Wochenschr. 106, 150-3 (1976).
- Бауст В., Мейер Д. и Ваксмут В. Периферическая невропатия после введения столбнячного анатоксина. Дж. Нейро/. 222, 131–33 (1979).
- Каттер, Р. Вовлечение слухового нерва после столбнячного антитоксина: первый зарегистрированный случай. J Am Med Ass 106, I006-7 (I 936).
- Вирт, Г. Reversibele kochlearisschadigung nach Столбняк-инъекция. Munch Med Wschr 101, 349-81 (1965).
- Harrer, G., Melnizky, V. & Wendt, H. Akkomodationsparese und Schlucklahmung nach Toxoid-Auffrlschungsimpfung. Wien Med Wochenschr 15, 296-7 (1971)
- Басек, М. Односторонний! паралич голосовых связок после введения противостолбнячного антитоксина (ТАТ). Ларингоскоп 68, 805-807 (1958).
- Каннингем, А.А. Анафилаксия после инъекции столбнячного анатоксина. Br.Med.J.2, 522-3 (1940).
- Риддер. Plexuslahmung nach Schutzimpfung mit Tetanusserum. Жевать. мед. Вщ. 81, 1035 (1934).
- Холлидей, П.Л. и Бауэр, Р.Б. Полирадикулоневрит, вторичный по отношению к иммунизации анатоксинами столбняка и дифтерии. Arch Neuro/ 40, 56-57 (1983).
- Эренгут, В. Reaktionen der Wundstarrkrampfimpfung. Dtsch Med Wochenschr 95, 1799-1800 (1970).
- 1Woolling, KR & Rushton, JG Сывороточный неврит; отчет о двух случаях и краткий обзор синдрома. Арх.Нейро/. Психиатрия 64, 568-73 (1950).
- Martin, GI & Weintraub, MI Плечевой неврит и паралич седьмого нерва: редкая опасность вакцинации DPT. клин. Педиатр. (фила). 12, 506-507 (1973).
- Поллард, Дж. Д. и Селби, Г. Рецидивирующая невропатия, вызванная столбнячным анатоксином. Отчет о случае. Дж. Нейро/. Sci., 37, 113-125 (1978).
- Побочные эффекты препаратов annua/. Том 09. (Эльзевир, 1985).
- Harrfeldt, HP [Смерть после активной и пассивной иммунизации против столбняка]. Монацшр. Unfallheilkd. Versicherungsmed. 66, 36-7 (1963).
- Elsasser, G. Zur Entstehung, Localization und Verhiitung der Serumpolyneuritis. Нервенарзт 15, 280 (1942).
- Уиттл, Э. и Робертсон, Н.Р. Поперечный миелит после иммунизации против дифтерии, столбняка и полиомиелита. Br.Med.J.1, 1450 (1977).
- Побочные эффекты препаратов annua/. Том 14. (Эльзевир, 1990).
- Hopf, HC [Синдром Гийена-Барре после введения столбнячного анатоксина. Обзор и отчет о случае]. Актуэль Нейро/. 7, 195-200 (1980).
- Палфти, Г. Ф. и Мерей, Т. Без названия. орв. Хетил. 102, 2321 (1961).
Эта статья обобщена и переведена Национальный центр информации о прививках.

