Первая рецензируемая публикация о вакцинах MMRV (Priorix Tetra)

Наконец, вот мы, спустя почти два года, выходит первая рецензируемая публикация нашего анализа, и многие другие будут опубликованы.
Целью данной статьи является обобщение следующих вопросов: что было опубликовано, какова его валидность и почему это важно для нашего исследования вакцин. Все эти аргументы будут рассмотрены в разговорной и нетехнической форме на первых страницах, а со страницы 3 будет проведено техническое исследование, чтобы позволить специалистам этого сектора оценить статью сама по себе.
Статья опубликована на "F1000 Research"1 является результатом первоначального исследования, проведенного одной из лабораторий, назначенных Ассоциацией Corvelva для проведения анализа. Напоминаем, что с момента начала этой работы прошло более двух лет, и к первым добавлено много других результатов, что Первой серьезной проблемой, которую нам пришлось исследовать, было аномальное количество человеческой ДНК, обнаруженное в проанализированных вакцинах.
Первоначальные анализы показали, что обе анализируемые четырехвалентные вакцины MMRV содержали от 1 до 2.7 мкг / флакон (как опубликовано в настоящей статье), и мы решили обнародовать и незамедлительно сообщить о таких результатах, поскольку просто не ожидалось, что такое количество ДНК может присутствовать в вакцине.
Помимо соображений и выводов, сделанных в ходе исследования, которые носят чисто технический характер и поэтому понятны только тем, кто работает в области метагеномных исследований, на графиках видно, что два образца вакцины содержат высокий процент показаний ДНК человека. в дополнение к тем, которые ожидаются от генома вируса ветряной оспы (вирус альфа-герпеса человека 3), в статье был представлен единственный обнаруживаемый из четырех, как тип анализа DNA-seq.
Тем не менее, мы хотели бы отметить, что количество ДНК, которое было найдено и подтверждено тот же метод, который сейчас проверен здесь были еще выше до 3.7 микрограмма на флакон, что приводит к значительной разнице между партиями. На самом деле, в нашем отчете от 22 декабря 2018 года2 результаты, полученные в результате анализа различных партий из обсуждавшихся в настоящей статье, были представлены, а затем подтверждены межлабораторным анализом, который все еще находится в процессе публикации.
Поэтому, что должно рассматриваться как основной интерес в настоящей публикации, это то, что она проверяет метод, который мы использовали, придает важное значение дискуссиям о «типе» проведенного анализа, и как следствие он однозначно подтверждает все исследования, которые были впоследствии проведены методом NGS: углубленный анализ типа генетического материала, наличия случайных вирусов, значительного отсутствия аттенуированных вирусов, которые должны присутствовать, и количества ДНК человека, которое полностью вышло из-под контроля (также потому, что оно сильно отличается от образца к образцу) мутантная популяция, фаги, ДНК других видов и т. д. Вы можете найти aВсе результаты подведены на нашем сайте3.
Все, что мы осуждали в последние годы, с биологической точки зрения, тщательно докладывая о результатах контрольным органам, приобретает более актуальный научный оттенок (даже если, повторяем еще раз, не экспертные проверки должны были беспокоиться, но представленные данные, очень серьезные по своему содержанию и их возможные последствия для здоровья человека). Однако теперь, когда публикация метода завершена, мы будем требовать ответы, которые нам еще не дали.
Эти результаты, несомненно, подтверждают присутствие эмбриональной ДНК в вакцинах Priorix tetra в различных количествах от партии к партии, что указывает на плохой контроль качества этих фармацевтических продуктов.
Мы также хотели бы напомнить отчет о секвенировании генома MRC-5, опубликованный на веб-сайте Corvelva 27 сентября 2019 года.4 демонстрируя глубокую модификацию этой ДНК даже в генах, связанных с развитием опухолевых заболеваний (эти данные также скоро будут опубликованы). Контаминирующая ДНК плода, обнаруженная во всех проанализированных образцах в различных (то есть неконтролируемых) количествах, до 300 раз превышает предел, установленный EMA для канцерогенной ДНК (10 нг / доза, что соответствует ДНК, содержащейся примерно в 1000 раковых клетках, на основе статистических расчетов, хотя предупредительный предел составляет 100 пг / доза), предел, который обязательно должен применяться также к ДНК плода, неизбежно загрязняющей вакцину Priorix Tetra.
Как следствие, эту вакцину следует считать дефектной и потенциально опасной для здоровья человека, особенно для педиатрической популяции, которая намного более уязвима для генетического и аутоиммунного повреждения из-за незрелости иммунных систем.
Как и ожидалось, следующая часть статьи является более «технической» и трудной для понимания неспециалистами, поэтому мы решили, даже в целях прозрачности, приложить к этому документу также «EMA Dossier - NGS Dossier Обсуждение результатов исследования качества вакцин», Нам пришлось экстраполировать только ту часть, которая могла быть опубликована, то есть 50 страниц досье по сравнению с 200 страницами NGS, поскольку большая часть информации, содержащейся и зарегистрированной для регулирующих органов, должна оставаться конфиденциальной. Строгий закон науки гласит, что часть информации может быть опубликована в журнале только в том случае, если она является оригинальной и поскольку у нас есть другая работа в процессе, мы не хотим подвергать ее риску.
EMA - NGS Dossier «Обсуждение результатов исследования качества вакцин». - https://bit.ly/342XKi7
Наконец, во избежание недоразумений, мы хотели бы выделить часть «Финансовой декларации» из вышеупомянутой публикации:
«Метагеномное секвенирование B1 и B2 было профинансировано Corvelva (некоммерческая ассоциация, Veneto, Италия) в рамках контракта на обслуживание с лабораторией. Никакого другого вклада в поддержку работы не было. Спонсоры не участвовали в разработке проекта. изучение, сбор и анализ данных, решение о публикации или подготовка рукописи "
Прикрепленный:
- Публикация - Ты меня понимаешь? Влияние снижения покрытия на исследования последовательности метагеномного дробовика
- CORVELVA-нить-NGS-ЭМА-анг
- Первая рецензируемая публикация о вакцинах MMRV (Priorix Tetra)
В статье «Ты меня укрываешь? Влияние снижения покрытия на исследования последовательности метагеномного дробовика »
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
Авторы обращаются к технико-методологическому вопросу, возможно ли использовать массивно параллельный метагеномный подход с низким охватом чтением для характеристики сложных биологических матриц. Оценки разнообразия, численности видов и способности реконструировать метагеном De Novo с точки зрения длины и полноты, рассчитываются, чтобы понять, насколько уменьшение глубины секвенирования, изменяемое случайным образом субсэмплированием показаний секвенирования, может повлиять на конечные результаты. Результаты показывают, что индексы разнообразия сложных прокариотических, эукариотических и вирусных сообществ можно точно оценить с помощью 500,000 1,000,000 показаний или менее, хотя для особенно сложных образцов может потребоваться 1,000,000 XNUMX XNUMX показаний. Напротив, проект, предусматривающий реконструкцию метагенома и его генов содержит требует более XNUMX XNUMX XNUMX чтений.
Среди различных и сильно отличающихся друг от друга сложных матриц, подвергнутых массированному метагеномному анализу, были включены два биологических препарата, а именно две разные партии живой ослабленной вакцины MPRV, используемой для иммунизации против кори, эпидемического паротита, краснухи и ветряной оспы у детей. ДНК извлекали из вакцин, геномные библиотеки создавали, используя стандартные коммерческие протоколы, и проводили массовое секвенирование с использованием технологии Illumina.
Помимо соображений и выводов, сделанных в работе, которые носят чисто технический характер и поэтому понятны только тем, кто проводит исследования в области метагеномики, то, что наблюдается в круговых диаграммах, содержащихся в «Расширенных данных» (https://osf.io/wq395/ образцы В1 и В2) показали, что два образца вакцины содержат высокий процент показаний ДНК человека в дополнение к тем, которые ожидаются от генома вируса ветряной оспы (человека альфогерпес вирус 3), единственный из четырех обнаруживаемых, так как в статье был представлен анализ типа DNA-seq.
71% показаний в одной партии и 88% в другой - человеческого происхождения, предположительно полученные из линии эмбриональных клеток MRC-5 (помните, что последующий анализ подтвердил, что это линия MRC5), в которой живут ослабленные вирусы краснухи и ветряной оспы выращен во время приготовления вакцины. Более того, как это было в разных партиях одной и той же вакцины MPRV, протестированной Corvelva в период между 2017 и 2019 годами, количество выделенной ДНК составляет порядка микрограмма.
В партиях вакцин, протестированных с использованием тех же протоколов и технологий, о которых сообщалось в материалах и методах статьи, обнаруженные количества варьировались от 1 до почти 3 микрограммов на флакон, количества варьировались между партиями, но всегда были значительными.
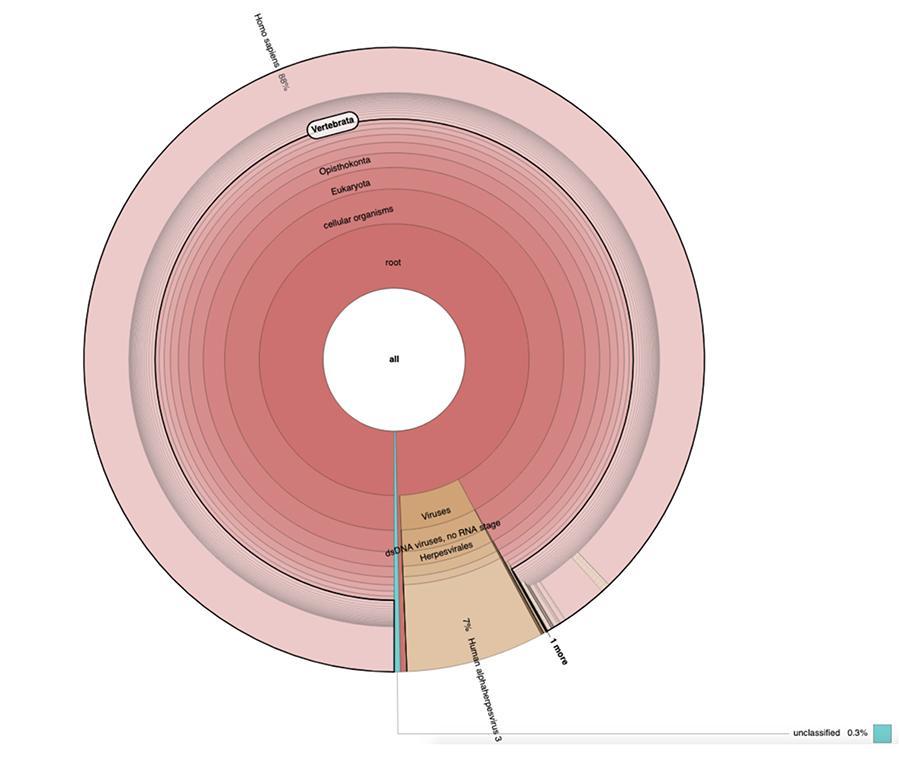
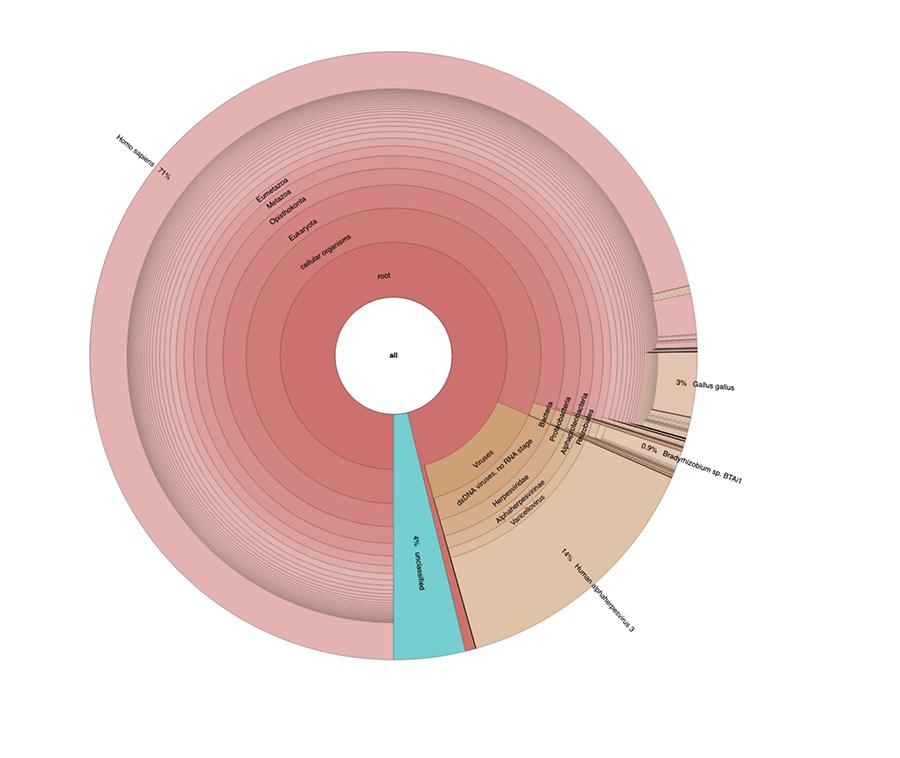
В отчете, опубликованном Corvelva 22.12.2018 5следующие результаты были сообщены для дальнейших партий, проанализированных после обсуждавшихся в статье, позднее подтвержденных межлабораторным анализом, все еще находящимся в процессе публикации.
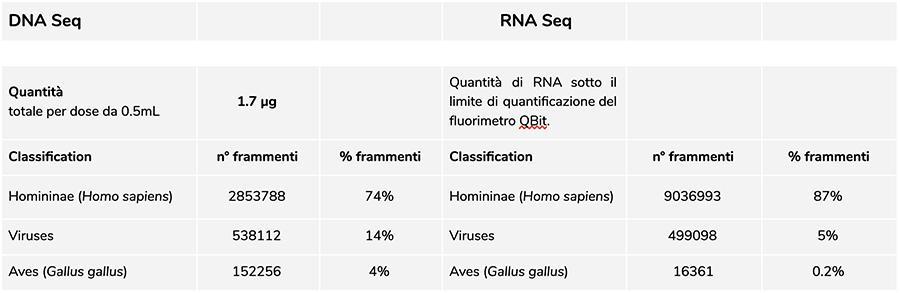
Приорикс тетра много. A71CB205A (июнь 2018 г.) - анализ ДНК
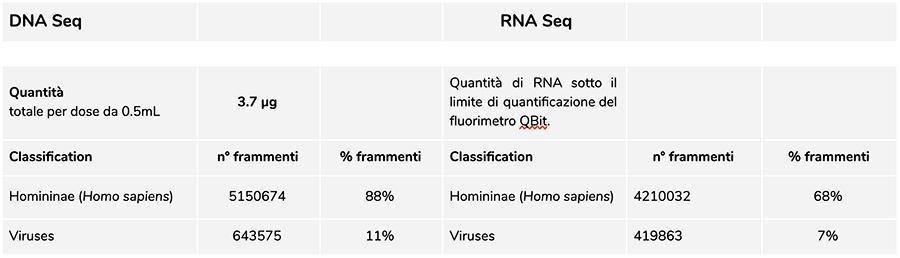
Приорикс тетра много. A71CB256A (декабрь 2018 г.) - анализ ДНК
Анализ ДНК
Измерение концентрации ДНК с помощью флуорометра QuBit показало, что партия A71CB205A содержит в общей сложности 1.7 мкг гДНК на дозу 0.5 мл, рассчитанную следующим образом: 9.41 нг / мкл (концентрация, определенная при QuBit) x 45 (конечный объем ресуспендирования ДНК после экстракции, выраженный в микролитрах) x 4 (начальный объем, представленный для процедуры экстракции, составляет ¼ от объема дозы, содержащейся во всем флаконе, 0.5 мл).
Измерение ДНК концентрация с помощью флуорометра QuBit показала, что A71CB256A много содержит всего гДНК 3.7 мкг на дозу 0.5 млрассчитывается следующим образом: 40.8 нг / мкл (концентрация определяется в QuBit) x 55 (конечный объем ресуспендирования ДНК после экстракции, выраженный в микролитрах) x 5/3 (начальный объем, представленный для процедуры экстракции, составляет 300 мкл на 500 мкл суспензии ).
ДНК человека, обнаруженная в этой партии, составляет примерно 8: 1 по отношению к ДНК ветряной оспы (см. Следующие результаты классификации фрагментов DNA-seq, которые показывают, что 88% всех секвенированных фрагментов ДНК имеют человеческое происхождение, а 11% генома вируса ветряной оспы).
Учитывая, что NGS является количественной технологией, флуориметрическое количественное определение всей ДНК, выделенной из вакцины (например, партия A71CB256A = 3.7 микрограмма на дозу), в сочетании с учетом относительного количественного определения, сделанного выше (8: 1), позволяет нам сказать, что человек ДНК может составлять около 2.9 микрограмма на дозу, по сравнению с примерно 740 нанограммами ДНК ветряной оспы. Также возможно, что по меньшей мере, одна часть ДНК с высокой молекулярной массой, видимая на геле, может представлять собой ДНК человека с высокой молекулярной массой.
Анализ РНК
Количество РНК входит в ампулу с вакциной лот A71CB256A оказался около 200 нг.
РИН, равный 8, обозначает отличное качество РНК и интактная эукариотическая РНК, поскольку присутствуют как пики 18S, так и 28S, типичные для эукариотической РНК.
Ответы на наши вопросы, которые со временем направляются в регулирующие органы, чрезвычайно важны. В настоящее время агентства еще не ответили на вопросы, касающиеся результатов полного анализа, представленного в EMA и AIFA.
Извлечение ответа EMA на наш вопрос о безопасности остатков MRC-5 в тетра-вакцине Priorix® (ссылка на запрос EMA ask-43967 3 августа 2018 г.) - «На основании опубликованной информации Priorix® Tetra содержит вирусные штаммы, полученные отдельно в клетках куриного эмбриона (эпидемический паротит и корь) или в диплоидных клетках человека MRC-5 (краснуха и ветряная оспа). Клеточные линии, используемые для Priorix® Tetra, включают диплоидные клеточные линии человека, которые не могут непрерывно делиться. Обратите внимание, что, согласно Европейской Фармакопее, линии диплоидных клеток MRC-5 не являются онкогенными, что продемонстрировано десятилетиями использования и контроля, и поэтому максимальный предел для ДНК клеток MRC-5 не применяется ».
На сегодняшний день не было предоставлено никаких доказательств (ни в отношении сертификатов анализа качества продукции, ни справочной научной литературы для EMA) этих средств контроля, которые гарантируют, что целесообразно не применять максимальный предел.
В руководстве FDA «Руководство для промышленности: характеристика и квалификация клеточных субстратов и других биологических материалов, используемых при производстве вирусных вакцин для индикации инфекционных заболеваний»6 заявлено, что:
- Штамм диплоидных клеток всегда должен оставаться диплоидным. Если эти характеристики не являются стабильными, необходимо продемонстрировать, что нестабильность не оказывает негативного влияния на производство или соответствие продукта.
- для широко используемых штаммов диплоидных клеток человека, таких как клетки MRC-5 и WI-38, измерение остаточной ДНК может быть необязательным, поскольку мы не считаем остаточную ДНК этих диплоидных клеток человека проблемой безопасности
- остаточная ДНК должна быть ограничена для неонкогенных непрерывных клеток, таких как ИСТИННЫЕ клетки с низким числом пассажей, менее 10 нг / доза для парентеральной инокуляции, как рекомендовано ВОЗ
И руководство ВОЗ «Приложение 3 - Рекомендации для оценки клеточных культур животных в качестве субстратов для производства биологических лекарственных средств и для характеристики банков клеток. Замена Приложения 1 серии технических докладов ВОЗ, n. 878 "добавляет: (...) накоплен значительный опыт в области цитогенетики WI-38 и MRC-5 с 1960-х годов и чтобы поддержать этот опыт, перечислены следующие статьи:
- Джейкобс Дж.П. Обновлены результаты по кариологии клеточных штаммов WI-38, MRC-5 и MRC-9. Разработки в области биологической стандартизации, 1976, 37: 155–156.
- Джейкобс Дж.П. и др. Руководство по приемлемости, управлению и тестированию серийно размножающихся диплоидных клеток человека для производства живых вирусных вакцин для применения у человека. Журнал биологической стандартизации, 1981, 9: 331–342.
- Petricciani JC et al. Стандарты кариологии для линии резус-диплоидных клеток DBS-FRhL-2. Журнал биологической стандартизации, 1976, 4: 43–49.
- Schollmayer et al. Анализ с высоким разрешением и дифференциальная конденсация в хромосомах человека с RBA-полосами. Human Genetics, 1981, 59: 187–193.
- Rønne M. Хромосомная подготовка и методы полосного разрешения высокого разрешения: обзор. Журнал молочной науки, 1989, 72: 1363–1377.
Можно ясно видеть, что справочная литература, в которой утверждается, что диплоидные клетки, используемые для производства вакцин, безопасны с точки зрения генетической стабильности, устарел, Уже 40 лет назад были обнаружены первые генетические аномалии, считающиеся незначительными для безопасности вакцин, и из того, что сообщается в руководящих принципах ВОЗ, с тех пор не было обновлений с новыми технологиями секвенирования, в частности в NGS, который к тому же экономический и быстрый, в результате чего в вакцинах вводят в течение десятилетий агентства допускали присутствие все более прогрессивно генетически модифицированных ДНК в неконтролируемых количествах. По этой теме см. Отчет о секвенировании всего генома MRC-5, опубликованный на веб-сайте Corvelva 27.09.2019, в котором глубокая модификация этой ДНК также очевидна в генах, связанных с развитием опухолевых патологий. (данные публикуются)
Ниже приводится выдержка из письма доктора Т. Дейшера, мирового эксперта по использованию стволовых клеток в терапевтических целях и генной терапии, в котором подчеркивается озабоченность рисками, связанными с использованием вакцин, загрязненных остатками человеческих эмбриональных клеток. :
Доктор Т. ДЕЙШЕР (письмо губернаторам - 8 апреля 2019 г.) - (...) инъекция нашим детям с заражением ДНК плода человека несет риск возникновения двух консолидированных патологий:
- инсерционный мутагенез: человеческая эмбриональная ДНК включена в ДНК ребенка, вызывая мутации. Генная терапия с использованием гомологичной рекомбинации небольших фрагментов показала, что такие небольшие количества, как 1.9 нг / мл фрагментов ДНК, приводят к вставке стволовых клеток в геном у 100% инъецированных мышей. Уровни фрагментов ДНК плода человека у наших детей после вакцинации вакцинами MMR, VARIVAX (ветряная оспа) или гепатита A достигают уровня выше 1.9 нг / мл.
- аутоиммунное заболевание: ДНК плода человека стимулирует реакцию иммунной системы на нападение на организм ребенка.
Наши результаты значительно усиливают экспериментальные наблюдения доктора Дайшера, прежде всего тот факт, что загрязняющая эмбриональная ДНК присутствует во всех образцах, анализируемых в различных количествах (поэтому неконтролируемых), до 300 раз выше, чем предел, установленный EMA для канцерогенной ДНК (10 нг / доза, соответствующая ДНК, содержащейся примерно в 1000 раковых клетках, полученная на основе статистического расчета, в то время как предел предосторожности составляет 100 пг / доза) предел, который также должен обязательно применяться к ДНК плода, которая неизбежно загрязняет Приорикс® Тетра.
Следовательно, эту вакцину следует считать дефектной и потенциально опасной для здоровья человека, особенно в педиатрической популяции, которая намного более уязвима для генетического и аутоиммунного повреждения из-за незрелости в системах восстановления.
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.corvelva.it/speciale-corvelva/vaccinegate.html
https://www.corvelva.it/speciale-corvelva/vaccinegate-en.html - https://www.corvelva.it/speciale-corvelva/vaccinegate/sequenziamento-del-genoma-completo-di-mrc-5-contenuto-in-priorix-tetra.html
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.federalregister.gov/documents/2010/03/04/2010-4553/guidance-for-industry-characterization-and-qualification-of-cell-substrates-and-other-biological

