Le vaccin contre l’hépatite B peut-il provoquer des blessures et/ou la mort ?

NOTE IMPORTANTE: Corvelva vous invite à vous informer en profondeur en lisant toutes les rubriques et liens, ainsi que les notices produits et fiches techniques des fabricants, et à vous entretenir avec un ou plusieurs professionnels de confiance avant de décider de vous faire vacciner ou de vacciner votre enfant. Ces informations sont fournies à titre informatif uniquement et ne constituent pas un avis médical.
Le problème des vaccins multiples (cliquez pour ouvrir)
Le problème des vaccins multiples

Les calendriers de vaccination actuels, notamment pour l'âge pédiatrique, prévoient l'administration de plusieurs antigènes et vaccins en une seule séance, privilégiant le confort au détriment de la sécurité. Afin de pouvoir prononcer un discours précis sur la sécurité des vaccins, il faut nécessairement prendre en considération la complexité du phénomène, en conseillant à tous les lecteurs de s'informer adéquatement sur tous les aspects de la vaccination, les avantages et les inconvénients.
Le Dr Russell Blaylock, professeur assistant clinique de neurochirurgie au centre médical de l'Université du Mississippi, a étudié la "synergie toxique" pendant des années et a pu observer que lorsque deux pesticides faiblement toxiques, où aucun n'est capable de provoquer le syndrome de Parkinson chez des animaux de laboratoire, sont combinés les uns aux autres, peuvent provoquer la maladie même rapidement et compare ce phénomène à celui de plusieurs vaccins administrés simultanément : "Les vaccinations, si elles sont trop nombreuses et trop rapprochées, se comportent comme une maladie chronique".(une). Autres Deux études ont confirmé que la mort subite du nourrisson peut survenir après l'inoculation de plusieurs vaccins en une seule administration.(avant JC)
Une étude publiée dans Human and Experimental Toxicology a montré que les pays qui prescrivent plus de vaccins aux enfants ont tendance à avoir des taux de mortalité infantile plus élevés.(D) Par exemple, aux États-Unis, où les enfants reçoivent 26 vaccins, plus de 6 enfants meurent pour 1000 12 naissances vivantes, tandis qu'en Suède et au Japon, où 3 vaccins pédiatriques sont administrés, 1000 décès sont signalés pour XNUMX XNUMX naissances vivantes. Dans l'étude susmentionnée, le lien entre les vaccins et le SMSN est également pris en compte.
D'après une étude suisse publiée en 2005 dans le European Journal of Pediatrics(E) il en résulte que, concernant les effets sur les prématurés, l'incidence des apnées et bradycardies récurrentes ou accrues après administration de vaccins hexavalents est de 13 %. Cette même année, le même journal a publié une étude allemande qui avait examiné les morts subites du nourrisson après hexavalent. Les auteurs écrivent : « Ces résultats, basés sur des rapports spontanés, ne prouvent pas une relation causale entre la vaccination et la mort subite du nourrisson, mais constituent un signal concernant l'un des deux hexavalents disponibles ; signal qui devrait conduire à intensifier la surveillance des morts subites du nourrisson après vaccination ».(F)
En 2006, il a été publié dans la revue médicale Vaccine(G) la lettre d'une équipe de chercheurs de l'Université de Munich qui fait état de « six cas de mort subite de nourrisson après vaccination hexavalente.. Tous retrouvés morts sans explication 1-2 jours après vaccination ». Ils avaient été classés comme cas typiques de mort subite du nourrisson mais la vérification autooptique avait révélé des anomalies neuropathologiques et histologiques et tous les enfants présentaient un œdème cérébral important qui les faisait faire exception par rapport aux autres cas de SMSN (Syndrome de mort subite du nourrisson). Les chercheurs ont écrit qu'« avant l'introduction du vaccin hexavalent (dans les années 1994-2000), nous n'avions observé le cas que d'un enfant sur 198 mort subite du nourrisson qui décédait peu après la vaccination DTC. Mais entre 2001 et 2004, ils avaient identifié cinq cas similaires sur 74 avec le SMSN. Cela indiquerait une multiplication par treize."
Aussi en 2006 sur Virchows Archive(H), l'équipe de l'Institut de pathologie de l'Université de Milan a écrit : « Des experts de l'Agence européenne pour l'évaluation des produits médicaux ont analysé la possibilité qu'il puisse y avoir un lien entre les vaccins hexavalents et certains cas de décès. Parmi les participants figuraient des pathologistes expérimentés dans les vaccins et la mort subite du nourrisson qui ont effectué les autopsies.Mais, à notre connaissance, peu d'attention a été accordée à l'examen du tronc cérébral et du cœur sanguin sur des coupes en série et il n'y avait aucune possibilité d'établir un rôle déclencheur. du vaccin pour ces décès. Nous rapportons ici le cas d'une fillette de 3 mois décédée subitement après vaccination hexavalente. L'examen du tronc cérébral sur des coupes sériées a révélé une hypoplasie bilatérale du noyau arqué. Le système de conduction du cœur présentait une dispersion et une dégénérescence fœtale persistantes. Ce cas offre une compréhension unique du rôle possible du vaccin hexavalent dans le déclenchement d'une conséquence mortelle chez un enfant vulnérable. Tout cas de mort subite et inattendue qui survient peu après la naissance ou dans la petite enfance, surtout s'il fait suite à une vaccination, doit toujours subir une autopsie complète, conformément aux directives.
Références
- Blaylock R, "Vaccinations : les dangers cachés", The Blaylock Wellness Report, mai 2004, pp.1-9
- Ottaviani G. et al., "Syndrome de mort subite du nourrisson (SMSN) peu de temps après la vaccination hexavalente : une autre pathologie chez les suspects de SMSN ?", Virchows Archiv., 2006, 448, p. 100-104.
- Zinka B. et al., "Cas inexpliqués de mort subite du nourrisson peu de temps après la vaccination hexavalente", Vaccine, juillet 2006, 24 (31-32), pp. 5779-5780.
- Miller NZ et al1. , "Les taux de mortalité infantile ont régressé par rapport au nombre de doses de vaccin administrées en routine : existe-t-il une toxicité biochimique ou synergique ??", Hum. Exp. Toxicol., mai 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Le problème de l'aluminium (cliquez pour ouvrir)
Aluminium dans les vaccins : ce que les parents doivent savoir

1. Qu'est-ce que l'aluminium ?
L'aluminium est un métal léger blanc argenté, malléable et résistant. Ces qualités le rendent utile dans de nombreuses industries et produits, notamment les machines, la construction, les entrepôts, les ustensiles de cuisine, les ustensiles de cuisine, les textiles, les teintures et les cosmétiques. L'aluminium est également le métal le plus abondant dans la croûte terrestre, et pratiquement tout l'aluminium présent dans l'environnement se trouve dans le sol. Cependant, l'aluminium ne se trouve pas naturellement en quantités significatives dans les organismes vivants (tels que les plantes et les animaux) et n'a aucune fonction biologique connue. Au cours du siècle dernier, l'utilisation de l'aluminium dans certains produits a entraîné une exposition humaine accrue. Les principales sources d'exposition sont les aliments contenant de l'aluminium (p. ex. poudre à pâte, aliments transformés, préparations pour nourrissons, etc.), les produits médicaux (p. ex. antisudorifiques, antiacides, etc.), les injections contre les allergies et les vaccins .1-3
2. Pourquoi l'aluminium est-il présent dans les vaccins ?
Certains vaccins utilisent des composés d'aluminium (hydroxyde d'aluminium et phosphate d'aluminium) comme adjuvants, qui sont des ingrédients qui augmentent la réponse immunitaire à un antigène (substance étrangère).4-5 La Food and Drug Administration (FDA) des États-Unis affirme que si certains vaccins ne contiennent pas d'aluminium, la réponse immunitaire qu'ils déclenchent pourrait diminuer.6
3. Quels vaccins contiennent de l'aluminium ?
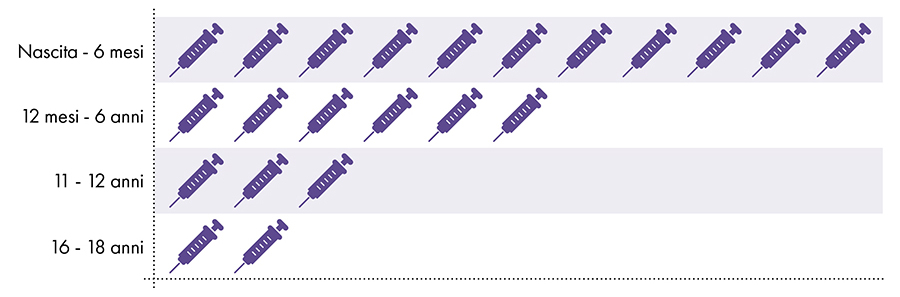
Les vaccins suivants contiennent de l'aluminium et sont administrés aux nourrissons, aux enfants et aux adolescents (Fig. 1) :
- Hépatite B (HepB)
- hexavalent
- Diphtérie, tétanos et coqueluche (DTaP et Tdap)
- Haemophilus influenzae de type b (PedvaxHIB)
- Pneumocoque (PCV)
- Hépatite A (HepA)
- Virus du papillome (VPH)
- Méningocoque B (MenB)
Figure 1 : Jusqu'à 18 doses de vaccins contenant de l'aluminium sont administrées de la naissance à 22 ans7-8
4. L'exposition à l'aluminium est-elle sans danger ?
La FDA considère l'aluminium généralement reconnu comme sûr (GRAS) depuis 1975.9 Cependant, avant 1990, il n'existait aucune technologie permettant de détecter avec précision de petites quantités d'aluminium administrées à des sujets dans le cadre d'études scientifiques.10 Par conséquent, la quantité d'aluminium pouvant être absorbée avant l'apparition des effets indésirables était inconnue.
Depuis les années 1990, grâce aux progrès technologiques, on a observé que les petites quantités d'aluminium qui restent dans le corps humain interfèrent avec un certain nombre de processus cellulaires et métaboliques dans le système nerveux et les tissus d'autres parties du corps.1-10-11 Les effets négatifs les plus importants de l'aluminium ont été observés sur le système nerveux et vont de l'altération de la motricité à l'encéphalopathie (altération de l'état mental, changements de personnalité, difficultés de réflexion, perte de mémoire, convulsions, coma, etc.).2-12
Le ministère américain de la Santé et des Services sociaux (HHS) reconnaît l'aluminium comme une neurotoxine connue.2 De plus, la FDA a mis en garde contre les risques de toxicité de l'aluminium chez les nourrissons et les enfants.13
FEDERAL REGISTER : Le quotidien du gouvernement des États-Unis"Même les nourrissons nés à terme avec une fonction rénale normale peuvent être à risque en raison de la croissance rapide et de l'immaturité du cerveau et du squelette, ainsi que de l'immaturité de la barrière hémato-encéphalique. Jusqu'à l'âge de 1 ou 2 ans, les nourrissons ont un taux de filtration glomérulaire supérieur à celui des adultes, ce qui affecte leur fonction rénale. L'agence craint que les jeunes enfants et les personnes dont la fonction rénale est immature présentent un risque accru d'exposition à l'aluminium." |
5. Quelle quantité d'aluminium par voie orale n'est pas sûre ?
En 2008, l'Agence pour les substances toxiques et le registre des maladies (ATSDR), une division du HHS, a utilisé des études sur les effets neurotoxiques de l'aluminium pour déterminer que pas plus de 1 milligramme (1.000 XNUMX microgrammes) d'aluminium par kilogramme de poids corporel par jour pour éviter les effets négatifs de l'aluminium.2
6. Quelle quantité d'aluminium injectée n'est pas sûre ?
Pour déterminer la quantité d'aluminium qui peut être injectée en toute sécurité, il est nécessaire de convertir la limite orale d'aluminium de l'ATSDR. La limite ATSDR pour l'aluminium par voie orale (1.000 0,1 microgrammes d'aluminium par kilogramme de poids corporel par jour) est basée sur XNUMX % de l'aluminium par voie orale qui est absorbé dans la circulation sanguine, car le tube digestif bloque la quasi-totalité de l'aluminium par voie orale .2 À l'inverse, l'aluminium injecté par voie intramusculaire contourne le tube digestif et 100 % de l'aluminium peut être absorbé dans la circulation sanguine avec le temps (c'est-à-dire que la proportion d'aluminium absorbée est 1.000 1000 fois supérieure). Pour tenir compte de ces différentes quantités d'absorption, la limite orale d'aluminium de l'ATSDR doit être divisée par 1. Cette conversion conduit à une limite d'aluminium sanguin dérivée de l'ATSDR de 0,1 microgramme d'aluminium (1.000% de 1 microgrammes) par kilogramme de poids corporel par jour. Par conséquent, pour éviter les effets neurotoxiques de l'aluminium, pas plus de 3 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine. La figure XNUMX montre la limite d'aluminium sanguin dérivée de l'ATSDR pour les nourrissons de différents âges en fonction de leur poids.
7. Combien d'aluminium y a-t-il dans les vaccins ?
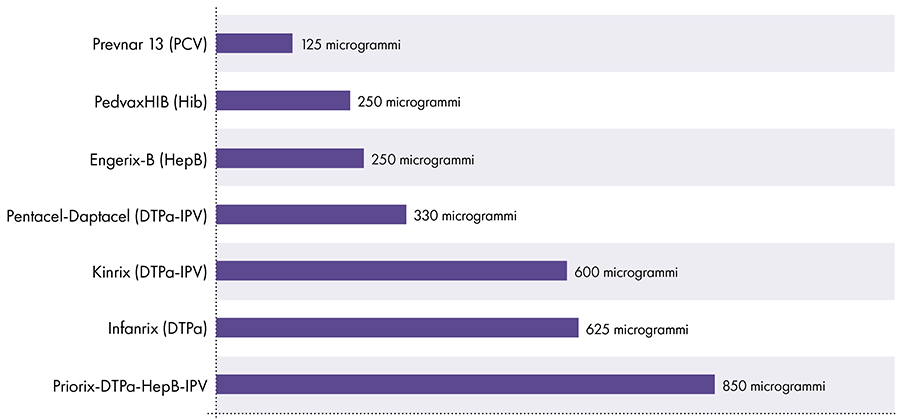
La quantité d'aluminium dans les vaccins varie.16 En 1968, le gouvernement fédéral américain a fixé la limite de la quantité d'aluminium dans les vaccins à 850 microgrammes par dose, en fonction de la quantité d'aluminium nécessaire pour rendre certains vaccins efficaces.6-17 Par conséquent, la quantité d'aluminium dans les vaccins pour nourrissons contenant de l'aluminium varie de 125 à 850 microgrammes par dose. La figure 4 montre la teneur en aluminium d'une dose de divers vaccins administrés aux enfants.
8. Des études ont-elles comparé la quantité d'aluminium dans les vaccins avec la limite dérivée de l'Agence pour les substances toxiques et le registre des maladies (ATSDR) ?
En 2011, une étude a été publiée qui visait à comparer la quantité d'aluminium dans les vaccins avec la limite de flux sanguin fixée par l'ATSDR.18 Cependant, cette étude a incorrectement basé ses calculs sur 0,78% d'aluminium oral absorbé dans la circulation sanguine, plutôt que sur la valeur de 0,1% utilisée par l'ATSDR dans ses calculs.19-20 En conséquence, l'étude de 2011 a émis l'hypothèse que près de 8 fois (0,78 % / 0,1 %) l'aluminium peut pénétrer en toute sécurité dans la circulation sanguine, ce qui a conduit à une conclusion erronée.
9. L'exposition à l'aluminium provenant des vaccins est-elle sans danger ?
Les vaccins sont injectés par voie intramusculaire, et la vitesse à laquelle l'aluminium des vaccins migre du muscle humain dans la circulation sanguine est inconnue. Des études animales suggèrent que l'aluminium des vaccins peut prendre de quelques mois à plus d'un an pour pénétrer dans la circulation sanguine, en raison de multiples variables.21-23 Étant donné que l'exposition cumulée à l'aluminium provenant des vaccins chez les enfants de moins d'un an dépasse de plusieurs centaines la limite quotidienne fixée par l'ATSDR (Fig. 3 et 4), la limite serait tout de même dépassée si l'aluminium provenant des vaccins pénétrait dans le flux sanguin au cours du cycle d'environ un an. De plus, certaines études ont montré que l'aluminium des vaccins est absorbé par les cellules immunitaires et atteint des parties du corps éloignées du site d'injection, y compris le cerveau.24
L'ampleur des effets indésirables de l'aluminium dans les vaccins est inconnue, car aucune étude de sécurité comparant une population vaccinée avec des vaccins contenant de l'aluminium à une population non vaccinée avec de tels vaccins n'a été menée.
Limitation en aluminium du flux sanguin dérivée de l'ATSDR2-14-15
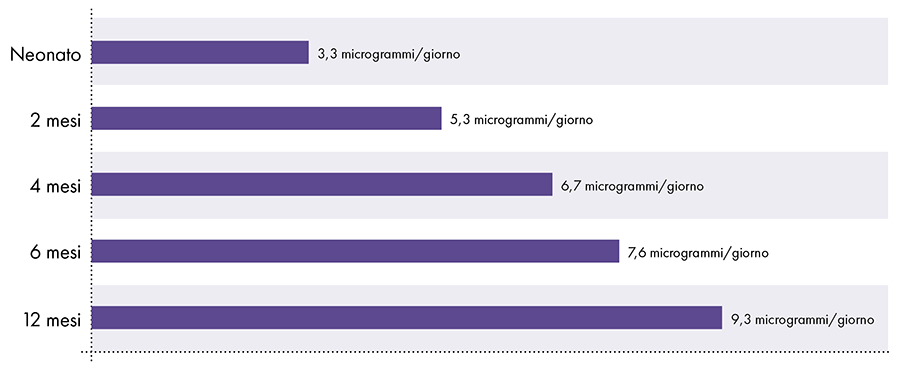 Figure 3 : Ce graphique montre la limite d'aluminium pour les enfants de différents âges, telle que dérivée du Registre des substances toxiques et des maladies, une division du Département de la santé et des services sociaux des États-Unis. La limite indique que pas plus de 1 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine pour éviter les effets neurotoxiques de l'aluminium.
Figure 3 : Ce graphique montre la limite d'aluminium pour les enfants de différents âges, telle que dérivée du Registre des substances toxiques et des maladies, une division du Département de la santé et des services sociaux des États-Unis. La limite indique que pas plus de 1 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine pour éviter les effets neurotoxiques de l'aluminium.
Quantité d'aluminium dans les vaccins
Références
- American Academy of Pediatrics, Comité sur la nutrition. Toxicité de l'aluminium chez les nourrissons et les enfants. Pédiatrie. 1996 mars; 97 (3): 413.
- Agence pour les substances toxiques et le registre des maladies (ATSDR). Profil toxicologique de l'aluminium. Washington, DC : Département américain de la santé et des services sociaux ; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. L'aluminium dans les aliments — la nature et la contribution des additifs alimentaires. Dans : El-Samragy Y, éditeur. Additif alimentaire. Rijeka (Croatie) : InTech ; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Vers une compréhension de l'action adjuvante de l'aluminium. Nat Rev Immunol. avril 2009; 9 (4): 287.
- Volk VK, Bunney WE. Immunisation contre la diphtérie avec l'anatoxine liquide et l'anatoxine précipitée à l'alun. Am J Santé publique Nations Health. juillet 1942; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Sels d'aluminium dans les vaccins - perspective américaine. Vaccin. 2002 mai 31 ; 20 Suppl 3 : S18-22.
- Administration américaine des aliments et médicaments. Silver Spring (MD) : Administration américaine des produits alimentaires et pharmaceutiques. Vaccins autorisés à être utilisés aux États-Unis ; [mis à jour le 2018 février 14 ; cité le 2018 février 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Calendrier de vaccination recommandé pour les enfants et les adolescents âgés de 18 ans ou moins, États-Unis, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Administration américaine des aliments et médicaments. Silver Spring (MD) : Administration américaine des produits alimentaires et pharmaceutiques. SCOGS (Comité restreint sur les substances GRAS); [cité le 2018 août 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Prêtre ND. Le comportement biologique et la biodisponibilité de l'aluminium chez l'homme, avec une référence particulière aux études utilisant l'aluminium-26 comme traceur : revue et mise à jour de l'étude. J EnvironMonit. 2004 ; 6 : 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminium dans les produits de nutrition parentérale pédiatrique : contenu mesuré par rapport au contenu indiqué sur l'étiquette. J Pediatr Pharmacol Ther. 2011 ; 16 (2) : 92-7.
- Sedman A. Toxicité de l'aluminium chez l'enfant. Pédiatre Néphrol. juillet 1992; 6 (4): 383-93.
- Food and Drug Administration des États-Unis, ministère de la Santé et des Services sociaux. Règles et règlements. Registre de la Fed. juin 2003; 68 (100): 34286.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Centre national des statistiques sur la santé : tableau de données pour les graphiques de longueur pour l'âge et de poids pour l'âge des garçons ; [cité le 2019 avril 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Centre national des statistiques sur la santé : tableau de données pour les graphiques taille-pour-âge et poids-pour-âge des filles ; [cité le 2019 avril 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Food and Drug Administration des États-Unis, ministère de la Santé et des Services sociaux. Révision des exigences relatives aux matériaux constitutifs. Règle finale. Registre de la Fed. 2011 avril 13 ; 76 (71) : 20513-8.
- Office of the Federal Register, National Archives and Records Service, General Services Administration. Règles et règlements. Registre de la Fed. janvier 1968 ; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Mise à jour de la pharmacocinétique de l'aluminium à la suite d'expositions infantiles par l'alimentation et la vaccination. Vaccin. 2011 28 novembre ; 29 (51) : 9538-43.
- Miller S, médecins pour le consentement éclairé. Erratum dans « Mise à jour de la pharmacocinétique de l'aluminium à la suite d'expositions infantiles par l'alimentation et la vaccination ». Dans : ResearchGate. Berlin (Allemagne) : ResearchGate GmbH ; 2020 mars 6 [cité le 2020 mars 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Médecins pour le consentement éclairé. Newport Beach (CA) : Médecins pour un consentement éclairé. Erratum dans « Mise à jour de la pharmacocinétique de l'aluminium suite à l'exposition de nourrissons par l'alimentation et la vaccination » ; [cité le 2020 mars 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorption in vivo d'adjuvants vaccinaux contenant de l'aluminium à l'aide de 26Al. Vaccine 1997 août-sept ; 15 (12-13) : 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminium dosage et évaluation de la réaction locale à plusieurs moments après l'administration intramusculaire de vaccins contenant de l'aluminium chez le singe Cynomolgus. Vaccin. 2005 février 3 ; 23 (11) : 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminium dans le plasma et les tissus après injection intramusculaire de vaccins humains avec adjuvant chez le rat. Arch Toxicol. 2019 octobre ; 93 (10) : 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Analyse critique des études de référence sur la toxicocinétique des adjuvants à base d'aluminium. J Inorg Biochem. avril 2018 ; 181 : 87-95.
Article traduit par Médecins pour un consentement éclairé
En 1981, la Food and Drug Administration (FDA) des États-Unis a autorisé un vaccin contre l’hépatite B dérivé du plasma qui contenait des antigènes prélevés sur des individus infectés. Ce vaccin a ensuite été retiré du marché car, comme tous les vaccins produits à partir de sang humain, il était capable de transmettre des virus indésirables et potentiellement dangereux. En 1986, le premier d’une série de vaccins génétiquement modifiés (ADN recombinant) a été autorisé.
De nombreuses études ont étudié la probabilité que ceux qui ont reçu le vaccin dérivé du plasma aient également pu contracter des virus indésirables, notamment le VIH, le précurseur du SIDA.(1) De plus, les études cliniques visant à attester de l'innocuité du vaccin actuel contre l'hépatite B n'ont été réalisées que sur 147 enfants en bonne santé, suivis pendant seulement 5 jours après l'administration.(3) Il ne s’agit pas d’un échantillon suffisamment grand ni d’une période suffisamment longue pour déterminer la véritable incidence des événements indésirables. Les fabricants eux-mêmes ont admis que "l'utilisation généralisée du vaccin pourrait conduire à l'apparition d'effets indésirables non observés lors des essais cliniques".(4)
Même les sujets adultes ont été surveillés pendant seulement cinq jours après la vaccination et, malgré cela, des effets systémiques tels que arthralgie, myalgie, paresthésies, douleurs au dos et au cou, lymphadénopathie, maux de tête, fièvre, malaises, frissons, vomissements ont toujours été rapportés. douleur, infections des voies respiratoires supérieures, maux d’oreilles et hypotension.(5)
Malgré les fiches techniques officielles, et autres documents qui se propagent(6) le vaccin contre l'hépatite B, tendent à minimiser ou à nier les effets indésirables graves, de nombreuses études publiées dans des revues médicales et scientifiques du monde entier et des rapports transmis au VAERS(7) confirmer diverses pathologies consécutives à la vaccination. Certaines de ces études sont résumées ci-dessous.
arthrite
En 1990, peu après l’introduction du vaccin contre l’hépatite B, le British Medical Journal a documenté un lien entre le vaccin et la polyarthrite, une inflammation douloureuse de cinq articulations ou plus.(8) La même année, le Journal of Rheumatology a publié un article sur l’arthrite réactive après vaccination contre l’hépatite B.(9)
En 1994, le British Journal of Rheumatology a publié des données documentant la polyarthrite rhumatoïde après l'administration du vaccin.(10) et le BMJ a publié trois autres rapports confirmant le lien entre le vaccin et l'arthrite réactive.(11) En 1995, deux études ont été publiées dans le Norwegian Journal of Rheumatology confirmant des cas d'arthrite post-vaccination.(13) et la même année, l'Irish Medical Journal a documenté le lien avec l'arthropathie.(15) En 1997, le British Journal of Rheumatology a publié deux autres études documentant plusieurs cas de polyarthrite inflammatoire après l'administration du vaccin.(16) et en 1998, le Journal of Rheumatology a de nouveau confirmé la polyarthrite rhumatoïde.(18) Cette année-là également, la revue française Revue de Médecine Interne a publié une étude sur la maladie de Still apparaissant à l'âge adulte - une forme d'arthrite rare et douloureuse - après une vaccination contre les hépatites A et B.(19) En 1999, la rhumatologie a documenté des troubles rhumatologiques après l'administration du vaccin.(20) et en 2000, l'American College of Rheumatology a publié une recherche dans la revue à comité de lecture Arthritis & Rheumatology qui documentait le syndrome de Sjögren - une forme rare d'arthrite chronique - après la vaccination contre l'hépatite B.(21)
Maladies auto-immunes et neurologiques, dont la sclérose en plaques
En 1983, le New England Journal of Medicine a publié une étude démontrant l’apparition d’une polyneuropathie – un dysfonctionnement simultané de nombreux nerfs – après une vaccination contre l’hépatite B.(22) En 1988, l’American Journal of Epidemiology a signalé plusieurs « événements indésirables neurologiques » après le vaccin, notamment de nombreux cas de syndrome de Guillain-Barré, de radiculopathie lombaire, de neuropathie du plexus brachial, de névrite optique et de myélite transverse.(23) La même année, la revue Archives of Internal Medicine a documenté à nouveau la myasthénie grave - une maladie neuromusculaire auto-immune chronique grave - après la vaccination contre l'hépatite B.(24)
En 1991, The Lancet a publié un rapport documentant la démyélinisation du système nerveux central après l'administration du vaccin.(25) et en 1992, Nephron a publié des données liant la vaccination au lupus érythémateux disséminé, une maladie auto-immune chronique qui affecte plusieurs organes.(26) Toujours en 1992, la revue Clinical Infectious Diseases a publié une étude liant le syndrome d'Evans - une maladie auto-immune et sanguine rare avec un taux de mortalité élevé - au vaccin.(27) et le magazine français Thérapie a de nouveau publié une étude sur la « paralysie faciale périphérique » après l'administration du médicament.(28) De plus, Infectious Disease News a publié un rapport faisant état de nombreux cas de lésions neurologiques ressemblant à la sclérose en plaques.(29) et en 1993, un article est paru dans le Journal of Hepatology sur la myélite transverse - inflammation de la moelle épinière - après vaccination anti-hépatite B.(30) La même année, le journal français La Nouvelle Presse Médicale a publié des données confirmant une "myélite aiguë" post-vaccination.(31) et les maladies infectieuses cliniques ont documenté la « sclérose en plaques classique ».(32) En 1994, les Archives de pédiatrie et de médecine de l'adolescence ont publié des données reliant le lupus au vaccin.(33) et la revue Acta Neurologica Scandinavica ont publié un rapport sur l'ataxie cérébelleuse aiguë - grave perte d'équilibre et de coordination motrice - après la vaccination en question.(34)
En 1995, une démyélinisation du système nerveux central a été rapportée dans le Journal of Neurology, Neurosurgery and Psychiatry.(35) et dans l'American Journal of Neuroradiology myélite. Les auteurs de cette dernière étude ont noté que les événements indésirables de cette nature pourraient être sous-déclarés parce que les symptômes sont tardifs.(36) En 1996, Nephron et la revue française Annales de Dermatologie et de Vénéréologie ont publié des études attestant de la corrélation entre le lupus érythémateux et le vaccin contre l'hépatite B.(37) La même année, le Journal of Hepatology publie un rapport sur le lien avec la leucoencéphalite, inflammation de la substance blanche du cerveau.(39) En 1996, le New England Journal of Medicine a documenté la cryoglobulinémie post-vaccination, une maladie auto-immune rare qui altère la circulation, provoque des saignements et d'autres problèmes.(40)
L'auto-immunité induite par le vaccin a été certifiée dans le Journal of Autoimmunity(41) et en 1997, l'Indian Journal of Pediatrics a publié une étude reliant le syndrome de Guillain-Barré, une maladie auto-immune qui provoque des lésions nerveuses, une faiblesse musculaire et une paralysie, au vaccin.(42) La même année, le Journal of Korean Medical Science a documenté une myélite aiguë.(43) et le lien avec la « neuropathie du nerf mental » est également apparu.(44)
Des données sont ensuite apparues dans JAMA sur 46 personnes – pour la plupart des femmes – qui avaient perdu leurs cheveux après une vaccination contre l'hépatite B.(45)
En 1998, un lupus érythémateux et une thrombocytopénie ont été documentés chez des sujets vaccinés.(46) et en 1999, plus d'alopécie dans l'American Journal of Gastroenterology.(47) La même année, l'Autoimmunité a documenté une polyneuropathie démyélinisante, tandis que la Neurologie a publié des données liant la sclérose en plaques et l'encéphalite au vaccin.(48) Toujours en 1999, La Nouvelle Presse Médicale écrivait sur la myélite cervicale post-vaccinale(50) et en 2000, la sclérose en plaques a été abordée dans Neurology.(51) Toujours en 2000, le Journal de l'Association médicale de Thaïlande a écrit sur le syndrome de Guillain-Barré après un vaccin à ADN recombinant contre l'hépatite B.(52) et en 2001, la clinique des maladies infectieuses a documenté la leucoencéphalite.(53) En 2004, Neurology a publié une étude montrant l'association entre le vaccin et un risque statistiquement significatif de sclérose en plaques ;(54) en 2006, le Chinese Medical Journal a également documenté la sclérose en plaques.(55) En 2008, Neurology a publié deux études montrant une corrélation statistiquement significative entre la vaccination contre l'hépatite B chez les enfants et le développement de la sclérose en plaques pédiatrique (démyélinisation du système nerveux central) plus de trois ans plus tard.(56)
Déficience sensorielle
De nombreuses publications médicales et scientifiques ont documenté des déficiences visuelles et auditives après la vaccination contre l’hépatite B. Par exemple, en 1987, The Lancet a publié un article sur l’uvéite – une inflammation de la paroi interne de l’œil qui conduit souvent à la cécité – après le vaccin.(58) En 1993, toujours dans The Lancet, d'autres données sont apparues documentant la perte de vision et l'éosinophilie - une maladie allergique du sang - encore une fois après la vaccination.(59) En 1994, Optometry and Vision Science a documenté une névrite optique post-vaccination.(50) et en 1995, l'épithéliopathie - un trouble oculaire rare qui entraîne une détérioration de la vision - a été abordée dans les Archives d'ophtalmologie.(61) En 1996, The Lancet a publié un rapport documentant « l’occlusion de la veine centrale de la rétine » après l’administration du vaccin,(62) tandis que dans l'American Journal of Ophthalmology, le syndrome des points blancs bilatéraux a été mentionné, qui entraîne une perte de vision des deux yeux.(63) Toujours en 1996, La Nouvelle Presse Médicale a documenté une neuropillite - inflammation et détérioration du nerf optique - après le vaccin.(64) et une autre revue française, Annales d'Otolaryngologie et de Chirurgie Cervico-Faciale, a mentionné la perte auditive.(65) En 1997, La Nouvelle Presse Médicale publie alors deux études différentes documentant des cas graves d'occlusion de la veine centrale de la rétine après vaccination.(66) La même année, la néphrologie, la dialyse et la transplantation confirment l'apparition d'une névrite optique après le vaccin.(68) et International Ophthalmology ont certifié « complications ophtalmiques » chez les sujets vaccinés.(69) Toujours en 1997, les Annals of the New York Academy of Sciences et la revue internationale Auris, Nasus, Larynx ont noté une perte auditive post-vaccination,(70) tandis qu'en 1998, le Journal d'Ophtalmologie Française a publié des données sur l'épithéliopathie.(72) En 1999, le BMJ a confirmé une névrite optique après une vaccination contre l'hépatite B.(73) et Acta Ophthalmologica Scandinavica papilledema - gonflement du disque optique.(74) En 2001, un magazine allemand, Klinische Monatsblätter Für Augenheilkunde, a également confirmé une névrite optique post-vaccination.(75)
Maladies du sang
En 1990, peu après l'introduction sur le marché de masse du vaccin contre l'hépatite B, le BMJ a documenté une vascularite, une inflammation des vaisseaux sanguins, après l'administration du médicament.(76) En 1993, le magazine anglais Thorax confirmait(77) et The Lancet a publié une étude sur l'éosinophilie, une maladie allergique du sang, toujours après la vaccination.(78) En 1994 et 1995, The Lancet a également documenté la thrombocytopénie, une maladie grave qui provoque des saignements excessifs, des ecchymoses et des problèmes de coagulation.(79) En 1998, la survenue d'une thrombocytopénie a été confirmée chez de nombreux patients récemment vaccinés.(81) également du Journal scandinave des maladies infectieuses confirmé et des Archives of Disease in Children ont publié des données confirmant que cette maladie est un événement indésirable du vaccin.(82) En 1999, le European Journal of Pediatrics a confirmé une fois de plus la thrombocytopénie après les vaccins contre l'hépatite B et ROR.(83) et la même année le Journal of Rheumatology publie deux études importantes dont la première avait démontré la corrélation entre vaccin et vascularite.(84) et la deuxième érythermalgie, spasmes vasculaires des mains et des pieds qui provoquent des douleurs et des brûlures.(85) En 2000, la Rhumatologie Clinique et Expérimentale a étudié des cas de polyarthrite noueuse(86) - un type de vascularite rare, systémique et nécrosant (endommageant les cellules) - et le British Journal of Hematology a documenté une pancytopénie sévère - une réduction dangereuse des globules rouges.(87) En 2001, le Journal of Rheumatology a publié des données supplémentaires confirmant la possibilité d'une vascularite après le vaccin recombinant contre l'hépatite B.(88) et la revue italienne Haematologica a confirmé la thrombocytopénie comme un événement indésirable.(89)
Maladies de la peau
En 1989, le New England Journal of Medicine a documenté un érythème noueux – une inflammation douloureuse de la peau avec des bosses molles – après une vaccination contre l'hépatite B.(90) En 1993, le Journal of Rheumatology a signalé des cas d'érythème noueux et d'arthrite de Takayasu, une forme rare de vascularite.(91) La même année, la revue suédoise Acta Dermato-Venereologica a écrit sur le lichen ruber plan après vaccination.(92) - une éruption cutanée avec démangeaisons caractérisée par des lésions épaisses et dures rapprochées qui ressemblent à des algues ou à des champignons poussant sur les rochers. En 1994, les Archives de Dermatologie ont également documenté un lichen plan après vaccination.(93) et la dermatologie pédiatrique ont démontré un lien avec l'érythème polymorphe.(94) En 1997, l’Australasian Journal of Dermatology a confirmé la « réaction lichénoïde » (lichen planus) après l’administration du vaccin.(95) et le Journal of the American Academy of Dermatology a écrit sur l'anethodermie(96) - rides localisées, perte d'élasticité et atrophie de la peau - après vaccination. En 1998, le British Journal of Dermatology a publié deux études documentant des maladies cutanées post-vaccinales : l'une concernait le lichen plan.(97) et l'autre sur l'urticaire et l'angio-œdème,(98) pathologies d'origine allergique caractérisées par des brûlures, des picotements et un gonflement douloureux. En 1999, le lichen plan a également été mentionné dans l'International Journal of Dermatology.(99) et en 2000, des données confirmant un érythème polymorphe post-vaccination ont été publiées dans Clinical and Experimental Dermatology.(100) La même année, le Nepal Journal of Dermatology a de nouveau écrit sur le lichen plan après la vaccination contre l'hépatite B.(101) en 2001, la mention est apparue dans le Journal of the American Academy of Dermatology(102) tandis que la dermatologie pédiatrique parlait d'éruption lichénoïde.(103)
Diabète, maladies du foie et des reins
En 1994, The Lancet a documenté un dysfonctionnement hépatique après une vaccination contre l'hépatite B.(104) et en 1995, Clinical Nephrology a publié une étude sur le syndrome néphrotique - lésions rénales - à nouveau après la vaccination.(105) En 1996, le New Zealand Medical Journal a publié deux documents corrélant l'antihépatite B aux épidémies de diabète sucré insulino-dépendant (IDDM). Les auteurs ont constaté qu’au cours des trois années qui ont suivi une campagne de vaccination de masse nouvellement introduite et très étendue, il y a eu une augmentation de 60 % des cas de diabète ID.(106) En 1997, Intensive Care Medicine a écrit sur l’inflammation du foie et les maladies respiratoires aiguës après la vaccination (108). En 2000, la néphrologie pédiatrique a confirmé la possibilité de souffrir d'un syndrome néphrotique après avoir reçu le vaccin.(109) D'autres publications ont également documenté des effets indésirables de ce vaccin.(110-111-112-113-114-115-116-117-118-119)
La France a supprimé l'antihépatite B du calendrier de vaccination pédiatrique
En juillet 1998, environ 15.000 XNUMX citoyens français appartenant à quinze associations ont porté plainte contre le gouvernement français, alléguant que celui-ci avait induit le public en erreur sur les risques et les bénéfices associés au vaccin contre l'hépatite B. Des centaines, voire des milliers, de personnes avaient souffert de maladies auto-immunes et troubles neurologiques, y compris la sclérose en plaques, après la vaccination.(120) Ainsi, en octobre 1998, la France est devenue le premier pays à supprimer l'obligation d'admission à l'école de ce vaccin.(121)
Le vaccin contre l'hépatite B contre le SIDA
En 1978, le New York Blood Center de Manhattan, New York, a injecté à des hommes homosexuels un vaccin expérimental contre l'hépatite B, produit par Merck, pour la préparation duquel des chimpanzés ont été utilisés. Peu de temps après, des homosexuels de San Francisco, Los Angeles, Denver, Chicago et St. Louis ont également reçu 3 doses du médicament sur une période de trois mois.
En 1980, 20 % des hommes homosexuels volontaires pour l’expérience de Manhattan ont été testés positifs au VIH – l’incidence la plus élevée au monde, y compris en Afrique. En 1981, l’épidémie de sida devient officielle. Bien qu’il n’y ait aucune preuve que le vaccin expérimental contre l’hépatite B chez ces volontaires homosexuels ait provoqué le SIDA, il ne fait aucun doute que la maladie a atteint son apogée peu après les injections.(122)
Quelle est l’efficacité du vaccin contre l’hépatite B ?
L'efficacité du vaccin contre l'hépatite B a été définie en injectant le médicament à des sujets sur lesquels les anticorps spécifiques produits dans le sang ont ensuite été mesurés. Ces anticorps doivent atteindre ou dépasser certains niveaux établis par des experts et qui sont présumés assurer une protection. Les scientifiques appellent cela « séroprotection ». Selon cette définition, le vaccin est considéré comme « hautement immunogène » lorsque les niveaux d’anticorps sont mesurables dans la courte période suivant la dernière dose d’un cycle de trois rappels.(123) Pourtant, selon les industries manufacturières, la durée de l’effet protecteur chez les personnes vaccinées en bonne santé n’est pas connue. Des études de suivi réalisées cinq à neuf ans plus tard montrent qu’environ la moitié de tous les sujets vaccinés ne possèdent plus de niveaux protecteurs d’anticorps.(124)
Par exemple, une étude publiée dans le New England Journal of Medicine a révélé qu’après cinq ans, les niveaux d’anticorps (qui sont présumés liés à l’immunité) avaient chuté de façon spectaculaire ou n’étaient plus détectables chez 42 % des personnes vaccinées. De plus, 34 des 773 sujets (4,4 %) étaient infectés par le virus.(126) Dans une autre étude, moins de 40 % des personnes vaccinées présentaient des anticorps protecteurs après cinq ans.(128)
Des recherches similaires ont montré que 48 % des sujets vaccinés présentaient des niveaux d’anticorps insuffisants après seulement quatre ans.(129) Selon l'OMS, jusqu'à « 60 % des adultes perdront tous les anticorps mesurables induits par le vaccin contre l'hépatite B d'ici six à dix ans ».(130) et la littérature médicale regorge de données confirmant l’échec de la vaccination.(131)
Références
- Jacobson IM et al., "Manque d'effet du vaccin contre l'hépatite B sur les phénotypes des cellules T", NEJM, 1984, 311 (16), pp. 1030h1032-XNUMXhXNUMX.
- Institut de médecine, Événements indésirables associés aux vaccins infantiles : preuves portant sur la causalité, National Academy Press, Washington, DC, 1994.
- Merck & Co., Inc. Recombivax HB Hepatitis B Vaccine (Recombinant), notice d'emballage en date de juin 2005.
- Ibid.
- Ibid.
- Tan LJ, « The hepatitis B vaccin », American Medical Association, AMA aidant les médecins à aider les patients, www.arna-assn.org, 9 décembre 2004.
- Système de notification des événements indésirables liés aux vaccins VAERS. Rockville, Maryland.
- Rogers ton SJ et coll. , "Vaccin contre l'hépatite B associé à l'érythème noueux et à la polyarthrite", BMJ, 1990, 301, p. 345.
- Hachulla E. et al., "Arthrite réactive après vaccination contre l'hépatite B Journal of Rheumatology", 1990, 17, pp. 1250-1251.
- Vautier G. et al., « Polyarthrite rhumatoïde séro-positive aiguë survenant après vaccination contre l'hépatite », Br. J. Rheumatol., octobre 1994, 33 (10), p. 991.
- Hassan W. et al., "Syndrome de Reiter et arthrite réactive chez les travailleurs de la santé après vaccination", BMJ, 9 juillet 1994, 309 (6967), p. 94.
- Birley HD et al., "Immunisation contre l'hépatite B et arthrite réactive", BMJ, décembre 1994, 309 (6967), p. 1514.
- Gross et al., "Arthrite après vaccination contre l'hépatite B. Rapport de trois cas", Scand. J. Rheumatol., 1995, 24 (1), p. 50-52.
- Biasi D. et al., "Manifestations rhumatologiques suite à la vaccination contre l'hépatite B. Rapport de trois cas", Scand. J. Rheumatol., 1995, 24, p. 50-52.
- Aherne P. et al., "Psoriatic arthropathy", Irish Medical Journal, mars-avril 1995, 88 (2), p. 72.
- Harrison BJ et al., "Les patients qui développent une polyarthrite inflammatoire (PH) après la vaccination sont cliniquement impossibles à distinguer des autres patients atteints de PH", Br. J. Rheum., mars 1997, 36 (3), pp. 366-369.
- Bracci M. et al., "Polyarthrite associée à la vaccination contre l'hépatite B", Br. J. Rheumatol., février 1997, 36 (2), pp. 300-301.
- Pope JE et al., "Le développement de la polyarthrite rhumatoïde après vaccination recombinante contre l'hépatite B", J. Rheum., septembre 1998, 25 (9), pp. 1687-1693.
- Grasland A et al., "Maladie de Still de l'adulte après vaccination contre l'hépatite A et B ?", Rev. Internal Med., février 1998, 19 (2), p. 134-136.
- Maillefert JF et al., « Troubles rhumatismaux développés après vaccination contre l'hépatite B », Rheumatol. (Oxford), octobre 1999, 38 (10), p. 978-983.
- Toussirot E. et al., « Syndrome de Gougerot-Sjögren survenant après vaccination contre l'hépatite B », Arthritis Rheuma, septembre 2000, 43 (9), pp. 2139-2140.
- Ribera ER et al., "Polyneuropathie associée à l'administration du vaccin contre l'hépatite B", N. Engl. J. Med., 8 septembre 1983, 309 (10), p. 614-615.
- Shaw FE Jr. et al., "Surveillance post-commercialisation des événements indésirables neurologiques rapportés après la vaccination contre l'hépatite B. Expérience des trois premières années", Am. J. Epidemiol., février 1988, 27 (s), pp. 337-352 .
- Biron P. et al., "Myasthénie grave après anesthésie générale et vaccin contre l'hépatite B", Arch. Intern. Med., décembre 1988, 148 (12), p. 2685.
- Herroelen L. et al. , "Démyélinisation du système nerveux central après immunisation avec le vaccin recombinant contre l'hépatite B", The Lancet, 9 novembre 1991, 338 (8776), pp. 1174-1175.
- Tudela P. et al., "Lupus érythémateux systémique et vaccination contre l'hépatite B", Nephron, 1992, 62 (2), p. 236.
- Martinez E. et al., "Syndrome d'Evan déclenché par le vaccin recombinant contre l'hépatite B", Clin. Infect. Dis., 1992, 15, p. 1051.
- Ganry 0. et al., « Paralysie faciale périphérique suite à une vaccination contre l'hépatite B. À propos d'un cas », Therapie, 1992, 47, pp. 437-438.
- Waisbren BA, "L'envers de la médaille (lettre)", Inf Dis. Actualités, 1992, 5, p. 2.
- Trevisani F. et al., "Myélite transverse après vaccination contre l'hépatite B",]. of Hepatology, septembre 1993, 19 (2), p. 317-318.
- Mahassin F. et coll. , « Myélite aiguë après vaccination contre l'hépatite B », Presse Med., décembre 1993, 22 (40), pp. 1997-1998.
- Nadler JP, "Vaccination contre la sclérose en plaques et l'hépatite B", Clin. Infecter. Dis., novembre 1993, 17 (5), p. 928-929.
- Mamoux V. et al., "Lupus erthymatosus disseminatus et vaccination contre le virus de l'hépatite B", Arch. Pediatr., 1994, 1, pp. 307-309.
- Deisenhammer F. et al., "Ataxie cérébelleuse aiguë après immunisation avec le vaccin recombinant contre l'hépatite B", Acta Neurol. Scand., juin 1994, 89 (6), p. 462-463.
- Kaplanski G. et al., "Démyélinisation du système nerveux central après vaccination contre l'hépatite B et l'haplotype HLA", J. Neurol. Neurochirurgie. Psychiatrie, juin 1995, 58 (6), p. 758-759.
- Tartaglino LM et al., « Imagerie IRM dans un cas de myélite post-vaccinale », Am. J. Neuroradiol., 1995, 16 (3), pp. 581-582.
- Guiserix J., "Lupus érythémateux disséminé après vaccin contre l'hépatite B", Nephron, 1996, 74 (2), p. 441.
- Grezard P. et al., "Lupus érythémateux cutané et aphtose buccale après vaccination contre l'hépatite B chez un enfant de 6 ans", Ann. Dermatol. Vénérien., 1996, 123 (10), pp. 657-659.
- Manna R. et al., "Leucoencéphalite après vaccin recombinant contre l'hépatite B", J. of Hepatology, juin 1996, 24 (6), pp. 764-765.
- Mathieu E. et al., "cryoglobulinémie après vaccination contre l'hépatite B", Nouvelle-Angleterre]. Med., août 1996, 335 (5), p.335.
- Cohen AD. et al., "Auto-immunité induite par le vaccin", J. Autoimmunity, décembre 1996, 9 (6), pp. 699-703.
- Kakar A. et al., "Le syndrome de Guillain Barre associé à la vaccination contre l'hépatite B", Ind. J. Ped., septembre-octobre 1997, 64 (5), 710-712.
- Song HK et al., "Acute Myelitis after hepatitis B vaccination", J. Korean Med. Sci., juin 1997, 12 (3), pp. 249-251.
- Maillefert JF et al., "Neuropathie du nerf mental suite à la vaccination contre l'hépatite B", Chirurgie buccale, Médecine buccale, Pathologie buccale, Radiologie buccale et Endodontologie, juin 1997, 83 (6), pp. 663-664.
- Wise RP et al., "Perte de cheveux après vaccinations de routine", JAMA, 8 octobre 1997, 278 (14), pp. 1176-1178.
- Finielz P. et al, "Lupus érythémateux systémique et purpura thrombocytopénique chez deux membres de la même famille après le vaccin contre l'hépatite B", Nephrol. Cadran. Transplantation., 1998, 13 (9), pp. 2420-2421.
- Flemrner M. et al., "The Bald Truth", Am. J. Gastroenterol., avril 1999, 94 (4), p. 1104.
- Creange A et al., « Polyneuropathie démyélinisante aiguë lombo-sacrée après vaccination contre l'hépatite B », Autoimmunity, 1999, 30, pp. 143-146.
- Tourbah A. et al., « Encéphalite après vaccination contre l'hépatite B : encéphalite disséminée récurrente ou SEP ? », Neurology, 22 juillet 1999, 53 (2), pp. 396-401.
- Renard JL et al., "Myélite cervicale transverse aiguë après vaccination contre l'hépatite B. Evolution des anticorps anti-HBs", Presse Med., 3-10 juillet 1999, 28 (24), pp. 1290-1292.
- Gran B. et al., "Martin R. Développement de la sclérose en plaques après vaccination contre l'hépatite B", Neurol., 2000, 54 (suppl 3), A164.
- Sinsawaiwong S. et al., "Syndrome de Guillain-Barré suite au vaccin recombinant contre l'hépatite B et revue de la littérature", J. Med. Assoc. Thai., septembre 2000, 83 (9), p. 1124-1126.
- Konstantinou D. et al., "Deux épisodes de leucoencéphalite associés à une vaccination recombinante contre l'hépatite B chez un seul patient", Clin. Inf. Dis., 15 novembre 2001, 33, pp. 1772-1773.
- Heman MA et al., « Vaccin recombinant contre l'hépatite B et risque de sclérose en plaques : une étude prospective », Neurology, 2004, 63, pp. 838-842.
- Terney D. et al., « Sclérose en plaques après vaccination contre l'hépatite B chez un patient de 16 ans », Chinese Medical Journal, 2006, 119 (1), pp. 77-79.
- Yann M. et al., « Le vaccin contre l'hépatite B et le risque de démyélinisation inflammatoire du SNC chez l'enfant », Neurologie, 8 octobre 2008 [publié en ligne].
- Ness JM et al « Vaccins contre l'hépatite et sclérose en plaques pédiatrique. Le timing ou le type sont-ils importants ? », Neurology, 17 décembre 2008 (publié en ligne).
- Fried Met al., "Uvéite après vaccination contre l'hépatite B", The Lancet, 12 septembre 1987, pp. 631-632.
- Brezin A. et al., "Perte visuelle et éosinophilie après vaccin recombinant contre l'hépatite B", The Lancet, 28 août 1993, 342 (8870), pp. 563-564.
- Achiron LR et al., "Névrite optique post-infectieuse de l'hépatite B", Optom. Voir Sci., 1994, 71, p. 53-56.
- Brezin AP et al., "Épithéliopathie pigmentaire placoïde multifocale postérieure aiguë après vaccin contre l'hépatite B", Arch. Ophthalmol., mars 1995, 113 (3), pp. 297-300.
- Devin F. et al., "Occlusion de la veine centrale de la rétine après vaccination contre l'hépatite B", The Lancet, juin 1996, 347 (9015), p. 1626.
- Baglivo E. et al., "Syndrome de points blancs évanescents multiples après le vaccin contre l'hépatite B", Am. J. Ophthalmol., septembre 1996, 122 (3), pp. 431-432.
- Berkman N. et al., « Neuro-papillite bilatérale après vaccination contre l'hépatite B », Presse Med., 28 septembre 1996, 25 (28), p. 1301 (français).
- Bonfils P. et al., "Perception auditive fluctuante après le vaccin contre l'hépatite B", Ann. Otolaryngol. Chir. Cervicofac., 1996, 113 (6), pp. 359-361 (français).
- Granel B. et al., "Occlusion de la veine centrale rétinienne après vaccination contre l'hépatite virale B par vaccins recombinants. 4 cas", Presse Med., 1er février 1997, 26 (2), pp. 62-65 [français].
- Berkman N., « Un cas d'occlusion segmentaire unilatérale de la veine centrale de la rétine suite à une vaccination contre l'hépatite B », Presse Med., 26 avril 1997, 26 (14), p. 670 [français].
- Albitar S. et al., "Névrite optique rétrobulbaire bilatérale avec vaccination contre l'hépatite B", Nephrol. Cadran. Transplant, octobre 1997, 12 (10), p. 2169-2170.
- Arya SC, "Complications ophtalmiques des vaccins contre le virus de l'hépatite B", Int. Ophth., 1997, 21 (3), pp. 177-178.
- Orlando MP et al., "Perte auditive soudaine consécutive à la vaccination contre l'hépatite B : un rapport de cas", Annals of the New York Academy of Sciences, 29 décembre 1997, 830, pp.319-321.
- Biacabe B. et al., « Un rapport de cas de perte auditive neurosensorielle fluctuante après vaccination contre l'hépatite B », Auris, Nasus, Larynx, octobre 1997, 24, (4), pp. 357-360.
- Bourges JL et al., « Épithéliopathie placoïde multifocale et vaccination anti-hépatite B », J. Fr. Ophtalmol., novembre 1998, 21(9), pp. 696-700.
- Stewart O. et al., « Administration simultanée de vaccins contre l'hépatite B et la polio associée à une névrite optique bilatérale », Br. J. Ophthalmol., octobre 1999, 83 (10), pp.1200-1201.
- Fledelius HC, « Œdème papillaire unilatéral après vaccination contre l'hépatite B chez un patient migraineux. Un rapport de cas incluant des aspects médico-légaux", Acta Ophthalmol. Scand., décembre 1999, 77 (6), pp. 722-724.
- Voigt toi. et al., "Névrite du nerf optique après vaccination contre l'hépatite A, l'hépatite B et la fièvre jaune", Klin. Monatsbl. Augenheilkd., octobre 2001, 218 (10), pp. 688-690 (allemand).
- Cockwell P. et al., "Vasculite liée au vaccin contre l'hépatite B", BMJ, 1er décembre 1990, 301 (6763) p.1281.
- Allen MB et al., "Vasculite pulmonaire et cutanée suite à une vaccination contre l'hépatite B", Thorax, mai 1993, 48 (5), pp. 580-581.
- Nagafuchi S. et al., "Eosinophilia after intradermal hepatitis B vaccination", The Lancet, 1993, 342, p. 998.
- Poullin P. et al., "Purpura thrombocytopénique après vaccin recombinant contre l'hépatite B", The Lancet, novembre 1994, 344 (8932), p. 1293.
- Meyboom RH et al., "Thrombocytopénie signalée en association avec les vaccins contre l'hépatite B et A", The Lancet juin 1995, 345 (8965), p. 1638.
- Neau D. et al., "Purpura thrombocytopénique immunitaire après vaccin recombinant contre l'hépatite B : étude rétrospective de sept cas", Scan J. Infect Dis., 1998, 30 (2), pp. 115-118.
- Ronchi F. et al., "Purpura thrombocytopénique comme réaction indésirable au vaccin recombinant contre l'hépatite B", Arch. Dis. Child., mars 1998, 78 (3), p. 273-274.
- Muller A. et al., "Purpura thrombocytopénique : réaction indésirable à une immunisation combinée (hépatite B recombinante et vaccin rougeole-oreillons-rubéole) et après un traitement par Co-trimoxazole", Eur.]. Pédiatr., décembre 1999, 158 Suppi. 3, S209-10.
- Le Hello C. et al., « Vasculitis suspecté d'être lié à la vaccination contre l'hépatite B », J. of Rheumatology, janvier 1999, 26 (1), pp. 191-194.
- Rabaud C. et al., « Premier cas d'érythermalgie lié à la vaccination contre l'hépatite B », J. de Rheum., janvier 1999, 26 (1), pp. 233-234.
- De Keyser F. et al., « Pathologie à médiation immunitaire suite à la vaccination contre l'hépatite B » Deux cas de périartérite noueuse et un cas d'éruption médicamenteuse de type pityriasis rosé », Clin. Exp. Rheumatol., janvier-février 2000, 18 (1), pp. 81-85.
- Viallard JF et al., « Pancytopénie sévère déclenchée par le vaccin recombinant contre l'hépatite B », Br. J. Haematol., juillet 2000, 110 (1), pp. 230-233.
- Zaas A. et al., Vascularite des grosses artères après vaccination recombinante contre l'hépatite B. 2 cas", J. Rheumatol., mai 2001, 28 (S), pp.1116-11120.
- Conesa V. et al., "Purpura thrombocytopénique après vaccin recombinant contre l'hépatite B. Une association rare", Haematologica, mars 2001, 86 (3), E09 [italien].
- Goolsby PL, « Érythème noueux après le vaccin Recombivax HB contre l'hépatite B », N. Engl. J. Med., octobre 1989, 321, 1198-1199.
- Castresana-Isla CJ et al., "Érythème noueux et artérite de Talkayasu après immunisation avec un vaccin contre l'hépatite B dérivé du plasma", J. Rheumatol., août 1993, 20(8), pp. 1417-1418.
- 109. Trevisian G. et al., "Lichen ruber planus après vaccination contre le VHB". Acta Dermato-Venereotogica, février 1993, 73 (1), p. 73.
- Aubin F. et al., « Lichen plan suite à la vaccination contre l'hépatite B », Archives of Dermatology, octobre 1994 ; 130 (10), p. 1329-1330.
- Di Lernia V. et al., "Bisighini G. Erythema multiforme suite au vaccin contre l'hépatite B", Ped. Derma., décembre 1994, 11 (4), p. 363-364.
- Saywell, Californie. et al., "Kossard S. Lichenoid réaction to hepatitis B vaccination", Australasian J. Derm., août 1997, 38 (3), pp. 152-154.
- Dauod MS et al., « Anétodermie après vaccination contre l'hépatite B chez deux frères et sœurs »,/. Amer. Acad. Dermatol., mai 1997, 36 (5 Pt 1), pp. 779-780.
- Ferrando MF et al., "Lichen plan suite à la vaccination contre l'hépatite B", Br. J. Dermatol., août 1998, 139 (2) p. 350.
- Barbaud A. et al., "Mécanismes allergiques et urticaire/angio-œdème après immunisation contre l'hépatite B", Bt. J. Dermatot, novembre 1998, 139 (5), pp. 925-926.
- Schupp P. et al., "Lichen plan après vaccination contre l'hépatite B", Inter. J. of Dermat., octobre 1999, 38 (10), p. 799-800.
- Loche F. et al., "Erythème polymorphe associé à la vaccination contre l'hépatite B", Cfin. Exp. Dermatol., mars 2000, 25 (2), p. 167-168.
- Agrawal S. et al., "Lichen plan après vaccination contre le VHB chez un enfant : un rapport de cas du Népal", J. Dermatol., septembre 2000, 27 (9), pp. 618-620.
- Al-Khenaizan S., "Lichen plan survenant après vaccination contre l'hépatite B : un nouveau cas", J. Am. Acad. Dermatol., octobre 2001, 4S (4), pp. 614-615.
- Usman A. et al., « Éruption lichénoïde suite à la vaccination contre l'hépatite B : premier rapport de cas nord-américain ». Pediatr. Dermato J., mars-avril 2001, 18 (2) pp. 123-126.
- Lilic D. et al., « Dysfonctionnement hépatique et anticorps ADN après vaccination contre l'hépatite B », The Lancet, novembre 1994, 344 (8932), pp. 1292-1293.
- Macario F. et al., « Syndrome néphrotique après vaccin recombinant contre l'hépatite B", Clin. Nephrol., mai 1995, 43 (5), p. 349.
- Classen John Barthelow, "Immunisation des enfants et diabète sucré", New Zealand Med. J., 24 mai 1996, p. 195.
- Classen John Barthelow, « L'épidémie de diabète et le vaccin contre l'hépatite B », New Z. Med. J., 24 mai 1996, p. 366.
- Ranieri VM et al., « Inflammation du foie et syndrome de détresse respiratoire aiguë chez un patient recevant le vaccin contre l'hépatite B : une relation possible ? », Intensive Care Medicine, janvier 1997, 23 (1), pp. 119-121.
- Islek I. et al., « Syndrome néphrotique après vaccination contre l'hépatite B", Pediatr. Nephrol., janvier 2000, 14, pp. 89-90.
- Snider GB et al., « Une possible réaction systémique au vaccin contre l'hépatite B », JAMA. 1er mars 1985, 253 (9), p. 1260-1261.
- AADRAC, "Australian Adverse Drug Reactions Advisory Committee: Reactions to hepatitis B vaccines", Australian Adverse Drug Reactions Bulletin, août 1990.
- Germanaud J. et al., "Un cas de cytolyse sévère après vaccination contre l'hépatite B", Amer. J. Med., juin 1995, 98 (6), p. 595-S96.
- Fisher BL, Ed., « Vaccin contre l'hépatite B : l'histoire inédite », The Vaccine Reaction, National Vaccine Information Center, septembre 1998.
- Belkin Michael, « Thalidomide mandatée par le gouvernement pour les bébés », WorldNetDaily, 25 janvier 1999, worldnetdaily.com
- Howd A., « Once of Prevention, Pound of Misery », Insight Magazine, 12 mars 1999,
- Bethell T., « Shots in the Dark ». American Spectator. Mai 1999.
- Wallstin B., « Immune to Reason », The Houston Press, 3 juin 1999, www.houstonpress.com
- Shaw FE, « Le tumulte suscité par un conservateur peu connu, le thimérosal, bouscule la politique américaine en matière de vaccin contre l'hépatite B », Hepatitis Control Report, été 1999, vol. 4, no. 2.
- Spalding BJ, « Miracle ou meurtre ? La controverse sur le vaccin contre l'hépatite B", Biospace.com, 11 novembre 1999, www.biospace.com
- Science, 31 juillet 1998.
- "La France suspend l'utilisation du vaccin contre l'hépatite B". https://www.bmj.com/content/317/7165/1034.2
- Cantwell A., "L'expérience gay qui a déclenché le SIDA en Amérique", Not Aids, 13 janvier 2006, maintenant dans http://rense.com/general68/gayex.htm
- Merck & Co.t Inc., Recombivax HB Hepatitis B Vaccine (Recombinant), notice d'emballage en date de juin 2005 ; GlaxoSmithKline Biologicals, Engerix-B (vaccin contre l'hépatite B (recombinant), notice d'emballage en décembre 2005.
- Wainwright RB et al., "Durée de l'immunogénicité et efficacité du vaccin contre l'hépatite B dans une population Yupik Eskimo, résultats préliminaires d'une étude de 8 ans", dans "hépatite virale et maladie du foie", Hollinger FB et al. (éd.) , Williams et Wilkins, 1990, pages 762 à 766.
- Hadler SC et al., « Évaluation de la protection à long terme par le vaccin contre l'hépatite B pendant 7 à 9 ans chez les hommes homosexuels ». dans Hépatite virale et maladie du foie, Hollinger FB et al. (éd.), Williams et Wilkinst 1990, p. 766-768.
- Hadler SC et al., « Immunogénicité à long terme et efficacité du vaccin contre l'hépatite B chez les hommes homosexuels », NEJM, 24 juillet 1986, 315, pp. 209-214.
- Stevens CE et al., "Perspectives de contrôle de l'infection par le virus de l'hépatite B : implications de la vaccination des enfants et de la protection à long terme", Pediatrics, 1992, 90, pp. 170-173.
- Street AC et al., « Persistance des anticorps chez les personnels soignants vaccinés contre l'hépatite B », Infec. Hôpital de contrôle. Epidem., 1990, 11, p. 525-530.
- Pasko MT et al., "Persistance des anti-HBs parmi le personnel de santé immunisé avec le vaccin contre l'hépatite B", American Journal of Public Health, 1990, 80, pp. 590-593.
- Organisation mondiale de la santé, ccVaccins contre l'hépatite B : immunogénicité réévaluée'', WHO Drug Infor., 1994, 8 (2).
- Ballinger, AB et al., "Infection aiguë sévère par l'hépatite B après vaccination", The Lancet, 1994, 344, pp.1292-1293
- Goffin E. et al., "Infection aiguë par l'hépatite B après vaccination", The Lancet, 1995, 345, p. 263.
Vaccins: A Guide to Informed Choice par Neil Z. Miller (Auteur) et Claudia Benatti (Traductrice)
Éditions Terra Nuova, 2018

