Le vaccin contre le pneumocoque peut-il causer des blessures et/ou la mort ?

NOTE IMPORTANTE: Corvelva vous invite à vous informer en profondeur en lisant toutes les rubriques et liens, ainsi que les notices produits et fiches techniques des fabricants, et à vous entretenir avec un ou plusieurs professionnels de confiance avant de décider de vous faire vacciner ou de vacciner votre enfant. Ces informations sont fournies à titre informatif uniquement et ne constituent pas un avis médical.
Le problème des vaccins multiples (cliquez pour ouvrir)
Le problème des vaccins multiples

Les calendriers de vaccination actuels, notamment pour l'âge pédiatrique, prévoient l'administration de plusieurs antigènes et vaccins en une seule séance, privilégiant le confort au détriment de la sécurité. Afin de pouvoir prononcer un discours précis sur la sécurité des vaccins, il faut nécessairement prendre en considération la complexité du phénomène, en conseillant à tous les lecteurs de s'informer adéquatement sur tous les aspects de la vaccination, les avantages et les inconvénients.
Le Dr Russell Blaylock, professeur assistant clinique de neurochirurgie au centre médical de l'Université du Mississippi, a étudié la "synergie toxique" pendant des années et a pu observer que lorsque deux pesticides faiblement toxiques, où aucun n'est capable de provoquer le syndrome de Parkinson chez des animaux de laboratoire, sont combinés les uns aux autres, peuvent provoquer la maladie même rapidement et compare ce phénomène à celui de plusieurs vaccins administrés simultanément : "Les vaccinations, si elles sont trop nombreuses et trop rapprochées, se comportent comme une maladie chronique".(une). Autres Deux études ont confirmé que la mort subite du nourrisson peut survenir après l'inoculation de plusieurs vaccins en une seule administration.(avant JC)
Une étude publiée dans Human and Experimental Toxicology a montré que les pays qui prescrivent plus de vaccins aux enfants ont tendance à avoir des taux de mortalité infantile plus élevés.(D) Par exemple, aux États-Unis, où les enfants reçoivent 26 vaccins, plus de 6 enfants meurent pour 1000 12 naissances vivantes, tandis qu'en Suède et au Japon, où 3 vaccins pédiatriques sont administrés, 1000 décès sont signalés pour XNUMX XNUMX naissances vivantes. Dans l'étude susmentionnée, le lien entre les vaccins et le SMSN est également pris en compte.
D'après une étude suisse publiée en 2005 dans le European Journal of Pediatrics(E) il en résulte que, concernant les effets sur les prématurés, l'incidence des apnées et bradycardies récurrentes ou accrues après administration de vaccins hexavalents est de 13 %. Cette même année, le même journal a publié une étude allemande qui avait examiné les morts subites du nourrisson après hexavalent. Les auteurs écrivent : « Ces résultats, basés sur des rapports spontanés, ne prouvent pas une relation causale entre la vaccination et la mort subite du nourrisson, mais constituent un signal concernant l'un des deux hexavalents disponibles ; signal qui devrait conduire à intensifier la surveillance des morts subites du nourrisson après vaccination ».(F)
En 2006, il a été publié dans la revue médicale Vaccine(G) la lettre d'une équipe de chercheurs de l'Université de Munich qui fait état de « six cas de mort subite de nourrisson après vaccination hexavalente.. Tous retrouvés morts sans explication 1-2 jours après vaccination ». Ils avaient été classés comme cas typiques de mort subite du nourrisson mais la vérification autooptique avait révélé des anomalies neuropathologiques et histologiques et tous les enfants présentaient un œdème cérébral important qui les faisait faire exception par rapport aux autres cas de SMSN (Syndrome de mort subite du nourrisson). Les chercheurs ont écrit qu'« avant l'introduction du vaccin hexavalent (dans les années 1994-2000), nous n'avions observé le cas que d'un enfant sur 198 mort subite du nourrisson qui décédait peu après la vaccination DTC. Mais entre 2001 et 2004, ils avaient identifié cinq cas similaires sur 74 avec le SMSN. Cela indiquerait une multiplication par treize."
Aussi en 2006 sur Virchows Archive(H), l'équipe de l'Institut de pathologie de l'Université de Milan a écrit : « Des experts de l'Agence européenne pour l'évaluation des produits médicaux ont analysé la possibilité qu'il puisse y avoir un lien entre les vaccins hexavalents et certains cas de décès. Parmi les participants figuraient des pathologistes expérimentés dans les vaccins et la mort subite du nourrisson qui ont effectué les autopsies.Mais, à notre connaissance, peu d'attention a été accordée à l'examen du tronc cérébral et du cœur sanguin sur des coupes en série et il n'y avait aucune possibilité d'établir un rôle déclencheur. du vaccin pour ces décès. Nous rapportons ici le cas d'une fillette de 3 mois décédée subitement après vaccination hexavalente. L'examen du tronc cérébral sur des coupes sériées a révélé une hypoplasie bilatérale du noyau arqué. Le système de conduction du cœur présentait une dispersion et une dégénérescence fœtale persistantes. Ce cas offre une compréhension unique du rôle possible du vaccin hexavalent dans le déclenchement d'une conséquence mortelle chez un enfant vulnérable. Tout cas de mort subite et inattendue qui survient peu après la naissance ou dans la petite enfance, surtout s'il fait suite à une vaccination, doit toujours subir une autopsie complète, conformément aux directives.
Références
- Blaylock R, "Vaccinations : les dangers cachés", The Blaylock Wellness Report, mai 2004, pp.1-9
- Ottaviani G. et al., "Syndrome de mort subite du nourrisson (SMSN) peu de temps après la vaccination hexavalente : une autre pathologie chez les suspects de SMSN ?", Virchows Archiv., 2006, 448, p. 100-104.
- Zinka B. et al., "Cas inexpliqués de mort subite du nourrisson peu de temps après la vaccination hexavalente", Vaccine, juillet 2006, 24 (31-32), pp. 5779-5780.
- Miller NZ et al1. , "Les taux de mortalité infantile ont régressé par rapport au nombre de doses de vaccin administrées en routine : existe-t-il une toxicité biochimique ou synergique ??", Hum. Exp. Toxicol., mai 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Le problème de l'aluminium (cliquez pour ouvrir)
Aluminium dans les vaccins : ce que les parents doivent savoir

1. Qu'est-ce que l'aluminium ?
L'aluminium est un métal léger blanc argenté, malléable et résistant. Ces qualités le rendent utile dans de nombreuses industries et produits, notamment les machines, la construction, les entrepôts, les ustensiles de cuisine, les ustensiles de cuisine, les textiles, les teintures et les cosmétiques. L'aluminium est également le métal le plus abondant dans la croûte terrestre, et pratiquement tout l'aluminium présent dans l'environnement se trouve dans le sol. Cependant, l'aluminium ne se trouve pas naturellement en quantités significatives dans les organismes vivants (tels que les plantes et les animaux) et n'a aucune fonction biologique connue. Au cours du siècle dernier, l'utilisation de l'aluminium dans certains produits a entraîné une exposition humaine accrue. Les principales sources d'exposition sont les aliments contenant de l'aluminium (p. ex. poudre à pâte, aliments transformés, préparations pour nourrissons, etc.), les produits médicaux (p. ex. antisudorifiques, antiacides, etc.), les injections contre les allergies et les vaccins .1-3
2. Pourquoi l'aluminium est-il présent dans les vaccins ?
Certains vaccins utilisent des composés d'aluminium (hydroxyde d'aluminium et phosphate d'aluminium) comme adjuvants, qui sont des ingrédients qui augmentent la réponse immunitaire à un antigène (substance étrangère).4-5 La Food and Drug Administration (FDA) des États-Unis affirme que si certains vaccins ne contiennent pas d'aluminium, la réponse immunitaire qu'ils déclenchent pourrait diminuer.6
3. Quels vaccins contiennent de l'aluminium ?
Les vaccins suivants contiennent de l'aluminium et sont administrés aux nourrissons, aux enfants et aux adolescents (Fig. 1) :
- Hépatite B (HepB)
- hexavalent
- Diphtérie, tétanos et coqueluche (DTaP et Tdap)
- Haemophilus influenzae de type b (PedvaxHIB)
- Pneumocoque (PCV)
- Hépatite A (HepA)
- Virus du papillome (VPH)
- Méningocoque B (MenB)
Figure 1 : Jusqu'à 18 doses de vaccins contenant de l'aluminium sont administrées de la naissance à 22 ans7-8
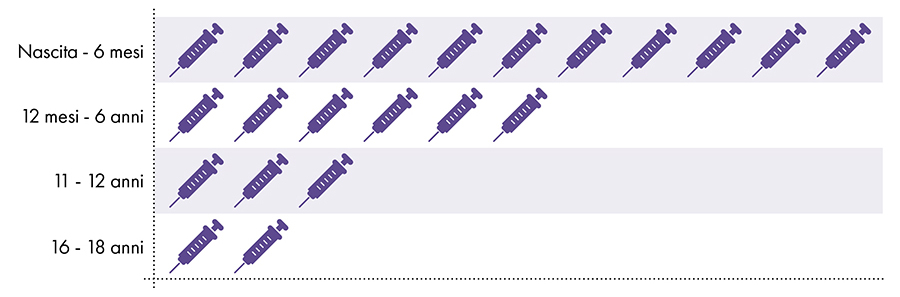
4. L'exposition à l'aluminium est-elle sans danger ?
La FDA considère l'aluminium généralement reconnu comme sûr (GRAS) depuis 1975.9 Cependant, avant 1990, il n'existait aucune technologie permettant de détecter avec précision de petites quantités d'aluminium administrées à des sujets dans le cadre d'études scientifiques.10 Par conséquent, la quantité d'aluminium pouvant être absorbée avant l'apparition des effets indésirables était inconnue.
Depuis les années 1990, grâce aux progrès technologiques, on a observé que les petites quantités d'aluminium qui restent dans le corps humain interfèrent avec un certain nombre de processus cellulaires et métaboliques dans le système nerveux et les tissus d'autres parties du corps.1-10-11 Les effets négatifs les plus importants de l'aluminium ont été observés sur le système nerveux et vont de l'altération de la motricité à l'encéphalopathie (altération de l'état mental, changements de personnalité, difficultés de réflexion, perte de mémoire, convulsions, coma, etc.).2-12
Le ministère américain de la Santé et des Services sociaux (HHS) reconnaît l'aluminium comme une neurotoxine connue.2 De plus, la FDA a mis en garde contre les risques de toxicité de l'aluminium chez les nourrissons et les enfants.13
FEDERAL REGISTER : Le quotidien du gouvernement des États-Unis"Même les nourrissons nés à terme avec une fonction rénale normale peuvent être à risque en raison de la croissance rapide et de l'immaturité du cerveau et du squelette, ainsi que de l'immaturité de la barrière hémato-encéphalique. Jusqu'à l'âge de 1 ou 2 ans, les nourrissons ont un taux de filtration glomérulaire supérieur à celui des adultes, ce qui affecte leur fonction rénale. L'agence craint que les jeunes enfants et les personnes dont la fonction rénale est immature présentent un risque accru d'exposition à l'aluminium." |
5. Quelle quantité d'aluminium par voie orale n'est pas sûre ?
En 2008, l'Agence pour les substances toxiques et le registre des maladies (ATSDR), une division du HHS, a utilisé des études sur les effets neurotoxiques de l'aluminium pour déterminer que pas plus de 1 milligramme (1.000 XNUMX microgrammes) d'aluminium par kilogramme de poids corporel par jour pour éviter les effets négatifs de l'aluminium.2
6. Quelle quantité d'aluminium injectée n'est pas sûre ?
Pour déterminer la quantité d'aluminium qui peut être injectée en toute sécurité, il est nécessaire de convertir la limite orale d'aluminium de l'ATSDR. La limite ATSDR pour l'aluminium par voie orale (1.000 0,1 microgrammes d'aluminium par kilogramme de poids corporel par jour) est basée sur XNUMX % de l'aluminium par voie orale qui est absorbé dans la circulation sanguine, car le tube digestif bloque la quasi-totalité de l'aluminium par voie orale .2 À l'inverse, l'aluminium injecté par voie intramusculaire contourne le tube digestif et 100 % de l'aluminium peut être absorbé dans la circulation sanguine avec le temps (c'est-à-dire que la proportion d'aluminium absorbée est 1.000 1000 fois supérieure). Pour tenir compte de ces différentes quantités d'absorption, la limite orale d'aluminium de l'ATSDR doit être divisée par 1. Cette conversion conduit à une limite d'aluminium sanguin dérivée de l'ATSDR de 0,1 microgramme d'aluminium (1.000% de 1 microgrammes) par kilogramme de poids corporel par jour. Par conséquent, pour éviter les effets neurotoxiques de l'aluminium, pas plus de 3 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine. La figure XNUMX montre la limite d'aluminium sanguin dérivée de l'ATSDR pour les nourrissons de différents âges en fonction de leur poids.
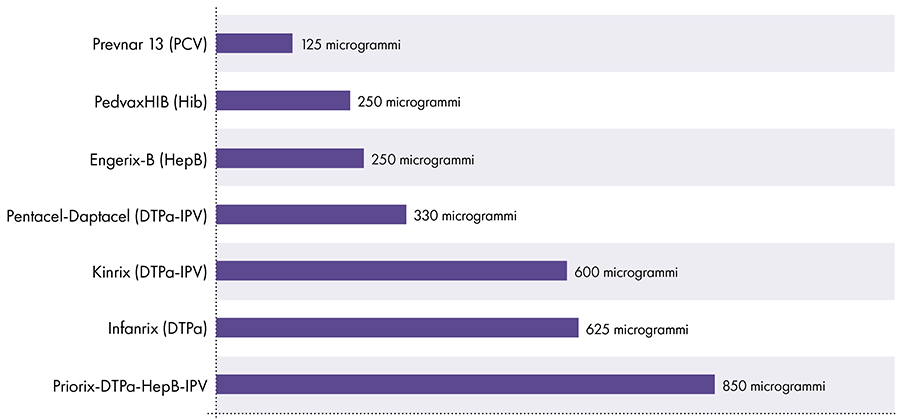
7. Combien d'aluminium y a-t-il dans les vaccins ?
La quantité d'aluminium dans les vaccins varie.16 En 1968, le gouvernement fédéral américain a fixé la limite de la quantité d'aluminium dans les vaccins à 850 microgrammes par dose, en fonction de la quantité d'aluminium nécessaire pour rendre certains vaccins efficaces.6-17 Par conséquent, la quantité d'aluminium dans les vaccins pour nourrissons contenant de l'aluminium varie de 125 à 850 microgrammes par dose. La figure 4 montre la teneur en aluminium d'une dose de divers vaccins administrés aux enfants.
8. Des études ont-elles comparé la quantité d'aluminium dans les vaccins avec la limite dérivée de l'Agence pour les substances toxiques et le registre des maladies (ATSDR) ?
En 2011, une étude a été publiée qui visait à comparer la quantité d'aluminium dans les vaccins avec la limite de flux sanguin fixée par l'ATSDR.18 Cependant, cette étude a incorrectement basé ses calculs sur 0,78% d'aluminium oral absorbé dans la circulation sanguine, plutôt que sur la valeur de 0,1% utilisée par l'ATSDR dans ses calculs.19-20 En conséquence, l'étude de 2011 a émis l'hypothèse que près de 8 fois (0,78 % / 0,1 %) l'aluminium peut pénétrer en toute sécurité dans la circulation sanguine, ce qui a conduit à une conclusion erronée.
9. L'exposition à l'aluminium provenant des vaccins est-elle sans danger ?
Les vaccins sont injectés par voie intramusculaire, et la vitesse à laquelle l'aluminium des vaccins migre du muscle humain dans la circulation sanguine est inconnue. Des études animales suggèrent que l'aluminium des vaccins peut prendre de quelques mois à plus d'un an pour pénétrer dans la circulation sanguine, en raison de multiples variables.21-23 Étant donné que l'exposition cumulée à l'aluminium provenant des vaccins chez les enfants de moins d'un an dépasse de plusieurs centaines la limite quotidienne fixée par l'ATSDR (Fig. 3 et 4), la limite serait tout de même dépassée si l'aluminium provenant des vaccins pénétrait dans le flux sanguin au cours du cycle d'environ un an. De plus, certaines études ont montré que l'aluminium des vaccins est absorbé par les cellules immunitaires et atteint des parties du corps éloignées du site d'injection, y compris le cerveau.24
L'ampleur des effets indésirables de l'aluminium dans les vaccins est inconnue, car aucune étude de sécurité comparant une population vaccinée avec des vaccins contenant de l'aluminium à une population non vaccinée avec de tels vaccins n'a été menée.
Limitation en aluminium du flux sanguin dérivée de l'ATSDR2-14-15
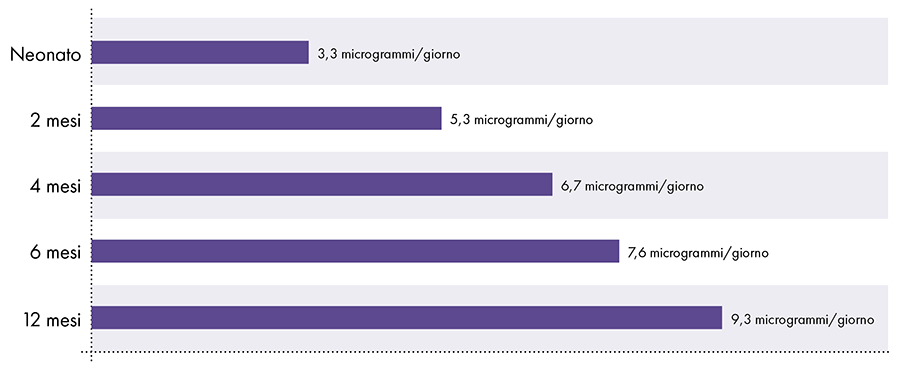 Figure 3 : Ce graphique montre la limite d'aluminium pour les enfants de différents âges, telle que dérivée du Registre des substances toxiques et des maladies, une division du Département de la santé et des services sociaux des États-Unis. La limite indique que pas plus de 1 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine pour éviter les effets neurotoxiques de l'aluminium.
Figure 3 : Ce graphique montre la limite d'aluminium pour les enfants de différents âges, telle que dérivée du Registre des substances toxiques et des maladies, une division du Département de la santé et des services sociaux des États-Unis. La limite indique que pas plus de 1 microgramme d'aluminium par kilogramme de poids corporel ne doit pénétrer quotidiennement dans la circulation sanguine pour éviter les effets neurotoxiques de l'aluminium.
Quantité d'aluminium dans les vaccins
Références
- American Academy of Pediatrics, Comité sur la nutrition. Toxicité de l'aluminium chez les nourrissons et les enfants. Pédiatrie. 1996 mars; 97 (3): 413.
- Agence pour les substances toxiques et le registre des maladies (ATSDR). Profil toxicologique de l'aluminium. Washington, DC : Département américain de la santé et des services sociaux ; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. L'aluminium dans les aliments — la nature et la contribution des additifs alimentaires. Dans : El-Samragy Y, éditeur. Additif alimentaire. Rijeka (Croatie) : InTech ; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Vers une compréhension de l'action adjuvante de l'aluminium. Nat Rev Immunol. avril 2009; 9 (4): 287.
- Volk VK, Bunney WE. Immunisation contre la diphtérie avec l'anatoxine liquide et l'anatoxine précipitée à l'alun. Am J Santé publique Nations Health. juillet 1942; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Sels d'aluminium dans les vaccins - perspective américaine. Vaccin. 2002 mai 31 ; 20 Suppl 3 : S18-22.
- Administration américaine des aliments et médicaments. Silver Spring (MD) : Administration américaine des produits alimentaires et pharmaceutiques. Vaccins autorisés à être utilisés aux États-Unis ; [mis à jour le 2018 février 14 ; cité le 2018 février 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Calendrier de vaccination recommandé pour les enfants et les adolescents âgés de 18 ans ou moins, États-Unis, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Administration américaine des aliments et médicaments. Silver Spring (MD) : Administration américaine des produits alimentaires et pharmaceutiques. SCOGS (Comité restreint sur les substances GRAS); [cité le 2018 août 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Prêtre ND. Le comportement biologique et la biodisponibilité de l'aluminium chez l'homme, avec une référence particulière aux études utilisant l'aluminium-26 comme traceur : revue et mise à jour de l'étude. J EnvironMonit. 2004 ; 6 : 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminium dans les produits de nutrition parentérale pédiatrique : contenu mesuré par rapport au contenu indiqué sur l'étiquette. J Pediatr Pharmacol Ther. 2011 ; 16 (2) : 92-7.
- Sedman A. Toxicité de l'aluminium chez l'enfant. Pédiatre Néphrol. juillet 1992; 6 (4): 383-93.
- Food and Drug Administration des États-Unis, ministère de la Santé et des Services sociaux. Règles et règlements. Registre de la Fed. juin 2003; 68 (100): 34286.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Centre national des statistiques sur la santé : tableau de données pour les graphiques de longueur pour l'âge et de poids pour l'âge des garçons ; [cité le 2019 avril 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centres pour le Contrôle et la Prévention des catastrophes. Washington, DC : Département américain de la santé et des services sociaux. Centre national des statistiques sur la santé : tableau de données pour les graphiques taille-pour-âge et poids-pour-âge des filles ; [cité le 2019 avril 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Food and Drug Administration des États-Unis, ministère de la Santé et des Services sociaux. Révision des exigences relatives aux matériaux constitutifs. Règle finale. Registre de la Fed. 2011 avril 13 ; 76 (71) : 20513-8.
- Office of the Federal Register, National Archives and Records Service, General Services Administration. Règles et règlements. Registre de la Fed. janvier 1968 ; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Mise à jour de la pharmacocinétique de l'aluminium à la suite d'expositions infantiles par l'alimentation et la vaccination. Vaccin. 2011 28 novembre ; 29 (51) : 9538-43.
- Miller S, médecins pour le consentement éclairé. Erratum dans « Mise à jour de la pharmacocinétique de l'aluminium à la suite d'expositions infantiles par l'alimentation et la vaccination ». Dans : ResearchGate. Berlin (Allemagne) : ResearchGate GmbH ; 2020 mars 6 [cité le 2020 mars 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Médecins pour le consentement éclairé. Newport Beach (CA) : Médecins pour un consentement éclairé. Erratum dans « Mise à jour de la pharmacocinétique de l'aluminium suite à l'exposition de nourrissons par l'alimentation et la vaccination » ; [cité le 2020 mars 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorption in vivo d'adjuvants vaccinaux contenant de l'aluminium à l'aide de 26Al. Vaccine 1997 août-sept ; 15 (12-13) : 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminium dosage et évaluation de la réaction locale à plusieurs moments après l'administration intramusculaire de vaccins contenant de l'aluminium chez le singe Cynomolgus. Vaccin. 2005 février 3 ; 23 (11) : 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminium dans le plasma et les tissus après injection intramusculaire de vaccins humains avec adjuvant chez le rat. Arch Toxicol. 2019 octobre ; 93 (10) : 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Analyse critique des études de référence sur la toxicocinétique des adjuvants à base d'aluminium. J Inorg Biochem. avril 2018 ; 181 : 87-95.
Article traduit par Médecins pour un consentement éclairé
Selon le CDC américain, les problèmes qui peuvent survenir après la vaccination avec le vaccin antipneumococcique conjugué 13-valent (PCV13), le vaccin antipneumococcique polysaccharidique 23-valent (PPSV23) et tout autre vaccin comprennent :(1)
- Réactions allergiques graves qui surviennent quelques minutes ou heures après la vaccination.
- Douleur intense à l'épaule qui limite les mouvements du bras dans lequel a eu lieu l'administration.
- Évanouissement ou effondrement après la vaccination. Il peut vous être conseillé de rester assis ou allongé pendant environ 15 minutes après la vaccination pour éviter les évanouissements et les blessures pouvant résulter d'une chute. Il est important d’informer votre médecin si vous ressentez des bourdonnements d’oreilles, des changements de vision ou des étourdissements après la vaccination.
Effets secondaires du vaccin PCV13 (vaccin conjugué contre le pneumocoque)
Les effets indésirables consécutifs à l'administration du PCV13 varient en fonction de la dose de la série et de l'âge du receveur. Chez les enfants, les réactions les plus fréquemment signalées étaient l'irritabilité, la somnolence, la perte d'appétit, la rougeur, la douleur ou l'enflure au site de vaccination et une fièvre légère ou modérée.
Les enfants qui ont reçu le PCV13 en même temps que le vaccin antigrippal inactivé couraient un risque accru de convulsions fébriles.
Chez les adultes, des rougeurs, des gonflements et des douleurs au site d'injection, de la fatigue, de la fièvre, des frissons, des maux de tête et des douleurs musculaires ont été rapportés.(3)
Effets indésirables de Prevenar 13 (PCV13) rapportés chez les nourrissons et les enfants au cours des essais cliniques préalables à l'approbation :(4) douleur au site d'injection, gonflement, rougeur, fièvre, diminution de l'appétit, augmentation et diminution de la somnolence, irritabilité, diarrhée, vomissements, éruption cutanée, urticaire, réaction d'hypersensibilité incluant bronchospasme, gonflement du visage et essoufflement, convulsions, pneumonie, gastro-entérite, bronchiolite, décès (déclaré comme PEID).
Effets indésirables de Prevenar 13 (PCV13) rapportés chez les adultes au cours des essais cliniques de pré-approbation :(5) douleur, gonflement et rougeur au site d'injection, limitation des mouvements du bras, fièvre, vomissements, frissons, douleurs musculaires, fatigue, maux de tête, diminution de l'appétit, éruption cutanée, douleurs articulaires, décès (les décès signalés lors de l'approbation des études précliniques comprenaient des décès dus au cancer). , maladie cardiaque, péritonite, infection pulmonaire à complexe Mycobacterium avium et choc septique).
Effets indésirables de Prevenar 13 (PCV13) rapportés après la commercialisation :(6) Cyanose, lymphadénopathie au site d'injection, anaphylaxie, choc, hypotonie, pâleur, apnée, œdème angioneurotique, érythème polymorphe, prurit au site d'injection, urticaire et éruption cutanée.
Essais cliniques de pré-approbation du premier vaccin antipneumococcique conjugué, Prevenar (PCV7), a comparé l'innocuité de Prevenar (PCV7) avec un vaccin expérimental contre la méningite C, compromettant sérieusement la validité scientifique de l'essai.
Lors des essais cliniques antérieurs à l'autorisation de Prevenar (PCV7), les enfants des groupes ayant reçu le vaccin antipneumococcique ont davantage souffert de convulsions, d'irritabilité, de forte fièvre et d'autres réactions. Dans le groupe Prevenar (PCV7), il y a eu 12 décès, dont 5 décès dus au syndrome de mort subite du nourrisson (SMSN). Aucune étude à long terme n'a été réalisée pour évaluer si le vaccin Prevenar (PCV7), administré seul ou en association avec d'autres vaccins, est associé à des maladies chroniques ou à des handicaps, tels que le développement du diabète, de l'asthme, des troubles épileptiques, des difficultés d'apprentissage. , TDAH.(7)
Les essais cliniques d'innocuité préalables à l'approbation du Prevenar 13 (PCV13) ont comparé ce vaccin de nouvelle génération au vaccin Prevenar original (PCV7), un vaccin dont l'innocuité n'a pas été suffisamment étudiée, et des inquiétudes concernant un lien ont été signalées en 2012 entre les convulsions fébriles et Prevenar 13 (PCV13).(8)
Le PCV13 était associé à un risque élevé de convulsions fébriles lorsqu'il était administré indépendamment(10) et lorsqu'il a été administré en association avec un vaccin antigrippal inactivé (VII) parentéral.(11)
Certaines études ont également établi un lien entre le vaccin PCV et le syndrome de Guillain-Barré,(12) à la polysérosite,(13) à l'épaule septique(14) et érythème polymorphe.(15)
Effets secondaires du vaccin PPSV23 (Pneumocoque polysaccharide)
Selon le CDC, environ 50 % des personnes qui reçoivent le vaccin polysaccharidique contre le pneumocoque (PPSV23) ressentent des douleurs et des rougeurs au site d'injection. Des douleurs musculaires, de la fièvre et des réactions localisées plus graves peuvent également survenir après l'administration de PPSV23.(16)
Effets indésirables du PNEUMOVAX23 (PPSV23) rapportés chez les adultes au cours des essais cliniques préalables à l'approbation aux États-Unis :(17) douleur au site d'injection, rougeur, démangeaisons, ecchymoses et gonflement, maux de tête, frissons, fièvre, diarrhée, dyspepsie, nausées, infection des voies respiratoires supérieures, maux de dos, douleurs au cou, pharyngite, douleurs musculaires, fatigue, dépression, colite ulcéreuse, douleur thoracique, angine de poitrine, insuffisance cardiaque, tremblements, raideur, transpiration, accident vasculaire cérébral, radiculopathie lombaire, pancréatite, infarctus du myocarde, décès.
Près de 80 % des sujets participant aux essais cliniques de pré-approbation ont présenté une réaction indésirable au site d'injection après une revaccination trois à cinq ans après le vaccin initial. Le taux d'effets indésirables systémiques (céphalées, fatigue, myalgie) suite à une revaccination par le PPSV23 était également plus élevé, avec 33 % des adultes âgés de 65 ans et plus et 37,5 % des adultes âgés de 50 à 64 ans ayant signalé un effet indésirable.(18)
Effets indésirables de PNEUMOVAX23 (PPSV23) rapportés après la commercialisation :(19) Réactions anaphylactoïdes, maladie sérique, œdème angioneurotique, arthrite, arthralgie, vomissements, nausées, diminution de la mobilité des membres, œdème périphérique du membre injecté, fièvre, malaise, cellulite, chaleur au site d'injection, lymphadénopathie, lymphadénite, leucocytose, thrombocytopénie chez les patients présentant purpura thrombocytopénique idiopathique stabilisé, anémie hémolytique chez les patients ayant présenté d'autres troubles hématologiques, paresthésies, syndrome de Guillain-Barré, radiculoneuropathie, convulsions fébriles, éruption cutanée, érythème polymorphe, urticaire, réactions de type cellulite.
Bien que PNEUMOVAX23 (PPSV23) soit approuvé pour une utilisation chez les enfants âgés de deux ans et plus atteints de maladies telles qu'une maladie cardiaque et pulmonaire chronique, le diabète, les implants cochléaires, les fuites de liquide céphalo-rachidien, la drépanocytose, l'asplénie fonctionnelle ou anatomique et l'immunosuppression, il existe aucune information sur l'innocuité ou l'efficacité du vaccin chez les enfants dans la notice du vaccin.(20)
Certaines études ont lié le PPSV23 à des réactions inflammatoires systémiques(21) et fièvre.(22-23-24-25-26)
Références (cliquez pour ouvrir)
- CDC Conjugué pneumococcique (PCV13) VIS. 5 novembre 2015
- CDC Polysaccharide pneumococcique VIS. Avril 24, 2015
- CDC Conjugué pneumococcique (PCV13) VIS. 5 novembre 2015
- FDA Notice d'emballage Prevnar 13 Août 22, 2017
- Ibid
- Ibid
- FDA Vaccin conjugué contre le pneumocoque à 7 valences (PREVNAR) - Notice du fabricant du produit. Le 1 octobre 2002
- Hitt, E. Prevnar 13 devrait être surveillé pour le risque de convulsions fébriles, selon le panel de la FDA. Paysage médical. Le 31 janvier 2012
- Tse A, Tseng HF, Greene SK et al. Identification et évaluation des signaux pour le risque de convulsions fébriles chez les enfants après un vaccin antigrippal trivalent inactivé dans le cadre du projet Vaccine Safety Datalink, 2010-2011. Vaccinez. 2012 mars 2;30(11):2024-31
- Baker M, Jankosky C, Yih K et al. Le risque de convulsions fébriles après les vaccins conjugués contre la grippe et le pneumocoque 13-valents. Forum ouvert Infect Dis. Automne 2017 ; 4 (Supplément 1) : S464 – S465.
- CDC Vaccins infantiles et convulsions fébriles Jun. 20, 2016
- Ravishankar,N Syndrome de Guillain-Barré après le vaccin PCV. J Neurol Neurochirurgie 4 (1): 134
- Tawfik P, Elie Gertner E, McEvoy CE Polysérosite sévère induite par le vaccin antipneumococcique conjugué 13-valent : à propos d'un cas J Med Case Rep. 2017; 11: 142.
- DeRogatis MJ, Parameswaran L, Lee P et al. Articulation septique de l'épaule après une vaccination contre le pneumocoque nécessitant un débridement chirurgical. HSS J. 2018 Oct;14(3):299-301
- Monastirli A, Pasmatzi E, Badavanis G et al. Érythème polymorphe suite à une vaccination antipneumococcique. Acta Dermatovenerol Alp Pannonica Adriat. 2017 Mar;26(1):25-26.
- CDC Polysaccharide pneumococcique VIS. Avril 24, 2015
- FDA Pneumovax 23 - Vaccin antipneumococcique, polyvalent. Notice d'emballage Le 30 décembre 2014
- Ibid
- Ibid
- Ibid
- von Elten, KA, Duran LL, Banks TA et al. Réaction inflammatoire systémique après vaccin antipneumococcique Une série de cas Immunother Vaccin Hum. 2014er juin 1 ; 10(6) : 1767-1770.
- Huang DT, Chiu NC, Chi H et al. Fièvre prolongée avec réaction de type cellulite chez les enfants vaccinés contre le pneumocoque polysaccharidique. Pédiatre Infect Dis J. 2008 Oct;27(10):937-9.
- Yousef E, Mannan S. Réaction systémique au vaccin antipneumococcique : quelle est sa fréquence en pédiatrie ? Allergie Asthme Proc. 2008 Jul-Aug;29(4):397-9
- Gabor EP, Seeman M. Réaction systémique fébrile aiguë au vaccin antipneumococcique polyvalent. JAMA. 1979 Nov 16;242(20):2208-9.
- Hasan S, Yousef M, Shridharani S Réaction systémique fébrile sévère au vaccin antipneumococcique. J Natl Med Assoc. Février 2005; 97 (2): 284–285.
- Lee A, Goyal R, Shan HY. Fièvre sévère et prolongée après un vaccin antipneumococcique. Suis J Med Sci. 2006 Dec;332(6):351-3.
Cet article est résumé et traduit par National Vaccine Information Center.

