Covid-19ワクチンの義務:それらに挑戦する20の科学的事実

仮説:COVID-19ワクチンは、COVID-19の蔓延を大幅に減らすため、普遍的なワクチン接種率が高いと、集団発生を防ぎ、パンデミックを終わらせることができます。 |
終わり #1: Eurosurveillanceに掲載された19年2021月のCOVID-XNUMXの発生に関する研究では、 「フィンランドでの発生のように、患者とスタッフの間のすべての感染は、マスクされた個人とワクチン接種された個人の間で発生しました。」。 著者は、研究は 「高い普遍的なワクチン接種率が集団免疫につながり、COVID-19の発生を防ぐという仮説に挑戦します」.1
終わり #2: 19年2021月に発生した別のCOVID-74の疾病管理予防センターの調査では、症例のXNUMX%が完全にワクチン接種されていることがわかりました。2
終わり #3: 19カ国と68の米国の郡でCOVID-2.947の症例を分析したハーバード大学の研究では、「完全にワクチン接種された集団のより高い割合の存在下でのCOVID-19症例の減少の有意な兆候はありません。.3
仮説: COVID-19ワクチンはCOVID-19による死亡を防ぎます |
終わり #4: 臨床試験では数万人の被験者が観察されており、対照群を含み、ワクチン接種の状態に関係なくすべての被験者がCOVID-19について監視および検査された唯一の試験です。 しかし、これらの研究では、ワクチン接種を受けた患者とワクチン接種を受けていない患者の死亡率の有意差を測定するのに十分な数のCOVID-19による死亡は見つかりませんでした。4-7 米国食品医薬品局(FDA)は、次のように述べています。 「死亡率に対するワクチンの有効性を確認するには、COVID-19のリスクが高く発病率が高い個人を増やす必要があります。」.4-7
終わり #5: Eurosurveillanceで発表された19年2021月のCOVID-100の発生に関する研究では、COVID-19の深刻な、重大な、そして致命的な症例のXNUMX%がワクチン接種を受けた個人で発生したことが示されました。1
終わり #6: CDCデータは、COVID-19ワクチンによる大量ワクチン接種が、米国のCOVID-19による死亡率に測定可能な影響を与えなかったことを示しています。 集団予防接種の導入に至るまでの2020か月間(2020年356.000月から19年39.500月)に、COVID-0,120による約1.000人の死亡、つまり2021か月あたり2021人の死亡がありました。これは342.000人あたり19人の死亡率です。 集団予防接種の導入後の38.000か月間(0,115年1.000月から2021年2022月)に、COVID-249.000による19人の死亡、または49.800か月あたり0,151人の死亡がありました。これは、1.000人あたりXNUMX人の死亡率です。 次のXNUMXか月間(XNUMX年XNUMX月からXNUMX年XNUMX月まで)に、COVID-XNUMXによる別のXNUMX人の死亡、つまりXNUMXか月あたりXNUMX人の死亡があり、XNUMX人あたりの死亡率はXNUMXでした。7
仮説:子供にとって、COVID-19ワクチン注射はSARS-CoV-2感染より安全です。 |
終わり #7:ファイザーの臨床試験では、ワクチンを接種しなかった子供に重症のCOVID-19の症例はありませんでした。8-9 対照的に、5歳以上の子供については、ファイザーのCOVID-19ワクチンの臨床研究により、ワクチンが3°Cを超える発熱、静脈経路への水分補給を必要とする嘔吐などの重度(グレード39)の全身反応を引き起こすことがわかりました24。 XNUMX時間の下痢と重度の倦怠感、重度の頭痛、重度の筋肉痛、または重度の関節痛により、日常生活に支障をきたします。9-12
終わり #8:臨床試験では、1〜59歳のワクチン接種を受けた子供1人に143人が5人に11人で、3回目の投与から8日以内に重度の全身反応を経験しました。 ワクチン接種群では、ワクチン未接種群の非重症COVID-10症例19例ごとにXNUMX〜XNUMX症例の重篤な全身反応が観察されました。9
終わり #9:臨床試験では、1歳から9歳までのワクチン接種を受けた青年の12人に15人が、7回目の投与を受けてから19日以内に重度の全身反応を経験しました。 ワクチン接種群で観察された重度の全身反応は、ワクチン未接種群のCOVID-XNUMXの非重症症例よりもXNUMX倍大きかった。10-12
終わり #10:臨床試験では、1〜1.100歳のワクチン接種を受けた子供約12人に15人が、緊急治療室への訪問と研究からの離脱を必要とする初回投与後にグレード4の全身反応(39°Cを超える発熱)を示しました。10-13
仮説:COVID-19ワクチンの臨床試験は、子供の安全性を実証するのに十分な大きさでした。
|
事実#11:ファイザーの臨床試験には、安全性を確立するのに十分な被験者が含まれていなかったため、ワクチンが18歳未満の子供に安全であることを示すのに十分な統計的検出力がありませんでした(つまり、臨床試験には、ワクチン接種を受けた子供が約2.600人しか含まれていませんでした。 5歳と15歳)。9-14 それに比べて、COVID-19による死亡は子供ではまれであることが知られています。 3年2021月17日の時点で、2歳以下がSARS-CoV-19に感染し、COVID-1で死亡する可能性は126.000人に0,0008人、つまりXNUMX%でした。15
COVID-19ワクチンの臨床試験は、子供の安全性を実証するには不十分です
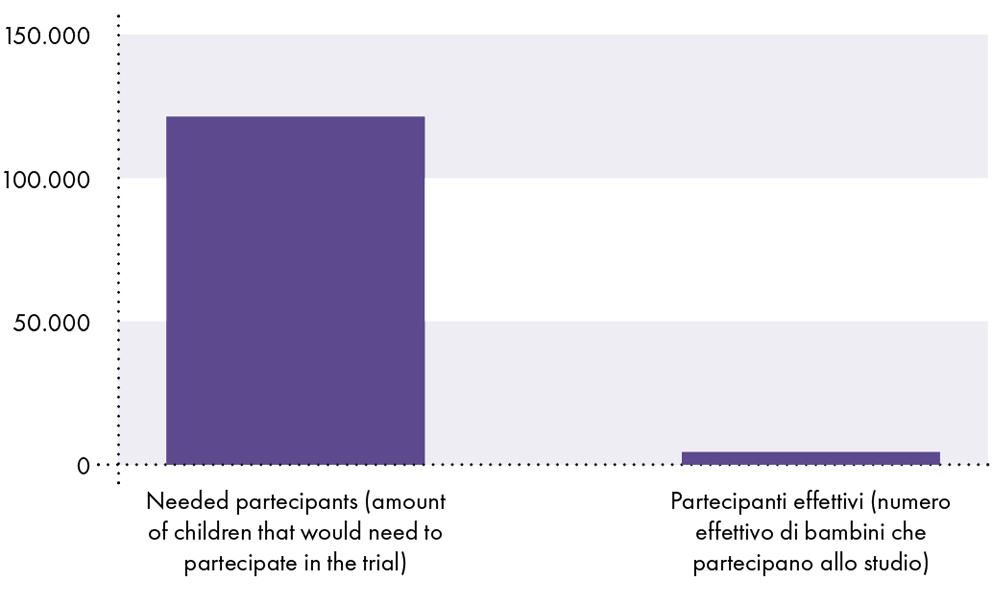
子供がSARS-CoV-2に感染し、COVID-19で死亡する可能性は0,0008%、つまり1人に126.000人であるため、COVID-126.000による死亡を検出するには少なくとも19人の子供が必要です。 したがって、COVID-126.000による死亡のリスクとワクチンによる死亡のリスクを比較するには、少なくとも19人のワクチン接種を受けた参加者が臨床試験に登録されている必要があります。 しかし、約2.600人のワクチン接種を受けた子供たちだけが臨床試験に参加しました。
仮説:COVID-19ワクチンには長期的な副作用がないことが知られています。
|
事実#12: すべての臨床試験の被験者は19〜XNUMXか月間しか観察されなかったため、どの年齢層でもCOVID-XNUMXワクチンの長期的な安全性は不明です。 FDAによると、現在、妊娠中および授乳中の個人や免疫不全の個人などの亜集団におけるファイザー、モデルナ、ジョンソン&ジョンソンのワクチンの安全性について結論を出すにはデータが不十分です。4-8-16 ファイザーの場合、ワクチン 「発癌性、遺伝子毒性、または男性の出生力の障害を引き起こす可能性については評価されていません」.17
事実#13:安全監視報告は、ワクチン接種から40日以内に、16歳未満の個人の心筋炎と心膜炎の深刻なリスクを特定しました。 17歳または1歳の少年では、FDAは、ファイザーCOVID-5.000ワクチンの19.18回目の接種後、および12〜17歳の少年では、19回目の接種後、心筋炎または心膜炎の1分の2.700.19の過剰リスクを報告しています。ファイザーCOVID-XNUMXワクチンの香港の研究では、XNUMX分のXNUMXの心筋炎または心膜炎の過剰リスクが見つかりました。
仮説:ブースターは、ワクチン免疫の低下の問題を解決します。
|
事実#14: 臨床研究では、ワクチンの免疫力が短期間に大幅に低下することがわかっています。 たとえば、ファイザーワクチンの有効性はわずか8か月で18%から25%に低下し、ジョンソン&ジョンソンワクチンの有効性はわずか29か月でXNUMX%からXNUMX%に低下しました。20-21 さらに、臨床試験で測定された有効性は、新しい変異株ではなく、元の武漢株に対してでした。
事実#15:臨床試験では、ファイザーまたはモデナワクチンのXNUMX回目の接種またはジョンソン&ジョンソンワクチンのXNUMX回目の接種は、病気に対する有効性について評価されませんでしたが、抗体数は、わずかXNUMXか月間少数のワクチン接種を受けた被験者で観察されました。18-21-22
仮説:ワクチンを除いて、COVID-19の有効な治療または予防の選択肢は知られていません。
|
事実#16COVID-19の治療法は、2020年初頭のパンデミックの開始以来大幅に改善され、入院患者の生存率が改善されました。23-24 実際、ナーシングホームに住んでいない人の場合、COVID-19の全生存率は米国で99,8%、特に子供で99,999%です。25-26
事実#17:何百もの研究がさまざまな治療法の有効性を調べており、その中で最も研究されているのはイベルメクチン、ビタミンD、ヒドロキシクロロキン(HCQ)およびモノクローナル抗体です。27-30 これらの治療法は、予防(すなわち、症候性COVID-19感染の曝露前または曝露後の予防)にも役立つ可能性があります。31-35
仮説: 以前にSARS-CoV-2に感染したことがある人は、自然免疫が不十分であるため、ワクチン接種を受ける必要があります。 |
事実#18以前のSARS-CoV-2感染は、COVID-2ワクチンよりもSARS-CoV-19感染の予防に効果的であることが示されています。 Johnson&JohnsonのCOVID-19ワクチン臨床試験には、研究前にSARS-CoV-2.000に感染した2人以上の被験者が含まれていました。 ワクチン接種を受けていない人とワクチン接種を受けた人を一貫してテストしたこの研究では、他の研究対象にワクチン接種してから少なくとも19日後にワクチン接種を受けていないグループでCOVID-28の発生率が記録されました。 以前にSARS-CoV-19に感染したワクチン未接種群のCOVID-2の発生率は0,1%(2 / 2.021)でしたが、ワクチン接種を受けた被験者のCOVID-19の発生率は0,59%(113 / 19.306)でした。 これらのデータは、ワクチン接種を受けた被験者のCOVID-19症例が、以前にSARS-CoV-6に感染したワクチン未接種の被験者よりも2倍高いことを示唆しています。36
事実#19Johnson&Johnsonの臨床研究のデータは、以前にSARS-CoV-2に感染したワクチン未接種の人は、99,9%の確率で新たな感染から保護されることも示しています。 1年2021月177,4日の時点で、米国では2億53,8万件のSARS-CoV-XNUMX感染が記録されており、これは米国の人口のXNUMX%に相当します。26-36
仮説: 必須のワクチンは、より安全な環境を作り出すことが示されています。 |
事実#20:SARS-CoV-2の感染と感染は、完全にワクチン接種された集団で高率に発生し、COVID-19の重症、重大、および致命的な症例のかなりの割合が完全にワクチン接種された個人で発生します。 CDCのデータは、COVID-19ワクチンの大量ワクチン接種が、米国のCOVID-19死亡率に測定可能な影響を与えなかったことを示しています。 さらに、短期臨床試験のデータによると、mRNAベースのCOVID-1ワクチンを接種した6〜1歳の9〜12人に55人は、重度の(グレード19)全身反応に苦しんでおり、長期的な安全性はありません。研究が行われています。13-37 したがって、科学的データは、強制予防接種がより安全な環境を作り出すことができないことを示しています。
リファレンス
- Shitrit P、Zuckerman NS、Mor O、Gottesman BS、Chowers M. 2年2021月、イスラエルの高度にワクチン接種された集団におけるSARS-CoV-2021デルタ変異体によって引き起こされた院内感染。EuroSurveill。 26年39月;XNUMX(XNUMX)。 https://pubmed.ncbi.nlm.nih.gov/34596015/.
- Brown CM、Vostok J、Johnson H、Burns M、Gharpure R、Sami S、Sabo RT、Hall N、Foreman A、Schubert PL、Gallagher GR、Fink T、Madoff LC、Gabriel SB、MacInnis B、Park DJ、Siddle KJ 、Harik V、Arvidson D、Brock-Fisher T、Dunn M、Kearns A、Laney AS 大規模な集会に関連する、COVID-2ワクチンの画期的な感染を含むSARS-CoV-19感染の発生—マサチューセッツ州バーンスタブル郡、2021年2021月。MMWRMorb Mortal WklyRep。6月70日;31(1059):62-XNUMX。 https://www.cdc.gov/mmwr/volumes/70/wr/mm7031e2.htm?s_cid=mm7031e2_w.
- Subramanian SV、Kumar A. COVID-19の増加は、米国の68か国と2947の郡での予防接種のレベルとは無関係です。 EurJエピデミオール。 2021年30月1日:4-XNUMX。 https://pubmed.ncbi.nlm.nih.gov/34591202/.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:最新のCOVID-19ワクチン。 ワクチンおよび関連生物製品諮問委員会会議:17年2020月XNUMX日。 https://www.fda.gov/media/144434/download.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:COVID-26の予防のためのJanssenAd2.COV19.Sワクチン。 ワクチンおよび関連生物製剤諮問委員会会議:26年2021月22日。表19:中等度から重度/重度および重度/重度のCOVID-14の最初の発生のワクチン有効性。ワクチン接種の数日後、参加国別、プロトコルごとのセット、28試験。 3001。 https://www.fda.gov/media/146217/download.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:ファイザー-BioNTechCOVID-19ワクチン。 ワクチンおよび関連生物製品諮問委員会会議:10年2020月XNUMX日。 https://www.fda.gov/media/144245/download.
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 COVIDデータトラッカー:州/地域ごとにCDCに報告された米国でのCOVID-19の症例数と死亡数の傾向。 [2022年2月XNUMX日引用]。 https://covid.cdc.gov/covid-data-tracker/#trends_totaldeaths.
- 米国食品医薬品局、生物製剤評価研究センター(CBER)ワクチン研究レビュー局(OVRR)。 ワシントンDC:米国保健社会福祉省。 未承認製品の緊急使用許可(EUA)の修正:覚書を確認します。 2021年9月23日:39、XNUMX。 https://www.fda.gov/media/148542/download.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:19〜5歳の子供に使用するファイザー-BioNTechCOVID-11ワクチンのEUA修正要求。 ワクチンおよび関連生物製品諮問委員会会議:26年2021月XNUMX日。 https://www.fda.gov/media/153447/download.
- ウォレスM.推奨、評価、開発、評価の等級付け(GRADE):ファイザー-BioNTechCOVID-19ワクチン。 COVID-19予防接種実施諮問委員会(ACIP)のワクチン作業部会。 疾病管理予防センター。 2021年12月24日:25、XNUMX。 https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-05-12/03-COVID-Wallace-508.pdf.
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 推奨事項の等級付け、評価、開発、および評価(GRADE):19〜12歳の人のためのファイザー-BioNTechCOVID-15ワクチン。 [2021年14月XNUMX日引用]。 https://www.cdc.gov/vaccines/acip/recs/grade/covid-19-pfizer-biontech-vaccine-12-15-years.html#table03d.
- ファイザー。 ニューヨーク(NY):ファイザー社。ワクチンを投与する医療提供者(予防接種提供者)向けのファクトシート。 2022年3月11日改訂。表19:ワクチン有効性-投与7後2日からの最初のCOVID-7発生:感染の証拠なし、および投与2後12日前の感染の証拠ありまたはなし-盲検プラセボ対照追跡期間、15歳から7歳までの青年の評価可能な有効性(48日)の人口; XNUMX。 https://www.fda.gov/media/153713/download.
- インフォームドコンセントのための医師。 ファイザーCOVID-19ワクチン:短期間の有効性と安全性のデータ。 2021年XNUMX月。 https://www.physiciansforinformedconsent.org/COVID-19-vaccines.
- ファイザー。 ニューヨーク(NY):ファイザー社。ワクチンを投与する医療提供者(予防接種提供者)向けのファクトシート。 2022年3月48日改訂:XNUMX。 https://www.fda.gov/media/153713/download.
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 選択された人口統計学的および地理的特性による毎週の更新:コロナウイルス病(COVID-19)の暫定死亡数。 [2021年3月XNUMX日引用]。 https://www.cdc.gov/nchs/nvss/vsrr/covid_weekly/index.htm#AgeAndSex.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:COVID-26の予防のためのJanssenAd2.COV19.Sワクチン。 ワクチンおよび関連生物製品諮問委員会会議:26年2021月XNUMX日。 https://www.fda.gov/media/146217/download.
- ファイザー。 ニューヨーク(NY):筋肉内使用のための注射用ファイザー社Comirnaty(COVID-19ワクチン、mRNA)懸濁液。 2021年XNUMX月改訂 https://www.fda.gov/media/151707/download.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:Comirnaty(COVID-19ワクチン、mRNA)の追加免疫の認可申請。 ワクチンおよび関連生物製品諮問委員会会議:17年2021月XNUMX日。 https://www.fda.gov/media/152176/download.
- Chua GT、Kwan MYW、Chui CSL、Smith RD、Cheung EC、Tian T、Leung MTY、Tsao SSL、Kan E、Ng WKC、Man Chan VC、Tai SM、Yu TC、Lee KP、Wong JSC、Lin YK、Shek CC、Leung ASY、Chow CK、Li KW、Ma J、Fung WY、Lee D、Ng MY、Wong WHS、Tsang HW、Kwok J、Leung D、Chung KL、Chow CB、Chan GCF、Leung WH、To KKW、 Yuen KY、Lau YL、Wong ICK、IpP.Comirnatyワクチン接種後の香港の青年における急性心筋炎/心膜炎の疫学。 臨床感染症2021年28月989日:ciabXNUMX。 https://pubmed.ncbi.nlm.nih.gov/34849657.
- Thomas SJ、Moreira ED Jr、Kitchin N、Absalon J、Gurtman A、Lockhart S、Perez JL、PérezMarc G、Polack FP、Zerbini C、Bailey R、Swanson KA、Xu X、Roychoudhury S、Koury K、Bouguermouh S、 Kalina WV、Cooper D、Frenck RW Jr、Hammitt LL、TüreciÖ、Nell H、Schaefer A、ÜnalS、Yang Q、Liberator P、Tresnan DB、Mather S、Dormitzer PR、ŞahinU、Gruber WC、Jansen KU; C4591001臨床試験グループ。 162か月間のBNT2b19mRNAcovid-6ワクチンの安全性と有効性。 N Engl JMed。2021月4日;385(19):1761-73。 https://pubmed.ncbi.nlm.nih.gov/34525277.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:ヤンセンCOVID-19ワクチンの追加免疫に関するEUA修正要求。 ワクチンおよび関連生物製品諮問委員会会議:15年2021月21日。39、XNUMX。 https://www.fda.gov/media/153037/download.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:ModernaCOVID-19ワクチンの追加免疫に関するEUA修正要求。 ワクチンおよび関連生物製品諮問委員会会議:14年2021月XNUMX日。 https://www.fda.gov/media/152991/download.
- Horwitz LI、Jones SA、Cerfolio RJ、Francois F、Greco J、Rudy B、PetrilliCM。 COVID-19リスク調整死亡率の傾向。 J HospMed。2021月;16(2):90-2。 https://www.journalofhospitalmedicine.com/jhospmed/article/230561/hospital-medicine/trends-covid-19-risk-adjusted-mortality-rates.
- Dennis JM、McGovern AP、Vollmer SJ、Mateen BA 英国における2019年のコロナウイルス病の救命救急患者の生存率の改善:全国コホート研究、2020年2021月から1月。CritCareMed。49月2日;209(14):XNUMX-XNUMX。 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7803441/.
- イオアニディス、JPA。 COVID-19の世界的な広がりと感染致死率の推定値の調整:体系的な評価の概要。 Eur JClinInvest。 2021; 51:e13554。 https://onlinelibrary.wiley.com/doi/epdf/10.1111/eci.13554.
- インフォームドコンセントのための医師。 COVID-19-疾病情報声明(DIS)。 2021年XNUMX月。 https://physiciansforinformedconsent.org/covid-19/.
- C19early.com。 COVID-19早期治療:1,298件の研究のリアルタイム分析。 [2022年11月XNUMX日引用]。 https://c19early.com/.
- リジェネロン。 Tarrytown、(NY):Regeneron Pharmaceuticals、Inc.医療提供者向けのファクトシート:REGEN-COV(casirivimabおよびimdevimab)の緊急使用許可(EUA)。 2021年XNUMX月改訂 https://www.regeneron.com/downloads/treatment-covid19-eua-fact-sheet-for-hcp.pdf.
- リリー。 インディアナポリス(IN):イーライリリーアンドカンパニー。 COVID-19に対する中和抗体; [2022年9月XNUMX日引用]。 https://www.lilly.com/news/media/media-kits/bamlanivimab-covid19.
- GSK。 ロンドン(英国):GlaxoSmithKlineplc。 GSKとVirBiotechnologyは、COVID-19の早期治療を認可されたソトロビマブの追加供給を購入するという米国政府の合意を発表しました。 2022年11月2022日[9年XNUMX月XNUMX日引用]。 https://www.gsk.com/en-gb/media/press-releases/gsk-and-vir-biotechnology-announce-united-states-government-agreement-to-purchase-additional-supply-of-sotrovimab.
- C19early.com。 COVID-19研究:イベルメクチン; [2022年12月XNUMX日引用]。 https://c19ivermectin.com.
- ブライアントA、ローリーTA、ダウズウェルT、フォーダムEJ、ミッチェルS、ヒルSR、タムTC COVID-19感染の予防と治療のためのイベルメクチン:系統的レビュー、メタアナリシス、および臨床ガイドラインに情報を提供するための試験的逐次分析。 JTherです。 2021年21月28日;4(434):e60-XNUMX。 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8248252/.
- C19early.com。 COVID-19研究:ビタミンD; [2022年12月XNUMX日引用]。 https://c19vitamind.com.
- Ilie PC、Stefanescu S、SmithL.コロナウイルス病2019感染と死亡の予防におけるビタミンDの役割。 Aging ClinExpRes。2020Jul;32(7):1195-8。 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7202265/.
- C19early.com。 COVID-19のHCQ:303件の研究のリアルタイムメタアナリシス。 [2022年10月XNUMX日引用]。 https://hcqmeta.com.
- 米国食品医薬品局、ワクチンおよび関連する生物学的製剤諮問委員会。 FDAブリーフィングドキュメント:COVID-26の予防のためのJanssenAd2.COV19.Sワクチン。 ワクチンおよび関連生物製剤諮問委員会会議:26年2021月14日。表19:中等度から重度/重大なCOVID-14の最初の発生のワクチン有効性。プロトコルセットごとのベースラインSARS-CoV-28ステータスによるワクチン接種。 2。 https://www.fda.gov/media/146217/download.
- El Sahly HM、Baden LR、Essink B、Doblecki-Lewis S、Martin JM、Anderson EJ、Campbell TB、Clark J、Jackson LA、Fichtenbaum CJ、Zervos M、Rankin B、Eder F、Feldman G、Kennelly C、Han- Conrad L、Levin M、Neuzil KM、Corey L、Gilbert P、Janes H、Follmann D、Marovich M、Polakowski L、Mascola JR、Ledgerwood JE、Graham BS、August A、Clouting H、Deng W、Han S、Leav B 、Manzo D、Pajon R、SchödelF、Tomassini JE、Zhou H、Miller J; COVE研究会。 盲検期の完了時のmRNA-1273SARS-CoV-2ワクチンの有効性。 N Engl JMed。2021月4日;385(19):1774-85。 付録付録; 36-7。 https://www.nejm.org/doi/suppl/10.1056/NEJMoa2113017/suppl_file/nejmoa2113017_appendix.pdf.
によって翻訳された記事 インフォームドコンセントのための医師

