帯状疱疹ワクチンは怪我や死亡を引き起こす可能性がありますか?

次の記事では、帯状疱疹に対する副作用を特に取り上げて、副作用の広大な世界に光を当てようとしていますが、複数の副作用の問題など、他の関連する問題を理解するために、以下にリストされている焦点をすべて読むことをお勧めします。ワクチン、ワクチンの XNUMX つまたは複数の化合物に対する過敏症、SIDS 問題およびアジュバントの問題。
複数のワクチンの問題 (クリックして開きます)
複数のワクチンの問題

特に小児期の現在の予防接種カレンダーでは、XNUMX 回のセッションで複数の抗原とワクチンを投与するため、安全性を犠牲にして快適さを優先しています。 ワクチンの安全性について具体的な発言をするためには、この現象の複雑さを考慮に入れなければならず、すべての読者に予防接種のあらゆる側面、長所と短所について十分な情報を提供するようアドバイスする必要があります。
ミシシッピ大学医療センターの神経外科の臨床助教授であるラッセル・ブレイロック博士は、何年にもわたって「毒性の相乗効果」を研究しており、どちらも実験動物でパーキンソン症候群を引き起こすことができないXNUMXつの弱い毒性の農薬が、この現象は、同時に投与された複数のワクチンの場合と比較されます。(a). その他 XNUMX つの研究で、XNUMX 回の投与で複数のワクチンを接種した後に乳児の突然死が発生する可能性があることが確認されています。(紀元前)
Human and Experimental Toxicology に掲載された研究によると、子供により多くのワクチンを処方する国は、乳児死亡率が高くなる傾向があります。(d) たとえば、子供が 26 のワクチンを接種されている米国では、出生 6 人あたり 1000 人以上の子供が死亡していますが、12 の小児用ワクチンが投与されているスウェーデンと日本では、出生 3 人ごとに 1000 人の死亡が報告されています。 前述の研究では、ワクチンと SIDS の関連も考慮されています。
2005 年に European Journal of Pediatrics に掲載されたスイスの研究から(e)の 早産児への影響に関しては、六価ワクチン投与後の無呼吸および徐脈の再発または増加の発生率は13%であるという結果が出ています。 その同じ年、同じ雑誌は、六価の後の乳幼児突然死を調査したドイツの研究を発表しました。 著者は次のように書いています。 ワクチン接種後の乳幼児突然死の監視強化につながるはずだ」と述べた。(f)は、
2006 年に、医学雑誌 Vaccine に掲載されました。(G) ミュンヘン大学の研究者チームからの手紙によると、「1 価ワクチンの接種後に 2 例の乳児が突然死した。ワクチン接種の XNUMX ~ XNUMX 日後に全員が説明なしに死亡していることが判明した」。 彼らは乳幼児突然死の典型的な症例として分類されていましたが、オートプティック検証により、神経病理学的および組織学的異常が明らかになり、すべての子供が重大な脳浮腫を示したため、他のSIDS症例と比較して例外となりました(乳幼児突然死症候群). 研究者は次のように書いています。 しかし、1994 年から 2000 年の間に、SIDS の 198 件のうち 2001 件が同様のケースであることが確認されました。 これは、2004 倍の増加を示しています。」
また、2006 年に Virchows アーカイブで(H)、ミラノ大学病理学研究所のチームは次のように書いています。 参加者には、ワクチンや乳幼児突然死症候群の経験を持つ病理学者が含まれており、剖検を行っていました.しかし、私たちが知る限り、連続切片での脳幹と血液心臓の検査にはほとんど注意が払われず、トリガーの役割を確立する可能性はありませんでした.これらの死のためのワクチンの。 ここでは、3 価ワクチン接種後に突然死亡した生後 XNUMX か月の女児の症例を報告します。 連続切片での脳幹の検査により、両側弓状核形成不全が明らかになった。 心臓の伝導系には、持続的な胎児の分散と変性がありました。 このケースは、脆弱な子供に致命的な結果を引き起こすという六価ワクチンの役割の可能性について独自の理解を提供します。 ガイドラインによると、出生直後または幼児期に突然の予期せぬ死亡が発生した場合、特にワクチン接種後の場合は、常に完全な剖検を受ける必要があります。
リファレンス
- Blaylock R、「予防接種: 隠れた危険」、The Blaylock Wellness Report、2004 年 1 月、pp.9-XNUMX
- Ottaviani G. et al.、「六価ワクチン接種直後の乳幼児突然死症候群 (SIDS): SIDS が疑われる場合の別の病状?」、 ヴィルヒョウ アーカイブ、2006年、448ページ。 100-104。
- Zinka B. et al.、「六価ワクチン接種直後の幼児突然死の原因不明のケース」、ワクチン、2006 年 24 月、31 (32-5779)、pp. 5780-XNUMX。
- Miller NZ et al1。 、 "乳児死亡率は、定期的に投与されるワクチンの投与回数に対して回帰しました: 生化学的または相乗的な毒性はありますか??」、Hum. Exp. Toxicol.、2011 年 XNUMX 月。
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
アルミニウムの問題 (クリックして開きます)
ワクチン中のアルミニウム:親が知っておくべきこと

1.アルミニウムとは何ですか?
アルミニウムは銀白色の軽金属で、展性があり、耐性があります。 これらの品質により、機械、建設、倉庫、調理器具、台所用品、繊維、染料、化粧品など、さまざまな産業や製品で役立ちます。 アルミニウムはまた、地球の地殻で最も豊富な金属であり、環境中の実質的にすべてのアルミニウムは土壌に含まれています。 しかし、アルミニウムは生物(植物や動物など)に自然に大量に含まれているわけではなく、生物学的機能は知られていません。 過去XNUMX世紀にわたって、一部の製品にアルミニウムを使用することで、人体への暴露が増加しました。 主な曝露源は、アルミニウム含有食品(ベーキングパウダー、加工食品、粉ミルクなど)、医療製品(制汗剤、制酸剤など)、アレルギー注射、ワクチンです。1-3
2.なぜアルミニウムがワクチンに含まれているのですか?
一部のワクチンは、抗原(異物)に対する免疫応答を高める成分であるアルミニウム化合物(水酸化アルミニウムとリン酸アルミニウム)をアジュバントとして使用します。4-5 米国食品医薬品局(FDA)は、一部のワクチンにアルミニウムが含まれていない場合、それらが引き起こす免疫応答が低下する可能性があると述べています。6
3.どのワクチンにアルミニウムが含まれていますか?
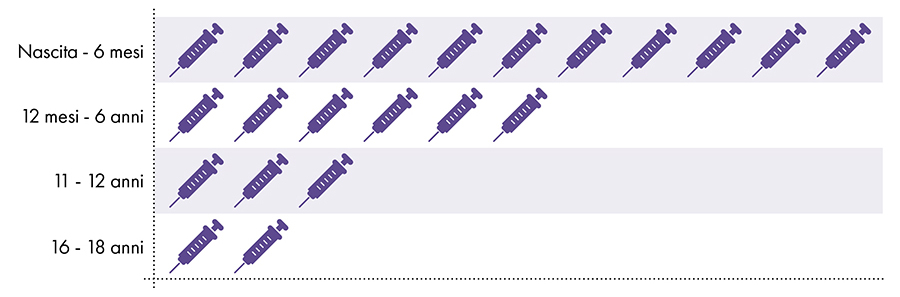
次のワクチンにはアルミニウムが含まれており、乳幼児、子供、青年に投与されます(図1)。
- B型肝炎(HepB)
- 六価
- ジフテリア、破傷風、百日咳(DTaPおよびTdap)
- インフルエンザ菌b型(PedvaxHIB)
- 肺炎球菌(PCV)
- A型肝炎(HepA)
- ヒトパピローマウイルス(HPV)
- 髄膜炎菌B(MenB)
図1:アルミニウム含有ワクチンの最大18回分が出生から22歳まで投与されます7-8
4.アルミニウムへの暴露は安全ですか?
FDAは、1975年以来、アルミニウムが一般に安全と認められている(GRAS)と見なしています。9 しかし、1990年以前は、科学的研究で被験者に投与された少量のアルミニウムを正確に検出する技術はありませんでした。10 その結果、悪影響が発生する前に吸収される可能性のあるアルミニウムの量は不明でした。
1990年代以降、技術の進歩のおかげで、人体に残っている少量のアルミニウムが、神経系や体の他の部分の組織の多くの細胞および代謝プロセスを妨げることが観察されています。1-10-11 アルミニウムの最大の悪影響は神経系で観察されており、運動能力の低下から脳症(精神状態の変化、性格の変化、思考困難、記憶喪失、発作、昏睡など)にまで及びます。2-12
米国保健社会福祉省(HHS)は、アルミニウムを既知の神経毒として認識しています。2 さらに、FDAは乳幼児および子供におけるアルミニウム毒性のリスクについて警告しています。13
連邦官報:米国政府の日刊紙「腎機能が正常な満期産児でさえ、脳と骨格の急速な成長と未熟さ、および血液脳関門の未熟さのためにリスクにさらされる可能性があります。1歳または2歳までの乳児は、成人よりも糸球体濾過率が高く、腎機能に影響を及ぼします。この機関は、幼児や腎機能が未熟な子供がアルミニウムにさらされるリスクが高くなることを恐れています。」 |
5.どのくらいの経口アルミニウムは安全ではありませんか?
2008年、HHSの一部門である有害物質疾病登録局(ATSDR)は、アルミニウムの神経毒性作用に関する研究を使用して、1日あたり体重1.000キログラムあたりXNUMXミリグラム(XNUMXマイクログラム)以下のアルミニウムを測定しました。アルミニウムの悪影響を避けてください。2
6.注入されたアルミニウムの量は安全ではありませんか?
安全に注入できるアルミニウムの量を決定するには、ATSDRの経口アルミニウム制限を変換する必要があります。 経口アルミニウムのATSDR制限(1.000日あたり体重0,1キログラムあたりXNUMXマイクログラムのアルミニウム)は、消化管がほとんどすべての経口アルミニウムを遮断するため、血流に吸収される経口アルミニウムのXNUMX%に基づいています。2 逆に、筋肉内に注入されたアルミニウムは消化管を迂回し、アルミニウムの100%が時間の経過とともに血流に吸収される可能性があります(つまり、吸収されるアルミニウムの割合は1.000倍になります)。 これらの異なる吸収量を説明するには、ATSDRの経口アルミニウム制限を1000で割る必要があります。この変換により、体重1キログラムあたり0,1マイクログラムのアルミニウム(1.000マイクログラムの1%)というATSDR由来の血中アルミニウム制限になります。 3日あたり。 したがって、アルミニウムの神経毒性作用を回避するために、体重XNUMXキログラムあたりXNUMXマイクログラム以下のアルミニウムが毎日血流に入る必要があります。 図XNUMXは、体重に基づいたさまざまな年齢の乳児のATSDR由来の血中アルミニウム制限を示しています。
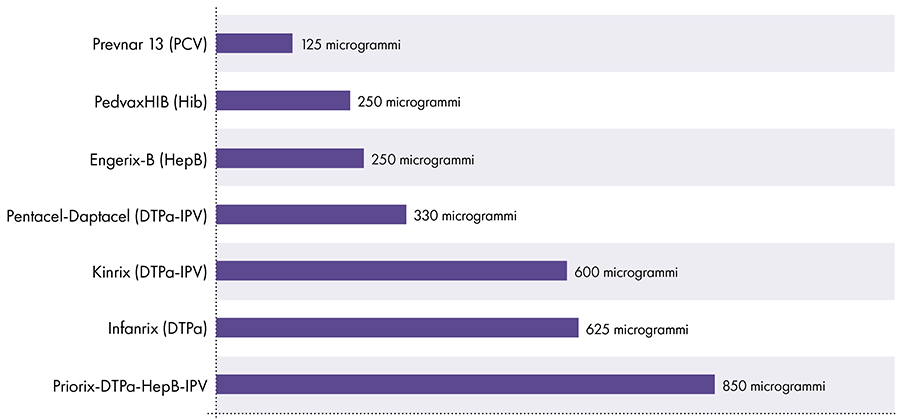
7.ワクチンにはどのくらいのアルミニウムが含まれていますか?
ワクチンに含まれるアルミニウムの量はさまざまです。16 1968年、米国連邦政府は、一部のワクチンを有効にするために必要なアルミニウムの量に基づいて、ワクチンに含まれるアルミニウムの量の制限を850回の投与あたりXNUMXマイクログラムに設定しました。6-17 その結果、アルミニウムを含む乳児用ワクチンに含まれるアルミニウムの量は、125回の投与あたり850〜4マイクログラムの範囲になります。 図XNUMXは、子供に与えられたさまざまなワクチンのXNUMX回投与のアルミニウム含有量を示しています。
8.ワクチン中のアルミニウムの量を、有害物質疾病登録局(ATSDR)から導き出された制限と比較した研究はありますか?
2011年に、ワクチン中のアルミニウムの量をATSDRによって設定された血流制限と比較することを目的とした研究が発表されました。18 ただし、この研究では、ATSDRが計算に使用した0,78%の値ではなく、血流に吸収された0,1%の経口アルミニウムに誤って計算が基づいていました。19-20 その結果、2011年の研究では、アルミニウムのほぼ8倍(0,78%/ 0,1%)が安全に血流に入ることができると仮定されており、これは誤った結論につながっています。
9.ワクチンによるアルミニウム曝露は安全ですか?
ワクチンは筋肉内注射され、ワクチンからのアルミニウムが人間の筋肉から血流に移動する速度は不明です。 動物実験によると、ワクチンからのアルミニウムは、複数の変数があるため、血流に入るまでに数か月からXNUMX年以上かかる可能性があります。21-23 3歳未満の子供におけるワクチンからのアルミニウムへの累積曝露はATSDRによって設定された4日あたりの制限を数百超えているため(図XNUMXおよびXNUMX)、ワクチンからのアルミニウムがコース中に血流に入った場合でも制限を超えます約XNUMX年の。 さらに、ワクチンからのアルミニウムは免疫細胞に吸収され、脳を含む注射部位から遠く離れた体の部分に到達することが研究によって示されています。24
アルミニウム含有ワクチンでワクチン接種された集団とそのようなワクチンでワクチン接種されていない集団を比較する安全性研究が実施されていないため、ワクチンにおけるアルミニウムの悪影響の程度は不明です。
ATSDRに由来する血流のアルミニウム制限2-14-15
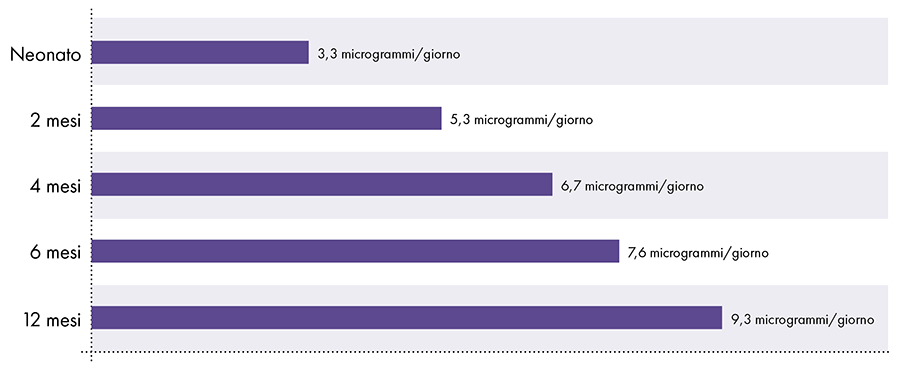 図3:このグラフは、米国保健社会福祉省の一部門である有害物質疾病登録局から導き出された、さまざまな年齢の子供たちのアルミニウム制限を示しています。 この制限は、アルミニウムの神経毒性作用を回避するために、体重1キログラムあたりXNUMXマイクログラム以下のアルミニウムが毎日血流に入る必要があることを示しています。
図3:このグラフは、米国保健社会福祉省の一部門である有害物質疾病登録局から導き出された、さまざまな年齢の子供たちのアルミニウム制限を示しています。 この制限は、アルミニウムの神経毒性作用を回避するために、体重1キログラムあたりXNUMXマイクログラム以下のアルミニウムが毎日血流に入る必要があることを示しています。
ワクチン中のアルミニウムの量
リファレンス
- アメリカ小児科学会、栄養委員会。 乳幼児および小児におけるアルミニウムの毒性。 小児科。 1996年97月;3(413):XNUMX。
- 有害物質疾病登録局(ATSDR)。 アルミニウムの毒性プロファイル。 ワシントンDC:米国保健社会福祉省; 2008.3、13-24、145、171-7、208。
- ヨーケルRA。 食品中のアルミニウム—食品添加物の性質と寄与。 In:El-Samragy Y、編集者。 食品添加物。 リエカ(クロアチア):InTech; 2012-203。
- マラックP、マッキーAS、マンクスMW アルミニウムの補助作用の理解に向けて。 NatRevImmunol。 2009年9月;4(287):XNUMX。
- Volk VK、BunneyWE。 液体トキソイドおよびミョウバン沈殿トキソイドによるジフテリア免疫。 J公衆衛生国の健康です。 1942年32月;7(690):9-XNUMX。
- Baylor NW、Egan W、Richman P.ワクチン中のアルミニウム塩—米国の展望。 ワクチン。 2002年31月20日;3補足18:S22-XNUMX。
- 米国食品医薬品局。 シルバースプリング(MD):米国食品医薬品局。 米国での使用が許可されているワクチン。 [2018年14月2018日更新; 27年XNUMX月XNUMX日引用]。 https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 18歳以下の子供および青年に推奨される予防接種スケジュール、米国、2018年。 https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- 米国食品医薬品局。 シルバースプリング(MD):米国食品医薬品局。 SCOGS(GRAS物質に関する特別委員会); [2018年16月XNUMX日引用]。 https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- プリーストND。 トレーサーとしてアルミニウム-26を採用した研究に特に関連した、人間におけるアルミニウムの生物学的挙動とバイオアベイラビリティ:レビューと研究の最新情報。 Jエンバイロンモニット。 2004; 6:376,392。
- Poole RL、Pieroni KP、Gaskari S、Dixon TK、Park KT、KernerJA。 小児用非経口栄養製品中のアルミニウム:測定された含有量とラベル付けされた含有量。 J PediatrPharmacolTher。 2011; 16(2):92-7。
- セドマンA.小児期のアルミニウム毒性。 PediatrNephrol。 1992年6月;4(383):93-XNUMX。
- 米国食品医薬品局、保健福祉省。 ルールと規則。 連邦準備制度理事会。 2003年68月;100(34286):XNUMX
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 国立衛生統計センター:男児の年齢別の体長と年齢別の体重のグラフのデータ表。 [2019年2月XNUMX日引用]。 https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- 疾病管理予防センター。 ワシントンDC:米国保健社会福祉省。 国立衛生統計センター:女の子の年齢別の長さおよび年齢別の体重のグラフのデータテーブル。 [2019年2月XNUMX日引用]。 https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- 米国食品医薬品局、保健福祉省。 構成材料の要件の改訂。 最終規則。 連邦準備制度理事会。 2011年13月76日;71(20513):8-XNUMX。
- 連邦官報局、国立公文書記録管理局、一般サービス局。 ルールと規則。 連邦準備制度理事会。 1968年33月; 6(369):XNUMX。
- Mitkus RJ、King DB、Hess MA、Forshee RA、WalderhaugMO。 食事療法と予防接種による乳児への曝露後のアルミニウムの薬物動態を更新しました。 ワクチン。 2011年28月29日;51(9538):43-XNUMX。
- ミラーS、インフォームドコンセントのための医師。 「食事療法と予防接種による乳児への曝露後のアルミニウムの薬物動態の更新」の正誤表。 で:ResearchGate。 ベルリン(ドイツ):ResearchGate GmbH; 2020年6月2020日[6年XNUMX月XNUMX日引用]。 https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- インフォームドコンセントのための医師。 ニューポートビーチ(CA):インフォームドコンセントのための医師。 「食事と予防接種による乳児への曝露後のアルミニウムの薬物動態の更新」の正誤表。 [2020年6月XNUMX日引用]。 https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE、Hem SL、White JL、Elmore D、Suckow MA、Rudy AC、DandashliEA。 26Alを使用したアルミニウム含有ワクチンアジュバントのinvivo吸収。 ワクチン1997年15月-12月;13(1314-8):XNUMX-XNUMX。
- Verdier F、Burnett R、Michelet-Habchi C、Moretto P、Fievet-Groyne F、SauzeatE.カニクイザルにアルミニウム含有ワクチンを筋肉内投与した後のいくつかの時点でのアルミニウムアッセイと局所反応の評価。 ワクチン。 2005月3日;23(11):1359-67。
- Weisser K、GöenT、Oduro JD、Wangorsch G、Hanschmann KO、Keller-StanislawskiB.ラットにアジュバント添加ヒトワクチンを筋肉内注射した後の血漿および組織中のアルミニウム。 アーチトキシコル。 2019年93月;10(2787):96-XNUMX。
- Masson JD、CrépeauxG、Authier FJ、Exley C、GherardiRK。 アルミニウムベースのアジュバントのトキシコキネティクスに関する参照研究の批判的分析。 JInorgBiochem。 2018年181月;87:95-XNUMX。
によって翻訳された記事 インフォームドコンセントのための医師
Shingrixワクチンの添付文書によると、臨床試験中に報告された有害事象には、注射部位の痛み、腫れと発赤、頭痛、発熱、疲労、悪寒、胃腸障害、痛風、虚血性視神経障害などが含まれていた。(1) グラクソ・スミスクラインは、2017年に認可したSHINGRIXワクチンの複数の市販後研究を実施することを約束した。米国疾病管理予防センター(CDC)が2018年XNUMX月の予防接種実施に関する諮問委員会(ACIP)会議で提示したデータによると、ほとんどの報告は女性に関するものであり、重大な出来事ではなかった。 最も一般的な反応は注射部位の痛みでした。(2)
2019年XNUMX月のACIP会議で、CDC予防接種安全室(ISO)のトム・シマブクロ博士は、SHINGRIXワクチンの潜在的な安全性シグナルを報告した。 ギラン・バレー症候群(GBS)とワクチンとの関連性が、ワクチン安全性データリンク(VSD)およびワクチン有害事象報告システム(VAERS)で判明した。 GBS は、末梢神経の炎症を引き起こす稀な神経疾患です。 合併症には、身体の完全な麻痺を含む、一時的または慢性的な麻痺が含まれる場合があります。(3)
CDC、FDA、およびメディケアおよびメディケイド サービス センター (CMS) は、メディケア請求データベースのデータのレビューを実施しました。 FDA によると:(4) 「Shingrix ワクチン接種後の GBS のリスクは、ワクチン接種後 1 ~ 42 日のリスク ウィンドウとワクチン接種後 43 ~ 183 日の対照ウィンドウを使用した自己制御症例シリーズの分析で評価されました。一次分析では、GBS のリスクが増加していることが判明しました。 Shingrix ワクチン接種後 42 日間の GBS 発症率は、3 歳以上の成人に 65 万回接種するごとに 42 人の GBS 過剰症例と推定されています。 6歳以上の成人に対する65万回の投与当たりGBS過剰症例はXNUMX人と推定されているが、ShingrixのXNUMX回目の投与後にGBSのリスクは増加していなかった。請求データにおけるGBS診断のこれらの分析は、医療記録の検討によって確認されたGBS症例の分析によって裏付けられた。 。」
FDAはShingrixとGBSとの関連性を確立したが、因果関係を立証するための現在のデータは入手できないと述べた。 ただし、このセクションのレビューは、 「警告と注意事項」 GBS のリスクに関する SHINGRIX パッケージのリーフレットの説明は正当化されました。(5)
Shingrix ワクチンが承認された後に報告された追加の有害事象には、アレルギー反応、血管浮腫、蕁麻疹および発疹、ワクチン投与群における可動性の低下などが含まれます。(6)
ゾスタバックスワクチンの臨床試験や市販後に報告された有害事象には、注射部位の痛み、腫れや発赤、頭痛、帯状疱疹様の発疹、発熱、ショック、関節痛や筋肉痛、腺の腫れ、呼吸器症状などがあります。(7) ゾスタバックスワクチン投与後の視神経炎も、公表された症例研究で報告されています。(8)
ゾスタバックスの添付文書には、「ワクチンウイルスの伝播は、ワクチン接種者と感染しやすい接触者の間で発生する可能性がある」と記載されています。(9) つまり、ワクチン接種を受けた人はそのワクチン株の水痘に感染しており、これまでに水痘にかかったことのない人には他の人に水痘を感染させる可能性があります。
ゾスタバックスのメーカーであるメルクは現在、ワクチンが死亡を含む重篤な副作用を引き起こしたとして60件の訴訟から弁護している。 これらの訴訟の結果は保留中である。(10) 米国におけるゾスタバックスの販売は2020年XNUMX月に中止された。(11)
ゾスタバックスを製造するメルク社は現在、ワクチンが死亡を含む重篤な副作用を引き起こしたとして訴訟と弁護を行っている。(12) 2022年1.200月、ペンシルベニア州の連邦判事は、ゾスタバックスワクチン接種後に帯状疱疹が発生したと主張する約XNUMX件の請求を棄却した。 伝えられるところによると、帯状疱疹の発疹がワクチンに関連しているという証拠が不足していたために、裁判官によってこの主張は却下されたという。 自己免疫疾患と難聴をめぐる他の訴訟も係争中である。(13)
リファレンス (クリックして開きます)
- グラクソ・スミスクライン・バイオロジカルズ. 添付文書 - SHINGRIX. 米国食品医薬品局 8月2、2021。
- 米国疾病管理予防センター。 2018 年 XNUMX 月の ACIP 議事録。 6月2018。
- ランガム T. ACIP: 2018-2019 年のインフルエンザワクチンの有効率は 44%. ワクチン情報センター 7年2019月XNUMX日。
- 米国食品医薬品局。 FDA、Shingrixの処方情報にギラン・バレー症候群(GBS)に関する警告を含めるよう要求。 24年2021月XNUMX日。
- 米国食品医薬品局。 FDA、Shingrixの処方情報にギラン・バレー症候群(GBS)に関する警告を含めるよう要求。 24年2021月XNUMX日。
- グラクソ・スミスクライン・バイオロジカルズ. 添付文書 - SHINGRIX. 米国食品医薬品局 8月2、2021。
- Merck&Co。 添付文書 - ゾスタバックス (冷凍). 米国食品医薬品局 12月26、2019。
- ハン S. 水痘・帯状疱疹ワクチン接種後の視神経炎:XNUMX 例の報告. ワクチン 3 年 2014 月 32 日。 39(4881):4-XNUMX 。
- Merck&Co。 添付文書 - ゾスタバックス (冷凍). 米国食品医薬品局 12月26、2019。
- ルハナ、R. メルク、フロリダ州のゾスタバックス訴訟を統合する申し立てを提出. 法務調査官 、30を2018ことがあります。
- 米国疾病管理予防センター。 ゾスタバックスについて誰もが知っておくべきこと。 10月5、2020。
- ルハナ、R. メルク、フロリダ州のゾスタバックス訴訟を統合する申し立てを提出. 法務調査官 、30を2018ことがあります。
- カンシュタイナー F. メルク社、原告らの証言が不十分で約1,200件のゾスタバックス帯状疱疹ワクチン訴訟から逃れる. 激しい製薬 12月8、2022。
この記事の要約と翻訳は ワクチン情報センター.

