A vacina contra o herpes-zóster pode causar ferimentos e/ou morte?

O artigo a seguir tenta lançar luz sobre o vasto mundo das reações adversas, com um olhar específico para a do Herpes Zoster, mas recomendamos que você leia todos os focos listados abaixo para entender as outras questões relacionadas, como o problema das múltiplas vacinas, hipersensibilidade a um ou mais compostos da vacina, o problema da SIDS e dos adjuvantes.
O problema das vacinas múltiplas (clique para abrir)
O problema das vacinas múltiplas

Os calendários vacinais atuais, principalmente para a idade pediátrica, preveem a administração de múltiplos antígenos e vacinas em uma única sessão, privilegiando o conforto em detrimento da segurança. Para poder fazer um discurso específico sobre a segurança das vacinas, devemos necessariamente levar em consideração a complexidade do fenômeno, aconselhando todos os leitores a se informarem adequadamente sobre todos os aspectos da vacinação, prós e contras.
O Dr. Russell Blaylock, professor clínico assistente de neurocirurgia no Centro Médico da Universidade do Mississippi, estudou a "sinergia tóxica" por anos e foi capaz de observar que quando dois pesticidas fracamente tóxicos, onde nenhum é capaz de causar a síndrome de Parkinson em animais experimentais, se combinam entre si, podem causar a doença até rapidamente e compara esse fenômeno ao de múltiplas vacinas administradas simultaneamente: "As vacinas, se muito numerosas e muito próximas, comportam-se como uma doença crônica".(A). Outros Dois estudos confirmaram que a morte infantil súbita pode ocorrer após a inoculação de múltiplas vacinas em uma única administração.(bc)
Um estudo publicado na Human and Experimental Toxicology mostrou que os países que prescrevem mais vacinas em crianças tendem a ter taxas de mortalidade infantil mais altas.(D) Por exemplo, nos Estados Unidos, onde as crianças recebem 26 vacinas, morrem mais de 6 crianças por 1000 nascidos vivos, enquanto na Suécia e no Japão, onde são administradas 12 vacinas pediátricas, são registradas 3 mortes para cada 1000 nascidos vivos. No estudo mencionado, a ligação entre vacinas e SIDS também é considerada.
De um estudo suíço publicado em 2005 no European Journal of Pediatrics(E) resulta que, em relação aos efeitos em prematuros, a incidência de apnéia e bradicardia recorrentes ou aumentadas após a administração de vacinas hexavalentes é de 13%. Nesse mesmo ano, a mesma revista publicou um estudo alemão que examinou mortes infantis súbitas após hexavalente. Os autores escrevem: «Estes resultados, baseados em relatos espontâneos, não provam uma relação causal entre vacinação e morte súbita infantil, mas constituem um sinal em relação a um dos dois hexavalentes disponíveis; sinal que deve levar a intensificar a vigilância de mortes súbitas infantis após a vacinação".(F)
Em 2006, foi publicado na revista médica Vaccine(g) a carta de uma equipe de pesquisadores da Universidade de Munique que relatou «seis casos de morte súbita infantil após a vacinação hexavalente.. Todos encontrados mortos sem explicação 1-2 dias após a vacinação». Eles foram classificados como casos típicos de morte súbita infantil, mas a verificação autóptica revelou anormalidades neuropatológicas e histológicas e todas as crianças apresentaram um edema cerebral significativo que as tornou uma exceção em comparação com os outros casos de SIDS (Síndrome de morte súbita infantil). Os pesquisadores escreveram que “Antes da introdução da vacina hexavalente (nos anos 1994-2000), observamos o caso de apenas uma em 198 crianças com morte súbita infantil que morreu logo após a vacinação DTP. Mas entre 2001 e 2004 eles identificaram cinco casos semelhantes de 74 com SIDS. Isso indicaria um aumento de treze vezes."
Também em 2006 em Virchows Archive(H), a equipe do Instituto de Patologia da Universidade de Milão escreveu: «Especialistas da Agência Européia de Avaliação de Produtos Médicos analisaram a possibilidade de haver uma ligação entre as vacinas hexavalentes e alguns casos de morte. Os participantes incluíram patologistas com experiência em vacinas e síndrome da morte súbita infantil que realizaram as autópsias. da vacina para essas mortes. Aqui relatamos o caso de uma menina de 3 meses que morreu repentinamente após vacinação hexavalente. O exame do tronco cerebral em cortes seriados revelou hipoplasia bilateral do núcleo arqueado. O sistema de condução do coração apresentava dispersão e degeneração fetal persistente. Este caso oferece uma compreensão única do possível papel da vacina hexavalente em desencadear uma consequência letal em uma criança vulnerável. Qualquer caso de morte súbita e inesperada que ocorra logo após o nascimento ou na primeira infância, principalmente se após vacinação, deve sempre ser submetido a necropsia completa, conforme orientações.
Referências
- Blaylock R, "Vacinações: os perigos ocultos", The Blaylock Wellness Report, maio de 2004, pp.1-9
- Ottaviani G. et al., "Síndrome da morte súbita infantil (SIDS) logo após a vacinação hexavalente: outra patologia na suspeita de SIDS?", Virchows Arquivo, 2006, 448, pp. 100-104.
- Zinka B. et al., "Casos inexplicados de morte súbita infantil logo após a vacinação hexavalente", Vaccine, julho de 2006, 24 (31-32), pp. 5779-5780.
- Miller NZ e cols.1. , "As taxas de mortalidade infantil regrediram em relação ao número de doses de vacina administradas rotineiramente: há toxicidade bioquímica ou sinérgica?”, Hum. Exp. Toxicol., maio de 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
O problema do alumínio (clique para abrir)
Alumínio em vacinas: o que os pais precisam saber

1. O que é alumínio?
O alumínio é um metal leve branco prateado, maleável e resistente. Essas qualidades o tornam útil em inúmeras indústrias e produtos, incluindo máquinas, construção, armazéns, panelas, utensílios de cozinha, têxteis, corantes e cosméticos. O alumínio também é o metal mais abundante na crosta terrestre, e praticamente todo o alumínio do meio ambiente é encontrado no solo. No entanto, o alumínio não é encontrado naturalmente em quantidades significativas em organismos vivos (como plantas e animais) e não tem função biológica conhecida. Ao longo do século passado, o uso de alumínio em alguns produtos levou ao aumento da exposição humana. As principais fontes de exposição são alimentos contendo alumínio (por exemplo, fermento em pó, alimentos processados, fórmulas infantis, etc.), produtos médicos (por exemplo, antitranspirantes, antiácidos, etc.), injeções de alergia e vacinas.1-3
2. Por que o alumínio está presente nas vacinas?
Algumas vacinas utilizam compostos de alumínio (hidróxido de alumínio e fosfato de alumínio) como adjuvantes, que são ingredientes que aumentam a resposta imune a um antígeno (substância estranha).4-5 A Food and Drug Administration (FDA) dos EUA diz que, se algumas vacinas não incluírem alumínio, a resposta imune que elas desencadeiam pode diminuir.6
3. Quais vacinas contêm alumínio?
As seguintes vacinas contêm alumínio e são administradas a lactentes, crianças e adolescentes (Fig. 1):
- Hepatite B (HepB)
- hexavalente
- Difteria, tétano e coqueluche (DTaP e Tdap)
- Haemophilus influenzae tipo b (PedvaxHIB)
- Pneumococo (PCV)
- Hepatite A (HepA)
- Vírus do Papilomavírus (HPV)
- Meningococo B (MenB)
Figura 1: Até 18 doses de vacinas contendo alumínio são administradas desde o nascimento até os 22 anos7-8
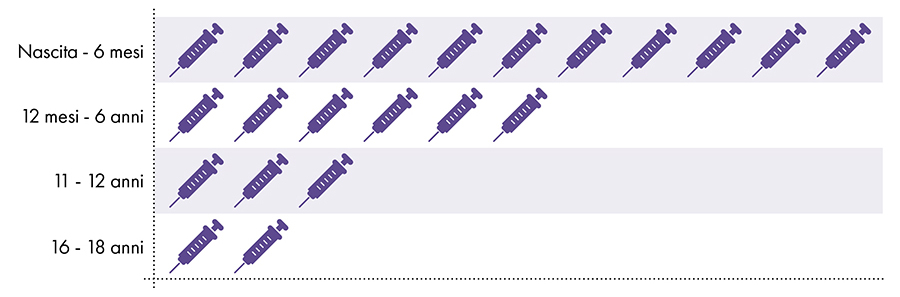
4. A exposição ao alumínio é segura?
A FDA considera o alumínio geralmente reconhecido como seguro (GRAS) desde 1975.9 No entanto, antes de 1990, não havia tecnologia para detectar com precisão pequenas quantidades de alumínio administradas a indivíduos em estudos científicos.10 Consequentemente, a quantidade de alumínio que poderia ser absorvida antes do início dos efeitos adversos era desconhecida.
Desde a década de 1990, graças aos avanços tecnológicos, observa-se que as pequenas quantidades de alumínio que permanecem no corpo humano interferem em uma série de processos celulares e metabólicos no sistema nervoso e tecidos de outras partes do corpo.1-10-11 Os maiores efeitos negativos do alumínio foram observados no sistema nervoso e variam de habilidades motoras prejudicadas a encefalopatia (estado mental alterado, alterações de personalidade, dificuldades de pensamento, perda de memória, convulsões, coma e muito mais).2-12
O Departamento de Saúde e Serviços Humanos dos Estados Unidos (HHS) reconhece o alumínio como uma neurotoxina conhecida.2 Além disso, o FDA alertou sobre os riscos de toxicidade do alumínio em bebês e crianças.13
REGISTRO FEDERAL: O jornal diário do governo dos Estados Unidos"Mesmo bebês a termo com função renal normal podem estar em risco devido ao rápido crescimento e imaturidade do cérebro e do esqueleto, bem como da barreira hematoencefálica. taxa de filtração glomerular do que os adultos, o que afeta sua função renal. A agência teme que crianças pequenas e aqueles com função renal imatura tenham maior risco de exposição ao alumínio ". |
5. Quanto alumínio oral não é seguro?
Em 2008, a Agência para Substâncias Tóxicas e Registro de Doenças (ATSDR), uma divisão do HHS, usou estudos sobre os efeitos neurotóxicos do alumínio para determinar que não mais de 1 miligrama (1.000 microgramas) de alumínio por quilograma de peso corporal por dia para evitar os efeitos negativos do alumínio.2
6. Quanto alumínio injetado não é seguro?
Para determinar a quantidade de alumínio que pode ser injetada com segurança é necessário converter o limite de alumínio oral do ATSDR. O limite ATSDR para alumínio oral (1.000 microgramas de alumínio por quilograma de peso corporal por dia) é baseado em 0,1% do alumínio oral que é absorvido pela corrente sanguínea, pois o trato digestivo bloqueia quase todo o alumínio oral.2 Em contraste, o alumínio injetado por via intramuscular contorna o trato digestivo e 100% do alumínio pode ser absorvido pela corrente sanguínea ao longo do tempo (ou seja, a proporção de alumínio absorvida é 1.000 vezes maior). Para levar em conta essas diferentes quantidades de absorção, o limite oral de alumínio do ATSDR deve ser dividido por 1000. Essa conversão leva a um limite de alumínio sanguíneo derivado do ATSDR de 1 micrograma de alumínio (0,1% de 1.000 microgramas) por quilograma de peso corporal por dia. Consequentemente, para evitar os efeitos neurotóxicos do alumínio, não mais do que 1 micrograma de alumínio por quilograma de peso corporal deve entrar na corrente sanguínea diariamente. A Figura 3 mostra o limite de alumínio no sangue derivado de ATSDR para bebês de várias idades com base em seu peso.
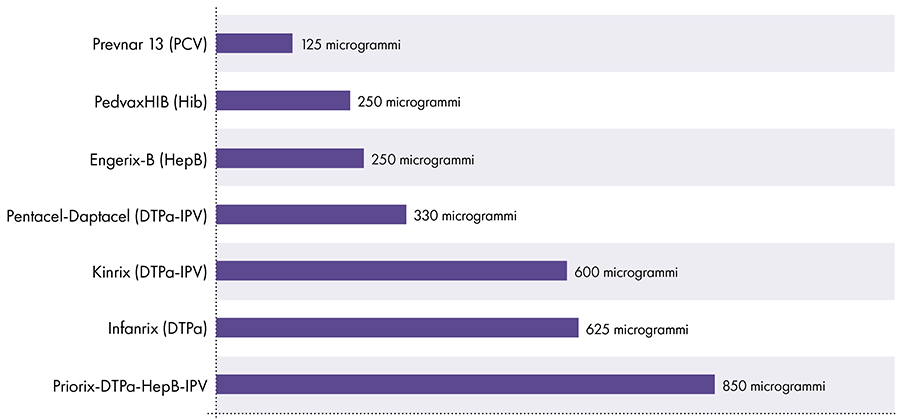
7. Quanto alumínio existe nas vacinas?
A quantidade de alumínio nas vacinas varia.16 Em 1968, o governo federal dos EUA estabeleceu o limite para a quantidade de alumínio nas vacinas em 850 microgramas por dose, com base na quantidade de alumínio necessária para tornar algumas vacinas eficazes.6-17 Consequentemente, a quantidade de alumínio nas vacinas infantis contendo alumínio varia de 125 a 850 microgramas por dose. A Figura 4 mostra o teor de alumínio de uma dose de várias vacinas administradas a crianças.
8. Algum estudo comparou a quantidade de alumínio nas vacinas com o limite derivado da Agência de Substâncias Tóxicas e Registro de Doenças (ATSDR)?
Em 2011, foi publicado um estudo que tinha como objetivo comparar a quantidade de alumínio nas vacinas com o limite de fluxo sanguíneo estabelecido pela ATSDR.18 No entanto, este estudo baseou incorretamente seus cálculos em 0,78% de alumínio oral absorvido na corrente sanguínea, em vez do valor de 0,1% usado pelo ATSDR em seus cálculos.19-20 Como resultado, o estudo de 2011 levantou a hipótese de que quase 8 vezes (0,78% / 0,1%) o alumínio pode entrar com segurança na corrente sanguínea, e isso levou a uma conclusão incorreta.
9. A exposição ao alumínio das vacinas é segura?
As vacinas são injetadas por via intramuscular, e a taxa na qual o alumínio das vacinas migra do músculo humano para a corrente sanguínea é desconhecida. Estudos em animais sugerem que o alumínio das vacinas pode levar de alguns meses a mais de um ano para entrar na corrente sanguínea, devido a múltiplas variáveis.21-23 Uma vez que a exposição cumulativa de alumínio das vacinas em crianças menores de um ano de idade excede o limite diário estabelecido pelo ATSDR em várias centenas (Fig. 3 e 4), o limite ainda seria excedido se o alumínio das vacinas entrasse no fluxo sanguíneo ao longo de cerca de um ano. Além disso, estudos mostraram que o alumínio das vacinas é absorvido pelas células do sistema imunológico e atinge partes do corpo distantes do local da injeção, incluindo o cérebro.24
A extensão dos efeitos adversos do alumínio nas vacinas não é conhecida, pois não foram realizados estudos de segurança comparando uma população vacinada com vacinas contendo alumínio com uma população não vacinada com essas vacinas.
Limitação de alumínio do fluxo sanguíneo derivado do ATSDR2-14-15
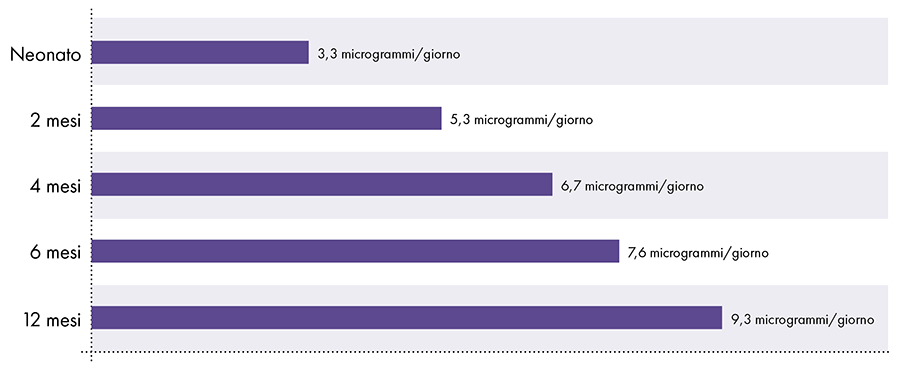 Figura 3: Este gráfico mostra o limite de alumínio para crianças de várias idades, conforme derivado do Registro de Substâncias Tóxicas e Doenças, uma divisão do Departamento de Saúde e Serviços Humanos dos Estados Unidos. O limite indica que não mais de 1 micrograma de alumínio por quilograma de peso corporal deve entrar na corrente sanguínea diariamente para evitar os efeitos neurotóxicos do alumínio.
Figura 3: Este gráfico mostra o limite de alumínio para crianças de várias idades, conforme derivado do Registro de Substâncias Tóxicas e Doenças, uma divisão do Departamento de Saúde e Serviços Humanos dos Estados Unidos. O limite indica que não mais de 1 micrograma de alumínio por quilograma de peso corporal deve entrar na corrente sanguínea diariamente para evitar os efeitos neurotóxicos do alumínio.
Quantidade de alumínio nas vacinas
Referências
- Academia Americana de Pediatria, Comitê de Nutrição. Toxicidade do alumínio em bebês e crianças. Pediatria. 1996 março; 97 (3): 413.
- Agência para Substâncias Tóxicas e Registro de Doenças (ATSDR). Perfil toxicológico para alumínio. Washington, DC: Departamento de Saúde e Serviços Humanos dos EUA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Alumínio nos alimentos — a natureza e contribuição dos aditivos alimentares. In: El-Samragy Y, editor. Aditivo alimentar. Rijeka (Croácia): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Para uma compreensão da ação adjuvante do alumínio. Nat Rev Immunol. 2009 abril; 9 (4): 287.
- Volk VK, Bunney WE. Imunização da difteria com toxóide fluido e toxóide precipitado com alúmen. Am J Saúde Pública Saúde das Nações. 1942 julho; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Sais de alumínio em vacinas — perspectiva dos EUA. Vacina. 2002 de maio de 31; 20 Supl 3: S18-22.
- Administração de Alimentos e Medicamentos dos EUA. Silver Spring (MD): US Food and Drug Administration. Vacinas licenciadas para uso nos Estados Unidos; [atualizado em 2018 de fevereiro de 14; citado em 2018 de fevereiro de 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centros de Controle e Prevenção de Doenças. Washington, DC: Departamento de Saúde e Serviços Humanos dos EUA. Calendário de vacinação recomendado para crianças e adolescentes com 18 anos ou menos, Estados Unidos, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Administração de Alimentos e Medicamentos dos EUA. Silver Spring (MD): US Food and Drug Administration. SCOGS (Comitê Selecionado de Substâncias GRAS); [citado em 2018 de agosto de 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Padre ND. O comportamento biológico e a biodisponibilidade do alumínio no homem, com especial referência aos estudos que empregam o alumínio-26 como traçador: revisão e atualização do estudo. J Environ Monit. 2004; 6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Alumínio em produtos de nutrição parenteral pediátrica: conteúdo medido versus conteúdo rotulado. J Pediatr Pharmacol Ther. 2011; 16 (2): 92-7.
- Sedman A. Toxicidade do alumínio na infância. Pediatra Nephrol. 1992 julho; 6 (4): 383-93.
- Administração de Alimentos e Medicamentos dos EUA, Departamento de Saúde e Serviços Humanos. Regras e regulamentos. Registro Federal. 2003 junho; 68 (100): 34286.
- Centros de Controle e Prevenção de Doenças. Washington, DC: Departamento de Saúde e Serviços Humanos dos EUA. Centro Nacional de Estatísticas de Saúde: Tabela de dados para gráficos de comprimento para idade e peso para idade de meninos; [citado em 2019 de abril de 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centros de Controle e Prevenção de Doenças. Washington, DC: Departamento de Saúde e Serviços Humanos dos EUA. Centro Nacional de Estatísticas de Saúde: Tabela de dados para gráficos de comprimento por idade e peso por idade das meninas; [citado em 2019 de abril de 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Administração de Alimentos e Medicamentos dos EUA, Departamento de Saúde e Serviços Humanos. Revisão dos requisitos para materiais constituintes. Regra definitiva. Registro Federal. 2011 de abril de 13; 76 (71): 20513-8.
- Escritório do Registro Federal, Serviço Nacional de Arquivos e Registros, Administração de Serviços Gerais. Regras e regulamentos. Registro Federal. 1968 janeiro; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Farmacocinética de alumínio atualizada após exposições infantis por meio de dieta e vacinação. Vacina. 2011 de novembro de 28; 29 (51): 9538-43.
- Miller S, Médicos pelo Consentimento Informado. Errata em 'Farmacocinética do alumínio atualizada após exposições infantis através de dieta e vacinação.' In: ResearchGate. Berlim (Alemanha): ResearchGate GmbH; 2020 de março de 6 [citado em 2020 de março de 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Médicos para Consentimento Informado. Newport Beach (CA): Médicos para consentimento informado. Errata em 'Farmacocinética do alumínio atualizada após exposições infantis através de dieta e vacinação'; [citado em 2020 de março de 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorção in vivo de adjuvantes de vacina contendo alumínio usando 26Al. Vacina 1997 Ago-Set; 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Ensaio de alumínio e avaliação da reação local em vários momentos após administração intramuscular de vacinas contendo alumínio no macaco Cynomolgus. Vacina. 2005 de fevereiro de 3; 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Alumínio em plasma e tecidos após injeção intramuscular de vacinas humanas com adjuvante em ratos. Arch Toxicol. 2019 outubro; 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Análise crítica de estudos de referência sobre a toxicocinética de adjuvantes à base de alumínio. J Inorg Biochem. 2018 abril; 181: 87-95.
Artigo traduzido por Médicos por consentimento informado
De acordo com a bula da vacina Shingrix, os eventos adversos relatados durante o ensaio clínico incluíram dor, inchaço e vermelhidão no local da injeção, dor de cabeça, febre, fadiga, calafrios, problemas gastrointestinais, gota e neuropatia óptica isquêmica.(1) A GlaxoSmithKline se comprometeu a realizar vários estudos pós-comercialização para a vacina SHINGRIX, que licenciou em 2017. relatos diziam respeito a mulheres e não eram eventos sérios; a reação mais comum foi dor no local da injeção.(2)
Na reunião do ACIP de fevereiro de 2019, o Dr. Tom Shimabukuro, do CDC's Immunization Safety Office (ISO), relatou um possível sinal de segurança com a vacina SHINGRIX. Uma associação entre a síndrome de Guillain Barré (GBS) e a vacina foi encontrada no Vaccine Safety Datalink (VSD) e no Vaccine Adverse Events Reporting System (VAERS). GBS é uma doença neurológica rara que causa inflamação dos nervos periféricos. As complicações podem incluir paralisia temporária ou crônica, incluindo paralisia completa do corpo.(3)
O CDC, o FDA e os Centros de Serviços Medicare e Medicaid (CMS) conduziram uma revisão dos dados do banco de dados de reivindicações do Medicare. De acordo com a FDA:(4) “O risco de GBS após a vacinação com Shingrix foi avaliado em análises de séries de casos autocontrolados usando uma janela de risco de 1 a 42 dias após a vacinação e uma janela de controle de 43 a 183 dias após a vacinação. GBS nos 42 dias após a vacinação com Shingrix, com um excesso estimado de 3 casos de GBS por milhão de doses administradas a adultos com 65 anos de idade ou mais. Foi observado um risco aumentado de GBS nos 42 dias após a primeira dose de Shingrix, com estimou 6 casos excessivos de GBS por milhão de doses administradas a adultos com 65 anos de idade ou mais, enquanto nenhum risco aumentado de GBS após a segunda dose de Shingrix. ."
A FDA estabeleceu uma associação entre Shingrix e GBS, mas disse que os dados atuais não estão disponíveis para estabelecer uma relação causal. No entanto, concluiu que uma revisão da seção "Avisos e Precauções" do folheto informativo do SHINGRIX sobre o risco de GBS foi justificado.(5)
Eventos adversos adicionais relatados após a vacina Shingrix ter sido aprovada incluíram reações alérgicas, angioedema, urticária e erupção cutânea e diminuição da mobilidade no braço da vacina.(6)
Os eventos adversos relatados em ensaios clínicos ou pós-comercialização com a vacina Zostavax incluem dor, inchaço e vermelhidão no local da injeção, dor de cabeça, erupção cutânea tipo zoster, febre, choque, dor nas articulações e músculos, gânglios inchados e sintomas respiratórios.(7) A neurite óptica após a administração da vacina Zostavax também foi relatada em um estudo de caso publicado.(8)
A bula do Zostavax afirma que "a transmissão do vírus da vacina pode ocorrer entre vacinados e contatos suscetíveis".(9) ou seja, o indivíduo vacinado é infeccioso com catapora da cepa vacinal e pode infectar outros com varicela se eles não tiveram varicela anteriormente.
A Merck, fabricante do Zostavax, está atualmente se defendendo de 60 ações judiciais alegando que a vacina causou sérios efeitos colaterais, incluindo a morte. O resultado desses processos está pendente.(10) As vendas de Zostavax nos Estados Unidos foram descontinuadas em novembro de 2020.(11)
A Merck, fabricante do Zostavax, está atualmente processando e se defendendo contra processos alegando que a vacina causou sérios efeitos colaterais, incluindo a morte.(12) Em dezembro de 2022, um juiz federal da Pensilvânia rejeitou quase 1.200 reclamações alegando herpes-zóster após a vacina Zostavax. As alegações foram negadas pelo juiz devido à falta de evidências de que a erupção cutânea estava relacionada à vacina. Outros processos judiciais sobre distúrbios autoimunes e perda auditiva estão pendentes.(13)
Referências (clique para abrir)
- GlaxoSmithKline Biologicals. Folheto Informativo - SHINGRIX. US Food and Drug Administration Agosto 2, 2021.
- Centros dos EUA para Controle e Prevenção de Doenças. Atas da ACIP de junho de 2018. Junho de 2018.
- Wranham T. ACIP: Vacina contra a gripe 2018-2019 44 por cento eficaz. Centro Nacional de Informações de Vacinas 7 de abril de 2019.
- Administração de Alimentos e Medicamentos dos EUA. FDA exige que um aviso sobre a síndrome de Guillain-Barré (GBS) seja incluído nas informações de prescrição para Shingrix. 24 de março de 2021.
- Administração de Alimentos e Medicamentos dos EUA. FDA exige que um aviso sobre a síndrome de Guillain-Barré (GBS) seja incluído nas informações de prescrição para Shingrix. 24 de março de 2021.
- GlaxoSmithKline Biologicals. Folheto Informativo - SHINGRIX. US Food and Drug Administration Agosto 2, 2021.
- Merck & Co. Folheto Informativo - Zostavax (Frozen). US Food and Drug Administration Dezembro 26, 2019.
- Han S. Neurite óptica após vacinação contra Varicella zoster: relato de dois casos. Vacine 3 de setembro de 2014; 32(39):4881-4.
- Merck & Co. Folheto Informativo - Zostavax (Frozen). US Food and Drug Administration Dezembro 26, 2019.
- Luana, R. Merck arquiva moção para consolidar ações judiciais contra Zostavax na Flórida. O examinador legal Maio 30, 2018.
- Centros dos EUA para Controle e Prevenção de Doenças. O que todos devem saber sobre Zostavax. 5 de outubro de 2020.
- Luana, R. Merck arquiva moção para consolidar ações judiciais contra Zostavax na Flórida. O examinador legal Maio 30, 2018.
- Kansteiner F. A Merck escapa de quase 1,200 ações judiciais contra a vacina contra herpes Zostavax, pois o testemunho dos queixosos é insuficiente. Fierce Pharma Dezembro 8, 2022.
Este artigo foi resumido e traduzido por Centro Nacional de Informações de Vacinas.

