Relatório Técnico Final - Análise do perfil molecular de vacinas

Prefácio
Antes de mais, gostaríamos de agradecer os comentários muito úteis fornecidos por aqueles que revisaram os resultados das análises realizadas no contexto de atividades de pesquisa científica relacionadas aos produtos Priorix tetra e Infanrix Hexa. As questões críticas apresentadas foram realmente muito úteis para adicionar integrações técnico-científicas capazes de esclarecer o trabalho realizado. Acreditamos que somente através de uma saudável comunhão de visões científicas é possível chegar a conclusões sobre os dados obtidos que podem ser úteis para toda a comunidade científica e para as pessoas que as abordam.
1. Estado da técnica
Estudos preliminares (triagem não sujeitos a confirmação) do perfil biomolecular, metabolômico e proteômico, realizados nos produtos Priorix Tetra e Infanrix Hexa, levaram a uma estrutura de composição resumida nos seguintes pontos:
- Presença de diferentes sinais analíticos que não podem ser associados a compostos conhecidos através de pesquisas nos bancos de dados Metlin 1-2 e KEGG3. Portanto, surgiu uma imagem associada a uma considerável complexidade na composição de produtos comerciais.
- Presença de proteínas não declaradas em um folheto no produto Priorix Tetra. Este último pode potencialmente ser associado a resíduos do processo de produção
- Não detecção dos antígenos declarados no produto Infanrix Hexa. A técnica de análise consistiu na digestão enzimática com tripsina associada às técnicas de espectrometria de massa. 4/5
Esses dados levantaram vários comentários, especialmente sobre o ponto C - A detecção de proteínas é de fato realizada usando uma abordagem padrão, internacionalmente reconhecida por mais de 10 anos 4, de digestão através da enzima tripsina 4. Os peptídeos assim obtidos são separados por cromatografia e analisados por espectrometria de massa 4-5. A principal observação foi inerente ao fato de que nas vacinas existem adjuvantes à base de alumínio que poderiam potencialmente inibir o processo de digestão enzimática. Os dados adquiridos posteriormente permitiram fornecer esclarecimentos substanciais, especialmente no que se refere à denúncia expressa no ponto C.
2. Novas idéias e análises
2.1 Informações relacionadas à análise do produto Infanrix Hexa
Antes de prosseguir com a ilustração dos novos dados adquiridos sobre as vacinas Hexyon e Gardas 9, é essencial responder à pergunta sobre a dúvida levantada sobre a inibição da atividade proteolítica da tripsina causada pela presença de adjuvantes à base de alumínio no Infanrix Hexa. vacina. A esse respeito, deve-se especificar que um controle de digestão está sempre presente na digestão tríptica. De fato, a tripsina usada para realizar a digestão, embora projetada para impedir a autólise, possui uma pequena porcentagem desta última que, no caso de atividade enzimática, leva à obtenção do fragmento com m / z 842 e a seguinte sequência peptídica: VATVSLPR. O referido fragmento foi realmente detectado na digestão tríptica do produto Infanrix Hexa como verificável pelo cromatograma de extração de íons (Figura 1).
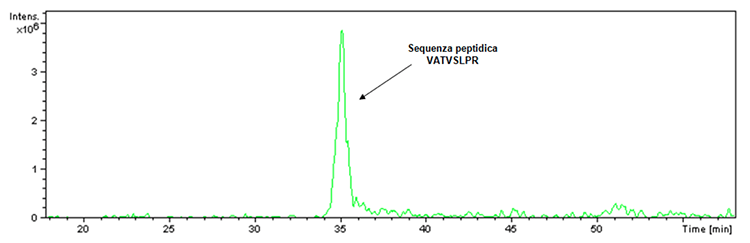
Figura 1: Cromatograma de extração iônica associado a íons com a razão m / z 842 encontrada na amostra do lote do produto Infanrix Hexa (lote nº A21CD072D).
Além disso, um controle externo é realizado por digestão da hemoglobina, a fim de verificar ainda mais a bondade do lote de tripsina utilizado. A hemoglobina, analisada na seção de análise em que o produto foi monitorado, foi reconhecida com um escore estatístico significativo (loge <- 100). Esses dados confirmaram o fato de que a atividade enzimática estava presente.
2.2 Novas análises relativas aos produtos Hexyon e Gardasil
A análise dos produtos Hexyon e Gardas 9 levou à detecção de perfis moleculares complexos. Neste caso, no entanto, foi detectada a presença da maioria dos antígenos relatados no folheto informativo. Eles foram detectados por digestão tríptica e na presença de adjuvantes.
Esse fato reforça ainda mais a evidência de que a reação de digestão triptica não é inibida na presença de adjuvantes. No caso das vacinas Hexyon e Gardas 9, a complexidade do perfil molecular foi atribuída principalmente à presença de numerosas espécies, com baixo peso molecular, não identificáveis pelas bases de dados de referência Metlin 1-2- e KEGG 3.
3. Conclusões e considerações finais
As análises realizadas levaram à conclusão do seguinte:
- O perfil molecular das vacinas analisadas é geralmente complexo e amplamente desconhecido.
- Existem contaminações proteicas, não declaradas no folheto, cuja composição é variável.
- Em vários casos, os antígenos declarados no folheto não foram detectados. Esse fato pode ser atribuído a vários fatores. Entre os últimos, podemos considerar a sensibilidade do método utilizado. No entanto, sentimos que podemos excluir o fenômeno da inibição da digestão devido à presença de adjuvantes na formulação da vacina. De fato, a atividade enzimática é confirmada principalmente pela presença de fragmentos de autólise tríptica, dentro das soluções das vacinas digeridas (controle interno).
4. Estudos futuros
Novos estudos serão realizados como parte das atividades de pesquisa e desenvolvimento destinadas a investigar os seguintes aspectos:
- composição macromolecular associada a resíduos sólidos presentes em vacinas (análise MALDI TOF MS); 5
- avaliação da concentração dos metais presentes nos produtos.
- Análise de segundo nível para confirmar a presença de compostos tóxicos detectados na fase de triagem. Sua concentração será então relacionada à toxicidade do mesmo, conforme indicado nas fichas de dados de segurança internacionais. As análises de segundo nível serão realizadas em conformidade com a diretiva européia UE 2002/657 / EC, útil para garantir altos padrões de qualidade no setor de espectrometria de massa. 6
Loretta Bolgan
5. Referências bibliográficas
- Autenhahn R, Cho K, Uritboonthai W, Zhu Z, Patti G, Siuzdak G (setembro de 2012). "Um fluxo de trabalho acelerado para metabolômica não segmentada usando o banco de dados METLIN". Nature Biotechnology. 30: 826-828. DOI: 10.1038 / nbt.2348. PMC 3666346. PMID 22965049.
- Smith CA, I'Maille G, Want EJ, Qin C, Trauger SA, Brandon TR, Custodio DE, Abagyan R, Siuzdak G (dezembro de 2005). "METLIN: um banco de dados espectral de massa de metabólitos" (PDF). Ther Drug Monit. 27 (6): 747-51. doi: 10.1097 / 01.ftd.0000179845.53213.39. PMID 16404815.
- Kanehisa M (2013). "Evolução química e genômica de redes de reação catalisadas por enzimas". FEBS Let. 587 (17): 2731–7.
- Cristoni S, Bernardi LR. "Bioinformática na análise de dados por espectrometria de massa para estudos de proteômica". Rev Rev Proteomics. Dezembro de 2004; 1 (4): 469-83.
- Cristoni S, Bernardi LR. "Desenvolvimento de novas metodologias para o estudo de espectrometria de massa de macromoléculas bioorgânicas." Mass Spectrom Rev. 2003 nov-dez; 22 (6): 369-406.
- O objetivo deste estudo foi avaliar a eficácia do uso de antimicrobianos em pacientes com insuficiência renal crônica em pacientes com insuficiência renal crônica. Noonan DM. "SANIST: otimização de uma tecnologia para identificação de compostos com base na diretiva da União Européia com aplicações em análises forenses, farmacêuticas e de alimentos". J. Mass Spectrom. Jan 2017; 52 (1): 16-21. doi: 10.1002 / jms.3895.
Download: CORVELVA-Final-Técnico-Report.pdf
Traduzido pela equipe do CLiVa - www.clivatoscana.com

