Resumo - Confirmação de dados por análise interlab

Queridos amigos,
estamos apresentando este relatório com um estado mental diferente e mais emocional, já que este é o último de 2019 e chegamos ao fim do que tínhamos planejado para este ano.
O relatório é um documento que resume os trabalhos que realizamos e apenas confirma o que era hipotético antes, e agora se tornou dados confiáveis.
Encerramos nossos fundos para este projeto e nos sentimos extremamente satisfeitos, porque os bolsos vazios nesses tempos difíceis significam que todas as nossas energias foram usadas para a causa, sem peças de reposição.
Como aconteceu desde 2017, financiaremos automaticamente nossos projetos graças às taxas de associação e doações e continuaremos em 2020, com toda uma série de investigações que devem levar o problema a um nível superior; enquanto isso, dedicaremos os próximos meses para informar e interagir com associações estrangeiras para prosseguir com a reclamação internacional. Temos muito trabalho, honestamente, existem mais idéias do que as energias e as possibilidades econômicas disponíveis.
Juntos, iniciamos uma jornada que dura há muito tempo e hoje conseguimos divulgar os resultados desse projeto para todo o mundo. Nossa determinação, como pais e cidadãos italianos, é hoje um exemplo para muitas outras nações que infelizmente estão se preparando para travar as mesmas batalhas em defesa dos direitos humanos fundamentais.
Sim, é verdade, as instituições parecem surdas e nenhuma vírgula foi movida ainda, pelo menos não de maneira clara; o mais triste é que nossos filhos são excluídos das escolas, mas vamos dar uma olhada: O sistema mundial gravita em torno do dogma da vacinação apoiado por uma "comunidade científica" que, somente na Itália, recebeu mais de meio bilhão de euros em alguns anos. 1 É um monte de dinheiro que moveu uma série de pseudo-cientistas, contratou médicos e políticos preguiçosos, prontos para proteger os interesses daquelas entidades que o Prof. Randy Schekman, Prêmio Nobel de Medicina em 2013, chamou de "casta". 2
"A ciência está em risco: não é mais confiável porque está nas mãos de uma casta fechada e qualquer coisa, menos independente" e isso agora é evidente até para o mais cético dos espectadores - se de boa fé. Persegue interesses que não são os que acompanham o método científico, pelo menos não como deveria ser; produz estudos que, para serem publicados, devem obedecer a alguns dogmas impostos, omitindo alguns dados que "não concordam" ou destacando outros que, ao contrário, "são convenientes" e isso é algo que experimentamos diretamente, embora apenas negligenciámos isso mundo.
Nessa situação desprezível, nos deparamos com uma imposição legal à administração de produtos farmacêuticos, uma lei que enriquece e aumenta o poder daquela casta da qual Nobel Schekman fala.
Diante de tal situação sócio-política, nós, como cidadãos e pais conscientes e determinados, nos fortalecemos, com a ajuda de outros cidadãos como nós; tomamos as ações que pareciam mais eficazes ou simplesmente mais "acessíveis", com base em nossas possibilidades: mostramos que com pouca força, mas com determinação, podemos produzir grandes resultados.
Começamos com essas poucas linhas de abertura porque hoje, como o último relatório da Corvelva, falaremos sobre os últimos resultados, que são confirmações obtidas através de análises realizadas tanto por uma prestigiada universidade européia quanto por outros laboratórios certificados localizados em diferentes partes do mundo . Os dados são sempre mais certos e o que era provável antes agora é DEMONSTRATIVO!
Entre outras coisas, investigamos alguns compostos tóxicos e / ou cancerígenos, como NDMA nitrosodimetilaminas e cianoidrinas, e os resultados foram realmente preocupantes. Iremos necessariamente falar sobre isso com as publicações de revisão por pares em mãos, para não comprometer as próprias publicações.
Como explicado, esses estudos aprofundados, bem como aqueles sobre sequenciamento de DNA fetal, são o assunto da próxima publicação de revisão por pares. Por isso, estamos realmente comunicando uma pequena parte do que será publicado, mas é isso que a ciência pede, que os dados são novos. Se reportarmos mais detalhes, colocaremos o trabalho em prática. O fato é que os órgãos de controle receberam tudo, no original!
Continuaremos com as informações e lutaremos para que os resultados perturbadores sejam considerados pelo que são, também dados analíticos, sem preconceitos ou ideologias. Os produtos analisados por nós devem ser retirados em massa e há uma grande pergunta a ser feita sobre os interesses que gravitam em torno de todos aqueles que se colocaram contra nossas análises e / ou a favor do dogma da vacinação.
Juntos, podemos tentar parar toda essa loucura.
Resumo dos resultados confirmados obtidos para cada vacina
Para realizar esta pesquisa, decidiu-se usar um limite entre nanogramas e microgramas, portanto, acima do limite residual para compostos desconhecidos não relatados na folha de dados técnicos.
Deve-se enfatizar que a quantidade cumulativa desses contaminantes está acima de microgramas por dose, embora não seja possível fazer uma quantificação exata no momento, como a maioria dos contaminantes não é conhecida e, portanto, não é possível realizar o estudo usando o controle de padrões analíticos.
A partir dos resultados da triagem e dos controles com os padrões, parece que a fração metabólica mostra compostos candidatos cuja presença só pode ser explicada com um controle inadequado e, consequentemente, com a má qualidade das matérias-primas e reagentes. Em particular, a contaminação cruzada com compostos químicos com atividade farmacológica conhecida está fora de controle, embora seja possível que o processo de produção da vacina mude sua estrutura e conformação original.
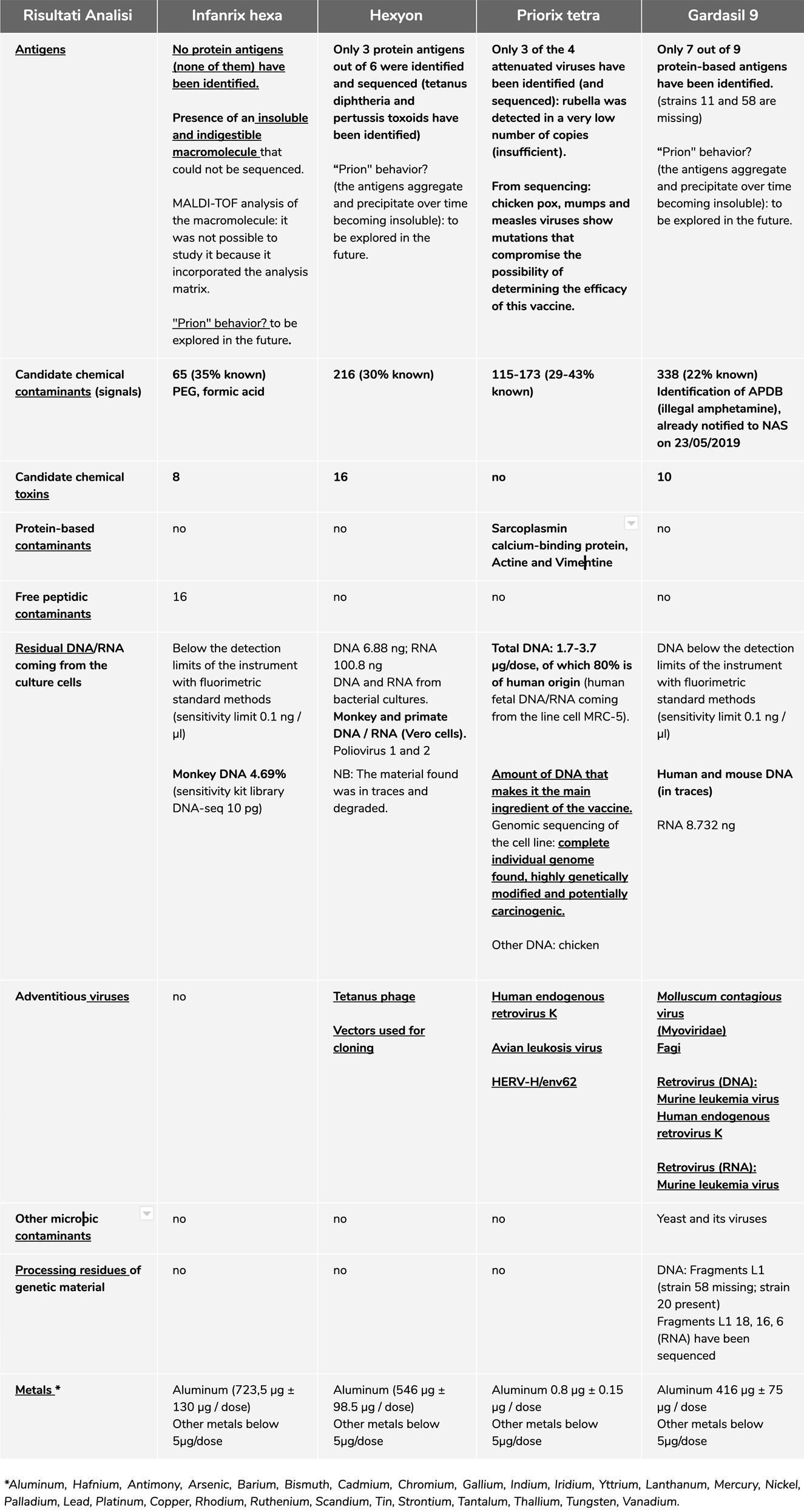
Especificação de resultados confirmados
No final deste resumo, reportaremos todos os links de todos os relatórios das análises realizadas. Consulte-os sempre para uma compreensão detalhada dos resultados, pois aqui abaixo, falaremos apenas das análises confirmatórias por meio de triagem de segundo nível. , normas de controle e / ou interlaboratorial.
Um exemplo para entender melhor: um provedor de serviços certificado realizou algumas análises mediante solicitação. Eles foram convidados a trabalhar em alvos, para identificar a presença ou ausência de alguns compostos orgânicos ou inorgânicos em certas vacinas (nem todas) ou em seqüências genéticas. Portanto, o resultado é apenas sobre o que pedimos para procurar, que é um elemento indispensável para confirmar a validade do método usado por nós.
O motivo de não ter utilizado numerosos padrões de controle e outras vacinas no mercado tem raízes econômicas e lógicas: não somos uma instituição de pesquisa e estamos fazendo estudos aprofundados. Depois de relatar a não conformidade aos órgãos reguladores, fato que vai além do que devemos competir, para todos os efeitos, estamos substituindo inadequadamente os próprios órgãos reguladores em investigações que caberiam a eles após um relatório dessa magnitude, e estamos fazendo isso porque nossos dados foram chamados incompletos.
Análise da vacina Hexyon®
metagenomic
A presença do material genético contaminante foi confirmada com a análise interlaboratorial em um provedor de serviços certificado europeu.
O DNA presente é igual a 6.88 ng total por dose (esta quantidade refere-se ao relatório divulgado. Os dados da análise interlaboratorial estão sujeitos a revisão por pares e, portanto, não são divulgados, mas confirma a ordem da magnitude), dos quais 0, 1% potencialmente provenientes de células Vero (Cercopithecidae), ou seja, 688 pg / dose. Identificamos o fago de Clostridium phiCT453A e SV40 juntamente com outros vetores para a clonagem.
Presença de poliovírus 1 e 2. Nesse caso, a resposta da EMA à ausência do Poliovírus 3 foi muito genérica: a ausência do Poliovírus 3 não é uma não conformidade para eles, porque consideram a presença do antígeno D, capaz de criar imunização. Obviamente, procuramos essa proteína, mas não conseguimos encontrá-la. Seria uma excelente análise aprofundada, porque atualmente deixamos uma resposta incerta sobre esse ponto.
DNA e RNA de bactérias utilizadas para produzir antígenos de Corynebacterium diphtheriae (Difteria), Clostridium tetani (Tétano), Bordetella pertussis (Pertussis) e Haemophilus influenzae.
NOTA: o material genético adventício presente na vacina pode ser ligado ao alumínio adjuvante com possível aprimoramento de efeitos tóxicos (capacidade inflamatória, autoimune e tumoral). Reiteramos que, a partir dos dados interlaboratoriais confirmados, a segurança e a eficácia desta vacina permanecem duvidosas, resultando em um produto completamente não conforme com referência à qualidade.
Análise de vacina Gardasil 9®
Chemical-proteico
Após os resultados anteriores, decidimos investigar, com confirmação interlaboratorial, a identificação do composto APDB (anfetamina ilegal), já notificado ao NAS em 23 de maio de 2019. Dois laboratórios diferentes confirmam a presença de uma substância pertencente a a classe de APDBs ilegais.
Repetimos novamente: não podemos comprar o padrão de controle, sendo o APDB classificado como narcótico, 3 não pode ser adquirido por pessoas sem autorização específica; portanto, fornecemos toda a documentação que confirma a presença de uma substância pertencente à classe APDB e a possível origem da contaminação (Nota: para o registro do Gardasil 9®, os relatórios de avaliação EMA que a L-tirosina é usada como matéria-prima para a produção desta vacina e é extraída do cabelo humano da China. 4 A principal produção desse narcótico é originária da China e os viciados têm um nível muito alto em seus cabelos. 5
metagenomic
A presença de material genético foi confirmada por análise interlaboratorial em um provedor de serviços certificado europeu e podemos repetir os dados anteriores, eles descobriram:
- DNA humano e de camundongo (abaixo dos limites de detecção do instrumento);
- Vírus adventícios;
- Fragmento L1 do vírus de DNA HPV de cadeia dupla;
- Os fagos;
- Vírus do molusco contagioso;
- retrovirus:
-
- Vírus da leucimia murina;
- Retrovírus endógeno humano K;
- Saccharomyces
NOTA: o material genético adventício encontrado na vacina pode ser ligado ao alumínio adjuvante com possível aprimoramento dos efeitos tóxicos (capacidade inflamatória, autoimune e tumoral)
Análise de vacina Priorix Tetra®
metagenomic
A presença de material genético foi confirmada por análise interlaboratorial em um fornecedor de serviços certificado europeu.
As quantidades referem-se aos relatórios divulgados. Os dados da análise interlaboratorial estão sujeitos a revisão por pares e, portanto, não são divulgados, mas confirmam a ordem de magnitude.
DNA - A quantidade total de DNA presente nesta vacina varia de: 1.7 - 3.7 µG / dose e é, de fato, o principal componente da vacina. Há cerca de 80% do DNA humano (74-88%) e do frango (0-4%).
O genoma humano é completo, ou seja, com genes e sequências não codificantes, de alto peso molecular, masculino, qualificados como pertencentes à linha fetal MRC-5, que é a linha celular contínua derivada do tecido pulmonar do feto abortivo masculino dos anos 60 . O sequenciamento desta linha celular provou ser altamente geneticamente modificado e potencialmente cancerígeno. A análise de seqüenciamento de todo o genoma do DNA fetal foi realizada em um prestador de serviços americano (laboratório).
RNA - Humano 68-87%. Frango 0-0.2%
Vírus atenuado - Os seguintes vírus atenuados foram confirmados muito. A71CB256A:
- Varicela (DNA) 11%;
- Caxumba (RNA) 0.008%;
- Sarampo (RNA) 0.004%;
- Rubéola 0.00004%. (114 de 260 milhões de sequências)
Uma presença irrelevante de rubéola na vacina (menor que os vírus adventícios mostrados abaixo) foi confirmada interlaboratoriamente. Isso prejudica seriamente a eficácia da vacina.
Quase-espécies virais: foram identificadas 245 variantes no genoma da varicela da vacina em relação ao genoma de referência usado para a análise (genoma selvagem da linhagem Dumas). Destas variantes, 154 são variantes principais, enquanto as 91 restantes são variantes de quase espécies. Não há diferença entre as variantes encontradas nos dois lotes. No genoma da vacina contra caxumba, foram identificadas 40 variantes de quase espécies com relação ao genoma de referência usado para a análise (genoma da vacina Jeryl-Lynn), a comparação entre as variantes encontradas nos dois lotes destaca quatro diferenças. A EMA não conseguiu fornecer as seqüências de vírus da vacina usadas pelo fabricante para esta vacina, uma vez que são cobertas por segredos comerciais, razão pela qual não sabemos quanto vírus da vacina foram alterados em comparação com o que o fabricante declarou.
Devido à baixa cobertura, não foi possível detectar variantes de quase espécies para os genomas do sarampo e da rubéola.
Vírus adventícios - Confirmamos a presença desses vírus adventícios:
- Retrovírus endógeno humano K;
- Vírus da leucose aviária;
- HERV-H / env62.
Para todas as vacinas
Análise de contaminações químicas com controle e normas interlaboratoriais
Dois compostos foram escolhidos para serem analisados com padrões de controle certificados, com base na disponibilidade, na consistência dos dados semiquantitativos e no impacto na saúde. Estes compostos foram confirmados como similares (isto é, com uma identidade estrutural de 75 a 80%: isômeros / isobares) também por análise interlaboratorial. A estrutura desses compostos será divulgada com a publicação da revisão por pares.
Triagem de segundo nível em contaminações químicas
A pesquisa de triagem de segundo nível, como já mencionado, é dividida em três análises:
- triagem aprofundada da parte submersa (65% do total de sinais) e comparação com o banco de dados das substâncias detectadas, incluindo o banco de dados de toxinas.
- Análises de perdas neutras: a detecção de fragmentações neutras estáveis nos permite hipotetizar a presença na vacina de moléculas que as contêm, de estrutura desconhecida, mas com potenciais efeitos tóxicos se os grupos funcionais tiverem uma atividade carcinogênica e mutagênica [a “Coorte de Preocupação” criada pela EMA para drogas orais inclui compostos do tipo aflatoxina, N-nitroso- e alquil-azoxi, conforme relatado na diretriz ICH M7 (R1). 6
Novos compostos candidatos: foram detectados compostos potencialmente tóxicos para todas as vacinas examinadas (contaminação cruzada) com base na comparação com bancos de dados. Seria útil investigá-lo usando padrões de verificação para confirmar sua identidade.
Perdas neutras: no nosso caso, foram examinados os grupos cianil (isto é, derivados do ácido cianeto usado para preparar a vacina contra o Haemophilus B) e a nitrosodimetilamina, uma impureza cancerígena encontrada em outros fármacos e sujeita a avaliação pela EMA. 7
Para entender o grupo funcional das nitrosodimetilaminas, considere que é da mesma classe que as contaminações encontradas nos medicamentos Sartan e Ranitidina, que saltam para a notícia da recente retirada maciça de medicamentos em toda a Europa. 8 O segundo grupo funcional é o dos cianetos, dos quais sabemos a presença declarada de cianeto de sódio, como mostrado nas folhas de dados técnicos da vacina Prevenar. 9
A triagem de segundo nível, portanto, deu uma resposta positiva para todas as vacinas. No momento, não é possível divulgar os resultados em detalhes porque eles estão na fase de publicação da revisão por pares, mas todos os órgãos reguladores foram informados sobre nossos resultados.
A legislação
Observe o que deve ser feito por lei sobre drogas comerciais: 10
O Programa Anual de Controle permite garantir que os medicamentos vendidos correspondam exatamente às especificações de qualidade dos procedimentos de autorização. É estabelecido anualmente pela AIFA, depois de ter ouvido o parecer do Istituto Superiore della Sanità, e é aprovado pelo Comitê Científico Técnico (CTS) da AIFA. O Escritório de Qualidade de Produtos da AIFA exige que o NAS (Unidade dos Carabinieri) responsável por impedir a adulteração de alimentos, medicamentos e bebidas) colete amostras dos medicamentos fornecidos no programa, que são enviados ao ISS para análise em farmácias ou atacadistas . Se os resultados da análise revelarem diferenças em relação ao que foi autorizado, o Escritório de Qualidade dos Produtos da AIFA tomará as medidas necessárias. As análises realizadas são baseadas na verificação do cumprimento das especificações de qualidade autorizadas para cada medicamento e relatadas no dossiê de registro e / ou nas monografias da Farmacopeia Europeia. (...)
O Escritório de Qualidade do Produto também gerencia a revogação e suspensão de autorizações de introdução no mercado.
A AIC de um medicamento pode ser revogada, com conseqüente retirada definitiva do mercado quando:
- o medicamento é prejudicial em condições normais de uso;
- o medicamento não tem o efeito terapêutico ou o efeito para o qual foi autorizado;
- a relação risco / benefício não é favorável em condições normais de uso;
- o medicamento não possui a composição qualitativa e quantitativa declarada;
- o medicamento foi produzido em estabelecimentos não autorizados.
A autorização pode ser revogada mesmo que as informações contidas no pedido de autorização do medicamento não sejam corretas ou na ausência de controles sobre o produto acabado, componentes ou produtos intermediários de produção.
Além das intervenções adotadas a nível nacional, as medidas do sistema de alerta rápido, definidas com base em procedimentos europeus compartilhados, são realizadas ao mesmo tempo; estes consistem em diferentes ações e notificações de acordo com o tipo de gravidade do defeito, de acordo com a classificação de urgências.
A Figura 2 descreve a classificação dos defeitos e as ações relacionadas a serem tomadas
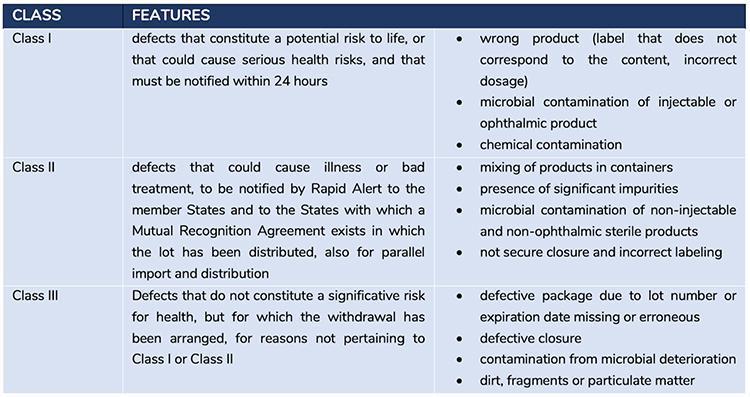
Por favor note que isso os defeitos detectados com a análise realizada por Corvelva se enquadram nas classes I e II, pois as vacinas são medicamentos para uso injetável e as contaminações detectadas são de um tipo de material químico e genético.
Sublinhamos que, atualizado, nenhuma medida foi tomada pelas agências reguladoras, apesar da notificação à AIFA dos resultados das análises preliminares e do NAS da presença do composto APDB na vacina Gardasil 9®: isso está em violação grave do princípio da precaução e da necessidade de intervenção rápida, conforme previsto pelo Sistema de Alerta para a proteção da saúde pública.
Download: CORVELVA-Sumário-Data-confirmação-Interlab-analysis.pdf
Observação:
- https://www.corvelva.it/it/approfondimenti/sistema-sanita/case-farmaceutiche/efpia-italia-tutti-i-trasferimenti-di-valore-delle-big-pharma.html
- http://www.medicinapiccoledosi.it/medicina-convenzionale/premio-nobel-la-medicina-randy-schekman-la-scienza-mano-ad-casta/
- http://www.cortedicassazione.it/cassazione-resources/resources/cms/documents/Legge_79_2014.pdf
http://www.rivistagiuridica.aci.it/fileadmin/Documenti/Decreto_25_giugno_M_Salute_02.pdf - https://www.unodc.org/documents/scientific/Trends_and_Patterns_of_ATS_and_NPS_2017.pdf
- Análise por Cromatografia Gasosa-Espectrometria de Massa (GC-MS)Journal of Food and Drug Analysis, Vol. 13, No. 3, 2005, Páginas 193-200 Análise por cromatografia gasosa-espectrometria de massa (GC-MS) Análise de anfetamina, metanfetamina, 3,4-metilenodioxi-anfetamina e 3,4-metilenodioximetanfetamina em Cabelo humano e seções de cabelosDONG-LIANG LIN1,2 *, REA-MING YIN1 E RAY H. LIU3
- https://www.ema.europa.eu/en/documents/ … /ich-guideline-m7r1-assessment-control-dna-reactive-mutagenic-impurities-pharmaceuticals-limit_en.pdf
- http://www.agenziafarmaco.gov.it/content/comunicazione-ema-sul-principio-attivo-valsartan-19112018
- https://www.repubblica.it/salute/medicina-e-ricerca/ … /news/non_solo_ranitidina_per_l_ema_vanno_testati_tutti_i_farmaci_per_impurita_cancerogene-237010173/
- https://www.ema.europa.eu/en/documents/scientific-discussion/prevenar-epar-scientific-discussion_en.pdf
- http://www.bollettinosifo.it/r.php?v=2598&a=26744&l=329640&f=allegati/02598_2016_06/fulltext/05_EspOpin_Cannizzo.pdf

