Primeira publicação revisada por pares sobre vacinas MMRV (Priorix Tetra)

Finalmente, aqui estamos - depois de quase dois anos - a primeira publicação revisada por pares de nossas análises está sendo lançada e muitas outras serão publicadas.
O objetivo deste artigo é resumir os seguintes problemas: o que foi publicado, qual é a sua validade e por que é importante para a nossa investigação sobre vacinas. Todos esses argumentos serão tratados de maneira coloquial e não técnica nas primeiras páginas, enquanto a partir da página 3 haverá um estudo técnico para permitir que os especialistas deste setor avaliem o artigo em si.
O artigo publicado em "F1000 Research"1 é o resultado do estudo inicial realizado por um dos laboratórios que a Associação Corvelva nomeou para realizar as análises. Lembramos - porque mais de dois anos se passaram desde o início deste trabalho e muitos outros resultados foram adicionados aos primeiros - que a primeira questão importante que tivemos que investigar foi a quantidade anormal de DNA humano encontrada nas vacinas analisadas.
As análises iniciais mostraram que ambas as vacinas quadrivalentes contra MMRV analisadas continham de 1 a 2.7 microgramas / frasco (conforme publicado no presente artigo) e decidimos relatar publicamente e imediatamente esses resultados, porque, simplesmente, não era esperado que tal quantidade de O DNA pode estar presente dentro de uma vacina.
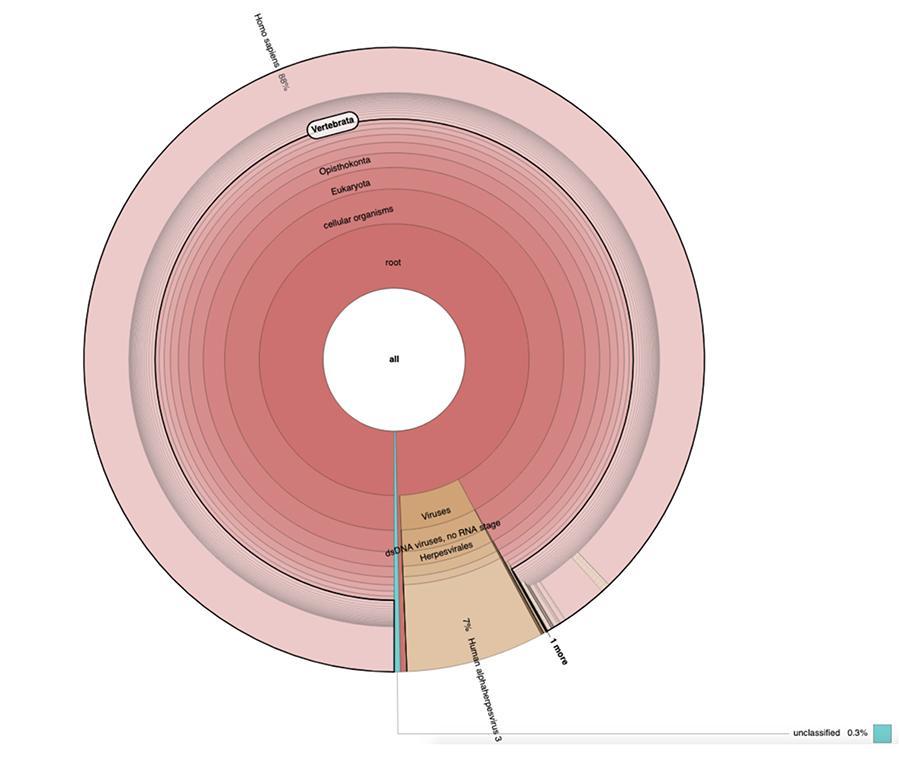
Além das considerações e conclusões alcançadas pelo estudo, que são estritamente técnicas e, portanto, compreensíveis apenas para aqueles que trabalham no campo da pesquisa metagenômica, o que é observado nos gráficos é que as duas amostras de vacina contêm uma alta porcentagem de leituras de DNA humano além dos esperados no genoma do vírus da varicela (vírus alfa-herpes humano 3), o único detectável entre quatro, como uma análise do tipo DNA-seq, foi apresentado no artigo.
No entanto, gostaríamos de salientar que as quantidades de DNA encontradas e confirmadas por o mesmo método que agora é validado aqui foram ainda maiores: até 3.7 microgramas por frasco, levando a uma diferença considerável de lote para lote. De fato, em nosso relatório divulgado em 22 de dezembro de 20182 os resultados obtidos da análise de diferentes lotes daqueles discutidos no presente artigo foram relatados e confirmados por análises interlaboratoriais que ainda estão em processo de publicação.
Portanto, o que deve ser considerado de grande interesse na presente publicação é que valide o método que usamos, dá um ponto importante às discussões sobre o "tipo" de análise realizada, e como conseqüência confirma de forma definitiva todos os estudos que foram subsequentemente realizados com o método NGS: a análise aprofundada sobre o tipo de material genético, a presença de vírus adventícios, a grande ausência de vírus atenuados que deveriam estar presentes e a quantidade de DNA humano completamente fora de controle (também porque muito diferente de amostra para amostra) , a população mutante, fagos, DNA de outras espécies e assim por diante. Você pode encontrar o atodos os resultados resumidos em nosso site3.
Tudo o que denunciamos nos últimos anos, do ponto de vista biológico, relatando minuciosamente os resultados aos órgãos de controle, assume uma conotação científica mais relevante (mesmo que, repetindo-a novamente, não foram as revisões por pares que tiveram que ser feitas). preocupação, mas os dados apresentados, muito sérios em seu conteúdo e suas possíveis implicações para a saúde humana). No entanto, agora que a publicação do método foi concluída, exigiremos as respostas que ainda não foram dadas.
Esses resultados confirmam inquestionavelmente a presença de DNA fetal nas vacinas Priorix tetra, em quantidades variáveis de lote para lote, indicando um controle de qualidade insuficiente desses produtos farmacêuticos.
Também gostaríamos de lembrar o relatório sobre todo o sequenciamento do genoma MRC-5 publicado no site da Corvelva em 27 de setembro de 20194 mostrando a profunda modificação desse DNA até mesmo em genes ligados ao desenvolvimento de doenças tumorais (esses dados também serão publicados em breve). O DNA fetal contaminante encontrado em todas as amostras analisadas em quantidades variáveis (ou seja, não controladas) é até 300 vezes maior do que o limite imposto pela EMA para DNA carcinogênico (10 ng / dose, correspondente ao DNA contido em cerca de 1000 células cancerosas, com base em cálculo estatístico, enquanto o limite de precaução é de 100 pg / dose), um limite que deve ser necessariamente aplicado também ao DNA fetal que contamina inevitavelmente a vacina Priorix Tetra.
Em consequência, esta vacina deve ser considerada defeituosa e potencialmente perigosa para a saúde humana, em particular para a população pediátrica, que é muito mais vulnerável a danos genéticos e autoimunes devido à imaturidade dos sistemas de imunidade.
Conforme previsto, a parte seguinte do artigo é mais "técnica" e difícil de entender para não especialistas; portanto, decidimos, mesmo para fins de transparência, anexar também a este documento o "Dossiê EMA - Dossiê NGS Discussão sobre os resultados da pesquisa de qualidade da vacina". Tivemos que extrapolar apenas a parte que poderia ser publicada, ou seja, 50 páginas do dossiê em comparação com as 200 páginas do NGS, uma vez que muitas das informações contidas e registradas nos órgãos reguladores devem permanecer confidenciais. A lei estrita da ciência determina que uma informação só pode ser publicada em um periódico se for original e, como temos outros trabalhos em andamento, não queremos colocá-la em risco.
Dossiê da EMA - NGS Discussão sobre os resultados da pesquisa de qualidade da vacina ". - https://bit.ly/342XKi7
Por fim, para evitar mal-entendidos, gostaríamos de destacar a parte da "Declaração de Financiamento" da publicação mencionada acima:
"O seqüenciamento metagenômico B1 e B2 foi financiado pela Corvelva (associação sem fins lucrativos, Veneto, Itália), sob um contrato de serviço com o laboratório. Nenhuma outra contribuição estava envolvida no apoio ao trabalho. Os financiadores não tiveram nenhum papel no design do projeto. estudo, coleta e análise de dados, decisão de publicação ou preparação do manuscrito "
Anexado:
- Publicação - Você me ama? Efeito da redução de cobertura nos estudos de sequenciamento de metagenoma
- CORVELVA fios de NGS-EMA-eng
- Primeira publicação revisada por pares sobre vacinas MMRV (Priorix Tetra)
No artigo “Você me ama? Efeito da redução da cobertura nos estudos de sequenciamento de metagenoma da espingarda "
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
Os autores abordam a questão técnico-metodológica se é possível usar uma abordagem metagenômica massivamente paralela com baixa cobertura de leitura para caracterizar matrizes biológicas complexas. Estimativas de diversidade, abundância de espécies e capacidade de reconstruir o metagenoma de novo em termos de comprimento e integridade são calculados, a fim de entender o quanto a diminuição na profundidade do seqüenciamento, variada por leituras aleatórias de subamostragem, pode afetar os resultados finais. Os resultados mostram que os índices de diversidade de comunidades procarióticas, eucarióticas e virais complexas podem ser estimados com precisão com 500,000 leituras ou menos, embora amostras particularmente complexas possam exigir 1,000,000 leituras. Pelo contrário, um projeto envolvendo a reconstrução do metagenoma e dos genes contém requer mais de 1,000,000 de leituras.
Entre as várias matrizes complexas, e muito diferentes umas das outras, submetidas a análises metagenômicas maciças, foram incluídos dois medicamentos biológicos, dois lotes diferentes de vacina viva MPRV atenuada usada para imunização contra sarampo, caxumba, rubéola e varicela em crianças. O DNA foi extraído das vacinas, as bibliotecas genômicas foram construídas usando protocolos comerciais padrão e o sequenciamento maciço foi realizado com a tecnologia Illumina.
Além das considerações e conclusões alcançadas pelo trabalho, que são estritamente técnicas e, portanto, compreensíveis apenas para quem pesquisa no campo da metagenômica, o que é observado nos gráficos de pizza contidos nos dados estendidos (https://osf.io/wq395/ amostras B1 e B2) é que as duas amostras de vacina contêm uma alta porcentagem de leituras de DNA humano, além das esperadas no genoma do vírus da varicela (Human alfaherpes vírus 3), o único detectável entre os quatro, uma vez que uma análise do tipo DNA-seq foi apresentada no artigo.
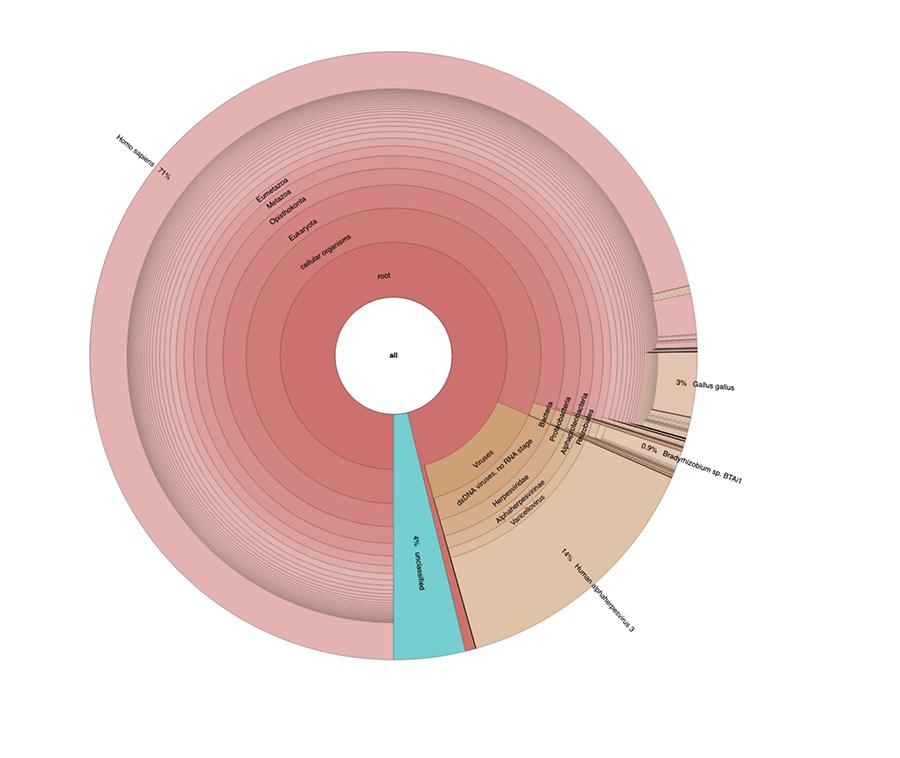
71% das leituras em um lote e 88% no outro são de origem humana, presumivelmente derivadas da linha celular fetal MRC-5 (lembre-se de que análises subsequentes confirmaram que a linha é MRC5) na qual os vírus vivos da rubéola e da varicela são atenuados. cultivada durante a preparação da vacina. Além disso, como aconteceu nos diferentes lotes da mesma vacina MPRV testada pela Corvelva entre 2017 e 2019, a quantidade de DNA extraído é da ordem de microgramas.
Nos lotes de vacinas testados com os mesmos protocolos e tecnologias relatados nos materiais e métodos do artigo, as quantidades detectadas variaram de 1 a quase 3 microgramas por frasco, quantidades variando entre os lotes, mas sempre significativas.
No relatório publicado por Corvelva em 22.12.2018 5, os seguintes resultados foram relatados para outros lotes analisados após os discutidos no artigo, posteriormente confirmados por análises interlaboratoriais ainda em processo de publicação.
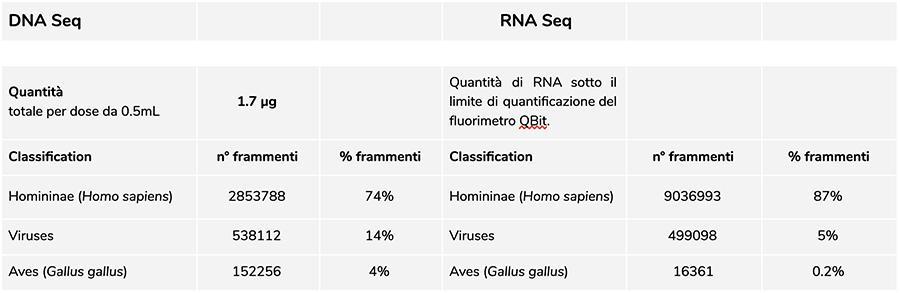
Lote Priorix Tetra. A71CB205A (junho 2018) - análise de DNA
Lote Priorix Tetra. A71CB256A (dezembro de 2018) - análise de DNA
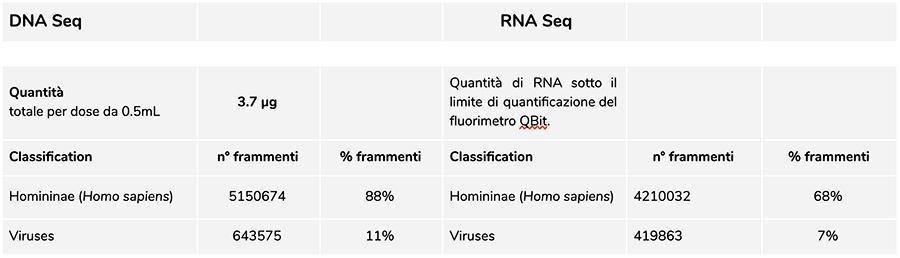
Análise de DNA
A medição da concentração de DNA com o fluorômetro QuBit mostrou que o lote A71CB205A contém um total de 1.7 µg de gDNA por dose de 0.5 mL, calculado da seguinte forma: 9.41ng / µl (concentração determinada em QuBit) x 45 (volume final de ressuspensão do DNA após a extração, expresso em microlitros) x 4 (o volume inicial submetido ao procedimento de extração é ¼ do volume da dose contido em todo o frasco de 0.5 ml).
A medição de DNA concentração com fluorômetro QuBit mostrou que o Lote A71CB256A contém um total gDNA de 3.7 µg por dose de 0.5 mL, calculado da seguinte forma: 40.8 ng / µl (concentração determinada em QuBit) x 55 (volume de ressuspensão final do DNA após extração expressa em microlitros) x 5/3 (o volume inicial submetido ao procedimento de extração é 300 µl em 500 µl de suspensão ).
O DNA humano encontrado neste lote é de cerca de 8 a 1 em relação ao DNA da varicela (veja os seguintes resultados da classificação de fragmentos de DNA-seq, que mostram que 88% do total de fragmentos de DNA seqüenciado são de origem humana e 11% são do genoma do vírus da varicela).
Considerando que o NGS é uma tecnologia quantitativa, a quantificação fluorimétrica do DNA total extraído da vacina (por exemplo, lote A71CB256A = 3.7 microgramas por dose), combinada com a consideração da quantificação relativa feita acima (8: 1), permite dizer que humanos O DNA pode ter cerca de 2.9 microgramas por dose, em comparação com cerca de 740 nanogramas de DNA de varicela. Também é plausível que pelo menos uma porção do DNA de alto peso molecular observado no gel pode ser DNA humano de alto peso molecular.
Análise de RNA
A quantidade de RNA incluído no frasco da vacina o lote A71CB256A acabou por ser aproximadamente 200ng.
O RIN igual a 8 indica uma excelente qualidade RNA e um RNA eucariótico intacto, uma vez que os picos 18S e 28S típicos do RNA eucariótico estão presentes.
As respostas às nossas perguntas encaminhadas às agências reguladoras ao longo do tempo são extremamente importantes. Atualmente, as agências ainda não responderam às perguntas sobre os resultados das análises completas entregues à EMA e à AIFA.
Extrato da resposta dada pela EMA à nossa pergunta sobre a segurança dos resíduos de MRC-5 na vacina Priorix® tetra (referência de solicitação da EMA ask-43967 3 de agosto de 2018) - "Com base nas informações publicadas, o Priorix® Tetra contém cepas virais produzidas separadamente em células embrionárias de galinha (caxumba e sarampo) ou em células diplóides humanas MRC-5 (rubéola e catapora). As linhas celulares usadas para Priorix® Tetra incluem linhas celulares diplóides humanas que não podem se dividir continuamente. Observe que, de acordo com a Farmacopeia Europeia, as linhas celulares diplóides MRC-5 não são tumorigênicas, como demonstrado por décadas de uso e controle, e, portanto, o limite máximo para o DNA das células MRC-5 não se aplica "
Atualmente, nenhuma evidência foi fornecida (nem em termos de certificados de análise da qualidade do produto nem de literatura científica de referência para a EMA) desses controles que garantem que é apropriado não aplicar um limite máximo.
Na diretriz da FDA, "Orientação para a indústria: caracterização e qualificação de substratos celulares e outros materiais biológicos usados na produção de vacinas virais para indicações de doenças infecciosas"6 afirma-se que:
- uma cepa de células diplóides deve sempre permanecer diplóide. Se essas características não forem estáveis, é necessário demonstrar que a instabilidade não afeta adversamente a produção ou a conformidade do produto.
- para cepas de células diplóides humanas amplamente usadas, como as células MRC-5 e WI-38, a medição do DNA residual pode não ser necessária porque não consideramos o DNA residual dessas células diplóides humanas uma preocupação de segurança
- o DNA residual deve ser limitado para células contínuas não tumorigênicas, como células TRUE com baixo número de passagens, inferiores a 10 ng / dose para inoculação parenteral, conforme recomendado pela OMS
E a diretriz da OMS "Anexo 3 - Recomendações para a avaliação de culturas de células animais como substratos para a fabricação de medicamentos biológicos e para a caracterização de bancos de células. Substituição do anexo 1 da série de relatórios técnicos da OMS, n. 878 "acrescenta: (...) acumulou-se uma experiência considerável na citogenética de WI-38 e MRC-5 desde os anos 1960 e para oferecer suporte a essa experiência, os seguintes artigos estão listados:
- Jacobs JP. Resultados atualizados sobre a cariologia das linhagens celulares WI-38, MRC-5 e MRC-9. Developments in Biological Standardization, 1976, 37: 155–156.
- Jacobs JP. et al. Diretrizes para a aceitabilidade, gerenciamento e teste de células diplóides humanas propagadas em série para a produção de vacinas de vírus vivos para uso no homem. Journal of Biological Standardization, 1981, 9: 331–342.
- Petricciani JC et al. Padrões de cariologia para a linha celular diplóide rhesus DBS-FRhL-2. Journal of Biological Standardization, 1976, 4: 43–49.
- Schollmayer et al. Análise de alta resolução e condensação diferencial em cromossomos humanos com bandas de RBA. Human Genetics, 1981, 59: 187–193.
- Rønne M. Preparação de cromossomos e técnicas de bandas de alta resolução: uma revisão. Journal of Dairy Science, 1989, 72: 1363–1377.
Pode-se observar claramente que a literatura de referência que sustenta que as células diplóides usadas para a produção de vacinas é segura do ponto de vista da estabilidade genética, é obsoleto. Já há 40 anos, as primeiras anomalias genéticas, consideradas insignificantes para a segurança das vacinas, foram encontradas e, conforme relatado na diretriz da OMS, desde então, nenhuma atualização foi feita com as novas tecnologias de sequenciamento, em particular no NGS, o que também é econômica e rápida, com a conseqüência de que nas vacinas administradas por décadas, as agências permitiram a presença de DNA geneticamente modificado cada vez mais progressivamente e em quantidades não controladas. Sobre este tópico, consulte o relatório sobre o seqüenciamento de todo o genoma MRC-5 publicado no site da Corvelva em 27.09.2019, no qual a profunda modificação desse DNA também é evidente em genes associados ao desenvolvimento de patologias tumorais. (dados sendo publicados)
Abaixo, é relatado um extrato da carta do Dr. T. Deisher - especialista mundial no uso de células-tronco para fins terapêuticos e terapia gênica-, que destaca a preocupação com os riscos associados ao uso de vacinas contaminadas com resíduos de células fetais humanas :
Dr. T. DEISHER (carta aos governadores - 8 de abril de 2019) - (...) injetar nossas crianças com contaminação de DNA fetal humano acarreta o risco de causar duas patologias consolidadas:
- mutagênese insercional: o DNA fetal humano é incorporado ao DNA da criança, causando mutações. A terapia gênica usando recombinação homóloga de pequenos fragmentos mostrou que quantidades tão pequenas quanto 1.9 ng / mL de fragmentos de DNA resultam na inserção de células-tronco no genoma em 100% dos camundongos injetados. Os níveis de fragmentos de DNA fetal humano em nossos filhos após a vacinação com as vacinas MMR, VARIVAX (catapora) ou hepatite A atingem níveis acima de 1.9 ng / ml.
- doença autoimune: o DNA humano fetal estimula a reação do sistema imunológico a atacar o corpo da criança.
Nossos resultados reforçam bastante as observações experimentais do Dr. Deisher, sobretudo o fato de que o DNA fetal contaminante presente em todas as amostras analisadas em quantidades variáveis (portanto não controladas) é até 300 vezes superior ao limite imposto pela EMA para o DNA carcinogênico (10 ng / dose, correspondente ao DNA contido em cerca de 1000 células cancerígenas, obtido com base em um cálculo estatístico, enquanto o limite de precaução é de 100 pg / dose), limite que também deve necessariamente ser aplicado ao DNA fetal que inevitavelmente contamina o Priorix® Tetra.
Portanto, esta vacina deve ser considerada defeituosa e potencialmente perigosa para a saúde humana, em particular na população pediátrica, que é muito mais vulnerável a danos genéticos e auto-imunes devido à imaturidade nos sistemas de reparo.
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.corvelva.it/speciale-corvelva/vaccinegate.html
https://www.corvelva.it/speciale-corvelva/vaccinegate-en.html - https://www.corvelva.it/speciale-corvelva/vaccinegate/sequenziamento-del-genoma-completo-di-mrc-5-contenuto-in-priorix-tetra.html
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.federalregister.gov/documents/2010/03/04/2010-4553/guidance-for-industry-characterization-and-qualification-of-cell-substrates-and-other-biological

