AstraZeneca, bajo fuego por la seguridad de las vacunas
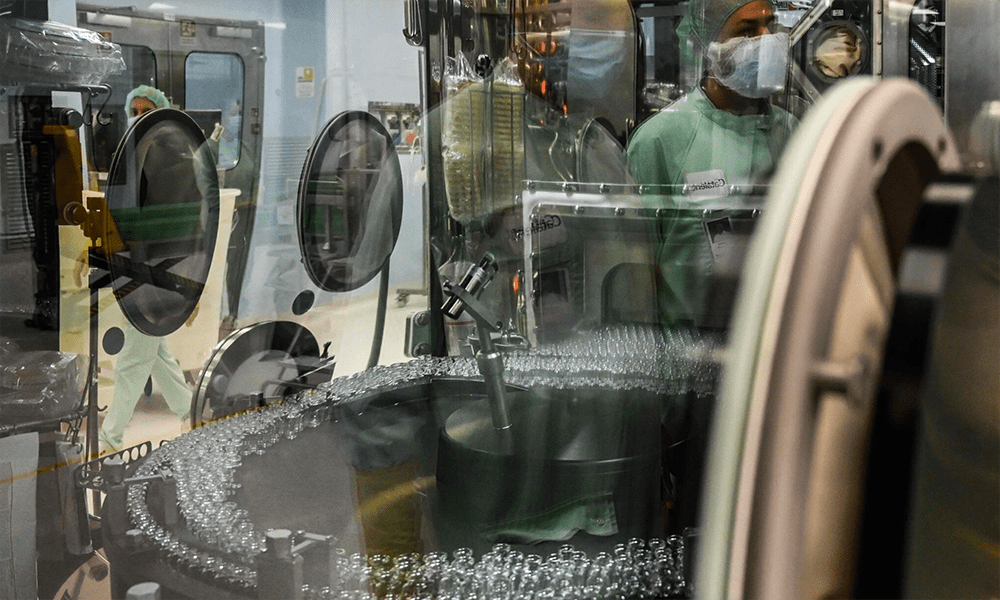
A los expertos les preocupa que la compañía no haya sido transparente sobre dos participantes que se enfermaron gravemente después de probar su vacuna experimental.
Las encuestas muestran que los estadounidenses son cada vez más cautelosos a la hora de aceptar una vacuna contra el coronavirus. A los científicos dentro y fuera del gobierno les preocupa que los reguladores bajo presión puedan lanzar una vacuna no probada o insegura.
Los expertos están particularmente preocupados por los estudios de vacunas de AstraZeneca, que comenzaron en abril en Gran Bretaña, debido a la negativa de la compañía a proporcionar detalles sobre enfermedades neurológicas graves en dos participantes, ambas mujeres, que recibieron la vacuna experimental. Estos casos llevaron a la compañía a dejar de probar dos veces, la segunda vez a principios de este mes. Los estudios se han reanudado en Gran Bretaña, Brasil, India y Sudáfrica, pero todavía están en pausa en Estados Unidos. Cerca de 18.000 personas en todo el mundo han recibido la vacuna de AstraZeneca hasta ahora.
El proyecto de prueba de 111 páginas de AstraZeneca, conocido como el protocolo, dice que su objetivo es una vacuna con una eficacia del 50%, el mismo umbral que la Administración de Alimentos y Medicamentos ha establecido en sus pautas para las vacunas contra el medicamento. coronavirus. Para determinar con certeza estadística si la empresa ha logrado ese objetivo, será necesario que haya 150 personas con coronavirus confirmado entre los participantes que hayan sido vacunados o hayan recibido placebo.
Sin embargo, el plan prevé que una comisión de seguridad llevará a cabo una investigación temprana después de que solo haya habido 75 casos. Si la vacuna tiene una efectividad del 50% en ese momento, es posible que la empresa detenga el ensayo antes de tiempo y solicite la autorización del gobierno para liberar la vacuna para uso de emergencia.
Al permitir solo uno de estos análisis provisionales, el plan de AstraZeneca es más riguroso que los otros que han sido publicados por Moderna y PfizerEl Dr. Eric Topol, experto en estudios clínicos de Scripps Research en San Diego, dijo en una entrevista. Moderna permite dos de estos análisis y Pfizer cuatro.
El problema de mirar los datos demasiadas veces, después de un número relativamente pequeño de casos, es que aumenta las posibilidades de encontrar un aspecto de seguridad y eficacia que puede no ser válido. La interrupción temprana de los ensayos también puede aumentar el riesgo de pasar por alto efectos secundarios raros que podrían ser significativos una vez que millones de personas reciban la vacuna.
El Dr. Topol dijo que el plan de AstraZeneca, como los de Moderna y Pfizer, tenía una característica problemática: todos cuentan los casos relativamente leves de Covid-19 al medir la eficacia, lo que puede obstaculizar los esfuerzos para determinar si la vacuna previene. enfermedad moderada o grave.
Por lo general, tales planes no se comparten con el público "debido a la importancia de mantener la confidencialidad e integridad de los juicios", dijo Michele Meixell, portavoz de AstraZeneca, en un comunicado.
La compañía ha dado a conocer pocos detalles sobre los dos casos de enfermedad grave en su juicio. El primer participante recibió una dosis de la vacuna antes de desarrollar una inflamación de la médula espinal conocida como mielitis transversa, según una hoja de información para el participante de la vacuna AstraZeneca de julio. La afección puede causar debilidad en los brazos y piernas, parálisis, dolor y problemas intestinales y de vejiga.
El caso pidió una pausa en los ensayos de vacunas de AstraZeneca para permitir una revisión de seguridad por parte de expertos independientes. Un portavoz de la compañía le dijo al Times la semana pasada que luego se determinó que el voluntario tenía un caso de esclerosis múltiple relacionado con la vacuna no diagnosticado previamente, y que el ensayo se reanudó poco después.
La mielitis transversa a veces puede ser el primer signo de esclerosis múltiple, que involucra síntomas más complejos. Pero la mielitis sola también puede ocurrir después de que el cuerpo se encuentra con un agente infeccioso como un virus.
La compañía dijo que no confirmó el diagnóstico en el segundo caso, un participante que se enfermó después de la segunda dosis de la vacuna. Una persona familiarizada con la situación, que habló con el Times bajo condición de anonimato, dijo que la enfermedad del participante había sido identificada como mielitis transversa. El juicio fue suspendido nuevamente el 6 de septiembre después de que ella se enfermara.
La afección es rara, pero grave, y los expertos dijeron que encontrar incluso un caso entre miles de participantes en el ensayo podría ser una llamada de atención. Más casos confirmados, dijeron, podrían ser suficientes para detener por completo la oferta de vacunas de AstraZeneca.
Una hoja informativa del participante fechada el 11 de septiembre sobre el ensayo de AstraZeneca en Gran Bretaña combinó los casos de los dos voluntarios, indicando que era poco probable que las enfermedades estuvieran asociadas con la vacuna o que no había evidencia suficiente para decir con certeza o no estaban relacionados con la vacuna ", según las revisiones de seguridad. Al día siguiente, AstraZeneca anunció que había reanudado las pruebas en el Reino Unido.
Pero la FDA hasta ahora no ha permitido que la compañía reinicie el ensayo en los Estados Unidos.
Un portavoz de la FDA se negó a comentar. Los Institutos Nacionales de Salud dijeron en un comunicado que "queda por ver" si el inicio de la enfermedad en los participantes del ensayo fue aleatorio o relacionado con la vacuna, y agregó que "una pausa para permitir una evaluación adicional es consistente con la práctica. estándar".
El Dr. Mark Goldberger, experto en enfermedades infecciosas de la Asociación Global de Investigación y Desarrollo de Antibióticos y ex funcionario de la FDA, dijo que encontró la rápida reanudación de los ensayos en el extranjero "un poco inquietante", especialmente dada la falta de detalles de los síntomas de los pacientes y la ambigüedad sobre su vínculo con la vacuna. "Quizás esto sea lo mejor que pudieron hacer, puede que no sea posible obtener más certeza en este momento", dijo. "Es un signo de interrogación sobre lo que está pasando.
La compañía no notificó de inmediato al público sobre los problemas neurológicos de ambos participantes. Tampoco advirtió de inmediato a la FDA que estaba pausando nuevamente sus experimentos después de que el segundo voluntario del Reino Unido desarrolló una enfermedad y un comité de seguridad independiente pidió una suspensión temporal, según varias personas que conocían la situación. El director general de la empresa informó a los inversores de los problemas, pero no habló de ello públicamente hasta que la información se filtró y fue reportado por el STAT.
"La comunicación a su alrededor ha sido horrible e inaceptable", dijo el Dr. Peter Jay Hotez, virólogo del Baylor College of Medicine en Houston. "No es así como el pueblo estadounidense debería enterarse".
El Dr. Hotez también criticó las declaraciones hechas por los funcionarios del gobierno, incluidos los reguladores del Reino Unido que, dijo, no proporcionaron una justificación para reanudar sus juicios.
El Dr. Paul Offit, profesor de la Universidad de Pennsylvania y miembro del Comité Asesor de Vacunas de la FDA, dijo que no está claro cómo la compañía, o el gobierno del Reino Unido, determinaron que el segundo caso no estaba relacionado con la vacuna.
Él y otros expertos señalaron que la mielitis transversa es poco común y se diagnostica solo en uno de cada 236.000 estadounidenses por año. El ensayo en Gran Bretaña involucró solo a unos 8.000 voluntarios.
La vacuna desarrollada por AstraZeneca, que se asoció con científicos de la Universidad de Oxford, utiliza un virus destinado a transportar genes del coronavirus a las células humanas y desencadenar una respuesta inmune que protegerá a las personas del coronavirus. Este llamado vector es una forma modificada de adenovirus que causa el resfriado común en los chimpancés, pero es considerado seguro para las personas. Varias otras compañías, incluidas Johnson & Johnson y CanSino, están aplicando enfoques similares basados en adenovirus, aunque existen diferentes tipos de adenovirus y los ingredientes específicos difieren de una vacuna a otra.
Si bien otros productos a base de adenovirus han tenido cierto éxito en el pasado, también se han relacionado con eventos adversos graves. El más famoso fue el caso de Jesse Gelsinger, de 1999 años, quien murió en XNUMX tras recibir terapia génica a través de un adenovirus que desencadenó una respuesta inflamatoria letal de su sistema inmunológico.
Si un efecto secundario grave estuviera vinculado permanentemente a la vacuna de AstraZeneca, los científicos tendrían que determinar si su desencadenante proviene del vector del adenovirus o quizás de los genes del coronavirus que porta, conexiones que podrían generar preocupaciones sobre los productos de otras empresas que dependen de él. en los mismos componentes.
fuente: https://www.nytimes.com/2020/09/19/health/astrazeneca-vaccine-safety-blueprints.html

