Informe técnico final - Análisis del perfil molecular de las vacunas.

Prefacio
En primer lugar, queremos agradecer los muy útiles comentarios proporcionados por quienes han revisado los resultados de los análisis realizados en el contexto de las actividades de investigación científica relacionadas con los productos Priorix tetra e Infanrix Hexa. Los temas críticos presentados fueron de hecho muy útiles para agregar integraciones técnico-científicas capaces de aclarar el trabajo realizado. Creemos que solo a través de una sana comunión de visiones científicas se puede llegar a conclusiones sobre los datos obtenidos que pueden ser útiles para toda la comunidad científica y para las personas que lo abordan.
1. Estado del arte
Los estudios preliminares (cribado no sujeto a confirmación) del perfil biomolecular, metabólico y proteómico, realizados en los productos Priorix Tetra e Infanrix Hexa han llevado a un marco de composición resumido en los siguientes puntos:
- Presencia de diferentes señales analíticas que no pueden asociarse con compuestos conocidos a través de la investigación en las bases de datos Metlin 1-2 y KEGG3. Por lo tanto, surgió una imagen asociada con una considerable complejidad en la composición de productos comerciales.
- Presencia de proteínas no declaradas en un prospecto en el producto Priorix Tetra. Este último puede estar asociado potencialmente con residuos del proceso de producción.
- No detección de los antígenos declarados dentro del producto Infanrix Hexa. La técnica de análisis consistió en la digestión enzimática con tripsina asociada con técnicas de espectrometría de masas. 4-5
Estos datos han generado varios comentarios, especialmente con respecto al punto C - De hecho, la detección de proteínas se lleva a cabo utilizando un enfoque estándar, reconocido internacionalmente por más de 10 años 4, de digestión a través de la enzima tripsina 4. Los péptidos así obtenidos se separan cromatográficamente y se analizan por espectrometría de masas 4-5. La observación principal ha sido inherente al hecho de que en las vacunas hay adyuvantes a base de aluminio que podrían inhibir el proceso de digestión enzimática. Los datos adquiridos posteriormente permitieron proporcionar aclaraciones sustanciales, especialmente con respecto a la queja expresada en el punto C.
2. Nuevas ideas y análisis
2.1 Perspectivas relacionadas con el análisis del producto Infanrix Hexa
Antes de continuar con la ilustración de los nuevos datos adquiridos sobre las vacunas Hexyon y Gardas 9, es esencial responder a la pregunta sobre la duda planteada con respecto a la inhibición de la actividad proteolítica de la tripsina causada por la presencia de adyuvantes a base de aluminio en Infanrix Hexa vacuna. A este respecto, debe especificarse que siempre hay un control de la digestión dentro de la digestión tríptica. De hecho, la tripsina utilizada para realizar la digestión, aunque diseñada para prevenir la autólisis, tiene un pequeño porcentaje de esta última que en el caso de la actividad enzimática conduce a la obtención del fragmento que tiene m / z 842 y la siguiente secuencia de péptidos: VATVSLPR. Dicho fragmento se detectó realmente dentro de la digestión tríptica del producto Infanrix Hexa como verificable por el cromatograma de extracción de iones (Figura 1).
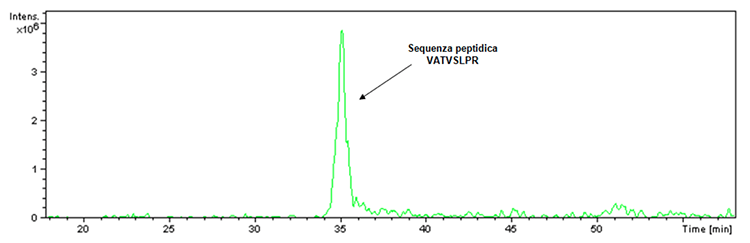
Figura 1: Cromatograma de extracción iónica asociada a iones con una relación m / z 842 encontrada en la muestra del lote de producto Infanrix Hexa (lote No. A21CD072D).
Además, se realiza un control externo mediante la digestión de la hemoglobina, con el fin de verificar aún más la bondad del lote de tripsina utilizado. La hemoglobina, analizada en la sección de análisis en la que se monitorizó el producto, se reconoció con una puntuación estadística significativa (loge <- 100). Estos datos confirmaron el hecho de que estaba presente la actividad enzimática.
2.2 Nuevos análisis sobre productos Hexyon y Gardasil
El análisis de los productos Hexyon y Gardas 9 condujo a la detección de perfiles moleculares complejos. En este caso, sin embargo, se detectó la presencia de la mayoría de los antígenos informados en el folleto informativo. Se detectaron por digestión tríptica y en presencia de adyuvantes.
Este hecho refuerza aún más la evidencia de que la reacción de digestión triptica no se inhibe en presencia de adyuvantes. En el caso de las vacunas Hexyon y Gardas 9, la complejidad del perfil molecular se atribuyó principalmente a la presencia de numerosas especies, con bajo peso molecular, no identificables por las bases de datos de referencia Metlin 1-2 y KEGG 3.
3. Conclusiones y consideraciones finales.
Los análisis realizados llevaron a la conclusión de lo siguiente:
- El perfil molecular de las vacunas analizadas es generalmente complejo y en gran parte desconocido.
- Existen contaminaciones proteicas, no declaradas en el prospecto, cuya composición es variable.
- En varios casos no se han detectado los antígenos declarados en el prospecto. Este hecho podría atribuirse a varios factores. Entre estos últimos, podemos considerar la sensibilidad del método utilizado. Sin embargo, creemos que podemos excluir el fenómeno de la inhibición de la digestión debido a la presencia de adyuvantes en la formulación de la vacuna. De hecho, la actividad enzimática se confirma principalmente por la presencia de fragmentos de autólisis tríptica, dentro de las soluciones de las vacunas digeridas (control interno).
4. Estudios futuros
Se realizarán más estudios como parte de las actividades de investigación y desarrollo destinadas a investigar los siguientes aspectos:
- composición macromolecular asociada con residuos sólidos presentes en vacunas (análisis MALDI TOF MS); 5
- evaluación de la concentración de los metales presentes en los productos.
- Análisis de segundo nivel para confirmar la presencia de compuestos tóxicos detectados en la fase de selección. Su concentración se relacionará con la toxicidad de la misma de acuerdo con lo indicado en las hojas de datos de seguridad internacional. Los análisis de segundo nivel se llevarán a cabo de conformidad con la directiva europea UE 2002/657 / CE, útil para garantizar altos estándares de calidad en el sector de la espectrometría de masas. 6
Loretta Bolgan
5. Referencias bibliográficas
- Autenhahn R, Cho K, Uritboonthai W, Zhu Z, Patti G, Siuzdak G (septiembre de 2012). "Un flujo de trabajo acelerado para la metabolómica no dirigida utilizando la base de datos METLIN". Biotecnología de la naturaleza. 30: 826–828. doi: 10.1038 / nbt.2348. PMC 3666346. PMID 22965049.
- Smith CA, I'Maille G, Want EJ, Qin C, Trauger SA, Brandon TR, Custodio DE, Abagyan R, Siuzdak G (diciembre de 2005). "METLIN: una base de datos espectral de masas de metabolitos" (PDF). Ther Drug Monit. 27 (6): 747–51. doi: 10.1097 / 01.ftd.0000179845.53213.39. PMID 16404815.
- Kanehisa M (2013). "Evolución química y genómica de las redes de reacción catalizadas por enzimas". FEBS Lett. 587 (17): 2731–7.
- Cristoni S, Bernardi LR. "Análisis de datos de bioinformática en espectrometría de masas para estudios de proteómica". Expert Rev Proteomics. Diciembre de 2004; 1 (4): 469-83.
- Cristoni S, Bernardi LR. "Desarrollo de nuevas metodologías para el estudio de espectrometría de masas de macromoléculas bioorgánicas". Mass Spectrom Rev.2003 noviembre-diciembre; 22 (6): 369-406.
- Cristoni S, Dusi G, Brambilla P, Albini A, Conti M, Brambilla M, Bruno A, Di Gaudio F, Ferlin L, Tazzari V, Mengozzi S, Barera S, Sialer C, Trenti T, Cantu M, Rossi Bernardi L, Noonan DM. "SANIST: optimización de una tecnología para la identificación de compuestos basada en la directiva de la Unión Europea con aplicaciones en análisis forenses, farmacéuticos y alimentarios". J. Mass Spectrom. 2017 enero; 52 (1): 16-21. doi: 10.1002 / jms.3895.
Descargar: CORVELVA-final-Técnica-Report.pdf
Traducido por el equipo de CLiVa - www.clivatoscana.com

