Resumen de confirmaciones de datos mediante análisis interlaboratorio.

Queridos amigos
Comenzamos este informe de una manera diferente, siendo más emotivo el último de 2019 y habiendo llegado al final de lo planeado para este año. Es un documento resumido del trabajo realizado que contiene exclusivamente las confirmaciones de los datos que inicialmente eran probables y que ahora se han convertido cierto.
Nos hemos quedado sin fondos para este proyecto y todavía estamos satisfechos porque tener cuentas vacías en este período de lucha significa que hemos utilizado toda la energía para la batalla, sin escatimarnos.
Como sucedió desde 2017 allí nos autofinanciaremos gracias a las cuotas de membresía y las donaciones de nuestros padres y procederemos en 2020 con toda una serie de investigaciones que deberían llevar el asunto a un nivel superior pero, mientras tanto, los dedicaremos los próximos meses para informar e interactuar con asociaciones extranjeras para proceder con la denuncia internacional. Tenemos mucho trabajo, sinceramente, hay más ideas que las energías y las posibilidades económicas disponibles.
Juntos nos embarcamos en un camino que ha durado mucho tiempo y hoy hemos logrado dar a conocer los resultados de este proyecto en todo el mundo. La determinación de nosotros, padres y ciudadanos italianos, es un ejemplo hoy para muchas otras naciones. que lamentablemente se están preparando para luchar en las mismas batallas en defensa de los derechos humanos fundamentales.
Sí, es muy cierto, las instituciones parecen sordas y una coma aún no se ha movido, al menos no de una manera obvia y, lo que es más angustiante, nuestros niños están excluidos de las escuelas, pero echemos un vistazo: El sistema mundial gravita en torno al dogma de la vacunación respaldado por una "comunidad científica" que, solo en Italia, ha recibido más de XNUMX millones de euros en pocos años.. 1 Es una verdadera lluvia de dinero lo que ha movido a una gran cantidad de pseudocientíficos, médicos contratados y políticos ignorantes, listos para proteger los intereses de aquellos organismos que el Prof. Randy Schekman, Premio Nobel de Medicina en 2013, llamó " castas". 2
"La ciencia está en riesgo: ya no es confiable porque está en manos de una casta cerrada y lejos de ser independiente" y esto ahora es evidente incluso para el espectador más escéptico, si es de buena fe. Persigue intereses que no son los que acompañan al método científico, al menos no como debería ser; produce estudios que, para ser publicados, deben respetar algunos dogmas impuestos, omitiendo algunos datos que "no están de acuerdo" o destacando otros que "son convenientes" y esto lo hemos experimentado en nuestra piel, a pesar de que solo nos hemos enfrentado a este mundo.
En esta situación despreciable, nos vimos obligados a enfrentar una imposición de ley para la administración de productos farmacéuticos, una ley que inevitablemente enriquece y aumenta el poder de esa casta mencionada por el noble Schekman.
Ante tal situación sociopolítica, nos fortalecimos, ciudadanos y padres conscientes y decididos, con la ayuda de otros ciudadanos como nosotros tomamos aquellas acciones que parecían más efectivas o simplemente más "asequibles" en función de las posibilidades que teníamos: Hemos demostrado que con pocas fuerzas, pero con determinación, se pueden producir grandes resultados.
Comenzamos con estas pocas líneas de apertura porque hoy, como el último informe de Corvelva, le informaremos sobre los últimos resultados, que son confirmaciones que provienen de análisis realizados tanto por una prestigiosa universidad europea como por otros laboratorios certificados ubicados en diferentes partes del mundo. ¡Los datos son cada vez más seguros y lo que antes era probable ahora se DEMUESTRA!
Entre otras cosas, hemos investigado una serie de compuestos tóxicos y / o cancerígenos como la NDMA de nitrosodimetilamina y las cianhidrinas y los resultados han sido realmente preocupantes. Hablaremos necesariamente de esto con publicaciones de revisión por pares para no comprometer las publicaciones mismas.
Como se explicó, incluso estas ideas, como las de la secuenciación del ADN fetal, son el tema de la próxima publicación en una revisión por pares, por lo tanto, realmente estamos comunicando una parte mínima de lo que se publicará, pero la ciencia pregunta que los datos no están publicados. Al informar más detalles, haremos el trabajo realizado. Sin embargo, el hecho es que los organismos de control han recibido todo, ¡en original!
Procederemos con la información y lucharemos para que los resultados impactantes sean considerados como lo que son, datos analíticos puros sin preconcepciones o ideologías. Esos productos analizados por nosotros deben recolectarse a granel y hay una gran pregunta sobre los intereses que gravitan en torno a todos aquellos que se han enfrentado a nuestros análisis y / o están a favor del dogma de la vacuna.
Juntos podemos tratar de detener toda esta locura.
Resumen de los resultados obtenidos y confirmados para cada vacuna.
Para llevar a cabo esta investigación, se decidió utilizar un límite entre los nanogramos y los microgramos, por lo tanto, por encima del límite residual para compuestos no conocidos y no informados en la hoja de datos técnicos.
Debe enfatizarse que la cantidad acumulativa de estos contaminantes es superior a microgramos por dosis, aunque actualmente no es posible realizar una cuantificación exacta, ya que la mayoría de los contaminantes son desconocidos y, por lo tanto, no es posible llevar a cabo el estudio mediante estándares de control analítico.
A partir de los resultados de la detección y los controles con los estándares, parece que la fracción metabólica tiene compuestos candidatos que pueden explicarse solo con un control deficiente.y, en consecuencia, con el mala calidad, materias primas y reactivos. En particular, la contaminación cruzada con compuestos químicos con actividad farmacológica conocida está fuera de control, aunque es posible que el proceso de producción de la vacuna cambie su estructura y conformación originales.
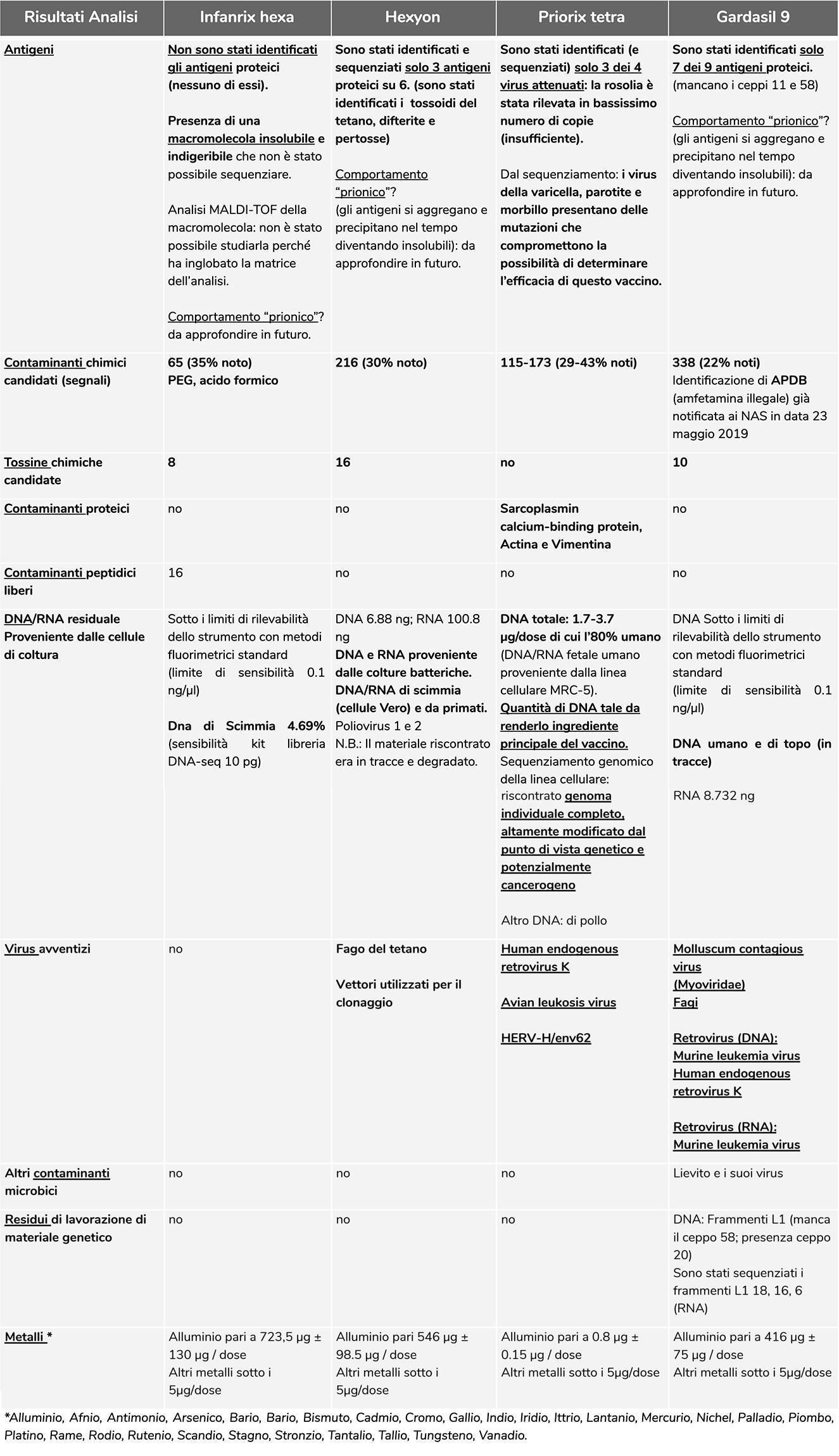
Especificar resultados confirmados
Al final de este resumen, informaremos todos los enlaces de todos los informes de los análisis realizados, siempre nos referiremos a ellos para una comprensión detallada de los resultados, ya que a continuación solo hablaremos de los análisis confirmatorios por medio de un examen de segundo nivel, estándares de control y / o interlaboratorio.
Un ejemplo para comprender mejor: un proveedor de servicios certificado realizó algunos análisis a pedido nuestro. Se les pidió que seleccionaran, identificaran la presencia o ausencia de ciertos compuestos orgánicos o inorgánicos en ciertas (no todas) vacunas o secuencias genéticas. Por lo tanto, el resultado es solo lo que pedimos buscar, un elemento esencial para confirmar la validez del método que utilizamos.
Las razones por las que no se han utilizado numerosos estándares de control y otras vacunas disponibles en el mercado tienen raíces económicas y lógicas: no somos un organismo de investigación y estamos realizando análisis en profundidad, después de informar el incumplimiento de los organismos reguladores, que van más allá de lo que hacemos debe competir a todos los efectos, estamos sustituyendo indebidamente a los organismos reguladores en investigaciones que dependerían de ellos después de un informe de esta magnitud, y lo estamos haciendo porque nuestros datos se han definido incompletos.
Análisis de vacuna Hexyon
metagenómica
La presencia del material genético contaminante se confirmó con análisis interlaboratorios en un proveedor de servicios europeo certificado.
El ADN presente es igual a 6,88 ng en total por dosis (esta cantidad se refiere al informe divulgado. Los datos del análisis interlaboratorio están sujetos a revisión por pares y, por lo tanto, no se divulgan pero confirman el orden de magnitud), de los cuales 0,1 , 688% potencialmente de células Vero (Cercopithecidae), es decir, XNUMX pg / dosis. Hemos identificado el fago de Clostridium phiCT453A y SV40 junto con otros vectores para la clonación.
Presencia de poliovirus 1 y 2. En este caso, la respuesta de la EMA a la ausencia de Poliovirus 3 fue muy genérica, la ausencia no es un incumplimiento para ellos ya que dan por sentado la presencia del antígeno D, capaz de crear inmunización. Obviamente hemos buscado esta proteína pero no hemos podido encontrarla, sería un excelente estudio para desarrollar porque actualmente dejamos una respuesta incierta sobre este punto.
El ADN y el ARN de las bacterias utilizadas para la producción de los antígenos de Corynebacterium diphtheriae (Difteria), Clostridium tetani (Tétanos), Bordetella pertussis (Tos ferina) y Haemophilus influenzae.
NOTA: el material genético adventicio presente en la vacuna se puede vincular al aluminio adyuvante con una posible mejora de los efectos tóxicos (capacidad inflamatoria, autoinmune y tumoral). Reiteramos que, a partir de los datos confirmados entre laboratorios, la seguridad y eficacia de esta vacuna sigue siendo dudosa, lo que resulta en un producto completamente no conforme con respecto a la calidad.
Análisis de la vacuna Gardasil 9
Química-proteína
Después de los resultados anteriores, decidimos profundizar la identificación, con confirmación entre laboratorios, del APDB compuesto (anfetamina ilegal) ya notificado al NAS el 23 de mayo de 2019.. Dos laboratorios diferentes confirman la presencia de una sustancia perteneciente a la clase de APDB ilegal.
Nosotros, repetimos, no podemos comprar el estándar de control que es elAPDB clasificado como sorprendente, 3 no puede ser adquirido por sujetos sin autorización específica, por lo tanto, hemos proporcionado toda la documentación que confirma la presencia de una sustancia perteneciente a la clase APDB y el posible origen de la contaminación (Nota: se informa en el informe de evaluación de EMA para el registro de Gardasil 9 que la L-tirosina se utiliza como materia prima para la producción de esta vacuna y se extrae del cabello humano de China. 4 La producción principal de este narcótico proviene de China y los drogadictos tienen un nivel muy alto en el cabello. 5
metagenómica
La presencia del material genético se confirmó con análisis interlaboratorios en un proveedor de servicios europeo certificado. y podemos repetir los datos anteriores, hay:
- ADN humano y de ratón (bajo los límites de detección del instrumento)
- Virus adventicios:
- Fragmento L1 del virus HPV de ADN de doble cadena;
- Los fagos;
- Virus del molusco contagioso;
- retrovirus:
- Virus de la leucemia murina;
- Retrovirus endógeno humano K.
- Saccharomyces
NOTA: el material genético adventicio presente en la vacuna se puede vincular al aluminio adyuvante con una posible mejora de los efectos tóxicos (capacidad inflamatoria, autoinmune y tumoral)
Análisis de la vacuna Priorix Tetra
metagenómica
La presencia del material genético se confirmó con análisis interlaboratorios en un proveedor de servicios europeo certificado. Las cantidades se refieren a los informes divulgados. Los datos del análisis interlaboratorio están sujetos a revisión por pares y, por lo tanto, no se divulgan, pero confirman el orden de magnitud.
ADN La cantidad de ADN total presente en esta vacuna varía de: 1.7 - 3.7 μg / dosis y es en todos los aspectos el componente principal de la vacuna. El ADN es aproximadamente 80% humano (74-88%) y pollo (0-4%).
El genoma humano está completo, es decir, con genes y secuencias masculinas no codificantes, de alto peso molecular, calificadas como pertenecientes a la línea fetal MRC-5, es decir, la línea celular continua derivada del tejido pulmonar de un feto abortivo masculino de los años 60. La secuenciación de esta línea celular ha demostrado cómo fue altamente modificado desde un punto de vista genético y potencialmente cancerígeno. El análisis de secuenciación del genoma completo del ADN fetal fue realizado por un proveedor de servicios estadounidense (laboratorio).
moléculas de ARN - Humanos 68-87%. Pollo 0-0.2%
Virus atenuados - Se ha confirmado lote de los siguientes virus atenuados. A71CB256A:
- Varicela (ADN) 11%;
- Paperas (ARN) 0.008%;
- Sarampión (ARN) 0.004%;
- Rubéola 0.00004%. (114 de 260 millones de secuencias)
Se confirmó una presencia irrelevante de rubéola en la vacuna (inferior a los virus adventicios indicados a continuación) entre laboratorios. Esto cuestiona seriamente la efectividad de la vacuna.
Cuasiespecies virales: Se identificaron 245 variantes en el genoma de la varicela de la vacuna en comparación con el genoma de referencia utilizado para el análisis (genoma salvaje de la cepa Dumas). De estas variantes, 154 son variantes principales mientras que el resto 91 son variantes cuasiespecies. No surge ninguna diferencia de la comparación entre las variantes encontradas en los dos lotes. En el genoma de la vacuna contra las paperas, se identificaron 40 variantes cuasiespecies con respecto al genoma de referencia utilizado para el análisis (genoma de la vacuna Jeryl-Lynn). De la comparación entre las variantes encontradas en los dos lotes surgen 4 diferencias. La EMA no pudo proporcionarnos las secuencias del virus de la vacuna utilizadas por el fabricante para esta vacuna, ya que están cubiertas por el secreto industrial, por lo que no sabemos cuánto han cambiado los virus de la vacuna en comparación con lo declarado por el fabricante.
Debido a la baja cobertura, no fue posible detectar variantes cuasiespecies para los genomas del sarampión y la rubéola.
Virus adventicios - Confirmamos la presencia de estos virus adventicios:
- Retrovirus K endógeno humano;
- Virus de la leucosis aviar;
- HERV-H / env62.
Para todas las vacunas
Análisis con control y normas interlaboratorios sobre contaminaciones químicas.
Se eligieron dos compuestos para ser analizados con estándares de control certificados, basados en la disponibilidad, la consistencia de los datos semicuantitativos y el impacto en la salud. Estos compuestos se confirmaron como similares (es decir, con una identidad estructural del 75-80%: isómeros / isobares) también a través de análisis entre laboratorios.. La estructura de estos compuestos se revelará en la publicación de revisión por pares.
Evaluación de segundo nivel de contaminaciones químicas.
La investigación de detección de segundo nivel, como ya se mencionó, se divide en tres análisis:
- cribado en profundidad de la parte sumergida (65% del total de las señales) y comparación en la base de datos de las sustancias detectadas, incluida la base de datos de toxinas.
- análisis de pérdidas neutrales: La detección de fragmentación estable neutra nos permite hipotetizar la presencia en la vacuna de moléculas que las contienen, de estructura desconocida, pero con posibles efectos tóxicos si los grupos funcionales tienen actividad carcinogénica y mutagénica (la "Cohorte de preocupación" creada por el La EMA para medicamentos orales incluye compuestos similares a aflatoxinas, N-nitroso y alquil-azoxi, como se informa en la directriz M7 (R1) de ICH. 6
Nuevos compuestos candidatos: se identificaron compuestos potencialmente tóxicos (contaminación cruzada) para todas las vacunas analizadas en comparación con las bases de datos. Sería útil profundizar a través de estándares de control para confirmar su identidad.
Pérdidas neutrales: en nuestro caso, se examinaron los grupos cianilo (es decir, derivados del ácido hidrocianico utilizado para la preparación de la vacuna Haemophilus B) y nitrosodimetilamina, una impureza cancerígena encontrada en otras drogas y sujeta a evaluación por la EMA. 7
Para comprender el grupo funcional de nitrosodimetilamina, piense que es de la misma clase que las contaminaciones encontradas en las drogas sartani y ranitidina, que ha saltado a los titulares por la reciente retirada masiva de drogas en toda Europa. 8 El segundo grupo funcional es el de los cianuros, del cual conocemos la presencia declarada de cianuro de sodio como se muestra en las hojas de datos técnicos de la vacuna Prevenar. 9
Por lo tanto, el examen de segundo nivel dio una respuesta positiva para todas las vacunas. Por el momento, no es posible divulgar los resultados en detalle porque en la fase de publicación de revisión por pares, pero todos los organismos reguladores han tenido conocimiento de nuestros resultados.
La legislación
Tenga en cuenta lo que debe hacer la ley sobre las drogas en el mercado: 10
El Programa de control anual permite garantizar que los medicamentos comercializados se correspondan exactamente con las especificaciones de calidad de los procedimientos de autorización. Se establece cada año por AIFA, después de escuchar la opinión del Istituto Superiore della Sanità, y es aprobado por la Comisión Científica Técnica de AIFA (CTS). La Oficina de Calidad de Producto de AIFA requiere que los carabinieri NAS tomen muestras de los medicamentos incluidos en el programa de farmacias o mayoristas, que se envían a la ISS para su análisis. Si los resultados del análisis revelan alguna discrepancia de lo que está autorizado, la Oficina de Calidad de Producto de AIFA toma las medidas necesarias. Los análisis realizados se basan en la verificación del cumplimiento de las especificaciones de calidad autorizadas para cada medicamento e informadas en el expediente de registro y / o en las monografías de la Farmacopea Europea. (...)
La Oficina de Calidad del Producto también gestiona el retiro de oficio y la suspensión de autorizaciones de comercialización de medicamentos.
La autorización de comercialización de un medicamento puede ser revocada, con la consiguiente retirada definitiva del mercado cuando:
- el medicamento es dañino en condiciones normales de uso;
- el medicamento no tiene el efecto terapéutico o el efecto para el cual fue autorizado;
- la relación riesgo / beneficio no es favorable en condiciones normales de uso;
- el medicamento no tiene la composición cualitativa y cuantitativa declarada;
- La medicina fue producida en fábricas no autorizadas.
La autorización también puede revocarse si se comprueba que la información presente en la solicitud de autorización del medicamento es incorrecta o si no se verifica el producto terminado, los componentes o los productos intermedios de la producción.
Además de las intervenciones adoptadas a nivel nacional, las medidas del Sistema de Alerta Rápida, definido sobre la base de procedimientos compartidos a nivel europeo, que prevé diferentes acciones y notificaciones en relación con el tipo de gravedad del defecto de acuerdo con la clasificación de emergencias, se llevan a cabo simultáneamente. .
La Figura 2 describe la clasificación de defectos y las acciones relacionadas que deben tomarse.
Cabe señalar que yo Los defectos detectados con los análisis realizados por Corvelva entran en las clases I y II, ya que las vacunas son drogas inyectables y las contaminaciones detectadas son químicas y genéticas.
Se enfatiza que hasta la fecha las agencias reguladoras no han tomado medidasa pesar de notificar a AIFA los resultados de los análisis preliminares y el NAS de la presencia del compuesto APDB en la vacuna Gardasil 9, y esto está en grave violación del principio de precaución y la necesidad de una intervención rápida según lo previsto por el Sistema de Alerta para la protección de la salud pública.
Descargar: CORVELVA-summary-confirmaciones-Data-análisis-interlaboratorio.pdf
Nota:
- https://www.corvelva.it/it/approfondimenti/sistema-sanita/case-farmaceutiche/efpia-italia-tutti-i-trasferimenti-di-valore-delle-big-pharma.html
- http://www.medicinapiccoledosi.it/medicina-convenzionale/premio-nobel-la-medicina-randy-schekman-la-scienza-mano-ad-casta/
- http://www.cortedicassazione.it/cassazione-resources/resources/cms/documents/Legge_79_2014.pdf
http://www.rivistagiuridica.aci.it/fileadmin/Documenti/Decreto_25_giugno_M_Salute_02.pdf - https://www.unodc.org/documents/scientific/Trends_and_Patterns_of_ATS_and_NPS_2017.pdf
- Análisis de cromatografía de gases-espectrometría de masas (GC-MS)Journal of Food and Drug Analysis, Vol. 13, No. 3, 2005, páginas 193-200 Análisis de cromatografía de gases-espectrometría de masas (GC-MS) de anfetamina, metanfetamina, 3,4-metilendioxianfetamina y 3,4-metilendioximetanfetamina en Cabello humano y secciones de cabello DONG-LIANG LIN1,2 *, REA-MING YIN1 Y RAY H. LIU3
- https://www.ema.europa.eu/en/documents/ … /ich-guideline-m7r1-assessment-control-dna-reactive-mutagenic-impurities-pharmaceuticals-limit_en.pdf
- http://www.agenziafarmaco.gov.it/content/comunicazione-ema-sul-principio-attivo-valsartan-19112018
- https://www.repubblica.it/salute/medicina-e-ricerca/ … /news/non_solo_ranitidina_per_l_ema_vanno_testati_tutti_i_farmaci_per_impurita_cancerogene-237010173/
- https://www.ema.europa.eu/en/documents/scientific-discussion/prevenar-epar-scientific-discussion_en.pdf
- http://www.bollettinosifo.it/r.php?v=2598&a=26744&l=329640&f=allegati/02598_2016_06/fulltext/05_EspOpin_Cannizzo.pdf

