Kann der Pneumokokken-Impfstoff Verletzungen und/oder den Tod verursachen?

WICHTIGER HINWEIS: Corvelva lädt Sie ein, sich ausführlich zu informieren, indem Sie alle Abschnitte und Links sowie die Produktbroschüren und technischen Datenblätter des Herstellers lesen und mit einem oder mehreren vertrauenswürdigen Fachleuten sprechen, bevor Sie sich oder Ihr Kind impfen lassen. Diese Informationen dienen nur zu Informationszwecken und sind nicht als medizinische Beratung gedacht.
Das Problem der Mehrfachimpfungen (zum Öffnen klicken)
Das Problem der Mehrfachimpfungen

Die aktuellen Impfkalender, insbesondere für das pädiatrische Alter, sehen die Verabreichung mehrerer Antigene und Impfstoffe in einer einzigen Sitzung vor, was den Komfort auf Kosten der Sicherheit bevorzugt. Um einen konkreten Vortrag über die Sicherheit von Impfstoffen halten zu können, müssen wir unbedingt die Komplexität des Phänomens berücksichtigen und allen Lesern raten, sich ausreichend über alle Aspekte der Impfung, Vor- und Nachteile zu informieren.
Dr. Russell Blaylock, klinischer Assistenzprofessor für Neurochirurgie am Medical Center der Universität von Mississippi, hat jahrelang „toxische Synergien“ untersucht und konnte beobachten, dass, wenn zwei schwach toxische Pestizide, bei denen keines von beiden das Parkinson-Syndrom bei Versuchstieren verursachen kann, miteinander kombiniert werden, die Krankheit sogar schnell auslösen können und vergleicht dieses Phänomen mit dem von mehreren gleichzeitig verabreichten Impfstoffen: "Impfungen, wenn sie zu zahlreich und zu eng beieinander liegen, verhalten sich wie eine chronische Krankheit".(A). Sonstiges Zwei Studien haben bestätigt, dass es nach Impfung mehrerer Impfstoffe in einer einzigen Verabreichung zum plötzlichen Kindstod kommen kann.(bc)
Eine in Human and Experimental Toxicology veröffentlichte Studie zeigte, dass Länder, die Kindern mehr Impfstoffe verschreiben, tendenziell höhere Kindersterblichkeitsraten aufweisen.(D) Beispielsweise sterben in den Vereinigten Staaten, wo Kinder 26 Impfstoffe erhalten, mehr als 6 Kinder pro 1000 Lebendgeburten, während in Schweden und Japan, wo 12 pädiatrische Impfstoffe verabreicht werden, 3 Todesfälle pro 1000 Lebendgeburten gemeldet werden. In der oben genannten Studie wird auch der Zusammenhang zwischen Impfstoffen und SIDS berücksichtigt.
Aus einer Schweizer Studie, die 2005 im European Journal of Pediatrics veröffentlicht wurde(E) wir erhalten, dass bezüglich der Auswirkungen auf Frühgeborene die Inzidenz von rezidivierender oder verstärkter Apnoe und Bradykardie nach Verabreichung von Sechsfachimpfstoffen 13 % beträgt. Im selben Jahr veröffentlichte dieselbe Zeitschrift eine deutsche Studie, die den plötzlichen Kindstod nach Hexavalent untersucht hatte. Die Autoren schreiben: «Diese Ergebnisse, basierend auf Spontanmeldungen, belegen keinen kausalen Zusammenhang zwischen Impfung und plötzlichem Kindstod, stellen aber ein Signal bezüglich eines der beiden verfügbaren Hexavalente dar; Signal, das zu einer verstärkten Überwachung des plötzlichen Kindstods nach der Impfung führen sollte".(F)
2006 wurde es in der medizinischen Fachzeitschrift Vaccine veröffentlicht(G) das Schreiben eines Forscherteams der Universität München, das von „sechs Fällen plötzlichen Kindstods nach sechswertiger Impfung. Alle 1-2 Tage nach der Impfung ohne Erklärung tot aufgefunden“ berichtet. Sie waren als typische Fälle von plötzlichem Kindstod eingestuft worden, aber die autoptische Überprüfung hatte neuropathologische und histologische Anomalien ergeben, und alle Kinder wiesen ein signifikantes Hirnödem auf, was sie im Vergleich zu den anderen SIDS-Fällen zu einer Ausnahme machte (Plötzlichen Kindstod). Die Forscher schrieben: „Vor der Einführung des sechswertigen Impfstoffs (in den Jahren 1994-2000) hatten wir den Fall von nur einem von 198 Kindern mit plötzlichem Kindstod beobachtet, das kurz nach der DTP-Impfung starb. Aber zwischen 2001 und 2004 hatten sie fünf ähnliche Fälle von 74 mit SIDS identifiziert. Das würde auf eine Verdreizehnfachung hindeuten."
Ebenfalls 2006 auf Virchows Archiv(H), schrieb das Team des Instituts für Pathologie der Universität Mailand: „Experten der Europäischen Agentur für die Bewertung von Medizinprodukten haben die Möglichkeit analysiert, dass es einen Zusammenhang zwischen sechswertigen Impfstoffen und einigen Todesfällen geben könnte. Beteiligt waren Pathologen mit Erfahrung in Impfstoffen und plötzlichem Kindstod, die die Autopsien durchführten, aber unseres Wissens wurde der Untersuchung des Hirnstamms und des Blutherzens auf Serienschnitten wenig Aufmerksamkeit geschenkt, und es gab keine Möglichkeit, eine Auslöserrolle festzustellen des Impfstoffs für diese Todesfälle. Hier berichten wir über den Fall eines 3 Monate alten Mädchens, das nach einer sechswertigen Impfung plötzlich verstarb. Die Untersuchung des Hirnstamms in Serienschnitten ergab eine bilaterale Hypoplasie des bogenförmigen Kerns. Das Erregungsleitungssystem des Herzens wies eine anhaltende fetale Dispersion und Degeneration auf. Dieser Fall bietet ein einzigartiges Verständnis der möglichen Rolle des sechswertigen Impfstoffs bei der Auslösung einer tödlichen Konsequenz bei einem gefährdeten Kind. Jeder plötzliche und unerwartete Tod, der kurz nach der Geburt oder in der frühen Kindheit auftritt, sollte gemäß den Richtlinien immer einer vollständigen Autopsie unterzogen werden, insbesondere nach einer Impfung.
Referenzen
- Blaylock R, „Impfungen: die versteckten Gefahren“, The Blaylock Wellness Report, Mai 2004, S. 1-9
- Ottaviani G. et al., „Plötzlicher Kindstod (SIDS) kurz nach sechswertiger Impfung: eine weitere Pathologie bei Verdacht auf SIDS?“, Virchows Archiv., 2006, 448, S. 100-104.
- Zinka B. et al., „Unerklärliche Fälle von plötzlichem Kindstod kurz nach sechswertiger Impfung“, Vaccine, Juli 2006, 24 (31-32), S. 5779-5780.
- Miller NZ et al1. , "Säuglingssterblichkeitsraten regressiert gegen die Anzahl der routinemäßig verabreichten Impfstoffdosen: Gibt es eine biochemische oder synergistische Toxizität??", Hum. Exp. Toxicol., Mai 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Das Aluminiumproblem (zum Öffnen klicken)
Aluminium in Impfstoffen: Was Eltern wissen müssen

1. Was ist Aluminium?
Aluminium ist ein silbrig-weißes Leichtmetall, formbar und widerstandsfähig. Diese Eigenschaften machen es in zahlreichen Branchen und Produkten nützlich, darunter Maschinen, Bau, Lager, Kochgeschirr, Küchenutensilien, Textilien, Farbstoffe und Kosmetika. Aluminium ist auch das am häufigsten vorkommende Metall in der Erdkruste, und praktisch das gesamte Aluminium in der Umwelt befindet sich im Boden. Aluminium kommt jedoch in lebenden Organismen (wie Pflanzen und Tieren) nicht in nennenswerten Mengen vor und hat keine bekannte biologische Funktion. Im vergangenen Jahrhundert hat die Verwendung von Aluminium in einigen Produkten zu einer erhöhten Exposition des Menschen geführt. Die wichtigsten Expositionsquellen sind aluminiumhaltige Lebensmittel (z. B. Backpulver, verarbeitete Lebensmittel, Babynahrung usw.), medizinische Produkte (z. B. Antitranspirantien, Antazida usw.), Allergieinjektionen und Impfstoffe.1-3
2. Warum ist Aluminium in Impfstoffen enthalten?
Einige Impfstoffe verwenden Aluminiumverbindungen (Aluminiumhydroxid und Aluminiumphosphat) als Adjuvantien, die die Immunantwort auf ein Antigen (Fremdsubstanz) verstärken.4-5 Die US Food and Drug Administration (FDA) sagt, dass die von ihnen ausgelöste Immunantwort abnehmen könnte, wenn einige Impfstoffe kein Aluminium enthalten würden.6
3. Welche Impfstoffe enthalten Aluminium?
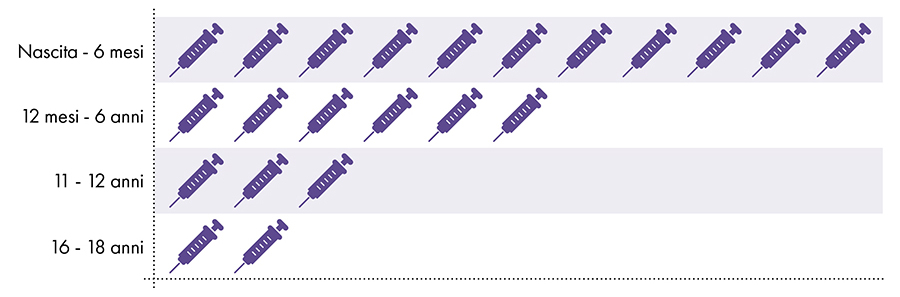
Folgende Impfstoffe enthalten Aluminium und werden Säuglingen, Kindern und Jugendlichen verabreicht (Abb. 1):
- Hepatitis B (HepB)
- sechswertiges
- Diphtherie, Tetanus und Keuchhusten (DTaP und Tdap)
- Haemophilus influenzae Typ b (PedvaxHIB)
- Pneumokokken (PCV)
- Hepatitis A (HepA)
- Humanes Papillomavirus (HPV)
- Meningokokken B (MenB)
Abbildung 1: Von der Geburt bis zum 18. Lebensjahr werden bis zu 22 Dosen aluminiumhaltiger Impfstoffe verabreicht7-8
4. Ist die Exposition gegenüber Aluminium sicher?
Die FDA betrachtet Aluminium seit 1975 als allgemein anerkannt als sicher (GRAS).9 Vor 1990 gab es jedoch keine Technologie, um kleine Mengen an Aluminium, die Probanden in wissenschaftlichen Studien verabreicht wurden, genau nachzuweisen.10 Folglich war die Menge an Aluminium, die absorbiert werden konnte, bevor Nebenwirkungen eintraten, unbekannt.
Seit den 1990er Jahren wurde dank des technologischen Fortschritts beobachtet, dass die geringen Mengen an Aluminium, die im menschlichen Körper verbleiben, eine Reihe von Zell- und Stoffwechselprozessen im Nervensystem und im Gewebe anderer Körperteile stören.1-10-11 Die größten negativen Auswirkungen von Aluminium wurden im Nervensystem beobachtet und reichen von beeinträchtigten motorischen Fähigkeiten bis hin zu Enzephalopathie (veränderter Geisteszustand, Persönlichkeitsveränderungen, Denkschwierigkeiten, Gedächtnisverlust, Krampfanfälle, Koma und mehr).2-12
Das US-Gesundheitsministerium (HHS) erkennt Aluminium als bekanntes Neurotoxin an.2 Darüber hinaus hat die FDA vor den Risiken der Aluminiumtoxizität bei Säuglingen und Kindern gewarnt.13
FEDERAL REGISTER: Die Tageszeitung der Regierung der Vereinigten Staaten„Sogar reifgeborene Säuglinge mit normaler Nierenfunktion können aufgrund des schnellen Wachstums und der Unreife des Gehirns und des Skeletts sowie der Unreife der Blut-Hirn-Schranke gefährdet sein. Bis zum Alter von 1 oder 2 Jahren haben Säuglinge eine niedrigere glomeruläre Filtrationsrate als Erwachsene, was ihre Nierenfunktion beeinträchtigt. Die Agentur befürchtet, dass kleine Kinder und Personen mit unreifer Nierenfunktion einem erhöhten Risiko einer Aluminiumexposition ausgesetzt sind. |
5. Wie viel orales Aluminium ist nicht sicher?
Im Jahr 2008 hat die Agency for Toxic Substances and Disease Registry (ATSDR), eine Abteilung von HHS, anhand von Studien zu den neurotoxischen Wirkungen von Aluminium festgestellt, dass nicht mehr als 1 Milligramm (1.000 Mikrogramm) Aluminium pro Kilogramm Körpergewicht pro Tag zu darf Vermeiden Sie die negativen Auswirkungen von Aluminium.2
6. Wie viel eingespritztes Aluminium ist nicht sicher?
Um die Aluminiummenge zu bestimmen, die sicher injiziert werden kann, ist es notwendig, den oralen Aluminiumgrenzwert des ATSDR umzurechnen. Der ATSDR-Grenzwert für orales Aluminium (1.000 Mikrogramm Aluminium pro Kilogramm Körpergewicht pro Tag) basiert auf 0,1 % des oralen Aluminiums, das in den Blutkreislauf aufgenommen wird, da der Verdauungstrakt fast das gesamte orale Aluminium blockiert.2 Umgekehrt umgeht intramuskulär injiziertes Aluminium den Verdauungstrakt und 100 % des Aluminiums können im Laufe der Zeit in den Blutkreislauf aufgenommen werden (d. h. der Anteil des absorbierten Aluminiums ist 1.000-mal größer). Um diese unterschiedlichen Resorptionsmengen zu berücksichtigen, muss der orale Aluminiumgrenzwert des ATSDR durch 1000 geteilt werden. Diese Umrechnung führt zu einem vom ATSDR abgeleiteten Aluminiumgrenzwert im Blut von 1 Mikrogramm Aluminium (0,1 % von 1.000 Mikrogramm) pro Kilogramm Körpergewicht pro Tag. Um die neurotoxischen Wirkungen von Aluminium zu vermeiden, sollte daher täglich nicht mehr als 1 Mikrogramm Aluminium pro Kilogramm Körpergewicht in den Blutkreislauf gelangen. Abbildung 3 zeigt den vom ATSDR abgeleiteten Blutaluminiumgrenzwert für Säuglinge unterschiedlichen Alters basierend auf ihrem Gewicht.
7. Wie viel Aluminium ist in Impfstoffen enthalten?
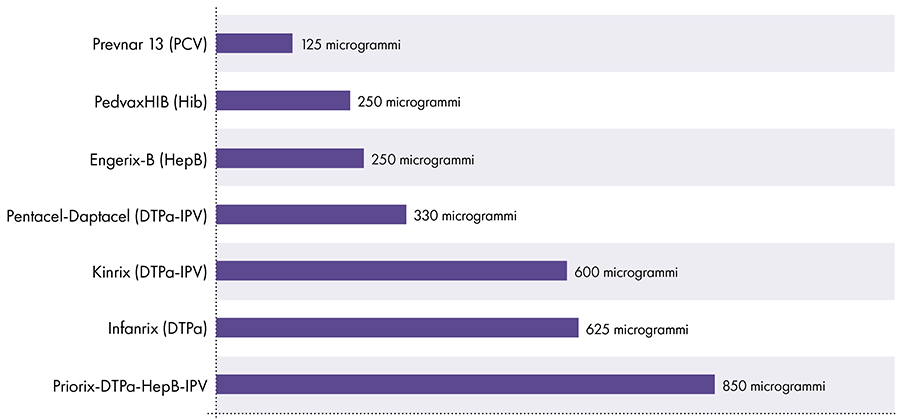
Die Menge an Aluminium in Impfstoffen variiert.16 1968 legte die US-Bundesregierung die Grenze für die Aluminiummenge in Impfstoffen auf 850 Mikrogramm pro Dosis fest, basierend auf der Menge an Aluminium, die benötigt wird, um einige Impfstoffe wirksam zu machen.6-17 Folglich reicht die Aluminiummenge in aluminiumhaltigen Säuglingsimpfstoffen von 125 bis 850 Mikrogramm pro Dosis. Abbildung 4 zeigt den Aluminiumgehalt einer Dosis verschiedener Impfstoffe, die Kindern verabreicht wurden.
8. Haben irgendwelche Studien die Aluminiummenge in Impfstoffen mit dem Grenzwert verglichen, der von der Agency for Toxic Substances and Disease Registry (ATSDR) abgeleitet wurde?
Im Jahr 2011 wurde eine Studie veröffentlicht, die darauf abzielte, die Aluminiummenge in Impfstoffen mit der von der ATSDR festgelegten Blutflussgrenze zu vergleichen.18 Diese Studie stützte ihre Berechnungen jedoch fälschlicherweise auf 0,78 % orales Aluminium, das in den Blutkreislauf aufgenommen wurde, und nicht auf den 0,1 %-Wert, der vom ATSDR in seinen Berechnungen verwendet wurde.19-20 Infolgedessen stellte die Studie von 2011 die Hypothese auf, dass fast das Achtfache (8 % / 0,78 %) Aluminium sicher in den Blutkreislauf gelangen kann, was zu einer falschen Schlussfolgerung geführt hat.
9. Ist die Exposition gegenüber Aluminium durch Impfstoffe sicher?
Impfstoffe werden intramuskulär injiziert, und die Geschwindigkeit, mit der Aluminium aus Impfstoffen aus dem menschlichen Muskel in den Blutkreislauf wandert, ist unbekannt. Tierversuche deuten darauf hin, dass Aluminium aus Impfstoffen aufgrund mehrerer Variablen einige Monate bis mehr als ein Jahr benötigen kann, um in den Blutkreislauf zu gelangen.21-23 Da die kumulierte Exposition gegenüber Aluminium aus Impfstoffen bei Kindern unter einem Jahr den von der ATSDR festgelegten Tagesgrenzwert um mehrere Hundert überschreitet (Abb. 3 und 4), wäre der Grenzwert immer noch überschritten, wenn Aluminium aus Impfstoffen im Laufe des Verlaufs in den Blutfluss gelangen würde von etwa einem Jahr. Darüber hinaus haben einige Studien gezeigt, dass Aluminium aus Impfstoffen von Immunzellen absorbiert wird und Teile des Körpers erreicht, die weit von der Injektionsstelle entfernt sind, einschließlich des Gehirns.24
Das Ausmaß der Nebenwirkungen von Aluminium in Impfstoffen ist nicht bekannt, da keine Sicherheitsstudien zum Vergleich einer mit aluminiumhaltigen Impfstoffen geimpften Population mit einer nicht mit solchen Impfstoffen geimpften Population durchgeführt wurden.
Aluminiumbegrenzung des Blutflusses abgeleitet von der ATSDR2-14-15
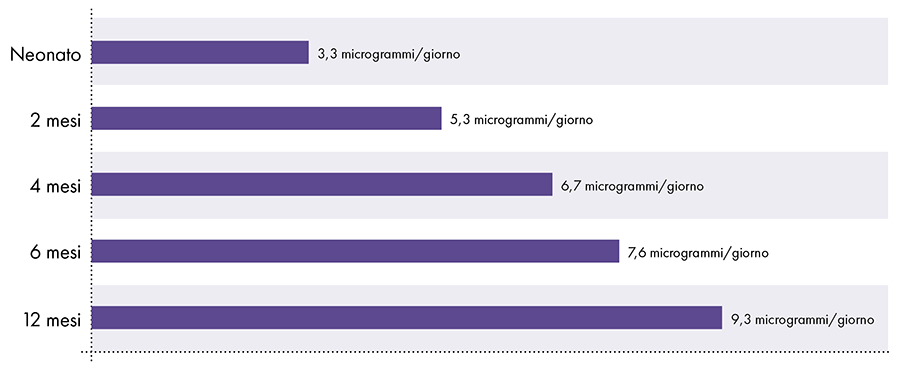 Abbildung 3: Diese Grafik zeigt den Aluminiumgrenzwert für Kinder unterschiedlichen Alters, abgeleitet vom Toxic Substances and Disease Registry, einer Abteilung des United States Department of Health and Human Services. Der Grenzwert besagt, dass täglich nicht mehr als 1 Mikrogramm Aluminium pro Kilogramm Körpergewicht in den Blutkreislauf gelangen sollte, um die neurotoxischen Wirkungen von Aluminium zu vermeiden.
Abbildung 3: Diese Grafik zeigt den Aluminiumgrenzwert für Kinder unterschiedlichen Alters, abgeleitet vom Toxic Substances and Disease Registry, einer Abteilung des United States Department of Health and Human Services. Der Grenzwert besagt, dass täglich nicht mehr als 1 Mikrogramm Aluminium pro Kilogramm Körpergewicht in den Blutkreislauf gelangen sollte, um die neurotoxischen Wirkungen von Aluminium zu vermeiden.
Aluminiumgehalt in Impfstoffen
Referenzen
- American Academy of Pediatrics, Ausschuss für Ernährung. Aluminiumtoxizität bei Säuglingen und Kindern. Pädiatrie. März 1996, 97 (3): 413.
- Agentur für Giftstoffe und Krankheitsregister (ATSDR). Toxikologisches Profil für Aluminium. Washington, DC: US-Gesundheitsministerium; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Aluminium in Lebensmitteln – Art und Beitrag von Lebensmittelzusatzstoffen. In: El-Samragy Y, Herausgeber. Lebensmittelzusatzstoff. Rijeka (Kroatien): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Zum Verständnis der adjuvanten Wirkung von Aluminium. Nat. Rev. Immunol. 2009. April 9 (4): 287.
- Volk VK, Bunney WE. Diphtherie-Immunisierung mit flüssigem Toxoid und mit Alaun ausgefälltem Toxoid. Bin J Public Health Nations Health. 1942 Juli, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Aluminiumsalze in Impfstoffen – US-Perspektive. Impfung. 2002. Mai 31, 20. Anhang 3: S18-22.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. Impfstoffe, die zur Verwendung in den Vereinigten Staaten zugelassen sind; [aktualisiert am 2018. Februar 14; zitiert am 2018. Februar 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Zentren für die Kontrolle und Prävention von Krankheiten. Washington, DC: US-Gesundheitsministerium. Empfohlener Impfplan für Kinder und Jugendliche bis 18 Jahre, USA, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. SCOGS (Select Committee on GRAS Substances); [zitiert am 2018. August 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Priester ND. Das biologische Verhalten und die Bioverfügbarkeit von Aluminium beim Menschen unter besonderer Berücksichtigung von Studien, die Aluminium-26 als Tracer verwenden: Überprüfung und Aktualisierung der Studie. J Umgebungsüberwachung. 2004;6:376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminium in parenteralen Ernährungsprodukten für Kinder: gemessen im Vergleich zum gekennzeichneten Gehalt. J Pediatr Pharmacol. Ther. 2011, 16 (2): 92-7.
- Sedman A. Aluminiumtoxizität in der Kindheit. Pediatr Nephrol. 1992 Juli, 6 (4): 383-93.
- US Food and Drug Administration, Ministerium für Gesundheit und menschliche Dienste. Regeln und Vorschriften. Bundesregistr. Juni 2003, 68 (100): 34286.
- Zentren für die Kontrolle und Prävention von Krankheiten. Washington, DC: US-Gesundheitsministerium. Nationales Zentrum für Gesundheitsstatistik: Datentabelle für Jungen-Länge-für-Alter- und Gewicht-für-Alter-Diagramme; [zitiert am 2019. April 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Zentren für die Kontrolle und Prävention von Krankheiten. Washington, DC: US-Gesundheitsministerium. Nationales Zentrum für Gesundheitsstatistik: Datentabelle für Mädchen mit Längen-für-Alter- und Gewicht-für-Alter-Diagrammen; [zitiert am 2019. April 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Ministerium für Gesundheit und menschliche Dienste. Überarbeitung der Anforderungen an Ausgangsstoffe. Letzte Regel. Bundesregistr. 2011. April 13, 76 (71): 20513-8.
- Amt des Bundesregisters, National Archives and Records Service, General Services Administration. Regeln und Vorschriften. Bundesregistr. 1968 Januar; 33 (6): 369.
- Mitkus RJ, König DB, Hess MA, Forshee RA, Walderhaug MO. Aktualisierte Aluminium-Pharmakokinetik nach Exposition von Säuglingen durch Ernährung und Impfung. Impfung. 2011. Nov. 28, 29 (51): 9538-43.
- Miller S, Ärzte für Einverständniserklärung. Erratum in „Aktualisierte Aluminium-Pharmakokinetik nach Exposition von Säuglingen durch Ernährung und Impfung“. In: Research Gate. Berlin (Deutschland): ResearchGate GmbH; 2020. März 6 [zitiert 2020. März 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Ärzte für Einverständniserklärung. Newport Beach (CA): Ärzte für Einverständniserklärung. Erratum in „Aktualisierte Aluminium-Pharmakokinetik nach Exposition von Säuglingen durch Ernährung und Impfung“; [zitiert 2020. März 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In-vivo-Absorption von aluminiumhaltigen Impfstoffadjuvantien unter Verwendung von 26Al. Vaccine 1997 Aug-Sept, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminium-Assay und Bewertung der lokalen Reaktion zu mehreren Zeitpunkten nach intramuskulärer Verabreichung von aluminiumhaltigen Impfstoffen beim Cynomolgus-Affen. Impfung. 2005. Februar 3, 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminium in Plasma und Gewebe nach intramuskulärer Injektion von adjuvantierten Humanimpfstoffen bei Ratten. Arch Toxicol. 2019 Okt. 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritische Analyse von Referenzstudien zur Toxikokinetik von Adjuvantien auf Aluminiumbasis. J Inorg Biochem. April 2018, 181: 87-95.
Artikel übersetzt von Ärzte mit Einverständniserklärung
Zu den Problemen, die nach der Impfung mit dem 13-valenten Pneumokokken-Konjugatimpfstoff (PCV13), dem 23-valenten Pneumokokken-Polysaccharid-Impfstoff (PPSV23) und anderen Impfstoffen auftreten können, gehören laut US CDC:(1-2)
- Schwere allergische Reaktionen, die innerhalb von Minuten bis Stunden nach der Impfung auftreten.
- Starke Schulterschmerzen, die die Bewegung des injizierten Arms einschränken.
- Ohnmacht oder Zusammenbruch nach der Impfung. Möglicherweise wird Ihnen geraten, sich nach der Impfung etwa 15 Minuten lang hinzusetzen oder hinzulegen, um eine Ohnmacht und Verletzungen zu vermeiden, die durch einen Sturz verursacht werden könnten. Es ist wichtig, dass Sie Ihren Arzt informieren, wenn Sie nach der Impfung Ohrensausen, Sehstörungen oder Schwindel bemerken.
Nebenwirkungen des PCV13-Impfstoffs (Pneumokokken-Konjugat-Impfstoff)
Die Nebenwirkungen nach der Verabreichung von PCV13 variieren je nach Dosis der Serie und dem Alter des Empfängers. Bei Kindern waren die am häufigsten berichteten Reaktionen Reizbarkeit, Schläfrigkeit, Appetitlosigkeit, Rötung, Schmerzen oder Schwellung an der Impfstelle und leichtes bis mäßiges Fieber.
Es wurde festgestellt, dass Kinder, die PCV13 gleichzeitig mit einem inaktivierten Grippeimpfstoff erhielten, ein erhöhtes Risiko für Fieberkrämpfe hatten.
Bei Erwachsenen wurde hauptsächlich über Rötung, Schwellung und Schmerzen an der Injektionsstelle, Müdigkeit, Fieber, Schüttelfrost, Kopf- und Gliederschmerzen berichtet.(3)
Nebenwirkungen von Prevenar 13 (PCV13), die bei Säuglingen und Kindern in klinischen Studien vor der Zulassung berichtet wurden:(4) Schmerzen an der Injektionsstelle, Schwellung, Rötung, Fieber, verminderter Appetit, vermehrter und verminderter Schlaf, Reizbarkeit, Durchfall, Erbrechen, Hautausschlag, Nesselsucht, Überempfindlichkeitsreaktion einschließlich Bronchospasmus, geschwollenes Gesicht und Kurzatmigkeit, Krampfanfälle, Lungenentzündung, Gastroenteritis, Bronchiolitis, Tod ( als SIDS gemeldet).
Nebenwirkungen von Prevenar 13 (PCV13), die bei Erwachsenen in klinischen Studien vor der Zulassung berichtet wurden:(5) Schmerzen, Schwellung und Rötung an der Injektionsstelle, Einschränkung der Armbewegung, Fieber, Erbrechen, Schüttelfrost, Muskelschmerzen, Müdigkeit, Kopfschmerzen, verminderter Appetit, Hautausschlag, Gelenkschmerzen, Tod (Todesfälle, die vor der Zulassung gemeldet wurden, umfassten Todesfälle durch Krebs, Herz Krankheit, Peritonitis, Lungeninfektion mit Mycobacterium avium-Komplex und septischer Schock).
Nebenwirkungen von Prevenar 13 (PCV13), die nach Markteinführung berichtet wurden:(6) Zyanose, Lymphadenopathie an der Injektionsstelle, Anaphylaxie, Schock, Hypotonie, Blässe, Apnoe, angioneurotisches Ödem, Erythema multiforme, Pruritus an der Injektionsstelle, Urtikaria und Hautausschlag.
Klinische Studien vor der Zulassung des ersten Pneumokokken-Konjugatimpfstoffs, Prevenar (PCV7)verglich die Sicherheit von Prevenar (PCV7) mit einem in der Erprobung befindlichen Impfstoff gegen Meningitis C, wodurch die wissenschaftliche Gültigkeit der Studie ernsthaft untergraben wurde.
In klinischen Studien vor der Zulassung von Prevenar (PCV7) litten Kinder in den Gruppen, die den Pneumokokken-Impfstoff erhielten, häufiger unter Krampfanfällen, Reizbarkeit, hohem Fieber und anderen Reaktionen. Es gab 7 Todesfälle in der Prevenar-Gruppe (PCV12), darunter 5 Todesfälle durch plötzlichen Kindstod (SIDS). Es wurden keine Langzeitstudien abgeschlossen, um zu beurteilen, ob der Prevenar-Impfstoff (PCV7), der allein oder in Kombination mit anderen Impfstoffen verabreicht wird, einen Zusammenhang mit chronischen Krankheiten oder Behinderungen hat, wie z. B. der Entwicklung von Diabetes, Asthma, Krampfanfällen oder Lernschwierigkeiten , ADHS.(7)
Sicherheitsstudien vor der Zulassung von Prevenar 13 (PCV13) verglichen diesen Impfstoff der nächsten Generation mit dem ursprünglichen Prevenar-Impfstoff (PCV7), einem Impfstoff, der unzureichend auf Sicherheit untersucht wurde, und 2012 wurden Bedenken bezüglich eines Zusammenhangs zwischen Fieberkrämpfen und Prevenar 13 (PCV13 ).(8-9)
PCV13 war bei unabhängiger Verabreichung mit einem erhöhten Risiko für Fieberkrämpfe verbunden(10) und bei Verabreichung in Kombination mit einem parenteral inaktivierten Influenza-Impfstoff (IIV).(11)
Einige Studien haben auch den PCV-Impfstoff mit dem Guillain-Barré-Syndrom in Verbindung gebracht,(12) zu Polyserositis,(13) zur septischen Schulter(14) und Erythema multiforme.(15)
Nebenwirkungen des PPSV23-Impfstoffs (Pneumococcus-Polysaccharid)
Laut CDC leiden etwa 50 Prozent der Menschen, die den Pneumokokken-Polysaccharid-Impfstoff (PPSV23) erhalten, an der Injektionsstelle an Schmerzen und Rötungen. Gliederschmerzen, Fieber und schwerere Lokalreaktionen können auch nach PPSV-Gabe auftreten23.(16)
Nebenwirkungen von PNEUMOVAX23 (PPSV23), die bei Erwachsenen in klinischen Studien vor der Zulassung in den USA berichtet wurden:(17) Schmerzen an der Injektionsstelle, Rötung, Juckreiz, Blutergüsse und Schwellungen, Kopfschmerzen, Schüttelfrost, Fieber, Durchfall, Dyspepsie, Übelkeit, Infektion der oberen Atemwege, Rückenschmerzen, Nackenschmerzen, Pharyngitis, Muskelschmerzen, Müdigkeit, Depression, Colitis ulcerosa, Brustschmerzen, Angina pectoris, Herzinsuffizienz, Tremor, Rigor, Schwitzen, Schlaganfall, lumbale Radikulopathie, Pankreatitis, Myokardinfarkt, Tod.
Bei fast 80 % der an den klinischen Studien vor der Zulassung teilnehmenden Probanden kam es nach einer Wiederholungsimpfung drei bis fünf Jahre nach der ersten Impfung zu einer unerwünschten Reaktion an der Injektionsstelle. Die Rate systemischer Nebenwirkungen (Kopfschmerzen, Müdigkeit, Myalgie) nach einer Wiederholungsimpfung mit PPSV23 war ebenfalls höher, wobei 33 % der Erwachsenen ab 65 Jahren und 37,5 % der Erwachsenen ab 50 Jahren zwischen 64 und XNUMX Jahren berichteten eine nachteilige Reaktion.(18)
Nebenwirkungen von PNEUMOVAX23 (PPSV23), die nach der Markteinführung gemeldet wurden:(19) Anaphylaktoide Reaktionen, Serumkrankheit, angioneurotisches Ödem, Arthritis, Arthralgie, Erbrechen, Übelkeit, verminderte Beweglichkeit der Extremitäten, peripheres Ödem in der injizierten Extremität, Fieber, Unwohlsein, Zellulitis, Wärme an der Injektionsstelle, Lymphadenopathie, Lymphadenitis, Leukozytose, Thrombozytopenie bei Patienten mit stabiler idiopathischer Erkrankung thrombozytopenische Purpura, hämolytische Anämie bei Patienten, die andere hämatologische Erkrankungen hatten, Parästhesie, Guillain-Barré-Syndrom, Radikuloneuropathie, Fieberkrämpfe, Hautausschlag, Erythema multiforme, Urtikaria, Zellulitis-ähnliche Reaktionen.
Obwohl PNEUMOVAX23 (PPSV23) für die Anwendung bei Kindern ab zwei Jahren mit Erkrankungen wie chronischer Herz- und Lungenerkrankung, Diabetes, Cochlea-Implantaten, Liquorlecks, Sichelzellenanämie, funktioneller oder anatomischer Asplenie und Immunsuppression zugelassen ist, liegen keine Informationen darüber vor die Sicherheit oder Wirksamkeit des Impfstoffs bei Kindern ist der Packungsbeilage des Impfstoffs zu entnehmen.(20)
Einige Studien haben PPSV23 mit systemischen Entzündungsreaktionen in Verbindung gebracht(21) und Fieber.(22-23-24-25-26)
Referenzen (zum Öffnen klicken)
- CDC Pneumokokken-Konjugat (PCV13) VIS. 5. November 2015
- CDC Pneumokokken-Polysaccharid VIS. April 24, 2015
- CDC Pneumokokken-Konjugat (PCV13) VIS. 5. November 2015
- FDA Prevnar 13 Packungsbeilage August 22, 2017
- Ebenda
- Ebenda
- FDA 7-wertiger Pneumokokken-Konjugatimpfstoff (PREVNAR) – Beilage des Produktherstellers. 1. Oktober 2002
- Hitt, E Prevnar 13 sollte auf das Risiko eines Fieberkrampfs überwacht werden, sagt das FDA-Gremium. Medscape. Jan 31, 2012
- Tse A, Tseng HF, Greene SK, et al. Signalidentifizierung und Bewertung des Risikos von Fieberkrämpfen bei Kindern nach trivalentem inaktiviertem Influenza-Impfstoff im Vaccine Safety Datalink Project, 2010-2011. Impfen Sie. 2012 Mär 2;30(11):2024-31
- Baker M., Jankosky C., Yih K. et al. Das Risiko von Fieberkrämpfen nach Influenza- und 13-wertigen Pneumokokken-Konjugatimpfstoffen. Öffnen Sie das Forum Infect Dis. Herbst 2017; 4 (Ergänzung 1): S464–S465.
- CDC Kinderimpfungen und Fieberkrämpfe Jun. 20, 2016
- Ravishankar, N Guillain-Barré-Syndrom nach PCV-Impfung. J Neurol Neurochirurg 4 (1): 134
- Tawfik P, Elie Gertner E, McEvoy CE Schwere Polyserositis, induziert durch den 13-valenten Pneumokokken-Konjugatimpfstoff: ein Fallbericht J Med Case Rep. 2017; 11: 142.
- MJ DeRogatis, L. Parameswaran, P. Lee et al. Septisches Schultergelenk nach Pneumokokken-Impfung, das ein chirurgisches Debridement erfordert. HSS J 2018 Oct;14(3):299-301
- Monastirli A, Pasmatzi E, Badavanis G et al. Erythema multiforme nach Pneumokokken-Impfung. Acta Dermatovenerol Alp Pannonica Adriat. 2017 Mar;26(1):25-26.
- CDC Pneumokokken-Polysaccharid VIS. April 24, 2015
- FDA Pneumovax 23 - Pneumokokken-Impfstoff, polyvalent. Packungsbeilage 30. Dezember 2014
- Ebenda
- Ebenda
- Ebenda
- von Elten, KA, Duran LL, Banks TA, et al. Systemische Entzündungsreaktion nach Pneumokokken-Impfung Eine Fallserie Hum Vaccine Immunother. 2014. Juni 1; 10(6): 1767–1770.
- Huang DT, Chiu NC, Chi H, et al. Langanhaltendes Fieber mit Zellulitis-ähnlicher Reaktion bei mit Pneumokokken-Polysaccharid geimpften Kindern. Pediatr Infect Dis J.. 2008 Oct;27(10):937-9.
- Yousef E, Mannan S. Systemische Reaktion auf Pneumokokken-Impfstoff: Wie häufig in der Pädiatrie? Allergie Asthma Proc. 2008 Jul-Aug;29(4):397-9
- Gabor EP, Seemann M. Akute fieberhafte systemische Reaktion auf polyvalenten Pneumokokken-Impfstoff. JAMA. 1979 Nov 16;242(20):2208-9.
- Hasan S., Yousef M., Shridharani S Schwere fieberhafte systemische Reaktion auf Pneumokokken-Impfstoff. J Natl Med Assoc. Februar 2005; 97 (2): 284–285.
- Lee A, Goyal R, Shan HY. Schweres langanhaltendes Fieber nach Pneumokokken-Impfung. Bin J Med Sci. 2006 Dec;332(6):351-3.
Dieser Artikel ist zusammengefasst und übersetzt von National Vaccine Information Center.

