Abschließender technischer Bericht - Analyse des molekularen Profils von Impfstoffen

Vorwort
Zunächst möchten wir uns bei den sehr nützlichen Kommentaren bedanken, die von denjenigen abgegeben wurden, die die Ergebnisse der Analysen überprüft haben, die im Rahmen wissenschaftlicher Forschungsaktivitäten im Zusammenhang mit Priorix Tetra- und Infanrix Hexa-Produkten durchgeführt wurden. Die vorgestellten kritischen Punkte waren in der Tat sehr nützlich, um technisch-wissenschaftliche Integrationen hinzuzufügen, die die geleistete Arbeit verdeutlichen können. Wir glauben, dass nur durch eine gesunde Verbindung von wissenschaftlichen Visionen Schlussfolgerungen zu den erhaltenen Daten gezogen werden können, die für die gesamte wissenschaftliche Gemeinschaft und für die Personen, die sich damit befassen, nützlich sein können.
1. Stand der Technik
Vorläufige Studien (Screening ohne Bestätigung) zum biomolekularen, metabolomischen und proteomischen Profil von Priorix Tetra- und Infanrix Hexa-Produkten haben zu einem Zusammensetzungsrahmen geführt, der in den folgenden Punkten zusammengefasst ist:
- Vorhandensein verschiedener analytischer Signale, die durch Recherchen in den Datenbanken Metlin 1-2 und KEGG3 nicht mit bekannten Verbindungen in Verbindung gebracht werden können. Daher ergab sich ein Bild, das mit einer erheblichen Komplexität bei der Zusammensetzung von Handelsprodukten verbunden war.
- Vorhandensein von Proteinen, die nicht in einer Packungsbeilage des Priorix Tetra-Produkts angegeben sind. Letzteres kann möglicherweise mit Rückständen des Produktionsprozesses in Verbindung gebracht werden
- Nichtnachweis der im Infanrix Hexa-Produkt deklarierten Antigene. Die Analysetechnik bestand aus einem enzymatischen Verdau mit Trypsin, der mit Massenspektrometrietechniken verbunden war. 4-5
Diese Daten haben insbesondere zu Punkt C - Der Proteinnachweis wird in der Tat unter Verwendung eines seit über 10 Jahren international anerkannten Standardansatzes 4 des Verdaus durch das Trypsinenzym 4 durchgeführt. Die so erhaltenen Peptide werden chromatographisch getrennt und durch Massenspektrometrie 4-5 analysiert. Die Hauptbeobachtung war der Tatsache inhärent, dass die Impfstoffe Hilfsstoffe auf Aluminiumbasis enthalten, die möglicherweise den enzymatischen Verdauungsprozess hemmen könnten. Die später erhobenen Daten ermöglichten es, insbesondere im Hinblick auf die Beschwerde unter Punkt C wesentliche Klarstellungen vorzunehmen.
2. Neue Erkenntnisse und Analysen
2.1 Erkenntnisse im Zusammenhang mit der Analyse des Infanrix Hexa-Produkts
Bevor mit der Veranschaulichung der neu gewonnenen Daten zu Hexyon- und Gardas 9-Impfstoffen fortgefahren wird, muss unbedingt die Frage beantwortet werden, welche die Hemmung der proteolytischen Aktivität von Trypsin betrifft, die durch das Vorhandensein von Hilfsstoffen auf Aluminiumbasis in Infanrix Hexa verursacht wird Impfstoff. In diesem Zusammenhang muss angegeben werden, dass im tryptischen Aufschluss immer eine Aufschlusskontrolle vorhanden ist. Tatsächlich hat das Trypsin, das zur Durchführung des Aufschlusses verwendet wird, obwohl es so konstruiert ist, dass es die Autolyse verhindert, einen kleinen Prozentsatz des letzteren, der im Fall der enzymatischen Aktivität zur Gewinnung des Fragments mit m / z 842 und der folgenden Peptidsequenz führt: VATVSLPR. Dieses Fragment wurde tatsächlich während des tryptischen Aufschlusses des Infanrix Hexa-Produkts nachgewiesen, was durch das Ionenextraktions-Chromatogramm (1) überprüft werden kann.
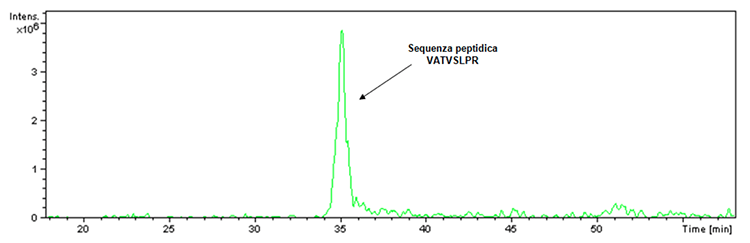
Abbildung 1: Ionenassoziiertes Ionenextraktions-Chromatogramm mit einem Verhältnis von m / z 842 in der Probe der Infanrix Hexa-Produktcharge (Chargennummer A21CD072D).
Darüber hinaus wird eine externe Kontrolle durch Verdauung von Hämoglobin durchgeführt, um die Güte der verwendeten Trypsincharge weiter zu überprüfen. Hämoglobin, das in dem Analyseabschnitt analysiert wurde, in dem das Produkt überwacht wurde, wurde mit einem signifikanten statistischen Score (loge <- 100) erkannt. Diese Daten bestätigten die Tatsache, dass die Enzymaktivität vorhanden war.
2.2 Neue Analysen zu Hexyon- und Gardasil-Produkten
Die Analyse von Hexyon- und Gardas 9-Produkten führte zum Nachweis komplexer Molekülprofile. In diesem Fall wurde jedoch das Vorhandensein der meisten in der Packungsbeilage angegebenen Antigene nachgewiesen. Sie wurden durch tryptische Verdauung und in Gegenwart von Adjuvantien nachgewiesen.
Diese Tatsache verstärkt den Beweis, dass die Triptica-Verdauungsreaktion in Gegenwart von Adjuvantien nicht gehemmt wird. Im Fall von Hexyon- und Gardas 9-Impfstoffen wurde die Komplexität des Molekularprofils hauptsächlich auf das Vorhandensein zahlreicher Arten mit niedrigem Molekulargewicht zurückgeführt, die mit den Referenzdatenbanken Metlin 1-2- und KEGG 3 nicht identifizierbar waren.
3. Schlussfolgerungen und abschließende Überlegungen
Die durchgeführten Analysen führten zu folgenden Ergebnissen:
- Das molekulare Profil der analysierten Impfstoffe ist im Allgemeinen komplex und weitgehend unbekannt.
- Es gibt Proteinkontaminationen, die nicht in der Packungsbeilage angegeben sind und deren Zusammensetzung unterschiedlich ist.
- In mehreren Fällen wurden die in der Packungsbeilage angegebenen Antigene nicht nachgewiesen. Diese Tatsache kann auf mehrere Faktoren zurückgeführt werden. Unter den letzteren können wir die Empfindlichkeit der verwendeten Methode betrachten. Wir sind jedoch der Meinung, dass wir das Phänomen der Verdauungshemmung aufgrund des Vorhandenseins von Adjuvantien in der Formulierung des Impfstoffs ausschließen können. Tatsächlich wird die enzymatische Aktivität hauptsächlich durch das Vorhandensein von Fragmenten der tryptischen Autolyse in den Lösungen der verdauten Impfstoffe (interne Kontrolle) bestätigt.
4. Zukünftige Studien
Weitere Studien werden im Rahmen der Forschungs- und Entwicklungsaktivitäten durchgeführt, um folgende Aspekte zu untersuchen:
- makromolekulare Zusammensetzung in Verbindung mit festen Rückständen in Impfstoffen (MALDI-TOF-MS-Analyse); 5
- Bewertung der Konzentration der in den Produkten enthaltenen Metalle.
- Analyse der zweiten Ebene zur Bestätigung des Vorhandenseins toxischer Verbindungen, die in der Screeningphase nachgewiesen wurden. Ihre Konzentration wird dann gemäß den Angaben in den internationalen Sicherheitsdatenblättern auf ihre Toxizität bezogen. Die Analysen der zweiten Ebene werden in Übereinstimmung mit der europäischen Richtlinie EU 2002/657 / EG durchgeführt, um hohe Qualitätsstandards im Massenspektrometriesektor zu gewährleisten. 6
widerspricht
5. Bibliographische Referenzen
- Autenhahn R., Cho K., Uritboonthai W., Zhu Z., Patti G., Siuzdak G. (September 2012). "Ein beschleunigter Workflow für nicht zielgerichtete Metabolomik mithilfe der METLIN-Datenbank". Naturbiotechnologie. 30: 826–828. doi: 10.1038 / nbt.2348. PMC 3666346. PMID 22965049.
- Smith CA, I'Maille G, Want EJ, Qin C, Trauger SA, Brandon TR, Custodio DE, Abagyan R, Siuzdak G (Dezember 2005). "METLIN: eine Metaboliten-Massenspektraldatenbank" (PDF). Ther Drug Monit. 27 (6): 747–51. doi: 10.1097 / 01.ftd.0000179845.53213.39. PMID 16404815.
- Kanehisa M (2013). "Chemische und genomische Evolution enzymkatalysierter Reaktionsnetzwerke". FEBS Lett. 587 (17): 2731–7.
- Cristoni S, Bernardi LR. "Bioinformatik in der massenspektrometrischen Datenanalyse für Proteomics-Studien." Expert Rev Proteomics. 2004 Dec; 1 (4): 469 & ndash; 83.
- Cristoni S, Bernardi LR. "Entwicklung neuer Methoden für die massenspektrometrische Untersuchung bioorganischer Makromoleküle." Mass Spectrom Rev. 2003 Nov-Dec; 22 (6): 369 & ndash; 406.
- Cristoni S., Dusi G., Brambilla P., Albini A., Conti M., Brambilla M., Bruno A., Di Gaudio F., Ferlin L., Tazzari V., Mengozzi S., Barera S., Sialer C., Trenti T., Cantu M., Rossi Bernardi L., Noonan DM. "SANIST: Optimierung einer Technologie zur Identifizierung von Verbindungen auf der Grundlage der EU-Richtlinie mit Anwendungen in der forensischen, pharmazeutischen und Lebensmittelanalytik." J. Mass Spectrom. 2017 Jan; 52 (1): 16-21. doi: 10.1002 / jms.3895.
Herunterladen: CORVELVA-Finale-Technische-Report.pdf
Übersetzt vom CLiVa-Team - www.clivatoscana.com

