Ali lahko pnevmokokno cepivo povzroči poškodbe in/ali smrt?

POMEMBNO OPOMBA: Corvelva vas vabi, da dobite poglobljene informacije tako, da preberete vse razdelke in povezave, kot tudi letake proizvajalca o izdelku in tehnične liste ter da se pogovorite z enim ali več zaupanja vrednimi strokovnjaki, preden se odločite za cepljenje sebe ali svojega otroka. Te informacije so zgolj informativne narave in niso mišljene kot zdravniški nasvet.
Problem večkratnih cepiv (kliknite za odpiranje)
Problem večkratnih cepiv

Trenutni koledarji cepljenja, zlasti za pediatrično starost, predvidevajo dajanje več antigenov in cepiv v eni seji, kar daje prednost udobju na račun varnosti. Da bi lahko posebej govorili o varnosti cepiv, moramo nujno upoštevati kompleksnost pojava, pri čemer vsem bralcem svetujemo, naj se ustrezno informirajo o vseh vidikih cepljenja, o prednostih in slabostih.
Dr. Russell Blaylock, klinični asistent profesor nevrokirurgije na Medicinskem centru Univerze Mississippi, je leta preučeval "strupeno sinergijo" in lahko opazil, da ko dva šibko toksična pesticida, pri čemer nobeden ne more povzročiti Parkinsonovega sindroma pri poskusnih živalih, se med seboj kombinirajo, lahko celo hitro povzročijo bolezen in ta pojav primerja s pojavom več cepiv, ki se dajejo hkrati: "Cepljenja, če jih je preveč in so preblizu skupaj, se obnašajo kot kronična bolezen".(A). Drugo Dve študiji sta potrdili, da lahko pride do nenadne smrti dojenčka po inokulaciji več cepiv v enem dajanju.(bc)
Študija, objavljena v Human and Experimental Toxicology, je pokazala, da imajo države, ki otrokom predpisujejo več cepiv, običajno višje stopnje umrljivosti dojenčkov.(D) Na primer, v ZDA, kjer otroci prejmejo 26 cepiv, umre več kot 6 otrok na 1000 živorojenih otrok, medtem ko na Švedskem in Japonskem, kjer se daje 12 pediatričnih cepiv, poročajo o 3 smrtih na vsakih 1000 živorojenih otrok. V omenjeni študiji je obravnavana tudi povezava med cepivi in SIDS-om.
Iz švicarske študije, objavljene leta 2005 v European Journal of Pediatrics(E) iz tega izhaja, da je glede na učinke na nedonošenčke incidenca ponavljajoče se ali povečane apneje in bradikardije po dajanju šestvalentnih cepiv 13 %. Istega leta je ista revija objavila nemško študijo, ki je preučevala nenadne smrti dojenčkov po heksavalentnem. Avtorji pišejo: »Ti rezultati, ki temeljijo na spontanih poročilih, ne dokazujejo vzročne povezave med cepljenjem in nenadno smrtjo dojenčka, ampak predstavljajo signal glede enega od dveh razpoložljivih heksavalentov; znak, ki bi moral voditi k intenzivnejšemu nadzoru nenadnih smrti dojenčkov po cepljenju".(F)
Leta 2006 je bil objavljen v medicinski reviji Vaccine(G) pismo skupine raziskovalcev z Univerze v Münchnu, ki je poročalo o "šestih primerih nenadne smrti dojenčkov po heksavalentnem cepljenju. Vsi so bili najdeni mrtvi brez pojasnila 1-2 dni po cepljenju". Uvrščeni so bili med tipične primere nenadne smrti dojenčka, vendar je avtoptična verifikacija razkrila nevropatološke in histološke nepravilnosti in vsi otroci so pokazali znaten možganski edem, zaradi česar so bili izjema v primerjavi z drugimi primeri SIDS (Sindrom nenadne smrti dojenčka). Raziskovalci so zapisali, da smo pred uvedbo šestvalentnega cepiva (v letih 1994–2000) opazili le enega od 198 otrok z nenadno smrtjo dojenčka, ki je umrl kmalu po cepljenju z DTP. Toda med letoma 2001 in 2004 so identificirali pet podobnih primerov od 74 s SIDS. To bi pomenilo trinajstkratno povečanje."
Tudi leta 2006 na Virchows Archive(H), je ekipa z Inštituta za patologijo Univerze v Milanu zapisala: »Strokovnjaki Evropske agencije za vrednotenje medicinskih izdelkov so analizirali možnost, da obstaja povezava med šestvalentnimi cepivi in nekaterimi smrtnimi primeri. Med udeleženci so bili patologi z izkušnjami s cepivi in sindromom nenadne smrti dojenčka, ki so izvajali obdukcije.Toda, kolikor vemo, je bilo malo pozornosti posvečeno pregledu možganskega debla in krvnega srca na serijskih odsekih in ni bilo možnosti ugotoviti vloge sprožilca. cepiva za te smrti. Tukaj poročamo o primeru 3-mesečne punčke, ki je nenadoma umrla po šestvalentnem cepljenju. Pregled možganskega debla na serijskih rezih je pokazal dvostransko hipoplazijo arkuatnega jedra. Prevodni sistem srca je imel vztrajno fetalno disperzijo in degeneracijo. Ta primer ponuja edinstveno razumevanje možne vloge šestvalentnega cepiva pri sprožitvi smrtonosnih posledic pri ranljivem otroku. Vsak primer nenadne in nepričakovane smrti, ki se pojavi kmalu po rojstvu ali v zgodnjem otroštvu, še posebej, če sledi cepljenju, je treba v skladu s smernicami vedno opraviti popolno obdukcijo.
Reference
- Blaylock R, "Vaccinations: the hidden dangers", The Blaylock Wellness Report, maj 2004, str. 1-9
- Ottaviani G. et al., "Sindrom nenadne smrti dojenčka (SIDS) kmalu po heksavalentnem cepljenju: druga patologija pri sumu na SIDS?", Virchows Arhiv, 2006, 448, str. 100-104.
- Zinka B. et al., "Nepojasnjeni primeri nenadne smrti dojenčka kmalu po heksavalentnem cepljenju", Vaccine, julij 2006, 24 (31-32), str. 5779-5780.
- Miller NZ et al1. , "Stopnje umrljivosti dojenčkov so nazadovale glede na število rutinsko danih odmerkov cepiva: ali obstaja biokemična ali sinergistična toksičnost?", Hum. Exp. Toxicol., maj 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Problem aluminija (kliknite za odpiranje)
Aluminij v cepivih: kaj morajo vedeti starši

1. Kaj je aluminij?
Aluminij je srebrno bela lahka kovina, temprana in odporna. Zaradi teh lastnosti je uporaben v številnih panogah in izdelkih, vključno s stroji, gradbeništvom, skladišči, kuhinjsko posodo, kuhinjskimi pripomočki, tekstilom, barvili in kozmetiko. Aluminij je tudi najbolj razširjena kovina v zemeljski skorji in skoraj ves aluminij v okolju se nahaja v tleh. Vendar se aluminij naravno ne nahaja v znatnih količinah v živih organizmih (kot so rastline in živali) in nima znane biološke funkcije. V zadnjem stoletju je uporaba aluminija v nekaterih izdelkih povzročila povečano izpostavljenost ljudi. Glavni viri izpostavljenosti so živila, ki vsebujejo aluminij (npr. pecilni prašek, predelana hrana, otroške formule itd.), medicinski izdelki (npr. antiperspiranti, antacidi itd.), injekcije proti alergijam in cepiva.1-3
2. Zakaj je aluminij prisoten v cepivih?
Nekatera cepiva uporabljajo aluminijeve spojine (aluminijev hidroksid in aluminijev fosfat) kot pomožne snovi, ki so sestavine, ki povečajo imunski odziv na antigen (tujko).4-5 Ameriška uprava za hrano in zdravila (FDA) pravi, da bi se lahko imunski odziv, ki ga sprožijo, zmanjšal, če nekatera cepiva ne bi vključevala aluminija.6
3. Katera cepiva vsebujejo aluminij?
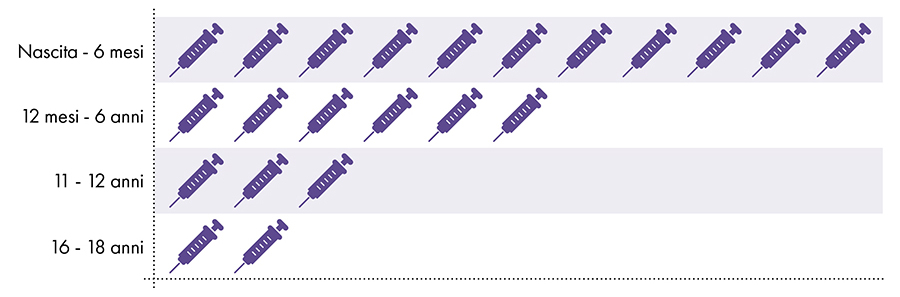
Naslednja cepiva vsebujejo aluminij in se dajejo dojenčkom, otrokom in mladostnikom (slika 1):
- Hepatitis B (HepB)
- šestvalentnega
- Davica, tetanus in oslovski kašelj (DTaP in Tdap)
- Haemophilus influenzae tipa b (PedvaxHIB)
- Pnevmokok (PCV)
- Hepatitis A (HepA)
- Humani papiloma virus (HPV)
- Meningokok B (MenB)
Slika 1: Od rojstva do 18 let se da do 22 odmerkov cepiv, ki vsebujejo aluminij7-8
4. Ali je izpostavljenost aluminiju varna?
FDA že od leta 1975 meni, da je aluminij splošno priznan kot varen (GRAS).9 Vendar pred letom 1990 ni bilo tehnologije za natančno odkrivanje majhnih količin aluminija, ki so jih dajali subjektom v znanstvenih študijah.10 Posledično je bila količina aluminija, ki bi jo lahko absorbirala pred pojavom škodljivih učinkov, neznana.
Od devetdesetih let prejšnjega stoletja so zaradi tehnološkega napredka opazili, da majhne količine aluminija, ki ostanejo v človeškem telesu, ovirajo številne celične in presnovne procese v živčnem sistemu in tkivih drugih delov telesa.1-10-11 Največje negativne učinke aluminija so opazili v živčnem sistemu in segajo od motenj motoričnih sposobnosti do encefalopatije (spremenjeno duševno stanje, osebnostne spremembe, težave z razmišljanjem, izguba spomina, napadi, koma in drugo).2-12
Ministrstvo za zdravje in človeške storitve Združenih držav Amerike (HHS) priznava aluminij kot znan nevrotoksin.2 Poleg tega je FDA opozorila na tveganja zastrupitve z aluminijem pri dojenčkih in otrocih.13
FEDERAL REGISTER: Dnevni časopis vlade Združenih držav"Tudi donošeni dojenčki z normalnim delovanjem ledvic so lahko ogroženi zaradi hitre rasti in nezrelosti možganov in okostja ter nezrelosti krvno-možganske pregrade. Do 1. ali 2. leta imajo dojenčki nižje Stopnja glomerulne filtracije kot pri odraslih, kar vpliva na njihovo delovanje ledvic. Agencija se boji, da so majhni otroci in tisti z nezrelim delovanjem ledvic izpostavljeni povečanemu tveganju izpostavljenosti aluminiju." |
5. Koliko oralnega aluminija ni varno?
Leta 2008 je Agencija za register strupenih snovi in bolezni (ATSDR), oddelek HHS, uporabila študije o nevrotoksičnih učinkih aluminija, da bi ugotovila, da ne več kot 1 miligram (1.000 mikrogramov) aluminija na kilogram telesne teže na dan izogibajte se negativnim učinkom aluminija.2
6. Koliko aluminija vbrizganega ni varno?
Za določitev količine aluminija, ki jo je mogoče varno vbrizgati, je treba pretvoriti oralno mejo aluminija v ATSDR. Meja ATSDR za peroralni aluminij (1.000 mikrogramov aluminija na kilogram telesne teže na dan) temelji na 0,1 % peroralnega aluminija, ki se absorbira v krvni obtok, saj prebavni trakt blokira skoraj ves peroralni aluminij.2 Nasprotno pa aluminij, injiciran intramuskularno, obide prebavni trakt in 100 % aluminija se lahko sčasoma absorbira v krvni obtok (tj. delež absorbiranega aluminija je 1.000-krat večji). Da bi upoštevali te različne količine absorpcije, je treba oralno mejo aluminija ATSDR deliti s 1000. Ta pretvorba vodi do mejne vrednosti aluminija v krvi, ki izhaja iz ATSDR, 1 mikrogram aluminija (0,1 % od 1.000 mikrogramov) na kilogram telesne teže na dan. Posledično, da bi se izognili nevrotoksičnim učinkom aluminija, ne sme priti v krvni obtok več kot 1 mikrogram aluminija na kilogram telesne teže na dan. Slika 3 prikazuje mejo aluminija v krvi, ki izhaja iz ATSDR, za dojenčke različnih starosti glede na njihovo težo.
7. Koliko aluminija je v cepivih?
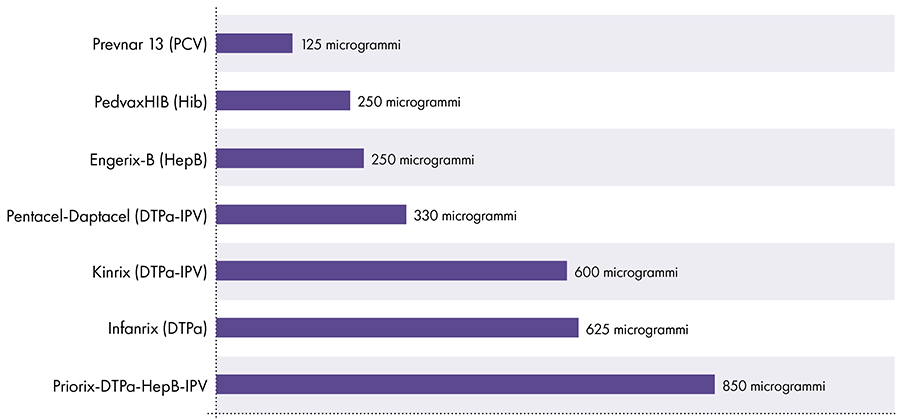
Količina aluminija v cepivih je različna.16 Leta 1968 je ameriška zvezna vlada postavila mejo za količino aluminija v cepivih na 850 mikrogramov na odmerek, ki temelji na količini aluminija, ki je potrebna za učinkovitost nekaterih cepiv.6-17 Posledično se količina aluminija v cepivih za dojenčke, ki vsebujejo aluminij, giblje od 125 do 850 mikrogramov na odmerek. Slika 4 prikazuje vsebnost aluminija v enem odmerku različnih cepiv, danih otrokom.
8. Ali so kakšne študije primerjale količino aluminija v cepivih z mejo, ki izhaja iz Agencije za toksične snovi in register bolezni (ATSDR)?
Leta 2011 je bila objavljena študija, katere namen je primerjati količino aluminija v cepivih z mejo pretoka krvi, ki jo je določil ATSDR.18 Vendar pa je ta študija napačno utemeljila svoje izračune na 0,78 % peroralnega aluminija, ki se absorbira v krvni obtok, namesto na 0,1 % vrednosti, ki jo je ATSDR uporabil v svojih izračunih.19-20 Posledično je študija iz leta 2011 domnevala, da lahko skoraj 8-krat (0,78 % / 0,1 %) aluminij varno vstopi v krvni obtok, kar je pripeljalo do napačnega zaključka.
9. Ali je izpostavljenost aluminiju zaradi cepiv varna?
Cepiva se injicirajo intramuskularno in hitrost, s katero aluminij iz cepiv migrira iz človeških mišic v krvni obtok, ni znana. Študije na živalih kažejo, da lahko aluminij iz cepiv zaradi več spremenljivk vstopi v krvni obtok od nekaj mesecev do več kot enega leta.21-23 Ker kumulativna izpostavljenost aluminiju s cepivi pri otrocih, mlajših od enega leta, presega dnevno mejo, ki jo določa ATSDR, za nekaj sto (sliki 3 in 4), bi bila meja še vedno presežena, če bi aluminij iz cepiv vstopil v krvni obtok med približno eno leto. Poleg tega so študije pokazale, da aluminij iz cepiv absorbirajo imunske celice in doseže dele telesa, ki so daleč od mesta injiciranja, vključno z možgani.24
Obseg škodljivih učinkov aluminija v cepivih ni znan, saj varnostne študije, ki bi primerjale populacijo, cepljeno s cepivi, ki vsebujejo aluminij, s populacijo, ki ni bila cepljena s takšnimi cepivi, niso bile izvedene.
Aluminijasta omejitev krvnega pretoka, ki izhaja iz ATSDR2-14-15
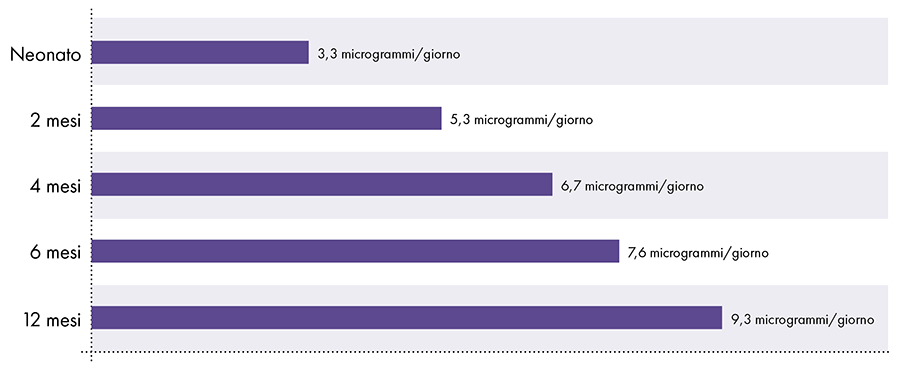 Slika 3: Ta graf prikazuje mejo aluminija za otroke različnih starosti, kot izhaja iz registra strupenih snovi in bolezni, oddelka Ministrstva za zdravje in človeške storitve Združenih držav Amerike. Omejitev kaže, da v krvni obtok ne sme priti več kot 1 mikrogram aluminija na kilogram telesne teže na dan, da bi se izognili nevrotoksičnim učinkom aluminija.
Slika 3: Ta graf prikazuje mejo aluminija za otroke različnih starosti, kot izhaja iz registra strupenih snovi in bolezni, oddelka Ministrstva za zdravje in človeške storitve Združenih držav Amerike. Omejitev kaže, da v krvni obtok ne sme priti več kot 1 mikrogram aluminija na kilogram telesne teže na dan, da bi se izognili nevrotoksičnim učinkom aluminija.
Količina aluminija v cepivih
Reference
- Ameriška akademija za pediatrijo, Odbor za prehrano. Toksičnost aluminija pri dojenčkih in otrocih. pediatrija. 1996 marec 97 (3): 413.
- Agencija za register strupenih snovi in bolezni (ATSDR). Toksikološki profil za aluminij. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Aluminij v hrani - narava in prispevek aditivov za živila. V: El-Samragy Y, urednik. Dodatek za živila. Reka (Hrvaška): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. K razumevanju adjuvantnega delovanja aluminija. Nat Rev Immunol. april 2009, 9 (4): 287.
- Volk VK, Bunney WE. Imunizacija proti davici s tekočim toksoidom in toksoidom, precipitiranim iz alum. Am J Javno zdravje Nations Health. julij 1942, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Aluminijeve soli v cepivih - perspektiva ZDA. Cepivo. 2002 31. maj 20 Suppl 3: S18-22.
- Ameriška uprava za hrano in zdravila. Silver Spring (MD): Ameriška uprava za hrano in zdravila. Cepiva, licencirana za uporabo v Združenih državah; [posodobljeno 2018. februarja 14; citirano 2018. februarja 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Priporočen razpored cepljenja za otroke in mladostnike, stare 18 let ali manj, Združene države, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Ameriška uprava za hrano in zdravila. Silver Spring (MD): Ameriška uprava za hrano in zdravila. SCOGS (Izbrani odbor za snovi GRAS); [citirano 2018. avgusta 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Duhovnik ND. Biološko obnašanje in biološka uporabnost aluminija pri človeku, s posebnim sklicevanjem na študije, ki uporabljajo aluminij-26 kot sledilnik: pregled in posodobitev študije. J Environ Monit. 2004; 6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminij v izdelkih za parenteralno prehrano za otroke: izmerjena v primerjavi z označeno vsebnostjo. J Pediatr Pharmacol Ther. 2011; 16 (2): 92-7.
- Sedman A. Toksičnost aluminija v otroštvu. Pediatr Nephrol. julij 1992, 6 (4): 383-93.
- US Food and Drug Administration, Department of Health and Human Services. Pravila in predpisi. Fed Regist. junij 2003, 68 (100): 34286.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Nacionalni center za zdravstveno statistiko: podatkovna tabela za tabele dolžine za starost in teža za starost; [citirano 2019. aprila 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Nacionalni center za zdravstveno statistiko: podatkovna tabela za tabele dolžine za starost in teža za starost; [citirano 2019. aprila 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Department of Health and Human Services. Revizija zahtev za sestavne materiale. Končno pravilo. Fed Regist. 2011. april 13 76 (71): 20513-8.
- Urad zveznega registra, Državna služba za arhive in evidence, Uprava za splošne službe. Pravila in predpisi. Fed Regist. 1968 Jan; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov z dieto in cepljenjem. Cepivo. 2011, 28. november 29 (51): 9538-43.
- Miller S, Zdravniki za informirano privolitev. Napaka v "Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov z dieto in cepljenjem." V: ResearchGate. Berlin (Nemčija): ResearchGate GmbH; 2020. marec 6 [citirano 2020. marca 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Zdravniki za informirano privolitev. Newport Beach (CA): Zdravniki za informirano privolitev. Erratum v „Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov s prehrano in cepljenjem“; [citirano 2020. marca 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorpcija in vivo adjuvansov za cepivo, ki vsebujejo aluminij, z uporabo 26Al. Cepivo 1997 avgust-september, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminij test in ocena lokalne reakcije v več časovnih točkah po intramuskularnem dajanju cepiv, ki vsebujejo aluminij, pri opici Cynomolgus. Cepivo. 2005. februar 3 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminij v plazmi in tkivih po intramuskularnem injiciranju humanih cepiv z adjuvansom pri podganah. Arch Toxicol. oktober 2019, 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritična analiza referenčnih študij o toksikokinetiki adjuvansov na osnovi aluminija. J Inorg Biochem. april 2018; 181: 87-95.
Članek prevedel Zdravniki za obveščanje
Po podatkih ameriškega CDC težave, ki se lahko pojavijo po cepljenju s 13-valentnim pnevmokoknim konjugiranim cepivom (PCV13), 23-valentnim pnevmokoknim polisaharidnim cepivom (PPSV23) in drugimi cepivi, vključujejo:(1-2)
- Hude alergijske reakcije, ki se pojavijo v nekaj minutah ali urah po cepljenju.
- Huda bolečina v rami, ki omejuje gibe roke, v kateri je potekalo dajanje.
- Omedlevica ali kolaps po cepljenju. Morda vam svetujemo, da ostanete sedeči ali ležeči približno 15 minut po cepljenju, da preprečite omedlevico in poškodbe, ki bi lahko nastale zaradi padca. Pomembno je, da obvestite svojega zdravnika, če po cepljenju čutite zvonjenje v ušesih, spremembe vida ali omotico.
Neželeni učinki cepiva PCV13 (konjugirano pnevmokokno cepivo)
Neželeni učinki po dajanju PCV13 se razlikujejo glede na odmerek serije in starost prejemnika. Pri otrocih so bile najpogosteje opisane reakcije razdražljivost, zaspanost, izguba apetita, rdečina, bolečina ali oteklina na mestu cepljenja ter blaga ali zmerna vročina.
Otroci, ki so prejeli PCV13 hkrati z inaktiviranim cepivom proti gripi, so imeli večje tveganje za febrilne napade.
Pri odraslih so poročali o rdečini, oteklini in bolečini na mestu injiciranja, utrujenosti, zvišani telesni temperaturi, mrzlici, glavobolu in bolečinah v mišicah.(3)
Neželeni učinki zdravila Prevenar 13 (PCV13), o katerih so poročali pri dojenčkih in otrocih med kliničnimi preskušanji pred odobritvijo:(4) bolečina na mestu injiciranja, oteklina, rdečina, zvišana telesna temperatura, zmanjšan apetit, povečan in zmanjšan spanec, razdražljivost, driska, bruhanje, izpuščaj, koprivnica, preobčutljivostna reakcija, vključno z bronhospazmom, oteklostjo obraza in težko dihanje, epileptični napadi, pljučnica, gastroenteritis, bronhiolitis, smrt (prijavljen kot SIDS).
Neželeni učinki zdravila Prevenar 13 (PCV13), o katerih so poročali pri odraslih med kliničnimi preskušanji pred odobritvijo:(5) bolečina, oteklina in rdečina na mestu injiciranja, omejitev gibanja roke, zvišana telesna temperatura, bruhanje, mrzlica, bolečine v mišicah, utrujenost, glavobol, zmanjšan apetit, izpuščaj, bolečine v sklepih, smrt (smrtni primeri, o katerih so poročali v odobritvi predkliničnih študij, so vključevali smrti zaradi raka bolezni srca, peritonitis, okužba pljuč z Mycobacterium avium complex in septični šok).
Neželeni učinki zdravila Prevenar 13 (PCV13), o katerih so poročali v obdobju trženja:(6) Cianoza, limfadenopatija na mestu injiciranja, anafilaksija, šok, hipotonija, bledica, apneja, angionevrotični edem, multiformni eritem, pruritus na mestu injiciranja, urtikarija in izpuščaj.
Klinična preskušanja pred odobritvijo prvega konjugiranega pnevmokoknega cepiva Prevenar (PCV7), je primerjal varnost Prevenarja (PCV7) z eksperimentalnim cepivom proti meningitisu C, kar je resno ogrozilo znanstveno veljavnost preskušanja.
V kliničnih preskušanjih pred odobritvijo zdravila Prevenar (PCV7) so otroci v skupinah, ki so prejele pnevmokokno cepivo, pogosteje trpeli zaradi krčev, razdražljivosti, visoke vročine in drugih reakcij. V skupini s Prevenarjem (PCV7) je bilo 12 smrti, vključno s 5 smrtnimi primeri zaradi sindroma nenadne smrti dojenčka (SIDS). Dokončane niso bile nobene dolgoročne študije, ki bi ocenile, ali je cepivo Prevenar (PCV7), dano samostojno ali v kombinaciji z drugimi cepivi, povezano s kroničnimi boleznimi ali invalidnostmi, kot je razvoj sladkorne bolezni, astme, napadov, težav pri učenju. , ADHD.(7)
Klinična varnostna preskušanja Prevenar 13 (PCV13) pred odobritvijo so primerjala to cepivo naslednje generacije z originalnim cepivom Prevenar (PCV7), cepivom, ki ni bilo ustrezno raziskano glede varnosti, in leta 2012 so poročali o pomislekih glede povezave med febrilnimi krči in Prevenar 13 (PCV13).(8-9)
PCV13 je bil povezan s povečanim tveganjem za febrilne napade, če so ga dajali samostojno(10) in kadar so ga dajali v kombinaciji s parenteralnim inaktiviranim cepivom proti gripi (IIV).(11)
Nekatere študije so cepivo PCV povezale tudi z Guillain-Barrejevim sindromom,(12) do poliserozitisa,(13) do septične rame(14) in multiformni eritem.(15)
Neželeni učinki cepiva PPSV23 (Pnevmokokni polisaharid)
Po podatkih CDC približno 50 % ljudi, ki prejmejo pnevmokokno polisaharidno cepivo (PPSV23), občuti bolečino in rdečico na mestu injiciranja. Po dajanju PPSV23 se lahko pojavijo tudi bolečine v mišicah, zvišana telesna temperatura in hujše lokalne reakcije.(16)
Neželeni učinki PNEUMOVAX23 (PPSV23), o katerih so poročali pri odraslih med kliničnimi preskušanji v ZDA pred odobritvijo:(17) bolečina na mestu injiciranja, rdečina, srbenje, podplutbe in otekline, glavobol, mrzlica, zvišana telesna temperatura, driska, dispepsija, slabost, okužba zgornjih dihalnih poti, bolečine v hrbtu, bolečine v vratu, faringitis, bolečine v mišicah, utrujenost, depresija, ulcerozni kolitis, bolečine v prsih, angina pektoris, srčno popuščanje, tremor, okorelost, znojenje, možganska kap, ledvena radikulopatija, pankreatitis, miokardni infarkt, smrt.
Skoraj 80 % preiskovancev, ki so sodelovali v kliničnih preskušanjih pred odobritvijo, je imelo neželene reakcije na mestu injiciranja po ponovnem cepljenju tri do pet let po prvem cepivu. Tudi stopnja sistemskih neželenih učinkov (glavobol, utrujenost, mialgija) po ponovnem cepljenju s PPSV23 je bila višja, saj je o neželenem učinku poročalo 33 % odraslih, starih 65 let in več, in 37,5 % odraslih, starih med 50 in 64 let.(18)
Neželeni učinki PNEUMOVAX23 (PPSV23), o katerih so poročali v obdobju trženja:(19) Pri bolnikih z stabilizirana idiopatska trombocitopenična purpura, hemolitična anemija pri bolnikih, ki so imeli druge hematološke bolezni, parestezija, Guillain-Barréjev sindrom, radikulonevropatija, febrilni krči, izpuščaj, multiformni eritem, urtikarija, celulitisu podobne reakcije.
Čeprav je PNEUMOVAX23 (PPSV23) odobren za uporabo pri otrocih, starih dve leti in več, s stanji, kot so kronične bolezni srca in pljuč, sladkorna bolezen, polževi vsadki, uhajanje cerebrospinalne tekočine, anemija srpastih celic, funkcionalna ali anatomska asplenija in imunosupresija, obstaja v navodilu za uporabo cepiva ni informacij o varnosti ali učinkovitosti cepiva pri otrocih.(20)
Nekatere študije so povezale PPSV23 s sistemskimi vnetnimi reakcijami(21) e febbre.(22-23-24-25-26)
Reference (kliknite za odpiranje)
- CDC Pnevmokokni konjugat (PCV13) VIS. 5. november 2015
- CDC Pnevmokokni polisaharid VIS. 24. april 2015
- CDC Pnevmokokni konjugat (PCV13) VIS. 5. november 2015
- FDA Prevnar 13 Vložek za paket Avgust 22, 2017
- Ibid
- Ibid
- FDA Pnevmokokno 7-valentno konjugirano cepivo (PREVNAR) – vložek proizvajalca izdelka. Oktober 1, 2002
- Hitt, E Prevnar 13 je treba paziti na tveganje za febrilne napade, pravi odbor FDA. Medscape. Jan 31, 2012
- Tse A, Tseng HF, Greene SK, et al. Identifikacija signala in ocena tveganja za febrilne napade pri otrocih po trivalentnem inaktiviranem cepivu proti gripi v projektu Vaccine Safety Datalink, 2010-2011. Cepivo. 2012, 2. marec; 30 (11): 2024-31
- Baker M, Jankosky C, Yih K, et al. Tveganje za vročinske napade po cepljenju proti gripi in 13-valentnim pnevmokoknim konjugiranim cepivom. Odprite forum Infect Dis. 2017 Jesen; 4 (dodatek 1): S464–S465.
- CDC Otroška cepiva in vročinski napadi Junij 20, 2016
- Ravišankar, N Guillain-Barrejev sindrom po cepivu PCV. J Neurol Neurosurg 4 (1): 134
- Tawfik P, Elie Gertner E, McEvoy CE Hud poliserozitis, povzročen s 13-valentnim konjugiranim pnevmokoknim cepivom: prikaz primera J Med Case Rep. 2017; 11: 142.
- DeRogatis MJ, Parameswaran L, Lee P, et al. Septični ramenski sklep po cepljenju proti pnevmokokom, ki zahteva kirurško debridement. HSS J. 2018 Oct;14(3):299-301
- Monastirli A, Pasmatzi E, Badavanis G et al. Multiformni eritem po cepljenju proti pnevmokokom. Acta Dermatovenerol Alp Pannonica Adriat. 2017 Mar;26(1):25-26.
- CDC Pnevmokokni polisaharid VIS. 24. april 2015
- FDA Pneumovax 23 - Pnevmokokno cepivo, polivalentno. Vložek paketa December 30, 2014
- Ibid
- Ibid
- Ibid
- von Elten, KA, Duran LL, Banks TA, et al. Sistemska vnetna reakcija po pnevmokoknem cepivu Serija primerov Hum cepivo še eno. 2014. junij 1; 10 (6): 1767–1770.
- Huang DT, Chiu NC, Chi H, et al. Dolgotrajna vročina s celulitisu podobno reakcijo pri otrocih, cepljenih s pnevmokoknimi polisaharidi. Pediatr Infect Dis J. 2008 Oct;27(10):937-9.
- Yousef E, Mannan S. Sistemska reakcija na pnevmokokno cepivo: kako pogosta pri pediatriji? Alergijska astma Proc. 2008 Jul-Aug;29(4):397-9
- Gabor EP, Seeman M. Akutna febrilna sistemska reakcija na polivalentno pnevmokokno cepivo. JAMA. 1979 Nov 16;242(20):2208-9.
- Hasan S, Yousef M, Shridharani S Huda febrilna sistemska reakcija na pnevmokokno cepivo. J Natl Med izr. februar 2005; 97(2): 284–285.
- Lee A, Goyal R, Shan HY. Huda dolgotrajna vročina po cepljenju s pnevmokoki. Am J Med Sci. 2006 Dec;332(6):351-3.
Ta članek je povzel in prevedel National Vaccine Information Center.

