Ali lahko cepivo proti tetanusu povzroči poškodbe in/ali smrt?

Naslednji članek poskuša osvetliti obsežen svet neželenih učinkov s posebnim pogledom na tistega proti tetanusu, vendar vas pozivamo, da preberete vsa spodaj navedena poudarka, da boste razumeli druga povezana vprašanja, kot je problem več cepiv. , preobčutljivost za eno ali več spojin cepiva, problem SIDS in adjuvansov. Večina cepiv na trgu se proizvaja v komercialne namene v pogosto različnih oblikah, zaradi česar je tema škode zaradi cepiva veliko širša.
Problem večkratnih cepiv (kliknite za odpiranje)
Problem večkratnih cepiv

Trenutni koledarji cepljenja, zlasti za pediatrično starost, predvidevajo dajanje več antigenov in cepiv v eni seji, kar daje prednost udobju na račun varnosti. Da bi lahko posebej govorili o varnosti cepiv, moramo nujno upoštevati kompleksnost pojava, pri čemer vsem bralcem svetujemo, naj se ustrezno informirajo o vseh vidikih cepljenja, o prednostih in slabostih.
Dr. Russell Blaylock, klinični asistent profesor nevrokirurgije na Medicinskem centru Univerze Mississippi, je leta preučeval "strupeno sinergijo" in lahko opazil, da ko dva šibko toksična pesticida, pri čemer nobeden ne more povzročiti Parkinsonovega sindroma pri poskusnih živalih, se med seboj kombinirajo, lahko celo hitro povzročijo bolezen in ta pojav primerja s pojavom več cepiv, ki se dajejo hkrati: "Cepljenja, če jih je preveč in so preblizu skupaj, se obnašajo kot kronična bolezen".(A). Drugo Dve študiji sta potrdili, da lahko pride do nenadne smrti dojenčka po inokulaciji več cepiv v enem dajanju.(bc)
Študija, objavljena v Human and Experimental Toxicology, je pokazala, da imajo države, ki otrokom predpisujejo več cepiv, običajno višje stopnje umrljivosti dojenčkov.(D) Na primer, v ZDA, kjer otroci prejmejo 26 cepiv, umre več kot 6 otrok na 1000 živorojenih otrok, medtem ko na Švedskem in Japonskem, kjer se daje 12 pediatričnih cepiv, poročajo o 3 smrtih na vsakih 1000 živorojenih otrok. V omenjeni študiji je obravnavana tudi povezava med cepivi in SIDS-om.
Iz švicarske študije, objavljene leta 2005 v European Journal of Pediatrics(E) iz tega izhaja, da je glede na učinke na nedonošenčke incidenca ponavljajoče se ali povečane apneje in bradikardije po dajanju šestvalentnih cepiv 13 %. Istega leta je ista revija objavila nemško študijo, ki je preučevala nenadne smrti dojenčkov po heksavalentnem. Avtorji pišejo: »Ti rezultati, ki temeljijo na spontanih poročilih, ne dokazujejo vzročne povezave med cepljenjem in nenadno smrtjo dojenčka, ampak predstavljajo signal glede enega od dveh razpoložljivih heksavalentov; znak, ki bi moral voditi k intenzivnejšemu nadzoru nenadnih smrti dojenčkov po cepljenju".(F)
Leta 2006 je bil objavljen v medicinski reviji Vaccine(G) pismo skupine raziskovalcev z Univerze v Münchnu, ki je poročalo o "šestih primerih nenadne smrti dojenčkov po heksavalentnem cepljenju. Vsi so bili najdeni mrtvi brez pojasnila 1-2 dni po cepljenju". Uvrščeni so bili med tipične primere nenadne smrti dojenčka, vendar je avtoptična verifikacija razkrila nevropatološke in histološke nepravilnosti in vsi otroci so pokazali znaten možganski edem, zaradi česar so bili izjema v primerjavi z drugimi primeri SIDS (Sindrom nenadne smrti dojenčka). Raziskovalci so zapisali, da smo pred uvedbo šestvalentnega cepiva (v letih 1994–2000) opazili le enega od 198 otrok z nenadno smrtjo dojenčka, ki je umrl kmalu po cepljenju z DTP. Toda med letoma 2001 in 2004 so identificirali pet podobnih primerov od 74 s SIDS. To bi pomenilo trinajstkratno povečanje."
Tudi leta 2006 na Virchows Archive(H), je ekipa z Inštituta za patologijo Univerze v Milanu zapisala: »Strokovnjaki Evropske agencije za vrednotenje medicinskih izdelkov so analizirali možnost, da obstaja povezava med šestvalentnimi cepivi in nekaterimi smrtnimi primeri. Med udeleženci so bili patologi z izkušnjami s cepivi in sindromom nenadne smrti dojenčka, ki so izvajali obdukcije.Toda, kolikor vemo, je bilo malo pozornosti posvečeno pregledu možganskega debla in krvnega srca na serijskih odsekih in ni bilo možnosti ugotoviti vloge sprožilca. cepiva za te smrti. Tukaj poročamo o primeru 3-mesečne punčke, ki je nenadoma umrla po šestvalentnem cepljenju. Pregled možganskega debla na serijskih rezih je pokazal dvostransko hipoplazijo arkuatnega jedra. Prevodni sistem srca je imel vztrajno fetalno disperzijo in degeneracijo. Ta primer ponuja edinstveno razumevanje možne vloge šestvalentnega cepiva pri sprožitvi smrtonosnih posledic pri ranljivem otroku. Vsak primer nenadne in nepričakovane smrti, ki se pojavi kmalu po rojstvu ali v zgodnjem otroštvu, še posebej, če sledi cepljenju, je treba v skladu s smernicami vedno opraviti popolno obdukcijo.
Reference
- Blaylock R, "Vaccinations: the hidden dangers", The Blaylock Wellness Report, maj 2004, str. 1-9
- Ottaviani G. et al., "Sindrom nenadne smrti dojenčka (SIDS) kmalu po heksavalentnem cepljenju: druga patologija pri sumu na SIDS?", Virchows Arhiv, 2006, 448, str. 100-104.
- Zinka B. et al., "Nepojasnjeni primeri nenadne smrti dojenčka kmalu po heksavalentnem cepljenju", Vaccine, julij 2006, 24 (31-32), str. 5779-5780.
- Miller NZ et al1. , "Stopnje umrljivosti dojenčkov so nazadovale glede na število rutinsko danih odmerkov cepiva: ali obstaja biokemična ali sinergistična toksičnost?", Hum. Exp. Toxicol., maj 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Problem aluminija (kliknite za odpiranje)
Aluminij v cepivih: kaj morajo vedeti starši

1. Kaj je aluminij?
Aluminij je srebrno bela lahka kovina, temprana in odporna. Zaradi teh lastnosti je uporaben v številnih panogah in izdelkih, vključno s stroji, gradbeništvom, skladišči, kuhinjsko posodo, kuhinjskimi pripomočki, tekstilom, barvili in kozmetiko. Aluminij je tudi najbolj razširjena kovina v zemeljski skorji in skoraj ves aluminij v okolju se nahaja v tleh. Vendar se aluminij naravno ne nahaja v znatnih količinah v živih organizmih (kot so rastline in živali) in nima znane biološke funkcije. V zadnjem stoletju je uporaba aluminija v nekaterih izdelkih povzročila povečano izpostavljenost ljudi. Glavni viri izpostavljenosti so živila, ki vsebujejo aluminij (npr. pecilni prašek, predelana hrana, otroške formule itd.), medicinski izdelki (npr. antiperspiranti, antacidi itd.), injekcije proti alergijam in cepiva.1-3
2. Zakaj je aluminij prisoten v cepivih?
Nekatera cepiva uporabljajo aluminijeve spojine (aluminijev hidroksid in aluminijev fosfat) kot pomožne snovi, ki so sestavine, ki povečajo imunski odziv na antigen (tujko).4-5 Ameriška uprava za hrano in zdravila (FDA) pravi, da bi se lahko imunski odziv, ki ga sprožijo, zmanjšal, če nekatera cepiva ne bi vključevala aluminija.6
3. Katera cepiva vsebujejo aluminij?
Naslednja cepiva vsebujejo aluminij in se dajejo dojenčkom, otrokom in mladostnikom (slika 1):
- Hepatitis B (HepB)
- šestvalentnega
- Davica, tetanus in oslovski kašelj (DTaP in Tdap)
- Haemophilus influenzae tipa b (PedvaxHIB)
- Pnevmokok (PCV)
- Hepatitis A (HepA)
- Humani papiloma virus (HPV)
- Meningokok B (MenB)
Slika 1: Od rojstva do 18 let se da do 22 odmerkov cepiv, ki vsebujejo aluminij7-8
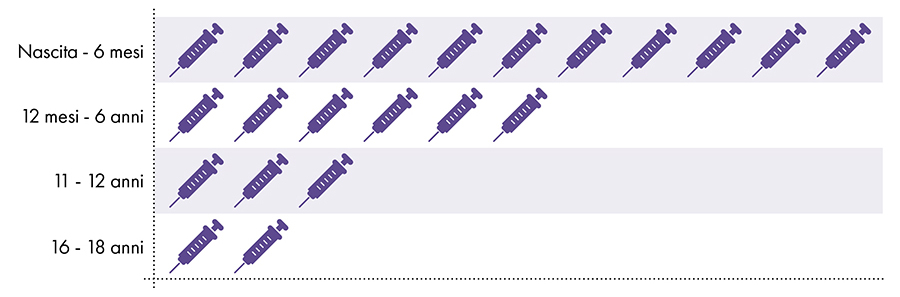
4. Ali je izpostavljenost aluminiju varna?
FDA že od leta 1975 meni, da je aluminij splošno priznan kot varen (GRAS).9 Vendar pred letom 1990 ni bilo tehnologije za natančno odkrivanje majhnih količin aluminija, ki so jih dajali subjektom v znanstvenih študijah.10 Posledično je bila količina aluminija, ki bi jo lahko absorbirala pred pojavom škodljivih učinkov, neznana.
Od devetdesetih let prejšnjega stoletja so zaradi tehnološkega napredka opazili, da majhne količine aluminija, ki ostanejo v človeškem telesu, ovirajo številne celične in presnovne procese v živčnem sistemu in tkivih drugih delov telesa.1-10-11 Največje negativne učinke aluminija so opazili v živčnem sistemu in segajo od motenj motoričnih sposobnosti do encefalopatije (spremenjeno duševno stanje, osebnostne spremembe, težave z razmišljanjem, izguba spomina, napadi, koma in drugo).2-12
Ministrstvo za zdravje in človeške storitve Združenih držav Amerike (HHS) priznava aluminij kot znan nevrotoksin.2 Poleg tega je FDA opozorila na tveganja zastrupitve z aluminijem pri dojenčkih in otrocih.13
FEDERAL REGISTER: Dnevni časopis vlade Združenih držav"Tudi donošeni dojenčki z normalnim delovanjem ledvic so lahko ogroženi zaradi hitre rasti in nezrelosti možganov in okostja ter nezrelosti krvno-možganske pregrade. Do 1. ali 2. leta imajo dojenčki nižje Stopnja glomerulne filtracije kot pri odraslih, kar vpliva na njihovo delovanje ledvic. Agencija se boji, da so majhni otroci in tisti z nezrelim delovanjem ledvic izpostavljeni povečanemu tveganju izpostavljenosti aluminiju." |
5. Koliko oralnega aluminija ni varno?
Leta 2008 je Agencija za register strupenih snovi in bolezni (ATSDR), oddelek HHS, uporabila študije o nevrotoksičnih učinkih aluminija, da bi ugotovila, da ne več kot 1 miligram (1.000 mikrogramov) aluminija na kilogram telesne teže na dan izogibajte se negativnim učinkom aluminija.2
6. Koliko aluminija vbrizganega ni varno?
Za določitev količine aluminija, ki jo je mogoče varno vbrizgati, je treba pretvoriti oralno mejo aluminija v ATSDR. Meja ATSDR za peroralni aluminij (1.000 mikrogramov aluminija na kilogram telesne teže na dan) temelji na 0,1 % peroralnega aluminija, ki se absorbira v krvni obtok, saj prebavni trakt blokira skoraj ves peroralni aluminij.2 Nasprotno pa aluminij, injiciran intramuskularno, obide prebavni trakt in 100 % aluminija se lahko sčasoma absorbira v krvni obtok (tj. delež absorbiranega aluminija je 1.000-krat večji). Da bi upoštevali te različne količine absorpcije, je treba oralno mejo aluminija ATSDR deliti s 1000. Ta pretvorba vodi do mejne vrednosti aluminija v krvi, ki izhaja iz ATSDR, 1 mikrogram aluminija (0,1 % od 1.000 mikrogramov) na kilogram telesne teže na dan. Posledično, da bi se izognili nevrotoksičnim učinkom aluminija, ne sme priti v krvni obtok več kot 1 mikrogram aluminija na kilogram telesne teže na dan. Slika 3 prikazuje mejo aluminija v krvi, ki izhaja iz ATSDR, za dojenčke različnih starosti glede na njihovo težo.
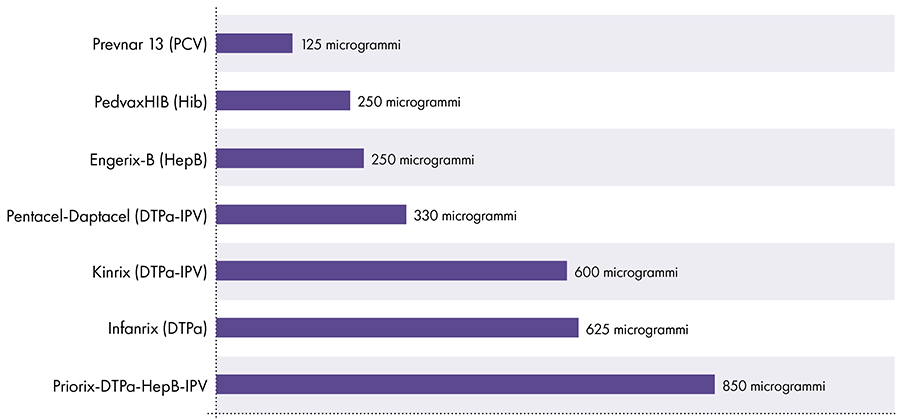
7. Koliko aluminija je v cepivih?
Količina aluminija v cepivih je različna.16 Leta 1968 je ameriška zvezna vlada postavila mejo za količino aluminija v cepivih na 850 mikrogramov na odmerek, ki temelji na količini aluminija, ki je potrebna za učinkovitost nekaterih cepiv.6-17 Posledično se količina aluminija v cepivih za dojenčke, ki vsebujejo aluminij, giblje od 125 do 850 mikrogramov na odmerek. Slika 4 prikazuje vsebnost aluminija v enem odmerku različnih cepiv, danih otrokom.
8. Ali so kakšne študije primerjale količino aluminija v cepivih z mejo, ki izhaja iz Agencije za toksične snovi in register bolezni (ATSDR)?
Leta 2011 je bila objavljena študija, katere namen je primerjati količino aluminija v cepivih z mejo pretoka krvi, ki jo je določil ATSDR.18 Vendar pa je ta študija napačno utemeljila svoje izračune na 0,78 % peroralnega aluminija, ki se absorbira v krvni obtok, namesto na 0,1 % vrednosti, ki jo je ATSDR uporabil v svojih izračunih.19-20 Posledično je študija iz leta 2011 domnevala, da lahko skoraj 8-krat (0,78 % / 0,1 %) aluminij varno vstopi v krvni obtok, kar je pripeljalo do napačnega zaključka.
9. Ali je izpostavljenost aluminiju zaradi cepiv varna?
Cepiva se injicirajo intramuskularno in hitrost, s katero aluminij iz cepiv migrira iz človeških mišic v krvni obtok, ni znana. Študije na živalih kažejo, da lahko aluminij iz cepiv zaradi več spremenljivk vstopi v krvni obtok od nekaj mesecev do več kot enega leta.21-23 Ker kumulativna izpostavljenost aluminiju s cepivi pri otrocih, mlajših od enega leta, presega dnevno mejo, ki jo določa ATSDR, za nekaj sto (sliki 3 in 4), bi bila meja še vedno presežena, če bi aluminij iz cepiv vstopil v krvni obtok med približno eno leto. Poleg tega so študije pokazale, da aluminij iz cepiv absorbirajo imunske celice in doseže dele telesa, ki so daleč od mesta injiciranja, vključno z možgani.24
Obseg škodljivih učinkov aluminija v cepivih ni znan, saj varnostne študije, ki bi primerjale populacijo, cepljeno s cepivi, ki vsebujejo aluminij, s populacijo, ki ni bila cepljena s takšnimi cepivi, niso bile izvedene.
Aluminijasta omejitev krvnega pretoka, ki izhaja iz ATSDR2-14-15
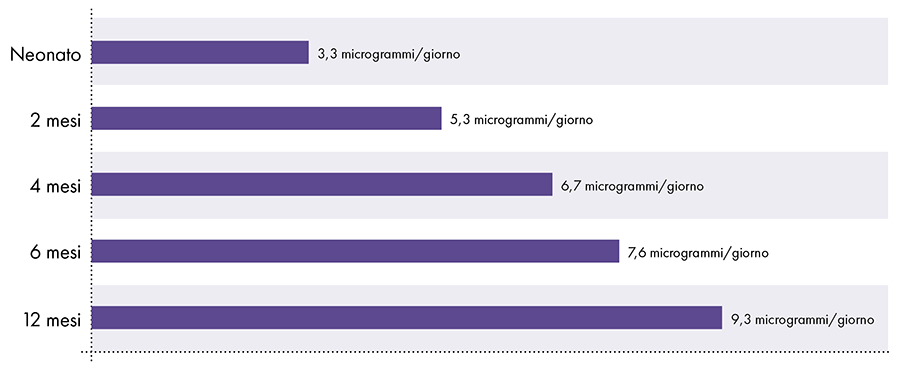 Slika 3: Ta graf prikazuje mejo aluminija za otroke različnih starosti, kot izhaja iz registra strupenih snovi in bolezni, oddelka Ministrstva za zdravje in človeške storitve Združenih držav Amerike. Omejitev kaže, da v krvni obtok ne sme priti več kot 1 mikrogram aluminija na kilogram telesne teže na dan, da bi se izognili nevrotoksičnim učinkom aluminija.
Slika 3: Ta graf prikazuje mejo aluminija za otroke različnih starosti, kot izhaja iz registra strupenih snovi in bolezni, oddelka Ministrstva za zdravje in človeške storitve Združenih držav Amerike. Omejitev kaže, da v krvni obtok ne sme priti več kot 1 mikrogram aluminija na kilogram telesne teže na dan, da bi se izognili nevrotoksičnim učinkom aluminija.
Količina aluminija v cepivih
Reference
- Ameriška akademija za pediatrijo, Odbor za prehrano. Toksičnost aluminija pri dojenčkih in otrocih. pediatrija. 1996 marec 97 (3): 413.
- Agencija za register strupenih snovi in bolezni (ATSDR). Toksikološki profil za aluminij. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Aluminij v hrani - narava in prispevek aditivov za živila. V: El-Samragy Y, urednik. Dodatek za živila. Reka (Hrvaška): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. K razumevanju adjuvantnega delovanja aluminija. Nat Rev Immunol. april 2009, 9 (4): 287.
- Volk VK, Bunney WE. Imunizacija proti davici s tekočim toksoidom in toksoidom, precipitiranim iz alum. Am J Javno zdravje Nations Health. julij 1942, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Aluminijeve soli v cepivih - perspektiva ZDA. Cepivo. 2002 31. maj 20 Suppl 3: S18-22.
- Ameriška uprava za hrano in zdravila. Silver Spring (MD): Ameriška uprava za hrano in zdravila. Cepiva, licencirana za uporabo v Združenih državah; [posodobljeno 2018. februarja 14; citirano 2018. februarja 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Priporočen razpored cepljenja za otroke in mladostnike, stare 18 let ali manj, Združene države, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Ameriška uprava za hrano in zdravila. Silver Spring (MD): Ameriška uprava za hrano in zdravila. SCOGS (Izbrani odbor za snovi GRAS); [citirano 2018. avgusta 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Duhovnik ND. Biološko obnašanje in biološka uporabnost aluminija pri človeku, s posebnim sklicevanjem na študije, ki uporabljajo aluminij-26 kot sledilnik: pregled in posodobitev študije. J Environ Monit. 2004; 6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminij v izdelkih za parenteralno prehrano za otroke: izmerjena v primerjavi z označeno vsebnostjo. J Pediatr Pharmacol Ther. 2011; 16 (2): 92-7.
- Sedman A. Toksičnost aluminija v otroštvu. Pediatr Nephrol. julij 1992, 6 (4): 383-93.
- US Food and Drug Administration, Department of Health and Human Services. Pravila in predpisi. Fed Regist. junij 2003, 68 (100): 34286.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Nacionalni center za zdravstveno statistiko: podatkovna tabela za tabele dolžine za starost in teža za starost; [citirano 2019. aprila 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centri za nadzor in preprečevanje bolezni. Washington, DC: Ministrstvo za zdravje in človeške storitve ZDA. Nacionalni center za zdravstveno statistiko: podatkovna tabela za tabele dolžine za starost in teža za starost; [citirano 2019. aprila 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Department of Health and Human Services. Revizija zahtev za sestavne materiale. Končno pravilo. Fed Regist. 2011. april 13 76 (71): 20513-8.
- Urad zveznega registra, Državna služba za arhive in evidence, Uprava za splošne službe. Pravila in predpisi. Fed Regist. 1968 Jan; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov z dieto in cepljenjem. Cepivo. 2011, 28. november 29 (51): 9538-43.
- Miller S, Zdravniki za informirano privolitev. Napaka v "Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov z dieto in cepljenjem." V: ResearchGate. Berlin (Nemčija): ResearchGate GmbH; 2020. marec 6 [citirano 2020. marca 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Zdravniki za informirano privolitev. Newport Beach (CA): Zdravniki za informirano privolitev. Erratum v „Posodobljena farmakokinetika aluminija po izpostavljenosti dojenčkov s prehrano in cepljenjem“; [citirano 2020. marca 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorpcija in vivo adjuvansov za cepivo, ki vsebujejo aluminij, z uporabo 26Al. Cepivo 1997 avgust-september, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminij test in ocena lokalne reakcije v več časovnih točkah po intramuskularnem dajanju cepiv, ki vsebujejo aluminij, pri opici Cynomolgus. Cepivo. 2005. februar 3 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminij v plazmi in tkivih po intramuskularnem injiciranju humanih cepiv z adjuvansom pri podganah. Arch Toxicol. oktober 2019, 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritična analiza referenčnih študij o toksikokinetiki adjuvansov na osnovi aluminija. J Inorg Biochem. april 2018; 181: 87-95.
Članek prevedel Zdravniki za obveščanje
Številne objavljene študije so poročale o resnih neželenih učinkih po cepljenju s tetanusnim toksoidom. Neželeni učinki vključujejo anafilaksijo,(1-2) brahialni nevritis,(3) bulozni pemfigoid(4-5-6) Guillain-Barrejev sindrom (GBS),(7-8) akutni diseminirani encefalomielitis (ADEM),(9) multiformni eritem,(10-11-12) miokarditis,(13-14-15-16-17) artritis,(18-19) optični nevritis,(20-21) in druge avtoimunske motnje.(22-23)
Neželene učinke, o katerih so poročali po cepljenju proti tetanusu, je zbral nemški avtor(24) in s sistemom spremljanja neželenih dogodkov po cepljenju(25) in jih lahko razdelimo v dve skupini: lokalne stranske učinke in sistemske stranske učinke.
Lahko rečemo, da so ti učinki odvisni od različnih dejavnikov:
- starost prejemnika cepiva;
- fiziološka in patološka stanja prejemnika cepiva;
- število prejetih odmerkov cepiva;
- količina danega tetanusnega toksina;
- prisotnost drugih bakterijskih in/ali virusnih antigenov, povezanih s tetanusnim toksinom;
- prisotnost pomožnih sredstev ali drugih povezanih strupenih snovi.
Domneva se, da so neželeni učinki, ki jih povzroči prvo dajanje cepiva proti tetanusu, primerljivi s tistimi, ki se lahko pojavijo pri poživitvenih odmerkih, in če jih dajemo prepogosto, povzročijo stanje hiperimunizacije, ki znatno poveča tveganje za poškodbe cepiva, zato številne študije znanstveniki priporočajo, da poživitvenega cepiva tega cepiva ne dajete v presledkih, krajših od 10 let.(26) K temu je dodano, da je pediatrični tetanusni anatoksin, ki ga vsebujejo kombinirana cepiva, večji od tistega, ki se uporablja za odrasle, ker je zaradi imunske nezrelosti potrebno prekomerno stimulirati novorojenčka, da se doseže ustrezen odziv protiteles.
Najpogostejši in običajno blažji in prehodni lokalni stranski učinki cepljenja proti tetanusu(32) nastanejo zaradi posebne preobčutljivosti na tetanusni toksin in so predstavljeni z: bolečino (50-85% primerov), rdečino, zatrdlino in oteklino (25-30% primerov) tudi do abscesa.(27) V nekaterih primerih so bile lokalne reakcije še posebej resne, kot je Lyellov sindrom (ali sindrom opečene kože), pri katerem je stopnja umrljivosti 50 % pri odraslih in 25 % pri otrocih.(28)
Vsi lokalni neželeni učinki so pogostejši, če je cepivo aplicirano subkutano kot intramuskularno. Ti učinki se povečujejo z večjo količino inokuliranega tetanusnega toksina(29) in to se zgodi zlasti pri osebah, ki so večkrat in pogosto prejele injekcije cepiva proti tetanusu.(30-27)
Študija iz leta 2017 kaže, da je bila pri otrocih z obsežno oteklino okončin po prejemu četrtega odmerka cepiva proti davici-tetanusu-acelularnemu oslovskemu kašlju ponovitev lokalne reakcije še posebej pogosta po petem odmerku cepiva (78 % cepljenih).(31)
Neželeni učinki se povečajo tudi, če se cepivo proti tetanusu kombinira z drugimi cepivi, namesto da se uporablja samostojno.(32)
Leta 1994 je Inštitut za medicino ZDA (IOM) poročal, da obstajajo prepričljivi znanstveni dokazi za sklep, da lahko cepiva proti tetanusu, DT in Td povzročijo Guillain-Barrejev sindrom (GBS), vključno s smrtjo, brahialnim nevritisom in smrtjo zaradi anafilaksije (šok). ).(33) IOM je tudi priznal, da obstaja individualna dovzetnost za reakcije na cepivo zaradi genetskih, bioloških in okoljskih razlogov, vendar dobavitelji cepiv ne morejo natančno predvideti, kdo bo utrpel zaplete, poškodbe ali smrt, preden bo cepivo dano zaradi cepljenja.(34)
Leta 2017 so raziskovalci iz Gvineje Bissau primerjali stopnjo umrljivosti dojenčkov, cepljenih proti davici, tetanusu in celoceličnemu oslovskemu kašlju (DTP), starih od 3 do 5 mesecev, s tistimi pri dojenčkih, ki še niso bili cepljeni s cepivom DTP. ker so bile stopnje umrljivosti bistveno višje med dojenčki, cepljenimi z DTP, kot med tistimi, ki še niso bili cepljeni. Raziskovalci so tudi ugotovili, da če je bilo oralno cepivo proti otroški paralizi (OPV) dano hkrati s cepivom DTP, se je stopnja umrljivosti zaradi vseh vzrokov zmanjšala, vendar je še vedno ostala znatno višja kot pri necepljenih otrocih.(35)
Pomemben lokalni neželeni učinek, ki ga relativno pogosto opazimo pri odraslih, je nevropatija brahialnega pleksusa,(36) če je cepljenje opravljeno v roki in se pojavi nekaj dni ali tednov po cepljenju(37). Za to nevropatijo so značilne bolečine v mišicah, šibkost in izguba mišic. Poleg nevropatij, lokaliziranih na območju, kjer je bilo cepivo cepljeno, najdemo v literaturi tudi različna druga poročila o lokaliziranih nevropatijah, ki jih povzroča dajanje antitetanusa,(38-39) kot je prizadetost različnih kranialnih živcev(40-41) ali očesnih živcev(42) ali povratni laringealni živec.(43)
Najpogostejši sistemski učinki cepljenja proti tetanusu(32) lahko razdelimo na:
- nespecifični učinki, kot so povišana telesna temperatura, glavobol (ki je precej pogost stranski učinek po cepljenju), mialgije, urtikarija, slabost, bruhanje,(44) astenija, anoreksija, razdražljivost, somnolenca,
- specifične učinke, kot so anafilaktični šok, generalizirane nevropatije, intenzivne bolečine v trebuhu z drisko, različne vnetne oblike, tudi resne, v nekaterih redkih primerih celo smrt.
Med vsemi najpogostejšimi in številnimi sistemskimi učinki najdemo nevrološke okvare(45) med temi pa je vsekakor treba na prvo mesto postaviti polinevropatijo perifernega živčevja, ki je pogostejša od prizadetosti centralnega živčnega sistema in se lahko pojavi tako po prvem odmerku cepiva kot po tretjem.(46) Polinevropatija se običajno pojavi v nekaj minutah do nekaj urah (v primeru akutnih alergijskih reakcij) ali v 12-48 urah (v primeru zapoznelih alergijskih reakcij) ali največ v 4-14 dneh po inokulaciji (v primeru nevritis).(47) Polinevropatija lahko prizadene nekaj živcev ali velikih delov telesa, vse do medule in možganske skorje, povzroči pa jo lahko samo cepivo proti tetanusu.(48) ali zaradi dajanja drugih cepiv v kombinaciji s cepivom proti tetanusu.(36-49)
Med različnimi oblikami polinevropatije so poročali o naslednjih: demielinizirajoča polinevropatija;(50) asimetrična polinevropatija; poliradikuloneuritis s parezo mehurja in danke;(51) skarlatiniformni izpuščaj,(40) akutne urtikarijske reakcije,(44) paraliza dihalnih živcev (Landryjeva paraliza), ki lahko povzroči tudi smrt;(52-53) tetanični krči;(44) transverzalni mielitis;(54) Guillain-Barréjev sindrom;(55-56) periferna motorična afazija;(57) in smrt.(28)
Reference (kliknite za odpiranje)
- Mayorga C, Torres MJ, Corzo JL et al. Takojšnja alergija na cepivo proti tetanusnemu toksoidu: določanje protiteles imunoglobulina E in imunoglobulina G proti alergenim proteinom. Ann Alergija Astma Imunol. 2003 Feb;90(2):238-43.
- Martín-Muñoz MF, Pereira MJ, Posadas S et al. Anafilaktična reakcija na cepivo proti davici in tetanusu pri otroku: specifične določitve IgE/IgG in študije navzkrižne reaktivnosti. Cepivo. 2002 Sep 10;20(27-28):3409-12.
- Hamati-Haddad A, Fenichel GM. Brahialni nevritis po rutinskem cepljenju otrok proti davici, tetanusu in oslovskemu kašlju (DTP): poročilo o dveh primerih in pregled literature. Pediatrija. 1997 Apr;99(4):602-3.
- Fournier B, Descamps V, Bouscarat F et al. Bulozni pemfigoid, povzročen s cepljenjem. Br J Dermatol. 1996 Jul;135(1):153-4.
- Venning VA, Wojnarowska F. Povzročen nasilni pemfigoid. Br J Dermatol. 1995 May;132(5):831-2.
- Sezin T, Egozi E, Hillou W et al. Pemfigoid sluznice proti laminin-332, ki se razvije po cepljenju proti davici in tetanusu. JAMA Dermatol. 2013 Jul;149(7):858-62.
- Bakshi R, Graves MC. Guillain-Barréjev sindrom po kombiniranem cepljenju s toksoidom tetanusa in davice. J Neurol Sci. 1997 Apr 15;147(2):201-2.
- Newton N Jr, Janati A. Guillain-Barréjev sindrom po cepljenju s prečiščenim tetanusnim toksoidom. South Med J. 1987 Aug;80(8):1053-4.
- Hamidon BB, Raymond AA. Akutni diseminirani encefalomielitis (ADEM), ki se kaže z napadi sekundarno po cepljenju proti tetanusnemu toksinu. Med J Malezija. 2003 Dec;58(5):780-2.
- Griffith RD, Miller OF III Multiformni eritem po cepljenju proti davici in tetanusnemu toksoidu. J Am Acad Dermatol. 1988 Oct;19(4):758-9.
- Frederiksen MS, Brenøe E, Trier J. Erythema multiforme minor po cepljenju s pediatričnimi cepivi. Scand J Infect Dis. 2004;36(2):154-5.
- Kaur S, Handa S. Multiformni eritem po cepljenju pri dojenčku. Indijski J Dermatol Venereol Leprol. 2008 May-Jun;74(3):251-3.
- Kumar V, Sidhu N, Roy S, Gaurav K. Miokarditis po cepljenju proti davici, oslovskemu kašlju in tetanusnemu toksoidu pri mladem dojenčku. Ann Pediatr Cardiol. 2018 May-Aug;11(2):224-226
- Yamamoto H, Hashimoto T, Ohta-Ogo K, et al. Primer z biopsijo dokazanega eozinofilnega miokarditisa, povezanega z imunizacijo s tetanusnim toksoidom. Cardiovasc Pathol. 2018 nov - dec;37:54-57
- Wu SJ, Sun S, Li JY et al. Akutni fulminantni miokarditis po cepljenju proti davici, otroški paralizi in tetanusu. Asian Cardiovasc Thorac Ann. 2006 Dec;14(6):e111-2.
- Dilber E, Karagöz T, Aytemir K et al. Akutni miokarditis, povezan s cepljenjem proti tetanusu. Mayo Clin Proc. 2003 Nov;78(11):1431-3.
- Amsel SG, Hanukoglu A, Fried D, Wolyvovics M Miokarditis po trojnem cepljenju. Arch Dis Child. 1986 april; 61 (4): 403–405.
- Jawad AS, Scott DG Imunizacija sproži revmatoidni artritis? Ann Rheum Dis. februar 1989; 48(2):174.
- Kaul A, Adler M, Alokaily F, Jawad A Ponovitev reaktivnega artritisa po obnovitvenem odmerku tetanusnega toksoida Ann Rheum Dis. februar 2002; 61(2):185.
- O'Brien P, Wong RW Optični nevritis po kombiniranem cepljenju proti davici, tetanusu, oslovskemu kašlju in inaktiviranemu poliovirusu: prikaz primera. J Med Case Rep. 2018 Nov 30;12(1):356
- Cabrera-Maqueda JM, Hernández-Clares R, Baidez-Guerrero AE et al. Optični nevritis v nosečnosti po cepljenju Tdap: Poročilo o dveh primerih. Clin Neurol Neurosurg. Septembra 2017; 160: 116-118.
- Ruhrman-Shahar N, Torres-Ruiz J, Rotman-Pikielny P, Levy Y Avtoimunska reakcija po cepljenju proti tetanusu - opis štirih primerov in pregled literature. Immunol Res. 2017 Feb;65(1):157-163.
- Shoenfeld Y, Aron-Maor A. Cepljenje in avtoimunost - "vakcinoza": nevarna zveza? J Avtoimunski. 2000 Feb;14(1):1-10.
- Neželeni učinki zdravil Letno. Zvezek 12. (Elsevier, I988).
- Neželeni učinki zdravil Letno. Zvezek 13. (Elsevier, 1989).
- Adebahr, G. [Smrt zaradi šoka pri prvi preventivni subkutankozni injekciji tetanusnega seruma]. Dtsch. Z. Gesamte Gerichtl. Med 41, 405-8 (1952).
- Neželeni učinki zdravil letno. Zvezek 11. (Elsevier, 1987).
- Frank, K.-H. Todliche Imptkomplikationen (Lyell-Syndrom) nach Tetatoxoid. Dt. Gesundh.wes. 29, 1430-4 (1974).
- Relihan, M. Reakcije na tetanusni toksoid. J. Jr. Med. izr. 62, 430-4 (1969).
- Levine, L., Ipsen, J. & McComb, J. Imunizacija odraslih. Priprava in vrednotenje kombiniranih tekočih toksoidov tetanusa in davice za uporabo pri odraslih. Am. J. Hyg. 73, 20 (1961).
- Zafack, JG et al. Tveganje ponovitve neželenih dogodkov po cepljenju: sistematični pregled. Pediatrija 140, (2017).
- Cody, CL, Baraff, LJ, Cherry, JD, Marcy, SM in Manclark, CR Narava in stopnje neželenih učinkov, povezanih z DTP in DT imunizacijami pri dojenčkih in otrocih. Pediatrics 68, 650-60 (1981).
- Odbor za medicinski inštitut za pregled neželenih učinkov cepiv. Neželeni učinki cepiv: dokazi in vzročnost. (Vrednotenje bioloških mehanizmov za neželene dogodke: povečana občutljivost). Washington DC.: Nacionalna akademija Press. 1994. Poglavje 5 Toksoidi proti davici in tetanusu str 67 - 117
- Odbor za medicinski inštitut za pregled neželenih učinkov cepiv. Neželeni učinki cepiv: dokazi in vzročnost. (Vrednotenje bioloških mehanizmov za neželene dogodke: povečana občutljivost). Washington DC.: Nacionalna akademija Press. 2012
- Mogensen SW, Andersen A, Rodrigues A et al. Uvedba cepiva proti davici, tetanusu in oslovskemu kašlju ter peroralnega cepiva proti otroški paralizi med mlade dojenčke v urbani afriški skupnosti: naravni poskus. EBioMedicina. 2017 mar; 17: 192–198.
- Tsairis, P., Dyck, PJ & Mulder, DW Naravna zgodovina nevropatije brahialnega pleksusa. Poročilo o 99 bolnikih. Arh. Nevro/. 27, I09-17 (1972).
- Blumstein, GI & Kreithen, H. Periferna nevropatija po dajanju tetanusnega toksoida. JAMA 198, I 030-1 (1966)
- Gersbach, P. & Waridel, D. [Paraliza po preprečevanju tetanusa]. Švica. Med. Wochenschr. 106, 150-3 (1976).
- Baust, W., Meyer, D. & Wachsmuth, W. Periferna nevropatija po dajanju tetanusnega toksoida. J. Neuro/. 222, 131-33 (1979).
- Cutter, R. Prizadetost slušnega živca po tetanusnem antitoksinu: prvi prijavljeni primer. J Am Med Ass 106, I006-7 (I 936).
- Wirth, G. Reversibele kochlearisschadigung nach Tetanus-injection. Munch Med Wschr 101, 349-81 (1965).
- Harrer, G., Melnizky, V. & Wendt, H. Akkomodationsparese und Schlucklahmung nach Tetanus-Toxoid-Auffrlschungsimpfung. Wien Med Wochenschr 15, 296-7 (1971)
- Basek, M. Enostransko! paraliza glasilk po dajanju tetanusnega antitoksina (TAT). Laringoskop 68, 805-807 (1958).
- Cunningham, AA Anafilaksija po injiciranju tetanusnega toksoida. Br. Med. J. 2, 522-3 (1940).
- Ridder. Plexuslahmung nach Schutzimpfung mit Tetanusserum. Munch. med. Wsch. 81, 1035 (1934).
- Holliday, PL & Bauer, RB Poliradikuloneuritis, ki je posledica imunizacije s toksoidi tetanusa in davice. Arch Neuro/ 40, 56-57 (1983).
- Ehrengut, W. Reaktionen der Wundstarrkrampfimpfung. Dtsch Med Wochenschr 95, 1799-1800 (1970).
- 1 Woolling, KR & Rushton, JG Serumski nevritis; poročilo o dveh primerih in kratek pregled sindroma. Arch. Neuro/. Psihiatrija 64, 568-73 (1950).
- Martin, GI & Weintraub, MI Brahialni nevritis in paraliza sedmega živca: redka nevarnost cepljenja z DPT. Clin. Pediater. (phila). 12, 506-507 (1973).
- Pollard, JD & Selby, G. Ponavljajoča se nevropatija zaradi tetanusnega toksoida. Poročilo o primeru. J. Neuro/. Sci. 37, 113-125 (1978).
- Neželeni učinki zdravil letno/. Zvezek 09. (Elsevier, 1985).
- Harrfeldt, HP [Smrt po aktivni in pasivni imunizaciji proti tetanusu]. Monatsschr. Unfallheilkd. Versicherungsmed. 66, 36-7 (1963).
- Elsasser, G. Zur Entstehung, Localization und Verhiitung der Serumpolyneuritis. Nervenarzt 15, 280 (1942).
- Whittle, E. & Robertson, NR Transverzalni mielitis po imunizaciji proti davici, tetanusu in otroški paralizi. Br. Med. J. 1, 1450 (1977).
- Neželeni učinki zdravil letno/. Zvezek 14. (Elsevier, 1990).
- Hopf, HC [Guillain-Barréjev sindrom po uporabi tetanusnega toksoida. Anketa in poročilo o primeru]. Aktuelle Neuro/. 7, 195-200 (1980).
- Palfty, G.F. in Merei, T. Brez naslova. Orv. Hetil. 102, 2321 (1961).
Ta članek je povzel in prevedel National Vaccine Information Center.

