Může vakcína proti hepatitidě B způsobit zranění a/nebo smrt?

DŮLEŽITÁ POZNÁMKA: Corvelva vás vyzývá, abyste získali podrobné informace přečtením všech sekcí a odkazů, jakož i produktových letáků a technických listů výrobce, a abyste si promluvili s jedním nebo více důvěryhodnými odborníky, než se rozhodnete očkovat sebe nebo své dítě. Tyto informace slouží pouze pro informační účely a nejsou určeny jako lékařská rada.
Problém více vakcín (kliknutím otevřete)
Problém více vakcín

Současné očkovací kalendáře, zejména pro dětský věk, počítají s podáním více antigenů a vakcín v jednom sezení, což zvýhodňuje komfort na úkor bezpečnosti. Abychom mohli pronést konkrétní projev o bezpečnosti vakcín, musíme nutně vzít v úvahu složitost tohoto fenoménu a doporučit všem čtenářům, aby se dostatečně informovali o všech aspektech očkování, výhodách a nevýhodách.
Dr. Russell Blaylock, klinický asistent profesora neurochirurgie na University of Mississippi Medical Center, léta studoval "toxickou synergii" a byl schopen pozorovat, že když dva slabě toxické pesticidy, kde ani jeden není schopen způsobit Parkinsonův syndrom u pokusných zvířat, se vzájemně kombinují, mohou způsobit onemocnění i rychle a srovnává tento jev s jevem více vakcín podaných současně: "Očkování, pokud je příliš mnoho a příliš blízko u sebe, se chovají jako chronické onemocnění".(). Ostatní Dvě studie potvrdily, že náhlá smrt kojence může nastat po naočkování více vakcín v jednom podání.(před naším letopočtem)
Studie publikovaná v Human and Experimental Toxicology ukázala, že země, které dětem předepisují více vakcín, mívají vyšší kojeneckou úmrtnost.(D) Například ve Spojených státech, kde děti dostávají 26 vakcín, zemře více než 6 dětí na 1000 12 živě narozených dětí, zatímco ve Švédsku a Japonsku, kde je aplikováno 3 dětských vakcín, jsou hlášena 1000 úmrtí na každých XNUMX XNUMX živě narozených dětí. Ve výše uvedené studii je také zvažována souvislost mezi vakcínami a SIDS.
Ze švýcarské studie publikované v roce 2005 v European Journal of Pediatrics(E) z toho vyplývá, že pokud jde o účinky na předčasně narozené děti, je výskyt recidivující nebo zvýšené apnoe a bradykardie po podání hexavalentních vakcín 13 %. Ten samý rok publikoval stejný časopis německou studii, která zkoumala náhlá úmrtí kojenců po šestimocném. Autoři píší: «Tyto výsledky, založené na spontánních zprávách, neprokazují kauzální vztah mezi očkováním a náhlým úmrtím kojence, ale představují signál týkající se jednoho ze dvou dostupných hexavalentů; signál, který by měl vést k intenzivnějšímu sledování náhlých úmrtí kojenců po očkování“.(F)
V roce 2006 byla publikována v lékařském časopise Vaccine(G) dopis od týmu výzkumníků z Mnichovské univerzity, který hlásil „šest případů náhlého úmrtí kojenců po šestimocném očkování. Všechny byly nalezeny mrtvé bez vysvětlení 1-2 dny po očkování“. Byly klasifikovány jako typické případy náhlého úmrtí kojenců, ale autoptické ověření odhalilo neuropatologické a histologické abnormality a všechny děti vykazovaly významný otok mozku, což z nich činilo výjimku ve srovnání s ostatními případy SIDS (Syndrom náhlého úmrtí dětí). Vědci napsali, že „Před zavedením hexavalentní vakcíny (v letech 1994-2000) jsme pozorovali případ pouze jednoho ze 198 dětí s náhlým úmrtím kojence, které zemřelo brzy po očkování proti DTP. V letech 2001 až 2004 však identifikovali pět podobných případů ze 74 se SIDS. To by znamenalo třináctinásobný nárůst.“
Také v roce 2006 na Virchows Archive(H), tým z Ústavu patologie Univerzity v Miláně napsal: «Odborníci z Evropské agentury pro hodnocení léčivých přípravků analyzovali možnost, že by mohla existovat souvislost mezi šestivalentními vakcínami a některými případy úmrtí. Mezi účastníky byli patologové se zkušenostmi s vakcínami a syndromem náhlého úmrtí kojenců, kteří prováděli pitvy. Pokud však víme, vyšetření mozkového kmene a krevního srdce na sériových řezech byla věnována malá pozornost a neexistovala možnost stanovit spouštěcí roli. vakcíny pro tato úmrtí. Zde uvádíme případ 3měsíční holčičky, která náhle zemřela po šestimocném očkování. Vyšetření mozkového kmene na sériových řezech odhalilo oboustrannou hypoplazii nucleus arcuate. Převodní systém srdce měl přetrvávající fetální disperzi a degeneraci. Tento případ nabízí jedinečné pochopení možné role hexavalentní vakcíny při vyvolání smrtelných následků u zranitelného dítěte. Jakýkoli případ náhlé a neočekávané smrti, ke kterému dojde brzy po narození nebo v raném dětství, zejména po očkování, by měl vždy projít úplnou pitvou podle pokynů.
Reference
- Blaylock R, "Očkování: skrytá nebezpečí", The Blaylock Wellness Report, květen 2004, s. 1-9
- Ottaviani G. et al., "Syndrom náhlého úmrtí kojenců (SIDS) krátce po hexavalentní vakcinaci: další patologie při podezření na SIDS?", Vircows Archiv., 2006, 448, pp. 100-104.
- Zinka B. et al., "Nevysvětlené případy náhlé smrti kojenců krátce po hexavalentní vakcinaci", Vaccine, červenec 2006, 24 (31-32), str. 5779-5780.
- Miller NZ a kol. ,“Míra kojenecké úmrtnosti klesla proti počtu dávek vakcíny běžně podávaných: existuje biochemická nebo synergická toxicita??", Hum. Exp. Toxicol., květen 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Problém hliníku (kliknutím otevřete)
Hliník ve vakcínách: co rodiče potřebují vědět

1. Co je hliník?
Hliník je stříbřitě bílý lehký kov, tvárný a odolný. Díky těmto vlastnostem je použitelný v mnoha průmyslových odvětvích a výrobcích, včetně strojů, stavebnictví, skladů, nádobí, kuchyňského náčiní, textilu, barviv a kosmetiky. Hliník je také nejrozšířenějším kovem v zemské kůře a prakticky veškerý hliník v životním prostředí se nachází v půdě. Hliník se však přirozeně nenachází ve významných množstvích v živých organismech (jako jsou rostliny a zvířata) a nemá žádnou známou biologickou funkci. V průběhu minulého století vedlo používání hliníku v některých výrobcích ke zvýšené expozici člověka. Hlavními zdroji expozice jsou potraviny obsahující hliník (např. prášek do pečiva, zpracované potraviny, kojenecká výživa atd.), lékařské produkty (např. antiperspiranty, antacida atd.), injekce proti alergii a vakcíny.1-3
2. Proč je hliník přítomen ve vakcínách?
Některé vakcíny používají jako adjuvans sloučeniny hliníku (hydroxid hlinitý a fosforečnan hlinitý), což jsou složky, které zvyšují imunitní odpověď na antigen (cizí látku).4-5 Americký úřad pro potraviny a léčiva (FDA) říká, že pokud by některé vakcíny neobsahovaly hliník, imunitní odpověď, kterou spouštějí, by se mohla snížit.6
3. Které vakcíny obsahují hliník?
Následující vakcíny obsahují hliník a podávají se kojencům, dětem a dospívajícím (obr. 1):
- Hepatitida B (HepB)
- šestimocný
- Záškrt, tetanus a černý kašel (DTaP a Tdap)
- Haemophilus influenzae typ b (PedvaxHIB)
- Pneumokok (PCV)
- Hepatitida A (HepA)
- Lidský papilomavirus (HPV)
- Meningokok B (MenB)
Obrázek 1: Od narození do 18 let se aplikuje až 22 dávek vakcín obsahujících hliník7-8
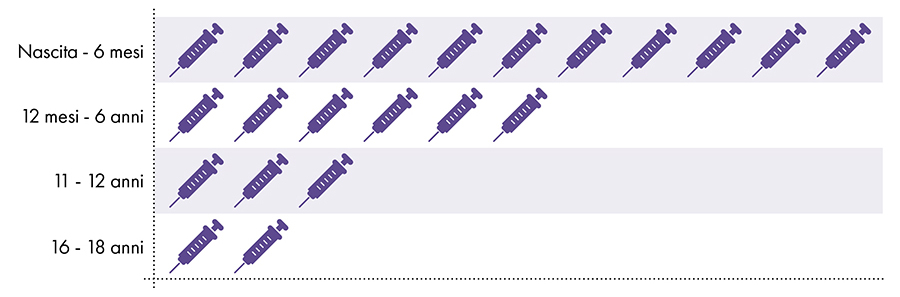
4. Je vystavení hliníku bezpečné?
FDA od roku 1975 považuje hliník obecně za bezpečný (GRAS).9 Před rokem 1990 však neexistovala žádná technologie, která by přesně detekovala malá množství hliníku podávaného subjektům ve vědeckých studiích.10 V důsledku toho nebylo známo množství hliníku, které by mohlo být absorbováno před nástupem nepříznivých účinků.
Od 1990. let XNUMX. století bylo díky technologickému pokroku pozorováno, že malé množství hliníku, které zůstává v lidském těle, zasahuje do řady buněčných a metabolických procesů v nervovém systému a tkáních jiných částí těla.1-10-11 Největší negativní účinky hliníku byly pozorovány v nervovém systému a sahají od zhoršené motoriky až po encefalopatii (změněný duševní stav, změny osobnosti, poruchy myšlení, ztráta paměti, záchvaty, kóma a další).2-12
Ministerstvo zdravotnictví a sociálních služeb Spojených států amerických (HHS) uznává hliník jako známý neurotoxin.2 Kromě toho FDA varoval před riziky toxicity hliníku u kojenců a dětí.13
FEDERÁLNÍ REGISTR: Deník vlády Spojených států"I donošení kojenci s normální funkcí ledvin mohou být ohroženi rychlým růstem a nezralostí mozku a skeletu a také nezralostí hematoencefalické bariéry. Do 1. až 2. roku věku mají kojenci nižší glomerulární filtrace než u dospělých, což ovlivňuje jejich funkci ledvin. Agentura se obává, že malé děti a osoby s nezralou funkcí ledvin jsou vystaveny zvýšenému riziku expozice hliníku.“ |
5. Kolik orálního hliníku není bezpečné?
V roce 2008 Agentura pro registr toxických látek a nemocí (ATSDR), divize HHS, použila studie o neurotoxických účincích hliníku k určení, že ne více než 1 miligram (1.000 XNUMX mikrogramů) hliníku na kilogram tělesné hmotnosti za den. vyhnout se negativním účinkům hliníku.2
6. Jaké množství vstřikovaného hliníku není bezpečné?
Pro stanovení množství hliníku, které lze bezpečně vstříknout, je nutné převést orální limit hliníku podle ATSDR. Limit ATSDR pro perorální hliník (1.000 0,1 mikrogramů hliníku na kilogram tělesné hmotnosti za den) je založen na XNUMX % perorálního hliníku, který je absorbován do krevního řečiště, protože trávicí trakt blokuje téměř veškerý perorální hliník.2 Naopak hliník injikovaný intramuskulárně obchází trávicí trakt a 100 % hliníku se může časem vstřebat do krevního řečiště (tj. podíl absorbovaného hliníku je 1.000krát větší). Aby byla zohledněna tato různá množství absorpce, musí se orální limit hliníku ATSDR vydělit 1000 1. Tento převod vede k limitu hliníku v krvi odvozenému z ATSDR ve výši 0,1 mikrogram hliníku (1.000 % z 1 3 mikrogramů) na kilogram tělesné hmotnosti. denně. Aby se předešlo neurotoxickým účinkům hliníku, nemělo by se denně do krevního oběhu dostat více než XNUMX mikrogram hliníku na kilogram tělesné hmotnosti. Obrázek XNUMX ukazuje limit hliníku v krvi odvozený od ATSDR pro kojence různého věku na základě jejich hmotnosti.
7. Kolik hliníku je ve vakcínách?
Množství hliníku ve vakcínách se liší.16 V roce 1968 federální vláda USA stanovila limit pro množství hliníku ve vakcínách na 850 mikrogramů na dávku na základě množství hliníku potřebného k tomu, aby byly některé vakcíny účinné.6-17 V důsledku toho se množství hliníku v kojeneckých vakcínách obsahujících hliník pohybuje od 125 do 850 mikrogramů na dávku. Obrázek 4 ukazuje obsah hliníku v jedné dávce různých vakcín podaných dětem.
8. Srovnávaly nějaké studie množství hliníku ve vakcínách s limitem odvozeným od Agentury pro registr toxických látek a nemocí (ATSDR)?
V roce 2011 byla publikována studie, která měla za cíl porovnat množství hliníku ve vakcínách s limitem průtoku krve stanoveným ATSDR.18 Tato studie však nesprávně založila své výpočty na 0,78 % perorálního hliníku absorbovaného do krevního řečiště, spíše než na hodnotě 0,1 %, kterou používá ATSDR ve svých výpočtech.19-20 V důsledku toho studie z roku 2011 předpokládala, že téměř 8krát (0,78 % / 0,1 %) se hliník může bezpečně dostat do krevního oběhu, což vedlo k nesprávnému závěru.
9. Je expozice hliníku z vakcín bezpečná?
Vakcíny se aplikují intramuskulárně a rychlost, jakou hliník z vakcín migruje z lidských svalů do krevního řečiště, není známa. Studie na zvířatech naznačují, že hliníku z vakcín může v důsledku mnoha proměnných trvat několik měsíců až více než rok, než se dostane do krevního řečiště.21-23 Vzhledem k tomu, že kumulativní expozice hliníku z vakcín u dětí mladších jednoho roku překračuje denní limit stanovený ATSDR o několik stovek (obr. 3 a 4), byl by limit stále překročen, pokud by se hliník z vakcín dostal do krevního oběhu v průběhu asi rok. Některé studie navíc ukázaly, že hliník z vakcín je absorbován imunitními buňkami a dostává se do částí těla daleko od místa vpichu, včetně mozku.24
Rozsah nepříznivých účinků hliníku ve vakcínách není znám, protože nebyly provedeny bezpečnostní studie srovnávající populaci očkovanou vakcínami obsahujícími hliník s populací neočkovanou takovými vakcínami.
Hliníkové omezení průtoku krve odvozené z ATSDR2-14-15
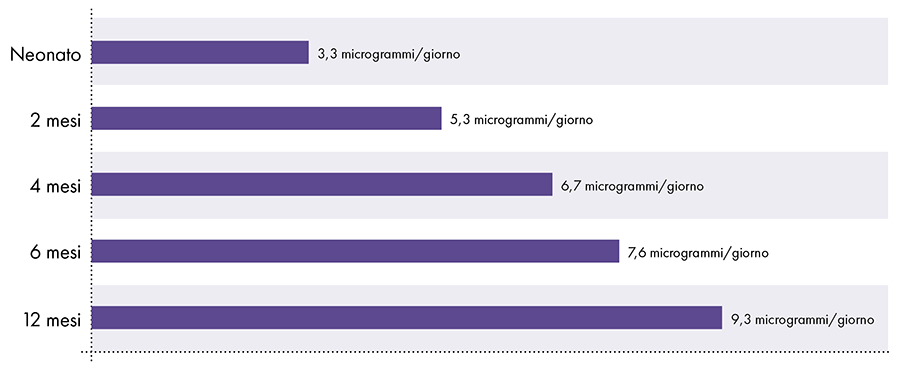 Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Množství hliníku ve vakcínách
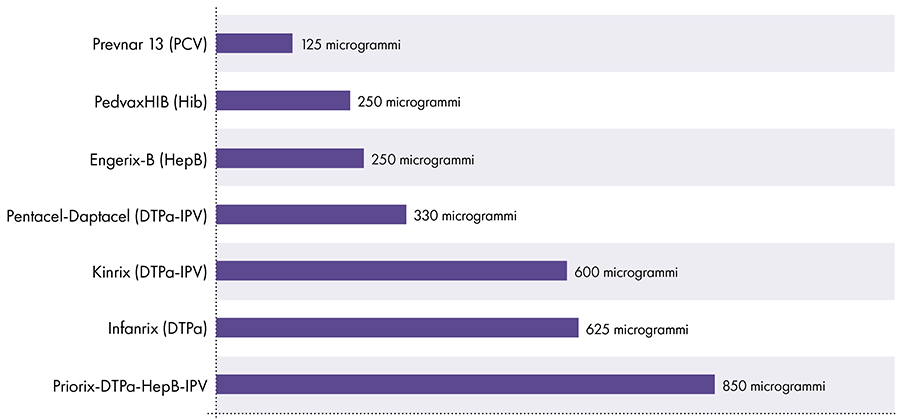
Reference
- Americká akademie pediatrie, Výbor pro výživu. Toxicita hliníku u kojenců a dětí. Pediatrie. březen 1996, 97 (3): 413.
- Agentura pro registr toxických látek a nemocí (ATSDR). Toxikologický profil pro hliník. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Hliník v potravinách – povaha a přínos potravinářských přídatných látek. In: El-Samragy Y, editor. Potravinová přísada. Rijeka (Chorvatsko): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. K pochopení adjuvantního působení hliníku. Nat Rev Immunol. 2009. dubna 9 (4): 287.
- Volk VK, Bunney WE. Imunizace proti záškrtu tekutým toxoidem a toxoidem vysráženým kamencem. Am J Veřejné zdraví Zdraví národů. července 1942, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Hliníkové soli ve vakcínách – perspektiva USA. Vakcína. 2002. května 31, 20 Suppl 3: S18-22.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. Vakcíny licencované pro použití ve Spojených státech amerických; [aktualizováno 2018. února 14; citováno 2018. února 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Doporučené schéma imunizace pro děti a dospívající ve věku 18 let nebo mladší, Spojené státy americké, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. SCOGS (Výběrový výbor pro látky GRAS); [citováno 2018. srpna 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Kněz ND. Biologické chování a biologická dostupnost hliníku u člověka, se zvláštním odkazem na studie využívající hliník-26 jako indikátor: přehled a aktualizace studie. J Environ Monit. 2004;6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Hliník ve výrobcích pro parenterální výživu dětí: měřeno versus obsah na etiketě. J Pediatr Pharmacol Ther. 2011, 16 (2): 92-7.
- Sedman A. Toxicita hliníku v dětství. Pediatr Nephrol. 1992 (6): 4-383, červenec 93.
- US Food and Drug Administration, Department of Health and Human Services. Pravidla a regulace. Registrátor Fedu. června 2003, 68 (100): 34286.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro chlapce v grafech délky k věku a hmotnosti k věku; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro grafy délky dívek na věk a hmotnosti na věk; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Department of Health and Human Services. Revize požadavků na základní materiály. Konečné pravidlo. Registrátor Fedu. 2011. dubna 13, 76 (71): 20513-8.
- Úřad federálního rejstříku, Národní archivy a spisová služba, Správa všeobecných služeb. Pravidla a regulace. Registrátor Fedu. 1968 leden; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím stravy a očkování. Vakcína. 2011. listopadu 28, 29 (51): 9538-43.
- Miller S, lékaři pro informovaný souhlas. Erratum v 'Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování.' In: ResearchGate. Berlín (Německo): ResearchGate GmbH; 2020. března 6 [citováno 2020. března 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Lékaři pro informovaný souhlas. Newport Beach (CA): Lékaři pro informovaný souhlas. Erratum v „Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování“; [citováno 2020. března 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In vivo absorpce adjuvans vakcín obsahujících hliník pomocí 26Al. Vaccine 1997 srpen-září, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Test hliníku a hodnocení lokální reakce v několika časových bodech po intramuskulárním podání vakcín obsahujících hliník u opice Cynomolgus. Vakcína. 2005. února 3, 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Hliník v plazmě a tkáních po intramuskulární injekci lidských vakcín s adjuvans u potkanů. Arch Toxicol. říjen 2019, 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritická analýza referenčních studií toxikokinetiky adjuvans na bázi hliníku. J Inorg Biochem. 2018 duben; 181: 87-95.
Článek přeložil Lékaři pro informovaný souhlas
V roce 1981 americký Úřad pro kontrolu potravin a léčiv (FDA) povolil vakcínu proti hepatitidě B pocházející z plazmy, která obsahovala antigeny odebrané infikovaným jedincům. Tato vakcína byla později stažena z trhu, protože stejně jako všechny vakcíny vyrobené z lidské krve byla schopna přenášet nežádoucí a potenciálně nebezpečné viry. V roce 1986 byla schválena první ze série geneticky modifikovaných (rekombinantních DNA) vakcín.
Četné studie zkoumaly pravděpodobnost, že ti, kteří dostali vakcínu získanou z plazmy, mohli také dostat nežádoucí viry, zejména HIV, předchůdce AIDS.(1-2) Kromě toho byly klinické studie k potvrzení bezpečnosti současné vakcíny proti hepatitidě B provedeny pouze na 147 zdravých dětech monitorovaných po dobu pouhých 5 dnů po podání.(3) Toto není dostatečně velký vzorek ani dostatečně dlouhé období pro stanovení skutečného výskytu nežádoucích účinků. Výrobní společnosti samy připustily, že „široké používání vakcíny by mohlo vést ke vzniku nežádoucích účinků, které nebyly pozorovány v klinických studiích“.(4)
Dokonce i dospělí jedinci byli sledováni pouze pět dní po očkování a přesto byly stále hlášeny systémové účinky jako artralgie, myalgie, parestézie, bolesti zad a krku, lymfadenopatie, bolest hlavy, horečka, malátnost, zimnice, zvracení. bolest, infekce horních cest dýchacích, bolest ucha a hypotenze.(5)
Navzdory oficiálním technickým listům a dalším dokumentům, které se šíří(6) vakcína proti hepatitidě B, mají tendenci minimalizovat nebo popírat závažné nežádoucí reakce, četné studie publikované v lékařských a vědeckých časopisech po celém světě a zprávy zasílané VAERS(7) potvrdit různé patologie v důsledku očkování. Některé z těchto studií jsou shrnuty níže.
Artritida
V roce 1990, brzy po zavedení vakcíny proti hepatitidě B, British Medical Journal zdokumentoval souvislost mezi vakcínou a polyartritidou, bolestivým zánětem pěti nebo více kloubů.(8) Ve stejném roce Journal of Rheumatology zveřejnil článek o reaktivní artritidě po očkování proti hepatitidě B.(9)
V roce 1994 zveřejnil British Journal of Rheumatology data dokumentující revmatoidní artritidu po očkování(10) a BMJ zveřejnily tři další zprávy potvrzující souvislost mezi vakcínou a reaktivní artritidou.(11-12) V roce 1995 byly ve Scandinavian Journal of Rheumatology publikovány dvě studie potvrzující případy postvakcinační artritidy.(13-14) a tentýž rok Irish Medical Journal zdokumentoval souvislost s artropatií.(15) V roce 1997 zveřejnil British Journal of Rheumatology dvě další studie dokumentující několik případů zánětlivé polyartritidy po očkování(16-17) a v roce 1998 Journal of Rheumatology znovu potvrdil revmatoidní artritidu.(18) V tomto roce také francouzský časopis Revue de Médecine Interne publikoval studii o Stillově nemoci s nástupem v dospělosti – vzácném a bolestivém typu artritidy – po očkování proti hepatitidě A a B.(19) V roce 1999 revmatologie zdokumentovala revmatologické poruchy po očkování(20) a v roce 2000 American College of Rheumatology zveřejnila výzkum v recenzovaném časopise Arthritis & Rheumatology, který dokumentoval Sjogrenův syndrom – vzácnou formu chronické artritidy – po očkování proti hepatitidě B.(21)
Autoimunitní a neurologická onemocnění včetně roztroušené sklerózy
V roce 1983 publikoval New England Journal of Medicine studii prokazující nástup polyneuropatie – současná porucha mnoha nervů – po očkování proti hepatitidě B.(22) V roce 1988 American Journal of Epidemiology ohlásil četné „neurologické nežádoucí příhody“ po vakcíně včetně četných případů Guillain-Barrého syndromu, lumbální radikulopatie, neuropatie brachiálního plexu, oční neuritidy a transverzální myelitidy.(23) Ve stejném roce časopis Archives of Internal Medicine dokumentoval myasthenia gravis - závažné chronické autoimunitní neuromuskulární onemocnění - znovu po očkování proti hepatitidě B.(24)
V roce 1991 Lancet zveřejnil zprávu dokumentující demyelinizaci centrálního nervového systému po vakcíně(25) a v roce 1992 Nephron zveřejnil údaje spojující očkování se systémovým lupus erythematodes, chronickým autoimunitním onemocněním, které postihuje více orgánů.(26) V roce 1992 také časopis Clinical Infectious Diseases zveřejnil studii spojující Evansův syndrom - vzácné autoimunitní a krevní onemocnění s vysokou úmrtností - s vakcínou.(27) a francouzský časopis Thérapie publikoval studii o „periferní obličejové paralýze“ opět po podání léku.(28) Infectious Disease News navíc zveřejnila zprávu uvádějící četné případy neurologického poškození připomínajícího roztroušenou sklerózu(29) a v roce 1993 vyšel v Journal of Hepatology článek o transverzální myelitidě – zánětu míchy – po očkování proti hepatitidě B.(30) Ve stejném roce francouzské noviny La Nouvelle Presse Médicale zveřejnily údaje potvrzující postvakcinační "akutní myelitidu"(31) a Klinické infekční choroby dokumentovaly „klasickou roztroušenou sklerózu“.(32) V roce 1994 Archives of Pediatrics and Adolescent Medicine zveřejnil údaje spojující lupus s vakcínou(33) a časopis Acta Neurologica Scandinavica zveřejnily zprávu o akutní cerebelární ataxii – těžké ztrátě rovnováhy a motorické koordinace – po příslušném očkování.(34)
V roce 1995 byla demyelinizace centrálního nervového systému popsána v Journal of Neurology, Neurosurgery and Psychiatry(35) a v American Journal of Neuroradiology myelitis. Autoři posledně jmenované studie poznamenali, že nežádoucí účinky této povahy mohou být podhodnoceny, protože příznaky jsou pozdní.(36) V roce 1996 Nephron i francouzský časopis Annales de Dermatologie et de Vénéréologie publikovaly studie potvrzující korelaci mezi lupus erythematodes a vakcínou proti hepatitidě B.(37-38) Ve stejném roce zveřejnil Journal of Hepatology zprávu o souvislosti s leukoencefalitidou, zánětem bílé hmoty mozku.(39) V roce 1996 New England Journal of Medicine zdokumentoval postvakcinační kryoglobulinémii, vzácné autoimunitní onemocnění, které zhoršuje oběh, způsobuje krvácení a další problémy.(40)
Autoimunita vyvolaná vakcínou byla certifikována v Journal of Autoimmunity(41) a v roce 1997 Indian Journal of Pediatrics zveřejnil studii spojující Guillain-Barré syndrom, autoimunitní onemocnění, které způsobuje poškození nervů, svalovou slabost a paralýzu, s vakcínou.(42) Ve stejném roce Journal of Korean Medical Science dokumentoval akutní myelitidu(43) a také se objevila souvislost s „neuropatií mentálních nervů“.(44)
V časopise JAMA se pak objevila data o 46 lidech – většinou o ženách –, kteří přišli o vlasy po očkování proti hepatitidě B.(45)
V roce 1998 byl u očkovaných osob dokumentován lupus erythematodes i trombocytopenie(46) a v roce 1999 více alopecie v American Journal of Gastroenterology.(47) Ve stejném roce Autoimunita dokumentovala demyelinizační polyneuropatii, zatímco Neurologie zveřejnila údaje spojující roztroušenou sklerózu a encefalitidu s vakcínou.(48-49) Také v roce 1999, La Nouvelle Presse Médicale napsal o postvakcinační cervikální myelitidě(50) a v roce 2000 byla roztroušená skleróza diskutována v neurologii.(51) Také v roce 2000 psal Journal of the Medical Association of Thailand o Guillain-Barrého syndromu po rekombinantní DNA vakcíně proti hepatitidě B(52) a v roce 2001 Klinická infekční onemocnění dokumentovala leukoencefalitidu.(53) V roce 2004 Neurology zveřejnila studii ukazující souvislost mezi vakcínou a statisticky významným rizikem roztroušené sklerózy;(54) v roce 2006 Čínský lékařský časopis také zdokumentoval roztroušenou sklerózu.(55) V roce 2008 vydala Neurologie dvě studie ukazující statisticky významnou korelaci mezi očkováním proti hepatitidě B u dětí a rozvojem dětské roztroušené sklerózy (demyelinizace centrálního nervového systému) o více než tři roky později.(56-57)
Smyslové postižení
Četné lékařské a vědecké publikace dokumentovaly poruchy zraku a sluchu po očkování proti hepatitidě B. Například v roce 1987 The Lancet publikoval práci o uveitidě – zánětu vnitřní výstelky oka, který často vede ke slepotě – po očkování.(58) V roce 1993 se opět v The Lancet objevily další údaje dokumentující ztrátu zraku a eozinofilii – alergické onemocnění krve – opět po očkování.(59) V roce 1994 Optometry and Vision Science zdokumentovala postvakcinační zánět zrakového nervu(50) a v roce 1995 byla v Archivech oftalmologie diskutována epiteliopatie - vzácná oční porucha, která způsobuje zhoršení vidění.(61) V roce 1996 The Lancet zveřejnil zprávu dokumentující „okluzi centrální retinální žíly“ po vakcíně,(62) zatímco v American Journal of Ophthalmology byl zmíněn syndrom bilaterálních bílých skvrn - který způsobuje ztrátu zraku v obou očích.(63) Také v roce 1996 La Nouvelle Presse Médicale dokumentoval neuropapilitidu - zánět a zhoršení zrakového nervu - po vakcíně(64) a další francouzský časopis Annales d'Otolaryngologie et de Chirurgie Cervico-Faciale zmínil ztrátu sluchu.(65) V roce 1997 pak La Nouvelle Presse Médicale publikoval dvě různé studie dokumentující závažné případy okluze centrální retinální žíly po očkování.(66-67) Ve stejném roce nefrologická dialyzační transplantace potvrdila vznik zánětu zrakového nervu po očkování(68) a International Oftalmology certifikované „oční komplikace“ u očkovaných subjektů.(69) Také v roce 1997 Annals of the New York Academy of Sciences a mezinárodní časopis Auris, Nasus, Larynx zaznamenaly postvakcinační ztrátu sluchu,(70-71) zatímco v roce 1998 publikoval Journal of French Ophthalmology údaje o epiteliopatii.(72) V roce 1999 BMJ potvrdil zánět zrakového nervu po očkování proti hepatitidě B(73) a Acta Ophthalmologica Scandinavica papilledema - otok terče zrakového nervu.(74) V roce 2001 německý časopis Klinische Monatsblätter Für Augenheilkunde také potvrdil postvakcinační zánět zrakového nervu.(75)
Nemoci krve
V roce 1990, brzy po masovém uvedení vakcíny proti hepatitidě B na trh, BMJ dokumentoval vaskulitidu, zánět krevních cév, po podání léku.(76) V roce 1993 to potvrdil anglický časopis Thorax(77) a The Lancet zveřejnili studii o eozinofilii, alergickém onemocnění krve, opět po očkování.(78) V letech 1994 a 1995 The Lancet také zdokumentoval trombocytopenii - závažné onemocnění, které způsobuje nadměrné krvácení, modřiny a problémy se srážlivostí.(79-80) V roce 1998 byl potvrzen nástup trombocytopenie u mnoha nedávno očkovaných pacientů(81) také z Scandinavian Journal of Infectious Diseases potvrzena a Archives of Disease in Children publikoval údaje potvrzující toto onemocnění jako nežádoucí účinek vakcíny.(82) V roce 1999 European Journal of Pediatrics znovu potvrdil trombocytopenii po vakcínách proti hepatitidě B a MMR(83) a téhož roku Journal of Rheumatology zveřejnil dvě důležité studie, z nichž první prokázala korelaci mezi vakcínou a vaskulitidou(84) a druhá erytermalgie, cévní křeče v rukou a nohou, které způsobují bolest a pálení.(85) Klinická a experimentální revmatologie studovala v roce 2000 případy polyarthritis nodosa(86) - vzácný, systémový, nekrotizující (buňky poškozující) typ vaskulitidy - a British Journal of Hematology dokumentoval těžkou pancytopenii - nebezpečné snížení počtu červených krvinek.(87) V roce 2001 zveřejnil Journal of Rheumatology další údaje potvrzující možnost vaskulitidy po rekombinantní vakcíně proti hepatitidě B(88) a italský časopis Haematologica potvrdily trombocytopenii jako nežádoucí příhodu.(89)
Kožní choroby
V roce 1989 New England Journal of Medicine dokumentoval erythema nodosum – bolestivý zánět kůže s měkkými hrbolky – po očkování proti hepatitidě B.(90) V roce 1993 Journal of Rheumatology informoval o případech erythema nodosum a Takayasu artritidy – vzácné formy vaskulitidy.(91) Ve stejném roce švédský časopis Acta Dermato-Venereologica psal o lichen ruber planus po očkování(92) - svědivá vyrážka na kůži charakterizovaná hustými, tvrdými lézemi blízko sebe, které připomínají řasy nebo houby rostoucí na kamenech. V roce 1994 zdokumentoval Dermatologický archiv také lichen planus po očkování(93) a dětská dermatologie prokázala souvislost s erythema multiforme.(94) V roce 1997 potvrdil Australasian Journal of Dermatology „lichenoidní reakci“ (lichen planus) po vakcíně.(95) a Journal of the American Academy of Dermatology psali o anethodermii(96) - lokalizované zvrásnění, ztráta elasticity a atrofie kůže - po očkování. V roce 1998 zveřejnil British Journal of Dermatology dvě studie dokumentující postvakcinační kožní onemocnění: jedna byla na lichen planus(97) a druhý na kopřivku a angioedém,(98) patologie alergického původu charakterizované pálením, štípáním a bolestivým otokem. V roce 1999 byl lichen planus zmíněn také v International Journal of Dermatology(99) a v roce 2000 byla v Clinical and Experimental Dermatology publikována data potvrzující postvakcinační erythema multiforme.(100) Ve stejném roce Nepal Journal of Dermatology opět psal o lichen planus po očkování proti hepatitidě B(101) v roce 2001 se zmínka objevila v Journal of the American Academy of Dermatology(102) zatímco dětská dermatologie hovořila o lichenoidní erupci.(103)
Diabetes onemocnění jater a ledvin
V roce 1994 Lancet zdokumentoval dysfunkci jater po očkování proti hepatitidě B(104) a v roce 1995 Clinical Nephrology publikoval studii o nefrotickém syndromu – poškození ledvin – opět po očkování.(105) V roce 1996 New Zealand Medical Journal zveřejnil dva dokumenty, které korelovaly antihepatitidu B s epidemiemi inzulín-dependentního diabetes mellitus (IDDM). Autoři zjistili, že během tří let po nově zavedené a velmi rozsáhlé masové očkovací kampani došlo k 60% nárůstu případů IDDM.(106-107) V roce 1997 Intensive Care Medicine psalo o zánětu jater a akutním respiračním onemocnění po očkování (108). V roce 2000 potvrdila dětská nefrologie možnost trpět nefrotickým syndromem po očkování.(109) Další publikace také dokumentovaly nežádoucí účinky této vakcíny.(110-111-112-113-114-115-116-117-118-119)
Francie vyřadila antihepatitidu B z očkovacího kalendáře dětí
V červenci 1998 podalo přibližně 15.000 XNUMX francouzských občanů patřících k patnácti sdružením žalobu na francouzskou vládu, která tvrdila, že uvedla veřejnost v omyl ohledně rizik a výhod spojených s vakcínou proti hepatitidě B. Stovky – možná tisíce – lidí prodělaly autoimunitní onemocnění a neurologické poruchy, včetně roztroušené sklerózy, po očkování.(120) Výsledkem bylo, že v říjnu 1998 se Francie stala první zemí, která zrušila požadavek na přijetí této vakcíny do školy.(121)
Vakcína proti hepatitidě B AIDS
V roce 1978 New York Blood Center na Manhattanu ve státě New York vstříklo homosexuálním mužům experimentální vakcínu proti hepatitidě B, kterou vyrobila společnost Merck, k jejíž přípravě byli používáni šimpanzi. Krátce poté dostali 3 dávky drogy během tří měsíců také mužští homosexuálové v San Franciscu, Los Angeles, Denveru, Chicagu a St. Louis.
V roce 1980 mělo 20 % gayů, kteří se dobrovolně zapojili do experimentu na Manhattanu, pozitivní test na HIV – nejvyšší výskyt na světě, včetně Afriky. V roce 1981 se epidemie AIDS stala oficiální. Ačkoli neexistuje žádný důkaz, že experimentální vakcína proti hepatitidě B u těchto homosexuálních dobrovolníků způsobila AIDS, není pochyb o tom, že nemoc vyvrcholila brzy po výstřelech.(122)
Jak účinná je vakcína proti hepatitidě B?
Účinnost vakcíny proti hepatitidě B byla definována injekčním podáním léku subjektům, kterým byly následně měřeny specifické protilátky produkované v krvi. Tyto protilátky musí splňovat nebo překračovat určité úrovně stanovené odborníky, u kterých se předpokládá, že poskytují ochranu. Vědci tomu říkají „séroprotekce“. Podle této definice je vakcína považována za „vysoce imunogenní“, když jsou hladiny protilátek měřitelné v krátkém období po poslední dávce cyklu se třemi posilovacími dávkami.(123) Podle zpracovatelského průmyslu však není doba trvání ochranného účinku u zdravých očkovaných lidí známa. Následné studie již o pět až devět let později ukazují, že asi polovina všech očkovaných osob již nemá ochranné hladiny protilátek.(124-125)
Například studie publikovaná v New England Journal of Medicine zjistila, že po pěti letech hladiny protilátek (o kterých se předpokládá, že souvisejí s imunitou) dramaticky poklesly nebo již nebyly zjistitelné u 42 % očkovaných. Kromě toho bylo virem infikováno 34 ze 773 subjektů (4,4 %).(126-127) V jiné studii mělo méně než 40 % očkovaných ochranné protilátky po pěti letech.(128)
Podobný výzkum ukázal, že 48 % očkovaných subjektů mělo nedostatečné hladiny protilátek již po čtyřech letech.(129) Podle WHO až „60 % dospělých ztratí během šesti až deseti let všechny měřitelné protilátky vyvolané vakcínou proti hepatitidě B“.(130) a lékařská literatura je plná údajů potvrzujících selhání očkování.(131-132)
Reference
- Jacobson IM a kol., "Nedostatek účinku vakcíny proti hepatitidě B na fenotypy T-buněk", NEJM, 1984, 311 (16), str. 1030-1032.
- Institute of Medicine, Nežádoucí události spojené s dětskými vakcínami: Důkazy týkající se kauzality, National Academy Press, Washington, DC, 1994.
- Merck & Co., Inc. Recombivax HB vakcína proti hepatitidě B (rekombinantní), příbalový leták k červnu 2005.
- Tamtéž.
- Tamtéž.
- Tan LJ, „Vakcína proti hepatitidě B“, Americká lékařská asociace, AMA pomáhající lékařům pomáhat pacientům, www.arna-assn.org, 9. prosince 2004.
- Systém hlášení nežádoucích příhod vakcín VAERS. Rockville, MD.
- Rogers ton SJ a kol. , "Vakcína proti hepatitidě B spojená s erythema nodosum a polyartritidou", BMJ, 1990, 301, str. 345.
- Hachulla E. a kol., "Reaktivní artritida po očkování proti hepatitidě B Journal of Rheumatology", 1990, 17, str. 1250-1251.
- Vautier G. a kol., "Akutní séropozitivní revmatoidní artritida vyskytující se po očkování proti hepatitidě", Br. J. Rheumatol., říjen 1994, 33 (10), str. 991.
- Hassan W. a kol., "Reiterův syndrom a reaktivní artritida u zdravotnických pracovníků po očkování", BMJ, 9. července 1994, 309 (6967), str. 94.
- Birley HD a kol., "Imunizace proti hepatitidě B a reaktivní artritida", BMJ, prosinec 1994, 309 (6967), str. 1514.
- Gross a kol., "Artritida po očkování proti hepatitidě B. Zpráva o třech případech," Scand. J. Rheumatol., 1995, 24 (1), str. 50-52.
- Biasi D. a kol., "Reumatologické projevy po očkování proti hepatitidě B. Zpráva o třech případech", Scand. J. Rheumatol., 1995, 24, str. 50-52.
- Aherne P. a kol., "Psoriatická artropatie", Irish Medical Journal, březen-duben 1995, 88 (2), str. 72.
- Harrison BJ a kol., "Pacienti, u kterých se po imunizaci rozvine zánětlivá polyartritida (PH), jsou klinicky nerozeznatelní od ostatních pacientů s PH," Br. J. Rheum., březen 1997, 36 (3), str. 366-369.
- Bracci M. a kol., "Polyartritida spojená s očkováním proti hepatitidě B", Br. J. Rheumatol., únor 1997, 36 (2), str. 300-301.
- Pope JE a kol., "Vývoj revmatoidní artritidy po rekombinantní vakcinaci proti hepatitidě B", J. Rheum., září 1998, 25 (9), str. 1687-1693.
- Grasland A et al., "Stillova choroba s nástupem v dospělosti po očkování proti hepatitidě A a B?", Rev. Internal Med., únor 1998, 19 (2), str. 134-136.
- Maillefert JF a kol., "Revmatické poruchy vzniklé po očkování proti hepatitidě B", Rheumatol. (Oxford), říjen 1999, 38 (10), str. 978-983.
- Toussirot E. a kol., "Sjogrenův syndrom vyskytující se po očkování proti hepatitidě B", Arthritis Rheuma, září 2000, 43 (9), str. 2139-2140.
- Ribera ER a kol., "Polyneuropatie spojená s podáváním vakcíny proti hepatitidě B", N. Engl. J. Med., 8. září 1983, 309 (10), str. 614-615.
- Shaw FE Jr. a kol., "Postmarketingový dohled nad neurologickými nežádoucími účinky hlášenými po očkování proti hepatitidě B. Zkušenosti z prvních tří let", Am. J. Epidemiol., únor 1988, 27 (s), str. 337-352 .
- Biron P. a kol., "Myasthenia gravis po celkové anestezii a vakcíně proti hepatitidě B", Arch. Intern. Med., prosinec 1988, 148 (12), str. 2685.
- Herroelen L. a kol. , "Demyelinizace centrálního nervového systému po imunizaci rekombinantní vakcínou proti hepatitidě B", The Lancet, 9. listopadu 1991, 338 (8776), str. 1174-1175.
- Tudela P. a kol., "Systémový lupus erythematodes a očkování proti hepatitidě B", Nephron, 1992, 62 (2), str. 236.
- Martinez E. a kol., "Evanův syndrom vyvolaný rekombinantní vakcínou proti hepatitidě B", Clin. Infect. Dis., 1992, 15, str. 1051.
- Ganry 0. a kol., "Periferní obličejová paralýza po očkování proti hepatitidě B. Apropos of a case", Therapie, 1992, 47, str. 437-438.
- Waisbren BA, "Druhá strana mince (dopis)", Inf Dis. Zprávy, 1992, 5, s. 2.
- Trevisani F. a kol., "Transverzní myelitida po očkování proti hepatitidě B",]. of Hepatology, září 1993, 19 (2), pp. 317-318.
- Mahassin F. a kol. , "Akutní myelitida po očkování proti hepatitidě B", Presse Med., prosinec 1993, 22 (40), str. 1997-1998.
- Nadler JP, "Očkování proti roztroušené skleróze a hepatitidě B", Clin. Infikovat. Dis., listopad 1993, 17 (5), str. 928-929.
- Mamoux V. a kol., "Lupus erthymatosus disseminatus a očkování proti viru hepatitidy B", Arch. Pediatr., 1994, 1, str. 307-309.
- Deisenhammer F. a kol., "Akutní cerebelární ataxie po imunizaci rekombinantní vakcínou proti hepatitidě B", Acta Neurol. Scand., červen 1994, 89 (6), str. 462-463.
- Kaplanski G. a kol., "Demyelinizace centrálního nervového systému po očkování proti hepatitidě B a HLA haplotyp", J. Neurol. Neurosurg. Psychiatrie, červen 1995, 58 (6), pp. 758-759.
- Tartaglino LM et al., "MR zobrazení v případě postvakcinační myelitidy", Am. J. Neuroradiol., 1995, 16 (3), str. 581-582.
- Guiserix J., "systémový lupus erythematodes po vakcíně proti hepatitidě B", Nephron, 1996, 74 (2), str. 441.
- Grezard P. a kol., "Kutánní lupus erythematodes a bukální aftóza po očkování proti hepatitidě B u 6letého dítěte", Ann. Dermatol. Venereal., 1996, 123 (10), str. 657-659.
- Manna R. a kol., "Leukoencefalitida po rekombinantní vakcíně proti hepatitidě B", J. of Hepatology, červen 1996, 24 (6), str. 764-765.
- Mathieu E. a kol., "Kryoglobulinémie po očkování proti hepatitidě B", Nová Anglie]. Med., srpen 1996, 335 (5), str. 335.
- Cohen AD. a kol., "Vaccine-induced autoimmunity", J. Autoimmunity, prosinec 1996, 9 (6), str. 699-703.
- Kakar A. a kol., "Guillain Barre syndrom spojený s očkováním proti hepatitidě B", Ind. J. Ped., září-říjen 1997, 64 (5), 710-712.
- Song HK a kol., "Akutní myelitida po očkování proti hepatitidě B", J. Korean Med. Sci., červen 1997, 12 (3), str. 249-251.
- Maillefert JF a kol., "Neuropatie mentálního nervu jako výsledek očkování proti hepatitidě B," Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontology, červen 1997, 83 (6), str. 663-664.
- Wise RP a kol., "Ztráta vlasů po rutinních imunizacích," JAMA, 8. října 1997, 278 (14), str. 1176-1178.
- Finielz P. a kol., "Systémový lupus erythematodes a trombocytopenická purpura u dvou členů stejné rodiny po vakcíně proti hepatitidě B", Nephrol. Vytáčení. Transplant., 1998, 13 (9), str. 2420-2421.
- Flemrner M. a kol., "The plešatá pravda", Am. J. Gastroenterol., duben 1999, 94 (4), str. 1104.
- Creange A a kol., "Lumbosakrální akutní demyelinizační polyneuropatie po očkování proti hepatitidě B", Autoimmunity, 1999, 30, str. 143-146.
- Tourbah A. et al., "Encefalitida po očkování proti hepatitidě B: recidivující diseminovaná encefalitida nebo RS?", Neurologie, 22. července 1999, 53 (2), str. 396-401.
- Renard JL a kol., "Akutní transverzální cervikální myelitida po vakcinaci proti hepatitidě B. Evoluce anti-HBs protilátek", Presse Med., 3-10. července 1999, 28 (24), str. 1290-1292.
- Gran B. et al., "Martin R. Development of roztroušená skleróza po očkování proti hepatitidě B", Neurol., 2000, 54 (suppl 3), A164.
- Sinsawaiwong S. a kol., "Guillain-Barreův syndrom po rekombinantní vakcíně proti hepatitidě B a přehled literatury", J. Med. Assoc. Thai., září 2000, 83 (9), str. 1124-1126.
- Konstantinou D. a kol., "Dvě epizody leukoencefalitidy spojené s rekombinantní vakcinací proti hepatitidě B u jednoho pacienta", Clin. Inf. Dis., 15. listopadu 2001, 33, str. 1772-1773.
- Heman MA a kol., "Rekombinantní vakcína proti hepatitidě B a riziko roztroušené sklerózy: prospektivní studie", Neurology, 2004, 63, pp. 838-842.
- Terney D. a kol., "Roztroušená skleróza po očkování proti hepatitidě B u 16letého pacienta", Chinese Medical Journal, 2006, 119 (1), str. 77-79.
- Yann M. et al., „Vakcína proti hepatitidě B a riziko zánětlivé demyelinizace CNS v dětství“, Neurology, 8. října 2008 [publikováno online].
- Ness JM et al „Vakcíny proti hepatitidě a dětská roztroušená skleróza. Záleží na načasování nebo typu?“, Neurologie, 17. prosince 2008 (zveřejněno online).
- Fried Met al., "Uveitida po očkování proti hepatitidě B", The Lancet, 12. září 1987, str. 631-632.
- Brezin A. a kol., "Ztráta zraku a eosinofilie po rekombinantní vakcíně proti hepatitidě B", The Lancet, 28. srpna 1993, 342 (8870), str. 563-564.
- Achiron LR a kol., "Postinfekční hepatitida B optická neuritida", Optom. Pohled Sci., 1994, 71, str. 53-56.
- Brezin AP a kol., "Acute posterior multifokální plakoidní pigmentová epiteliopatie po vakcíně proti hepatitidě B", Arch. Ophthalmol., březen 1995, 113 (3), str. 297-300.
- Devin F. a kol., "Okluze centrální retinální žíly po očkování proti hepatitidě B", The Lancet, červen 1996, 347 (9015), str. 1626.
- Baglivo E. a kol., "Syndrom mnohočetného evanescentního bílého bodu po vakcíně proti hepatitidě B", Am. J. Ophthalmol., září 1996, 122 (3), str. 431-432.
- Berkman N. a kol., "Bilaterální neuropapilitida po očkování proti hepatitidě B", Presse Med., 28. září 1996, 25 (28), str. 1301 (francouzsky).
- Bonfils P. a kol., "Fluctuantní percepční ztráta sluchu po vakcíně proti hepatitidě B", Ann. Otolaryngol. Chir. Cervicofac., 1996, 113 (6), str. 359-361 (francouzsky).
- Granel B. a kol., "Okluze centrální retinální žíly po očkování proti virové hepatitidě B rekombinantními vakcínami. 4 případy", Presse Med., 1. února 1997, 26 (2), str. 62-65 [francouzsky].
- Berkman N., "Případ segmentální unilaterální okluze centrální retinální žíly po očkování proti hepatitidě B", Presse Med., 26. dubna 1997, 26 (14), str. 670 [francouzsky].
- Albitar S. a kol., "Bilaterální retrobulbární optická neuritida s očkováním proti hepatitidě B", Nephrol. Vytáčení. Transplant, říjen 1997, 12 (10), pp. 2169-2170.
- Arya SC, "Oční komplikace vakcín proti viru hepatitidy B", Int. Ophth., 1997, 21 (3), str. 177-178.
- Orlando MP a kol., "Náhlá ztráta sluchu v důsledku očkování proti hepatitidě B: případová zpráva", Annals of the New York Academy of Sciences, 29. prosince 1997, 830, str. 319-321.
- Biacabe B. a kol., „Případová zpráva fluktuující senzorineurální ztráty sluchu po očkování proti hepatitidě B“, Auris, Nasus, Larynx, říjen 1997, 24, (4), str. 357-360.
- Bourges JL a kol., "Multifokální plakoidní epiteliopatie a očkování proti hepatitidě B", J. Fr. Ophtalmol., listopad 1998, 21(9), str. 696-700 [francouzsky].
- Stewart O. et al., "Simultane podávané vakcíny proti hepatitidě B a dětské obrně spojené s bilaterální optickou neuritidou", Br. J. Ophthalmol., říjen 1999, 83 (10), str. 1200-1201.
- Fledelius HC, „Unilaterální papilém po očkování proti hepatitidě B u pacienta s migrénou. Případová zpráva zahrnující forenzní aspekty", Acta Ophthalmol. Scand., prosinec 1999, 77 (6), str. 722-724.
- Voigt u. a kol., „Neuritida očního nervu po očkování proti hepatitidě A, hepatitidě B a žluté zimnici“, Klin. Monatsbl. Augenheilkd., říjen 2001, 218 (10), str. 688-690 (německy).
- Cockwell P. a kol., "Vaskulitida související s vakcínou proti hepatitidě B", BMJ, 1. prosince 1990, 301 (6763) str. 1281.
- Allen MB a kol., "Plicní a kožní vaskulitida po očkování proti hepatitidě B", Thorax, květen 1993, 48 (5), str. 580-581.
- Nagafuchi S. a kol., "Eosinofilie po intradermální vakcinaci proti hepatitidě B", The Lancet, 1993, 342, str. 998.
- Poullin P. a kol., "Trombocytopenická purpura po rekombinantní vakcíně proti hepatitidě B", The Lancet, listopad 1994, 344 (8932), str. 1293.
- Meyboom RH a kol., "Trombocytopenie hlášená v souvislosti s vakcínami proti hepatitidě B a A", The Lancet, červen 1995, 345 (8965), str. 1638.
- Neau D. a kol., "Imunitní trombocytopenická purpura po rekombinantní vakcíně proti hepatitidě B: retrospektivní studie sedmi případů", Scan J. Infect Dis., 1998, 30 (2), str. 115-118.
- Ronchi F. a kol., "Trombocytopenická purpura jako nežádoucí reakce na rekombinantní vakcínu proti hepatitidě B", Arch. Dis. Child., březen 1998, 78 (3), pp. 273-274.
- Muller A. et al., "Trombocytopenická purpura: nežádoucí reakce na kombinovanou imunizaci (rekombinantní hepatitida B a vakcína proti spalničkám, příušnicím a zarděnkám) a po léčbě co-trimoxazolem", Eur.]. Pediatr., prosinec 1999, 158 Suppi. 3, S209-10.
- Le Hello C. a kol., "Suspected hepatitis B injection related vasculitis", J. of Rheumatology, leden 1999, 26 (1), str. 191-194.
- Rabaud C. a kol., "První případ erytermalgie související s očkováním proti hepatitidě B", J. of Rheum., leden 1999, 26 (1), str. 233-234.
- De Keyser F. a kol., „Imunitně zprostředkovaná patologie po očkování proti hepatitidě B“ Dva případy polyarteritis nodosa a jeden případ erupce léku podobné pityriasis rosea, Clin. Exp. Rheumatol., leden-únor 2000, 18 (1), str. 81-85.
- Viallard JF a kol., "Těžká pancytopenie vyvolaná rekombinantní vakcínou proti hepatitidě B", Br. J. Haematol., červenec 2000, 110 (1), str. 230-233.
- Zaas A. et al., uVaskulitida velkých tepen po vakcinaci rekombinantní hepatitidou B. 2 případy", J. Rheumatol., květen 2001, 28 (S), str. 1116-11120.
- Conesa V. a kol., "Trombocytopenická purpura po rekombinantní vakcíně proti hepatitidě B. Vzácná asociace", Haematologica, březen 2001, 86 (3), E09 [italsky].
- Goolsby PL, „Erythema nodosum po vakcíně Recombivax HB proti hepatitidě B,“ N. Engl. J. Med., říjen 1989, 321, 1198-1199.
- Castresana-Isla CJ a kol., "Erythema nodosum a Talkayasuova arteritida po imunizaci vakcínou proti hepatitidě B odvozenou z plazmy", J. Rheumatol., srpen 1993, 20(8), str. 1417-1418.
- 109. Trevisian G. a kol., "Lichen ruber planus po očkování proti HBV". Acta Dermato-Venereotogica, únor 1993, 73 (1), str. 73.
- Aubin F. a kol., „Lichen planus po očkování proti hepatitidě B“, Archives of Dermatology, říjen 1994; 130 (10), str. 1329-1330.
- Di Lernia V. a kol., "Bisighini G. Erythema multiforme po vakcíně proti hepatitidě B", Ped. Derma., prosinec 1994, 11 (4), str. 363-364.
- Saywell CA. a kol., "Kossard S. Lichenoidní reakce na očkování proti hepatitidě B", Australasian J. Derm., srpen 1997, 38 (3), str. 152-154.
- Dauod MS a kol., „Anetoderma po imunizaci proti hepatitidě B u dvou sourozenců,“/. Amer. Akad. Dermatol., květen 1997, 36 (5 Pt 1), str. 779-780.
- Ferrando MF a kol., "Lichen planus po očkování proti hepatitidě B", Br. J. Dermatol., srpen 1998, 139 (2), str. 350.
- Barbaud A. a kol., "Alergické mechanismy a kopřivka/angioedém po imunizaci proti hepatitidě B", Bt. J. Dermatot, listopad 1998, 139 (5), str. 925-926.
- Schupp P. a kol., "Lichen planus po očkování proti hepatitidě B", Inter. J. of Dermat., říjen 1999, 38 (10), str. 799-800.
- Loche F. a kol., "Multiformní erytém spojený s imunizací proti hepatitidě B", Cfin. Exp.Dermatol., březen 2000, 25 (2), str. 167-168.
- Agrawal S. a kol., "Lichen planus po očkování proti HBV u dítěte: případová zpráva z Nepálu", J. Dermatol., září 2000, 27 (9), str. 618-620.
- Al-Khenaizan S., "Lichen planus vyskytující se po očkování proti hepatitidě B: nový případ", J. Am. Acad. Dermatol., říjen 2001, 4S (4), str. 614-615.
- Usman A. et al., „Lichenoidní erupce po očkování proti hepatitidě B: první severoamerická kazuistika". Pediatr. Dermato J., březen-duben 2001, 18 (2), str. 123-126.
- Lilic D. a kol., „Dysfunkce jater a protilátky proti DNA po očkování proti hepatitidě B“, The Lancet, listopad 1994, 344 (8932), str. 1292-1293.
- Macario F. a kol., "Nefrotický syndrom po rekombinantní vakcíně proti hepatitidě B", Clin. Nephrol., květen 1995, 43 (5), str. 349.
- Classen John Barthelow, "Dětská imunizace a diabetes mellitus", New Zealand Med. J., 24. května 1996, str. 195.
- Classen John Barthelow, Epidemie diabetu a vakcína proti hepatitidě B, New Z. Med. J., 24. května 1996, str. 366.
- Ranieri VM a kol., "Zánět jater a syndrom akutní respirační tísně u pacienta, který dostává vakcínu proti hepatitidě B: možný vztah?", Intensive Care Medicine, leden 1997, 23 (1), str. 119-121.
- Islek I. a kol., „Nefrotický syndrom po očkování proti hepatitidě B“, Pediatr. Nephrol., leden 2000, 14, str. 89-90.
- Snider GB a kol., „Možná systémová reakce na vakcínu proti hepatitidě B“, JAMA. 1. března 1985, 253 (9), str. 1260-1261.
- AADRAC, "Australian Adverse Drug Reactions Advisory Committee: Reactions to hepatitis B vakcíns", Australian Adverse Drug Reactions Bulletin, srpen 1990.
- Germanaud J. a kol., "Případ těžké cytolýzy po očkování proti hepatitidě B", Amer. J. Med., červen 1995, 98 (6), str. 595-S96.
- Fisher BL, Ed., „Vakcína proti hepatitidě B: nevyřčený příběh“, The Vaccine Reaction, National Vaccine Information Center, září 1998.
- Belkin Michael, „Vládou nařízený thalidomid pro děti“, WorldNetDaily, 25. ledna 1999, worldnetdaily.com
- Howd A., „Unce of Prevention, Pound of Misery“, Insight Magazine, 12. března 1999,
- Bethell T., „Shots in the Dark". Americký divák. Květen 1999.
- Wallstin B., „Immune to Reason“, The Houston Press, 3. června 1999, www.houstonpress.com
- Shaw FE, „Rozruch nad málo známým konzervantem, thimerosalem, narušuje politiku USA ohledně očkování proti hepatitidě B“, Zpráva o kontrole hepatitidy, léto 1999, svazek 4, č. 2.
- Spalding BJ: „Zázrak nebo vražda? Kontroverze vakcíny proti hepatitidě B, Biospace.com, 11. listopadu 1999, www.biospace.com
- Science, 31. července 1998.
- „Francie pozastavuje používání vakcíny proti hepatitidě B“. https://www.bmj.com/content/317/7165/1034.2
- Cantwell A., „Gay experiment, který odstartoval AIDS v Americe“, Not Aids, 13. ledna 2006, nyní v http://rense.com/general68/gayex.htm
- Merck & Co.t Inc., Recombivax HB vakcína proti hepatitidě B (rekombinantní), příbalový leták k červnu 2005; GlaxoSmithKline Biologicals, Engerix-B (Vakcína proti hepatitidě B (rekombinantní), příbalová informace k prosinci 2005).
- Wainwright RB a kol., „Trvání imunogenicity a účinnosti vakcíny proti hepatitidě B v populaci Yupik Eskymáků, předběžné výsledky 8leté studie“, v „Virová hepatitida a jaterní onemocnění“, Hollinger FB a kol. (eds.) , Williams & Wilkins, 1990, str. 762-766.
- Hadler SC a kol., „Hodnocení dlouhodobé ochrany vakcínou proti hepatitidě B po dobu 7 až 9 let u homosexuálních mužů“. u virové hepatitidy a onemocnění jater, Hollinger FB et al. (eds.), Williams & Wilkinst 1990, str. 766-768.
- Hadler SC a kol., „Dlouhodobá imunogenicita a účinnost vakcíny proti hepatitidě B u homosexuálních mužů“, NEJM, 24. července 1986, 315, str. 209-214.
- Stevens CE a kol., "Vyhlídky na kontrolu infekce virem hepatitidy B: důsledky očkování dětí a dlouhodobá ochrana", Pediatrics, 1992, 90, str. 170-173.
- Street AC a kol., "Přetrvávání protilátek u zdravotnických pracovníků očkovaných proti hepatitidě B", Infec. Control Hosp. Epidem., 1990, 11, pp. 525-530.
- Pasko MT a kol., "Přetrvávání anti-HBs mezi zdravotnickým personálem imunizovaným vakcínou proti hepatitidě B", American Journal of Public Health, 1990, 80, str. 590-593.
- Světová zdravotnická organizace, vakcíny proti hepatitidě B: přehodnocení imunogenicity, WHO Drug Infor., 1994, 8 (2).
- Ballinger, AB a kol., "Těžká akutní infekce hepatitidou B po očkování", The Lancet, 1994, 344, str. 1292-1293
- Goffin E. a kol., "Akutní infekce hepatitidou B po očkování", The Lancet, 1995, 345, str. 263.
Vaccines: A Guide to Informed Choice Neil Z. Miller (autor) a Claudia Benatti (překladatel)
Vydání Terra Nuova, 2018

