Může vakcína proti tetanu způsobit zranění a/nebo smrt?

Následující článek se pokouší osvětlit rozsáhlý svět nežádoucích účinků se specifickým pohledem na ten proti tetanu, ale vyzýváme vás, abyste si přečetli všechna níže uvedená zaměření, abyste pochopili další související problémy, jako je problém více vakcín. hypersenzitivita na jednu nebo více vakcínových sloučenin, problém SIDS a adjuvans. Většina vakcín na trhu je vyráběna pro komerční účely v často více formulacích, což činí téma poškození vakcín mnohem širší.
Problém více vakcín (kliknutím otevřete)
Problém více vakcín

Současné očkovací kalendáře, zejména pro dětský věk, počítají s podáním více antigenů a vakcín v jednom sezení, což zvýhodňuje komfort na úkor bezpečnosti. Abychom mohli pronést konkrétní projev o bezpečnosti vakcín, musíme nutně vzít v úvahu složitost tohoto fenoménu a doporučit všem čtenářům, aby se dostatečně informovali o všech aspektech očkování, výhodách a nevýhodách.
Dr. Russell Blaylock, klinický asistent profesora neurochirurgie na University of Mississippi Medical Center, léta studoval "toxickou synergii" a byl schopen pozorovat, že když dva slabě toxické pesticidy, kde ani jeden není schopen způsobit Parkinsonův syndrom u pokusných zvířat, se vzájemně kombinují, mohou způsobit onemocnění i rychle a srovnává tento jev s jevem více vakcín podaných současně: "Očkování, pokud je příliš mnoho a příliš blízko u sebe, se chovají jako chronické onemocnění".(). Ostatní Dvě studie potvrdily, že náhlá smrt kojence může nastat po naočkování více vakcín v jednom podání.(před naším letopočtem)
Studie publikovaná v Human and Experimental Toxicology ukázala, že země, které dětem předepisují více vakcín, mívají vyšší kojeneckou úmrtnost.(D) Například ve Spojených státech, kde děti dostávají 26 vakcín, zemře více než 6 dětí na 1000 12 živě narozených dětí, zatímco ve Švédsku a Japonsku, kde je aplikováno 3 dětských vakcín, jsou hlášena 1000 úmrtí na každých XNUMX XNUMX živě narozených dětí. Ve výše uvedené studii je také zvažována souvislost mezi vakcínami a SIDS.
Ze švýcarské studie publikované v roce 2005 v European Journal of Pediatrics(E) z toho vyplývá, že pokud jde o účinky na předčasně narozené děti, je výskyt recidivující nebo zvýšené apnoe a bradykardie po podání hexavalentních vakcín 13 %. Ten samý rok publikoval stejný časopis německou studii, která zkoumala náhlá úmrtí kojenců po šestimocném. Autoři píší: «Tyto výsledky, založené na spontánních zprávách, neprokazují kauzální vztah mezi očkováním a náhlým úmrtím kojence, ale představují signál týkající se jednoho ze dvou dostupných hexavalentů; signál, který by měl vést k intenzivnějšímu sledování náhlých úmrtí kojenců po očkování“.(F)
V roce 2006 byla publikována v lékařském časopise Vaccine(G) dopis od týmu výzkumníků z Mnichovské univerzity, který hlásil „šest případů náhlého úmrtí kojenců po šestimocném očkování. Všechny byly nalezeny mrtvé bez vysvětlení 1-2 dny po očkování“. Byly klasifikovány jako typické případy náhlého úmrtí kojenců, ale autoptické ověření odhalilo neuropatologické a histologické abnormality a všechny děti vykazovaly významný otok mozku, což z nich činilo výjimku ve srovnání s ostatními případy SIDS (Syndrom náhlého úmrtí dětí). Vědci napsali, že „Před zavedením hexavalentní vakcíny (v letech 1994-2000) jsme pozorovali případ pouze jednoho ze 198 dětí s náhlým úmrtím kojence, které zemřelo brzy po očkování proti DTP. V letech 2001 až 2004 však identifikovali pět podobných případů ze 74 se SIDS. To by znamenalo třináctinásobný nárůst.“
Také v roce 2006 na Virchows Archive(H), tým z Ústavu patologie Univerzity v Miláně napsal: «Odborníci z Evropské agentury pro hodnocení léčivých přípravků analyzovali možnost, že by mohla existovat souvislost mezi šestivalentními vakcínami a některými případy úmrtí. Mezi účastníky byli patologové se zkušenostmi s vakcínami a syndromem náhlého úmrtí kojenců, kteří prováděli pitvy. Pokud však víme, vyšetření mozkového kmene a krevního srdce na sériových řezech byla věnována malá pozornost a neexistovala možnost stanovit spouštěcí roli. vakcíny pro tato úmrtí. Zde uvádíme případ 3měsíční holčičky, která náhle zemřela po šestimocném očkování. Vyšetření mozkového kmene na sériových řezech odhalilo oboustrannou hypoplazii nucleus arcuate. Převodní systém srdce měl přetrvávající fetální disperzi a degeneraci. Tento případ nabízí jedinečné pochopení možné role hexavalentní vakcíny při vyvolání smrtelných následků u zranitelného dítěte. Jakýkoli případ náhlé a neočekávané smrti, ke kterému dojde brzy po narození nebo v raném dětství, zejména po očkování, by měl vždy projít úplnou pitvou podle pokynů.
Reference
- Blaylock R, "Očkování: skrytá nebezpečí", The Blaylock Wellness Report, květen 2004, s. 1-9
- Ottaviani G. et al., "Syndrom náhlého úmrtí kojenců (SIDS) krátce po hexavalentní vakcinaci: další patologie při podezření na SIDS?", Vircows Archiv., 2006, 448, pp. 100-104.
- Zinka B. et al., "Nevysvětlené případy náhlé smrti kojenců krátce po hexavalentní vakcinaci", Vaccine, červenec 2006, 24 (31-32), str. 5779-5780.
- Miller NZ a kol. ,“Míra kojenecké úmrtnosti klesla proti počtu dávek vakcíny běžně podávaných: existuje biochemická nebo synergická toxicita??", Hum. Exp. Toxicol., květen 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Problém hliníku (kliknutím otevřete)
Hliník ve vakcínách: co rodiče potřebují vědět

1. Co je hliník?
Hliník je stříbřitě bílý lehký kov, tvárný a odolný. Díky těmto vlastnostem je použitelný v mnoha průmyslových odvětvích a výrobcích, včetně strojů, stavebnictví, skladů, nádobí, kuchyňského náčiní, textilu, barviv a kosmetiky. Hliník je také nejrozšířenějším kovem v zemské kůře a prakticky veškerý hliník v životním prostředí se nachází v půdě. Hliník se však přirozeně nenachází ve významných množstvích v živých organismech (jako jsou rostliny a zvířata) a nemá žádnou známou biologickou funkci. V průběhu minulého století vedlo používání hliníku v některých výrobcích ke zvýšené expozici člověka. Hlavními zdroji expozice jsou potraviny obsahující hliník (např. prášek do pečiva, zpracované potraviny, kojenecká výživa atd.), lékařské produkty (např. antiperspiranty, antacida atd.), injekce proti alergii a vakcíny.1-3
2. Proč je hliník přítomen ve vakcínách?
Některé vakcíny používají jako adjuvans sloučeniny hliníku (hydroxid hlinitý a fosforečnan hlinitý), což jsou složky, které zvyšují imunitní odpověď na antigen (cizí látku).4-5 Americký úřad pro potraviny a léčiva (FDA) říká, že pokud by některé vakcíny neobsahovaly hliník, imunitní odpověď, kterou spouštějí, by se mohla snížit.6
3. Které vakcíny obsahují hliník?
Následující vakcíny obsahují hliník a podávají se kojencům, dětem a dospívajícím (obr. 1):
- Hepatitida B (HepB)
- šestimocný
- Záškrt, tetanus a černý kašel (DTaP a Tdap)
- Haemophilus influenzae typ b (PedvaxHIB)
- Pneumokok (PCV)
- Hepatitida A (HepA)
- Lidský papilomavirus (HPV)
- Meningokok B (MenB)
Obrázek 1: Od narození do 18 let se aplikuje až 22 dávek vakcín obsahujících hliník7-8
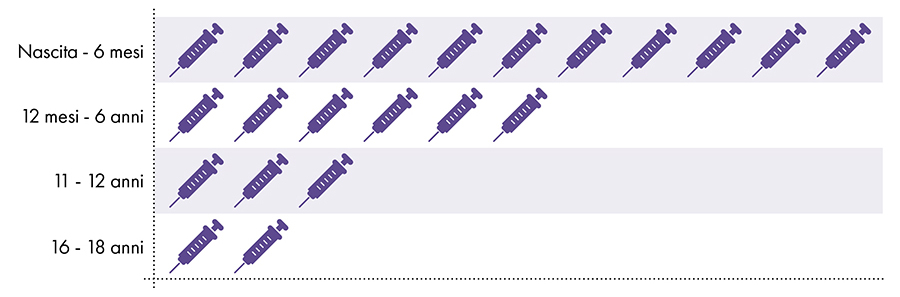
4. Je vystavení hliníku bezpečné?
FDA od roku 1975 považuje hliník obecně za bezpečný (GRAS).9 Před rokem 1990 však neexistovala žádná technologie, která by přesně detekovala malá množství hliníku podávaného subjektům ve vědeckých studiích.10 V důsledku toho nebylo známo množství hliníku, které by mohlo být absorbováno před nástupem nepříznivých účinků.
Od 1990. let XNUMX. století bylo díky technologickému pokroku pozorováno, že malé množství hliníku, které zůstává v lidském těle, zasahuje do řady buněčných a metabolických procesů v nervovém systému a tkáních jiných částí těla.1-10-11 Největší negativní účinky hliníku byly pozorovány v nervovém systému a sahají od zhoršené motoriky až po encefalopatii (změněný duševní stav, změny osobnosti, poruchy myšlení, ztráta paměti, záchvaty, kóma a další).2-12
Ministerstvo zdravotnictví a sociálních služeb Spojených států amerických (HHS) uznává hliník jako známý neurotoxin.2 Kromě toho FDA varoval před riziky toxicity hliníku u kojenců a dětí.13
FEDERÁLNÍ REGISTR: Deník vlády Spojených států"I donošení kojenci s normální funkcí ledvin mohou být ohroženi rychlým růstem a nezralostí mozku a skeletu a také nezralostí hematoencefalické bariéry. Do 1. až 2. roku věku mají kojenci nižší glomerulární filtrace než u dospělých, což ovlivňuje jejich funkci ledvin. Agentura se obává, že malé děti a osoby s nezralou funkcí ledvin jsou vystaveny zvýšenému riziku expozice hliníku.“ |
5. Kolik orálního hliníku není bezpečné?
V roce 2008 Agentura pro registr toxických látek a nemocí (ATSDR), divize HHS, použila studie o neurotoxických účincích hliníku k určení, že ne více než 1 miligram (1.000 XNUMX mikrogramů) hliníku na kilogram tělesné hmotnosti za den. vyhnout se negativním účinkům hliníku.2
6. Jaké množství vstřikovaného hliníku není bezpečné?
Pro stanovení množství hliníku, které lze bezpečně vstříknout, je nutné převést orální limit hliníku podle ATSDR. Limit ATSDR pro perorální hliník (1.000 0,1 mikrogramů hliníku na kilogram tělesné hmotnosti za den) je založen na XNUMX % perorálního hliníku, který je absorbován do krevního řečiště, protože trávicí trakt blokuje téměř veškerý perorální hliník.2 Naopak hliník injikovaný intramuskulárně obchází trávicí trakt a 100 % hliníku se může časem vstřebat do krevního řečiště (tj. podíl absorbovaného hliníku je 1.000krát větší). Aby byla zohledněna tato různá množství absorpce, musí se orální limit hliníku ATSDR vydělit 1000 1. Tento převod vede k limitu hliníku v krvi odvozenému z ATSDR ve výši 0,1 mikrogram hliníku (1.000 % z 1 3 mikrogramů) na kilogram tělesné hmotnosti. denně. Aby se předešlo neurotoxickým účinkům hliníku, nemělo by se denně do krevního oběhu dostat více než XNUMX mikrogram hliníku na kilogram tělesné hmotnosti. Obrázek XNUMX ukazuje limit hliníku v krvi odvozený od ATSDR pro kojence různého věku na základě jejich hmotnosti.
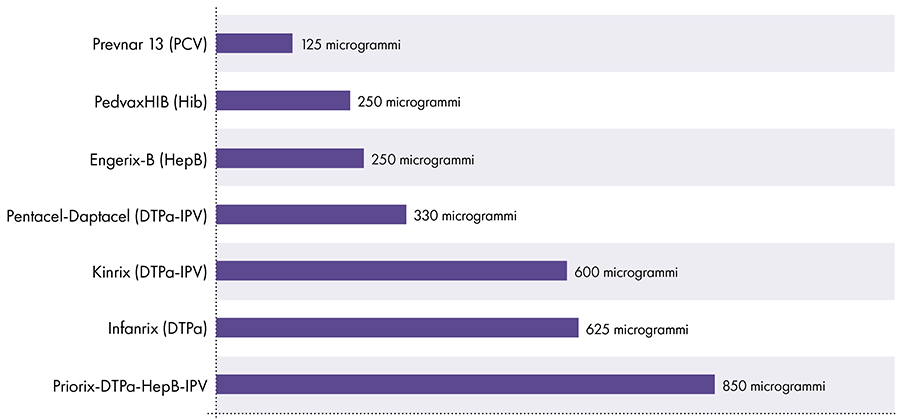
7. Kolik hliníku je ve vakcínách?
Množství hliníku ve vakcínách se liší.16 V roce 1968 federální vláda USA stanovila limit pro množství hliníku ve vakcínách na 850 mikrogramů na dávku na základě množství hliníku potřebného k tomu, aby byly některé vakcíny účinné.6-17 V důsledku toho se množství hliníku v kojeneckých vakcínách obsahujících hliník pohybuje od 125 do 850 mikrogramů na dávku. Obrázek 4 ukazuje obsah hliníku v jedné dávce různých vakcín podaných dětem.
8. Srovnávaly nějaké studie množství hliníku ve vakcínách s limitem odvozeným od Agentury pro registr toxických látek a nemocí (ATSDR)?
V roce 2011 byla publikována studie, která měla za cíl porovnat množství hliníku ve vakcínách s limitem průtoku krve stanoveným ATSDR.18 Tato studie však nesprávně založila své výpočty na 0,78 % perorálního hliníku absorbovaného do krevního řečiště, spíše než na hodnotě 0,1 %, kterou používá ATSDR ve svých výpočtech.19-20 V důsledku toho studie z roku 2011 předpokládala, že téměř 8krát (0,78 % / 0,1 %) se hliník může bezpečně dostat do krevního oběhu, což vedlo k nesprávnému závěru.
9. Je expozice hliníku z vakcín bezpečná?
Vakcíny se aplikují intramuskulárně a rychlost, jakou hliník z vakcín migruje z lidských svalů do krevního řečiště, není známa. Studie na zvířatech naznačují, že hliníku z vakcín může v důsledku mnoha proměnných trvat několik měsíců až více než rok, než se dostane do krevního řečiště.21-23 Vzhledem k tomu, že kumulativní expozice hliníku z vakcín u dětí mladších jednoho roku překračuje denní limit stanovený ATSDR o několik stovek (obr. 3 a 4), byl by limit stále překročen, pokud by se hliník z vakcín dostal do krevního oběhu v průběhu asi rok. Některé studie navíc ukázaly, že hliník z vakcín je absorbován imunitními buňkami a dostává se do částí těla daleko od místa vpichu, včetně mozku.24
Rozsah nepříznivých účinků hliníku ve vakcínách není znám, protože nebyly provedeny bezpečnostní studie srovnávající populaci očkovanou vakcínami obsahujícími hliník s populací neočkovanou takovými vakcínami.
Hliníkové omezení průtoku krve odvozené z ATSDR2-14-15
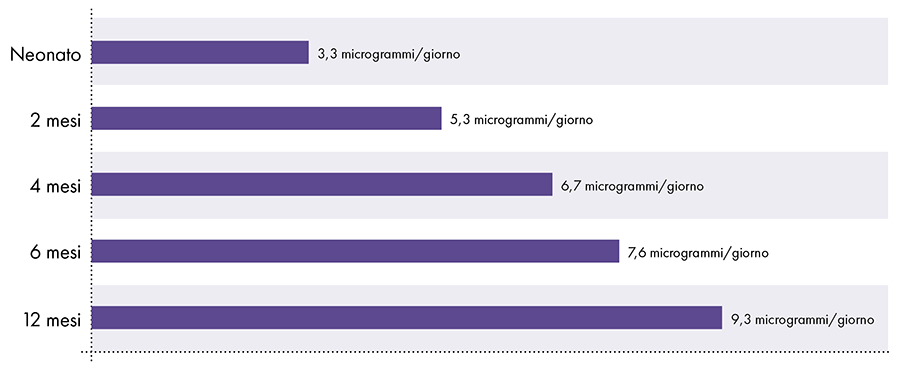 Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Množství hliníku ve vakcínách
Reference
- Americká akademie pediatrie, Výbor pro výživu. Toxicita hliníku u kojenců a dětí. Pediatrie. březen 1996, 97 (3): 413.
- Agentura pro registr toxických látek a nemocí (ATSDR). Toxikologický profil pro hliník. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Hliník v potravinách – povaha a přínos potravinářských přídatných látek. In: El-Samragy Y, editor. Potravinová přísada. Rijeka (Chorvatsko): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. K pochopení adjuvantního působení hliníku. Nat Rev Immunol. 2009. dubna 9 (4): 287.
- Volk VK, Bunney WE. Imunizace proti záškrtu tekutým toxoidem a toxoidem vysráženým kamencem. Am J Veřejné zdraví Zdraví národů. července 1942, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Hliníkové soli ve vakcínách – perspektiva USA. Vakcína. 2002. května 31, 20 Suppl 3: S18-22.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. Vakcíny licencované pro použití ve Spojených státech amerických; [aktualizováno 2018. února 14; citováno 2018. února 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Doporučené schéma imunizace pro děti a dospívající ve věku 18 let nebo mladší, Spojené státy americké, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. SCOGS (Výběrový výbor pro látky GRAS); [citováno 2018. srpna 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Kněz ND. Biologické chování a biologická dostupnost hliníku u člověka, se zvláštním odkazem na studie využívající hliník-26 jako indikátor: přehled a aktualizace studie. J Environ Monit. 2004;6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Hliník ve výrobcích pro parenterální výživu dětí: měřeno versus obsah na etiketě. J Pediatr Pharmacol Ther. 2011, 16 (2): 92-7.
- Sedman A. Toxicita hliníku v dětství. Pediatr Nephrol. 1992 (6): 4-383, červenec 93.
- US Food and Drug Administration, Department of Health and Human Services. Pravidla a regulace. Registrátor Fedu. června 2003, 68 (100): 34286.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro chlapce v grafech délky k věku a hmotnosti k věku; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro grafy délky dívek na věk a hmotnosti na věk; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Department of Health and Human Services. Revize požadavků na základní materiály. Konečné pravidlo. Registrátor Fedu. 2011. dubna 13, 76 (71): 20513-8.
- Úřad federálního rejstříku, Národní archivy a spisová služba, Správa všeobecných služeb. Pravidla a regulace. Registrátor Fedu. 1968 leden; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím stravy a očkování. Vakcína. 2011. listopadu 28, 29 (51): 9538-43.
- Miller S, lékaři pro informovaný souhlas. Erratum v 'Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování.' In: ResearchGate. Berlín (Německo): ResearchGate GmbH; 2020. března 6 [citováno 2020. března 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Lékaři pro informovaný souhlas. Newport Beach (CA): Lékaři pro informovaný souhlas. Erratum v „Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování“; [citováno 2020. března 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In vivo absorpce adjuvans vakcín obsahujících hliník pomocí 26Al. Vaccine 1997 srpen-září, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Test hliníku a hodnocení lokální reakce v několika časových bodech po intramuskulárním podání vakcín obsahujících hliník u opice Cynomolgus. Vakcína. 2005. února 3, 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Hliník v plazmě a tkáních po intramuskulární injekci lidských vakcín s adjuvans u potkanů. Arch Toxicol. říjen 2019, 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritická analýza referenčních studií toxikokinetiky adjuvans na bázi hliníku. J Inorg Biochem. 2018 duben; 181: 87-95.
Článek přeložil Lékaři pro informovaný souhlas
Mnoho publikovaných studií uvádělo závažné nežádoucí účinky po očkování proti tetanovému toxoidu. Nežádoucí účinky zahrnují anafylaxi,(1-2) pažní neuritida,(3) bulózní pemfigoid(4-5-6) Guillain-Barre syndrom (GBS),(7-8) akutní diseminovaná encefalomyelitida (ADEM),(9) multiformní erytém,(10-11-12) myokarditida,(13-14-15-16-17) artritida,(18-19) oční neuritida,(20-21) a další autoimunitní poruchy.(22-23)
Nežádoucí účinky hlášené po očkování proti tetanu byly shromážděny německým autorem(24) a Monitorovacím systémem pro nežádoucí příhody po imunizaci(25) a lze je rozdělit do dvou skupin: lokální nežádoucí účinky a systémové nežádoucí účinky.
Můžeme říci, že tyto účinky závisí na různých faktorech:
- věk příjemce vakcíny;
- fyziologické a patologické stavy příjemce vakcíny;
- počet odebraných dávek vakcíny;
- množství podaného tetanového toxinu;
- přítomnost dalších bakteriálních a/nebo virových antigenů spojených s tetanovým toxinem;
- přítomnost adjuvans nebo jiných souvisejících toxických látek.
Má se za to, že nežádoucí účinky způsobené prvním podáním vakcíny proti tetanu se překrývají s těmi, které se mohou vyskytnout při posilovacích dávkách, a pokud jsou podávány příliš často, vytvářejí stav hyperimunizace, který významně zvyšuje riziko poškození vakcíny, a z tohoto důvodu mnoho studií vědci doporučují nepodávat posilovací dávky této vakcíny v intervalech kratších než 10 let.(26) K tomu se přidává, že dětský tetanový anatoxin obsažený v kombinovaných vakcínách je větší než anatoxin používaný pro dospělé, protože kvůli imunitní nezralosti je nutné novorozence nadměrně stimulovat, aby se dosáhlo adekvátní protilátkové odpovědi.
Nejčastější a obvykle mírnější a přechodné lokální nežádoucí účinky očkování proti tetanu(32) jsou způsobeny zvláštní přecitlivělostí na tetanový toxin a jsou reprezentovány: bolestí (50-85 % případů), zarudnutím, ztvrdnutím a otokem (25-30 % případů) až abscesem.(27) V některých případech byly místní reakce zvláště závažné, jako je Lyellův syndrom (nebo syndrom opařené kůže), který má úmrtnost 50 % u dospělých a 25 % u dětí.(28)
Všechny lokální nežádoucí účinky jsou častější, pokud je vakcína podána spíše subkutánně než intramuskulárně. Tyto účinky se zvyšují se zvyšujícím se množstvím naočkovaného tetanového toxinu(29) a to se vyskytuje zejména u jedinců, kteří dostali několik a často injekcí vakcíny proti tetanu.(30-27)
Studie z roku 2017 ukazuje, že u dětí s rozsáhlými otoky končetin po podání čtvrté dávky vakcíny proti záškrtu, tetanu a acelulárnímu pertusi byla recidiva lokální reakce zvláště častá po páté dávce vakcíny (78 % očkovaných).(31)
Nežádoucí účinky se také zvyšují, pokud je vakcína proti tetanu kombinována s jinými vakcínami, spíše než pokud se používá samostatně.(32)
V roce 1994 Americký lékařský institut (IOM) oznámil, že existují přesvědčivé vědecké důkazy k závěru, že vakcíny proti tetanu, DT a Td mohou způsobit Guillain-Barreův syndrom (GBS), včetně úmrtí, brachiální neuritidy a úmrtí na anafylaxi (šok ).(33) IOM také uznala, že existuje individuální náchylnost k očkovacím reakcím z genetických, biologických a ekologických důvodů, ale že dodavatelé vakcín nemohou přesně předpovědět, kdo utrpí komplikace, zranění nebo smrt, než bude vakcína aplikována v důsledku očkování.(34)
V roce 2017 výzkumníci z Guineje-Bissau porovnali úmrtnost kojenců očkovaných proti záškrtu, tetanu a celobuněčnému pertusi (DTP) ve věku 3 až 5 měsíců s úmrtností kojenců, kteří ještě nebyli očkováni DTP vakcínou. úmrtnost byla významně vyšší u kojenců očkovaných DTP než u dětí, které ještě nebyly očkované. Výzkumníci také poznamenali, že pokud byla orální vakcína proti obrně (OPV) podána současně s vakcínou DTP, míra úmrtnosti ze všech příčin se snížila, ale stále zůstala výrazně vyšší než u neočkovaných dětí.(35)
Důležitým lokálním nežádoucím účinkem, který lze s relativní četností nalézt u dospělých, je neuropatie brachiálního plexu,(36) pokud je očkování provedeno do paže a objeví se několik dní nebo týdnů po očkování(37). Tato neuropatie je charakterizována svalovou bolestí, slabostí a úbytkem svalů. Kromě neuropatií lokalizovaných v oblasti, kde byla vakcína naočkována, najdeme v literatuře také různé další zprávy o lokalizovaných neuropatiích způsobených podáním antitetanu,(38-39) jako je postižení různých hlavových nervů(40-41) nebo oční nervy(42) nebo recidivující laryngeální nerv.(43)
Nejčastější systémové účinky očkování proti tetanu(32) lze rozdělit na:
- nespecifické účinky, jako je horečka, bolest hlavy (což je poměrně častý nežádoucí účinek po očkování), myalgie, kopřivka, nevolnost, zvracení,(44) astenie, anorexie, podrážděnost, somnolence,
- specifické účinky, jako je anafylaktický šok, generalizovaná neuropatie, intenzivní bolesti břicha s průjmem, různé zánětlivé formy, i závažné, v některých vzácných případech i smrt.
Mezi všemi nejčastějšími a četnými systémovými účinky najdeme neurologická poškození(45) a mezi nimi je určitě na prvním místě polyneuropatie postihující periferní nervový systém, která je častější než postižení centrálního nervového systému a může se objevit jak po první dávce vakcíny, tak po třetí.(46) Polyneuropatie se obvykle objeví během několika minut až několika hodin (v případě akutních alergických reakcí) nebo během 12-48 hodin (v případě opožděných alergických reakcí) nebo nejvýše do 4-14 dnů po očkování (v případě neuritida).(47) Polyneuropatie může postihnout několik nervů nebo velké oblasti těla až po postižení dřeně a mozkové kůry a může být způsobena pouze vakcínou proti tetanu(48) nebo z aplikace jiných vakcín kombinovaných s vakcínou proti tetanu.(36-49)
Mezi různými formami polyneuropatie byly hlášeny následující: demyelinizační polyneuropatie;(50) asymetrická polyneuropatie; polyradikuloneuritida s parézou močového měchýře a konečníku;(51) skarlatiniformní vyrážka,(40) akutní kopřivkové reakce,(44) paralýza dýchacích nervů (Landryho obrna), která může vést i ke smrti;(52-53) tetanické křeče;(44) příčná myelitida;(54) syndrom Guillain-Barré;(55-56) periferní motorická afázie;(57) a smrt.(28)
Reference (kliknutím otevřete)
- Mayorga C, Torres MJ, Corzo JL a kol. Okamžitá alergie na vakcínu proti tetanovému toxoidu: stanovení protilátek imunoglobulinu E a imunoglobulinu G proti alergenním proteinům. Ann Allergy Asthma Immunol. 2003 Feb;90(2):238-43.
- Martín-Muñoz MF, Pereira MJ, Posadas S a kol. Anafylaktická reakce na vakcínu proti záškrtu a tetanu u dítěte: stanovení specifických IgE/IgG a studie zkřížené reaktivity. Vakcína. 2002 Sep 10;20(27-28):3409-12.
- Hamati-Haddad A, Fenichel GM. Brachiální neuritida po rutinní dětské imunizaci proti záškrtu, tetanu a černému kašli (DTP): zpráva o dvou případech a přehled literatury. Pediatrie. 1997 Apr;99(4):602-3.
- Fournier B, Descamps V, Bouscarat F a kol. Bulózní pemfigoid vyvolaný očkováním. Br J Dermatol. 1996 Jul;135(1):153-4.
- Venning VA, Wojnarowska F. Indukovaný prudký pemfigoid. Br J Dermatol. 1995 May;132(5):831-2.
- Sezin T, Egozi E, Hillou W a kol. Slizniční pemfigoid anti-laminin-332 vznikající po očkování proti záškrtu a tetanu. JAMA Dermatol. 2013 Jul;149(7):858-62.
- Bakshi R, Graves MC. Guillain-Barrého syndrom po kombinované vakcinaci tetanus-difterický toxoid. J Neurol Sci. 1997 Apr 15;147(2):201-2.
- Newton N Jr, Janati A. Guillain-Barrého syndrom po očkování purifikovaným tetanovým toxoidem. South Med J. 1987 Aug;80(8):1053-4.
- Hamidon BB, Raymond AA. Akutní diseminovaná encefalomyelitida (ADEM) projevující se sekundárními záchvaty po očkování proti tetanovému toxinu. Med J Malajsie. 2003 Dec;58(5):780-2.
- Griffith RD, Miller z III Erythema multiforme po očkování proti záškrtu a tetanu. J Am Acad Dermatol. 1988 Oct;19(4):758-9.
- Frederiksen MS, Brenøe E, Trier J. Erythema multiforme minor po očkování dětskými vakcínami. Scand J Infect Dis. 2004;36(2):154-5.
- Kaur S, Handa S. Erythema multiforme po očkování u kojence. Indický J Dermatol Venereol Leprol. 2008 May-Jun;74(3):251-3.
- Kumar V, Sidhu N, Roy S, Gaurav K. Myokarditida po očkování proti záškrtu, celobuněčnému pertusi a tetanovému toxoidu u malého dítěte. Ann Pediatr Cardiol. 2018 May-Aug;11(2):224-226
- Yamamoto H, Hashimoto T, Ohta-Ogo K a kol. Případ biopsií prokázané eozinofilní myokarditidy související s imunizací tetanovým toxoidem. Cardiovasc Pathol. 2018 Listopad - Prosinec;37:54-57
- Wu SJ, Sun S, Li JY a kol. Akutní fulminantní myokarditida po očkování proti záškrtu, dětské obrně a tetanu. Asian Cardiovasc Thorac Ann. 2006 Dec;14(6):e111-2.
- Dilber E, Karagöz T, Aytemir K a kol. Akutní myokarditida spojená s očkováním proti tetanu. Mayo Clin Proc. 2003 Nov;78(11):1431-3.
- Amsel SG, Hanukoglu A, Fried D, Wolyvovics M Myokarditida po trojité imunizaci. Arch Dis Child, 1986 duben; 61 (4): 403–405.
- Jawad AS, Scott DG Imunizace spouštějící revmatoidní artritidu? Ann Rheum Dis. únor 1989; 48(2):174.
- Kaul A, Adler M, Alokaily F, Jawad A Recidiva reaktivní artritidy po posilovací dávce tetanového toxoidu Ann Rheum Dis. únor 2002; 61(2):185.
- O'Brien P, Wong RW Optická neuritida po kombinovaném očkování proti záškrtu, tetanu, černému kašli a inaktivovanému polioviru: kazuistika. J Med věc Rep. 2018 Nov 30;12(1):356
- Cabrera-Maqueda JM, Hernández-Clares R, Baidez-Guerrero AE et al. Zánět zrakového nervu v těhotenství po očkování Tdap: Hlášení dvou případů. Clin Neurol Neurosurg. září 2017;160:116-118.
- Ruhrman-Shahar N, Torres-Ruiz J, Rotman-Pikielny P, Levy Y Autoimunitní reakce po očkování proti tetanu - popis čtyř případů a přehled literatury. Immunol Res. 2017 Feb;65(1):157-163.
- Shoenfeld Y, Aron-Maor A. Očkování a autoimunita – „vakcinóza“: nebezpečné spojení? J Autoimunitní. 2000 Feb;14(1):1-10.
- Roční vedlejší účinky léků. Svazek 12. (Elsevier, I988).
- Roční vedlejší účinky léků. Svazek 13. (Elsevier, 1989).
- Adebahr, G. [Smrt šokem při první preventivní subkutánní injekci tetanového séra]. Dtsch. Z. Gesamte Gerichtl. Med., 41, 405-8 (1952).
- Nežádoucí účinky léků roční. Svazek 11. (Elsevier, 1987).
- Frank, K.-H. Todliche Imptkomplikationen (Lyell-Syndrom) nach Tetatoxoid. Dt. Gesundh.wes. 29, 1430-4 (1974).
- Relihan, M. Reakce na tetanový toxoid. J. Jr. Med. Assoc. 62, 430-4 (1969).
- Levine, L., Ipsen, J. & McComb, J. Imunizace dospělých. Příprava a hodnocení kombinovaných tekutých tetanových a difterických toxoidů pro dospělé. Am. J. Hyg. 73, 20 (1961).
- Zafack, JG a kol. Riziko opakování nežádoucích příhod po imunizaci: Systematický přehled. Pediatrie 140, (2017).
- Cody, CL, Baraff, LJ, Cherry, JD, Marcy, SM & Manclark, ČR Povaha a míra nežádoucích reakcí spojených s imunizací DTP a DT u kojenců a dětí. Pediatrics 68, 650-60 (1981).
- Výbor lékařského institutu pro kontrolu nežádoucích účinků vakcín. Nežádoucí účinky vakcín: důkazy a kauzalita. (Hodnocení biologických mechanismů pro nepříznivé události: zvýšená náchylnost). Washington DC.: Národní akademie Press. 1994. Kapitola 5 Toxoidy záškrtu a tetanu str. 67-117
- Výbor lékařského institutu pro kontrolu nežádoucích účinků vakcín. Nežádoucí účinky vakcín: důkazy a kauzalita. (Hodnocení biologických mechanismů pro nepříznivé události: zvýšená náchylnost). Washington DC.: Národní akademie Press. 2012
- Mogensen SW, Andersen A, Rodrigues A et al. Zavedení vakcíny proti záškrtu, tetanu a černému kašli a orální vakcíny proti dětské obrně mezi malými kojenci v městské africké komunitě: přirozený experiment. EBioMedicine. 2017; 17: 192-198.
- Tsairis,P., Dyck,PJ & Mulder,DW Přirozená historie neuropatie brachiálního plexu. Zpráva 99 pacientů. Arch. Neuro/. 27, 09-17 (1972).
- Blumstein, GI & Kreithen, H. Periferní neuropatie po podání tetanového toxoidu. JAMA 198, I 030-1 (1966)
- Gersbach, P. & Waridel, D. [Paralýza po prevenci tetanu]. Švýcarsko. Wochenschr. 106, 150-3 (1976).
- Baust, W., Meyer, D. & Wachsmuth, W. Periferní neuropatie po podání tetanového toxoidu. J. Neuro/. 222, 131-33 (1979).
- Cutter, R. Postižení sluchového nervu po tetanovém antitoxinu: první hlášený případ. J Am Med Ass 106, 006-7 (I 936).
- Wirth, G. Reversibele kochlearisschadigung nach Tetanus-injection. Munch Med Wschr 101, 349-81 (1965).
- Harrer, G., Melnizky, V. & Wendt, H. Akkomodationsparese und Schlucklahmung nach Tetanus-Toxoid-Auffrlschungsimpfung. Wien Med Wochenschr 15, 296-7 (1971)
- Bašek, M. Jednostranné! paralýza hlasivek po podání tetanového antitoxinu (TAT). Laryngoskop 68, 805-807 (1958).
- Cunningham, AA Anafylaxe po injekci tetanového toxoidu. Br.Med.J.2, 522-3 (1940).
- Ridder. Plexuslahmung nach Schutzimpfung mit Tetanusserum. Žvýkat. med. Wsch. 81, 1035 (1934).
- Holliday, PL & Bauer, RB Polyradikuloneuritida sekundární k imunizaci tetanovými a difterickými toxoidy. Arch Neuro/40, 56-57 (1983).
- Ehrengut, W. Reaktionen der Wundstarrkrampfimpfung. Dtsch Med Wochenschr 95, 1799-1800 (1970).
- 1Woolling, KR & Rushton, JG Sérová neuritida; zpráva o dvou případech a stručný přehled syndromu. arch. Neuro/. Psychiatry 64, 568-73 (1950).
- Martin, GI & Weintraub, MI Brachiální neuritida a obrna sedmého nervu: vzácné riziko očkování proti DPT. Clin. Dětský lékař. (phila). 12, 506-507 (1973).
- Pollard, JD & Selby, G. Recidivující neuropatie v důsledku tetanového toxoidu. Zpráva o případu. J. Neuro/. Sci., 37, 113-125 (1978).
- Nežádoucí účinky léků ročně/. Svazek 09. (Elsevier, 1985).
- Harrfeldt, HP [Smrt po aktivní a pasivní imunizaci proti tetanu]. Monatsschr. Unfallheilkd. Versicherungsmed. 66, 36-7 (1963).
- Elsasser, G. Zur Entstehung, Localization und Verhiitung der Serumpolyneuritis. Nervenarzt 15, 280 (1942).
- Whittle, E. & Robertson, NR Transverzní myelitida po imunizaci proti záškrtu, tetanu a dětské obrně. Br.Med.J. 1, 1450 (1977).
- Nežádoucí účinky léků ročně/. Svazek 14. (Elsevier, 1990).
- Hopf, HC [Guillain-Barrého syndrom po podání tetanového toxoidu. Průzkum a zpráva o případu]. Aktuální Neuro/. 7, 195-200 (1980).
- Palfty, G. F. & Merei, T. Bez názvu. Orv. Hetil. 102, 2321 (1961).
Tento článek shrnuje a překládá Vakcína Národní informační centrum.

