Může vakcína proti pneumokokům způsobit zranění a/nebo smrt?

DŮLEŽITÁ POZNÁMKA: Corvelva vás vyzývá, abyste získali podrobné informace přečtením všech sekcí a odkazů, jakož i produktových letáků a technických listů výrobce, a abyste si promluvili s jedním nebo více důvěryhodnými odborníky, než se rozhodnete očkovat sebe nebo své dítě. Tyto informace slouží pouze pro informační účely a nejsou určeny jako lékařská rada.
Problém více vakcín (kliknutím otevřete)
Problém více vakcín

Současné očkovací kalendáře, zejména pro dětský věk, počítají s podáním více antigenů a vakcín v jednom sezení, což zvýhodňuje komfort na úkor bezpečnosti. Abychom mohli pronést konkrétní projev o bezpečnosti vakcín, musíme nutně vzít v úvahu složitost tohoto fenoménu a doporučit všem čtenářům, aby se dostatečně informovali o všech aspektech očkování, výhodách a nevýhodách.
Dr. Russell Blaylock, klinický asistent profesora neurochirurgie na University of Mississippi Medical Center, léta studoval "toxickou synergii" a byl schopen pozorovat, že když dva slabě toxické pesticidy, kde ani jeden není schopen způsobit Parkinsonův syndrom u pokusných zvířat, se vzájemně kombinují, mohou způsobit onemocnění i rychle a srovnává tento jev s jevem více vakcín podaných současně: "Očkování, pokud je příliš mnoho a příliš blízko u sebe, se chovají jako chronické onemocnění".(). Ostatní Dvě studie potvrdily, že náhlá smrt kojence může nastat po naočkování více vakcín v jednom podání.(před naším letopočtem)
Studie publikovaná v Human and Experimental Toxicology ukázala, že země, které dětem předepisují více vakcín, mívají vyšší kojeneckou úmrtnost.(D) Například ve Spojených státech, kde děti dostávají 26 vakcín, zemře více než 6 dětí na 1000 12 živě narozených dětí, zatímco ve Švédsku a Japonsku, kde je aplikováno 3 dětských vakcín, jsou hlášena 1000 úmrtí na každých XNUMX XNUMX živě narozených dětí. Ve výše uvedené studii je také zvažována souvislost mezi vakcínami a SIDS.
Ze švýcarské studie publikované v roce 2005 v European Journal of Pediatrics(E) z toho vyplývá, že pokud jde o účinky na předčasně narozené děti, je výskyt recidivující nebo zvýšené apnoe a bradykardie po podání hexavalentních vakcín 13 %. Ten samý rok publikoval stejný časopis německou studii, která zkoumala náhlá úmrtí kojenců po šestimocném. Autoři píší: «Tyto výsledky, založené na spontánních zprávách, neprokazují kauzální vztah mezi očkováním a náhlým úmrtím kojence, ale představují signál týkající se jednoho ze dvou dostupných hexavalentů; signál, který by měl vést k intenzivnějšímu sledování náhlých úmrtí kojenců po očkování“.(F)
V roce 2006 byla publikována v lékařském časopise Vaccine(G) dopis od týmu výzkumníků z Mnichovské univerzity, který hlásil „šest případů náhlého úmrtí kojenců po šestimocném očkování. Všechny byly nalezeny mrtvé bez vysvětlení 1-2 dny po očkování“. Byly klasifikovány jako typické případy náhlého úmrtí kojenců, ale autoptické ověření odhalilo neuropatologické a histologické abnormality a všechny děti vykazovaly významný otok mozku, což z nich činilo výjimku ve srovnání s ostatními případy SIDS (Syndrom náhlého úmrtí dětí). Vědci napsali, že „Před zavedením hexavalentní vakcíny (v letech 1994-2000) jsme pozorovali případ pouze jednoho ze 198 dětí s náhlým úmrtím kojence, které zemřelo brzy po očkování proti DTP. V letech 2001 až 2004 však identifikovali pět podobných případů ze 74 se SIDS. To by znamenalo třináctinásobný nárůst.“
Také v roce 2006 na Virchows Archive(H), tým z Ústavu patologie Univerzity v Miláně napsal: «Odborníci z Evropské agentury pro hodnocení léčivých přípravků analyzovali možnost, že by mohla existovat souvislost mezi šestivalentními vakcínami a některými případy úmrtí. Mezi účastníky byli patologové se zkušenostmi s vakcínami a syndromem náhlého úmrtí kojenců, kteří prováděli pitvy. Pokud však víme, vyšetření mozkového kmene a krevního srdce na sériových řezech byla věnována malá pozornost a neexistovala možnost stanovit spouštěcí roli. vakcíny pro tato úmrtí. Zde uvádíme případ 3měsíční holčičky, která náhle zemřela po šestimocném očkování. Vyšetření mozkového kmene na sériových řezech odhalilo oboustrannou hypoplazii nucleus arcuate. Převodní systém srdce měl přetrvávající fetální disperzi a degeneraci. Tento případ nabízí jedinečné pochopení možné role hexavalentní vakcíny při vyvolání smrtelných následků u zranitelného dítěte. Jakýkoli případ náhlé a neočekávané smrti, ke kterému dojde brzy po narození nebo v raném dětství, zejména po očkování, by měl vždy projít úplnou pitvou podle pokynů.
Reference
- Blaylock R, "Očkování: skrytá nebezpečí", The Blaylock Wellness Report, květen 2004, s. 1-9
- Ottaviani G. et al., "Syndrom náhlého úmrtí kojenců (SIDS) krátce po hexavalentní vakcinaci: další patologie při podezření na SIDS?", Vircows Archiv., 2006, 448, pp. 100-104.
- Zinka B. et al., "Nevysvětlené případy náhlé smrti kojenců krátce po hexavalentní vakcinaci", Vaccine, červenec 2006, 24 (31-32), str. 5779-5780.
- Miller NZ a kol. ,“Míra kojenecké úmrtnosti klesla proti počtu dávek vakcíny běžně podávaných: existuje biochemická nebo synergická toxicita??", Hum. Exp. Toxicol., květen 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Problém hliníku (kliknutím otevřete)
Hliník ve vakcínách: co rodiče potřebují vědět

1. Co je hliník?
Hliník je stříbřitě bílý lehký kov, tvárný a odolný. Díky těmto vlastnostem je použitelný v mnoha průmyslových odvětvích a výrobcích, včetně strojů, stavebnictví, skladů, nádobí, kuchyňského náčiní, textilu, barviv a kosmetiky. Hliník je také nejrozšířenějším kovem v zemské kůře a prakticky veškerý hliník v životním prostředí se nachází v půdě. Hliník se však přirozeně nenachází ve významných množstvích v živých organismech (jako jsou rostliny a zvířata) a nemá žádnou známou biologickou funkci. V průběhu minulého století vedlo používání hliníku v některých výrobcích ke zvýšené expozici člověka. Hlavními zdroji expozice jsou potraviny obsahující hliník (např. prášek do pečiva, zpracované potraviny, kojenecká výživa atd.), lékařské produkty (např. antiperspiranty, antacida atd.), injekce proti alergii a vakcíny.1-3
2. Proč je hliník přítomen ve vakcínách?
Některé vakcíny používají jako adjuvans sloučeniny hliníku (hydroxid hlinitý a fosforečnan hlinitý), což jsou složky, které zvyšují imunitní odpověď na antigen (cizí látku).4-5 Americký úřad pro potraviny a léčiva (FDA) říká, že pokud by některé vakcíny neobsahovaly hliník, imunitní odpověď, kterou spouštějí, by se mohla snížit.6
3. Které vakcíny obsahují hliník?
Následující vakcíny obsahují hliník a podávají se kojencům, dětem a dospívajícím (obr. 1):
- Hepatitida B (HepB)
- šestimocný
- Záškrt, tetanus a černý kašel (DTaP a Tdap)
- Haemophilus influenzae typ b (PedvaxHIB)
- Pneumokok (PCV)
- Hepatitida A (HepA)
- Lidský papilomavirus (HPV)
- Meningokok B (MenB)
Obrázek 1: Od narození do 18 let se aplikuje až 22 dávek vakcín obsahujících hliník7-8
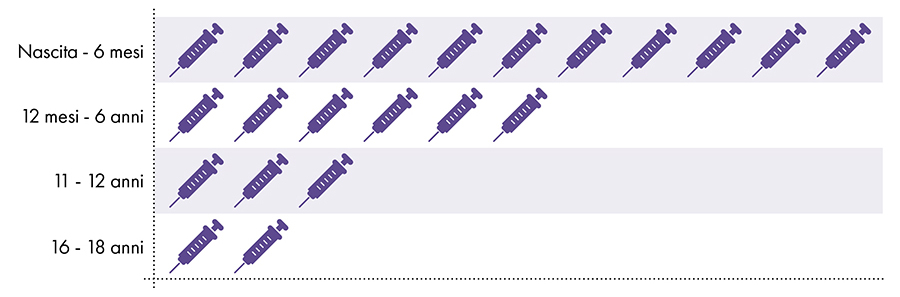
4. Je vystavení hliníku bezpečné?
FDA od roku 1975 považuje hliník obecně za bezpečný (GRAS).9 Před rokem 1990 však neexistovala žádná technologie, která by přesně detekovala malá množství hliníku podávaného subjektům ve vědeckých studiích.10 V důsledku toho nebylo známo množství hliníku, které by mohlo být absorbováno před nástupem nepříznivých účinků.
Od 1990. let XNUMX. století bylo díky technologickému pokroku pozorováno, že malé množství hliníku, které zůstává v lidském těle, zasahuje do řady buněčných a metabolických procesů v nervovém systému a tkáních jiných částí těla.1-10-11 Největší negativní účinky hliníku byly pozorovány v nervovém systému a sahají od zhoršené motoriky až po encefalopatii (změněný duševní stav, změny osobnosti, poruchy myšlení, ztráta paměti, záchvaty, kóma a další).2-12
Ministerstvo zdravotnictví a sociálních služeb Spojených států amerických (HHS) uznává hliník jako známý neurotoxin.2 Kromě toho FDA varoval před riziky toxicity hliníku u kojenců a dětí.13
FEDERÁLNÍ REGISTR: Deník vlády Spojených států"I donošení kojenci s normální funkcí ledvin mohou být ohroženi rychlým růstem a nezralostí mozku a skeletu a také nezralostí hematoencefalické bariéry. Do 1. až 2. roku věku mají kojenci nižší glomerulární filtrace než u dospělých, což ovlivňuje jejich funkci ledvin. Agentura se obává, že malé děti a osoby s nezralou funkcí ledvin jsou vystaveny zvýšenému riziku expozice hliníku.“ |
5. Kolik orálního hliníku není bezpečné?
V roce 2008 Agentura pro registr toxických látek a nemocí (ATSDR), divize HHS, použila studie o neurotoxických účincích hliníku k určení, že ne více než 1 miligram (1.000 XNUMX mikrogramů) hliníku na kilogram tělesné hmotnosti za den. vyhnout se negativním účinkům hliníku.2
6. Jaké množství vstřikovaného hliníku není bezpečné?
Pro stanovení množství hliníku, které lze bezpečně vstříknout, je nutné převést orální limit hliníku podle ATSDR. Limit ATSDR pro perorální hliník (1.000 0,1 mikrogramů hliníku na kilogram tělesné hmotnosti za den) je založen na XNUMX % perorálního hliníku, který je absorbován do krevního řečiště, protože trávicí trakt blokuje téměř veškerý perorální hliník.2 Naopak hliník injikovaný intramuskulárně obchází trávicí trakt a 100 % hliníku se může časem vstřebat do krevního řečiště (tj. podíl absorbovaného hliníku je 1.000krát větší). Aby byla zohledněna tato různá množství absorpce, musí se orální limit hliníku ATSDR vydělit 1000 1. Tento převod vede k limitu hliníku v krvi odvozenému z ATSDR ve výši 0,1 mikrogram hliníku (1.000 % z 1 3 mikrogramů) na kilogram tělesné hmotnosti. denně. Aby se předešlo neurotoxickým účinkům hliníku, nemělo by se denně do krevního oběhu dostat více než XNUMX mikrogram hliníku na kilogram tělesné hmotnosti. Obrázek XNUMX ukazuje limit hliníku v krvi odvozený od ATSDR pro kojence různého věku na základě jejich hmotnosti.
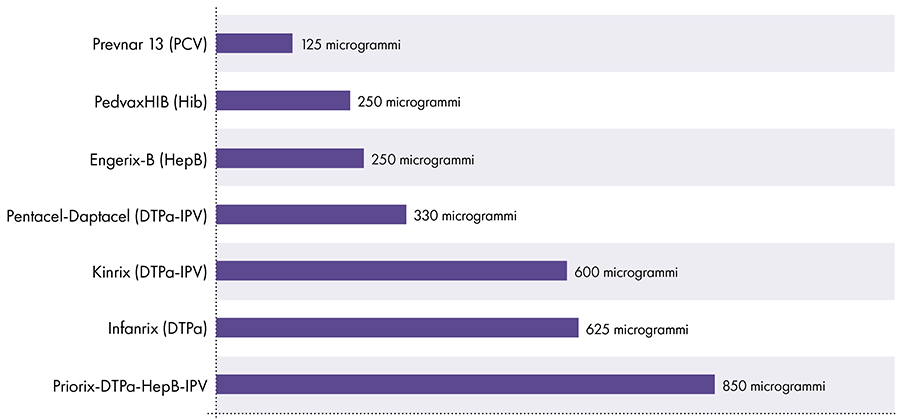
7. Kolik hliníku je ve vakcínách?
Množství hliníku ve vakcínách se liší.16 V roce 1968 federální vláda USA stanovila limit pro množství hliníku ve vakcínách na 850 mikrogramů na dávku na základě množství hliníku potřebného k tomu, aby byly některé vakcíny účinné.6-17 V důsledku toho se množství hliníku v kojeneckých vakcínách obsahujících hliník pohybuje od 125 do 850 mikrogramů na dávku. Obrázek 4 ukazuje obsah hliníku v jedné dávce různých vakcín podaných dětem.
8. Srovnávaly nějaké studie množství hliníku ve vakcínách s limitem odvozeným od Agentury pro registr toxických látek a nemocí (ATSDR)?
V roce 2011 byla publikována studie, která měla za cíl porovnat množství hliníku ve vakcínách s limitem průtoku krve stanoveným ATSDR.18 Tato studie však nesprávně založila své výpočty na 0,78 % perorálního hliníku absorbovaného do krevního řečiště, spíše než na hodnotě 0,1 %, kterou používá ATSDR ve svých výpočtech.19-20 V důsledku toho studie z roku 2011 předpokládala, že téměř 8krát (0,78 % / 0,1 %) se hliník může bezpečně dostat do krevního oběhu, což vedlo k nesprávnému závěru.
9. Je expozice hliníku z vakcín bezpečná?
Vakcíny se aplikují intramuskulárně a rychlost, jakou hliník z vakcín migruje z lidských svalů do krevního řečiště, není známa. Studie na zvířatech naznačují, že hliníku z vakcín může v důsledku mnoha proměnných trvat několik měsíců až více než rok, než se dostane do krevního řečiště.21-23 Vzhledem k tomu, že kumulativní expozice hliníku z vakcín u dětí mladších jednoho roku překračuje denní limit stanovený ATSDR o několik stovek (obr. 3 a 4), byl by limit stále překročen, pokud by se hliník z vakcín dostal do krevního oběhu v průběhu asi rok. Některé studie navíc ukázaly, že hliník z vakcín je absorbován imunitními buňkami a dostává se do částí těla daleko od místa vpichu, včetně mozku.24
Rozsah nepříznivých účinků hliníku ve vakcínách není znám, protože nebyly provedeny bezpečnostní studie srovnávající populaci očkovanou vakcínami obsahujícími hliník s populací neočkovanou takovými vakcínami.
Hliníkové omezení průtoku krve odvozené z ATSDR2-14-15
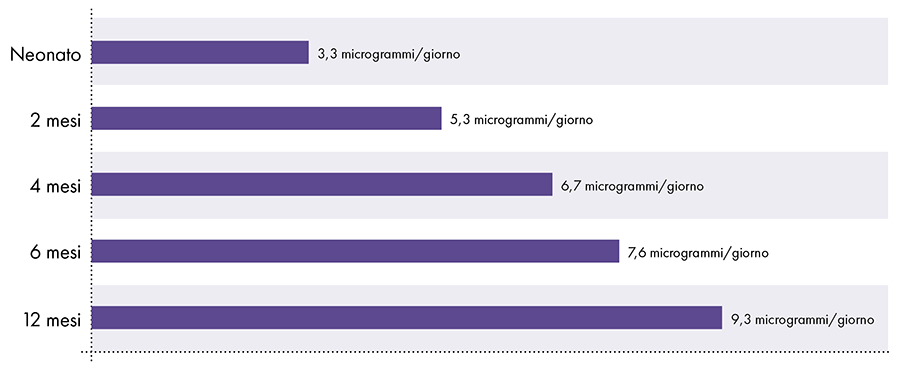 Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Obrázek 3: Tento graf ukazuje limit hliníku pro děti různého věku, jak je odvozen z Registru toxických látek a nemocí, divize Ministerstva zdravotnictví a sociálních služeb Spojených států amerických. Limit udává, že do krevního oběhu by se denně nemělo dostat více než 1 mikrogram hliníku na kilogram tělesné hmotnosti, aby se předešlo neurotoxickým účinkům hliníku.
Množství hliníku ve vakcínách
Reference
- Americká akademie pediatrie, Výbor pro výživu. Toxicita hliníku u kojenců a dětí. Pediatrie. březen 1996, 97 (3): 413.
- Agentura pro registr toxických látek a nemocí (ATSDR). Toxikologický profil pro hliník. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Hliník v potravinách – povaha a přínos potravinářských přídatných látek. In: El-Samragy Y, editor. Potravinová přísada. Rijeka (Chorvatsko): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. K pochopení adjuvantního působení hliníku. Nat Rev Immunol. 2009. dubna 9 (4): 287.
- Volk VK, Bunney WE. Imunizace proti záškrtu tekutým toxoidem a toxoidem vysráženým kamencem. Am J Veřejné zdraví Zdraví národů. července 1942, 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Hliníkové soli ve vakcínách – perspektiva USA. Vakcína. 2002. května 31, 20 Suppl 3: S18-22.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. Vakcíny licencované pro použití ve Spojených státech amerických; [aktualizováno 2018. února 14; citováno 2018. února 27]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Doporučené schéma imunizace pro děti a dospívající ve věku 18 let nebo mladší, Spojené státy americké, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- US Food and Drug Administration. Silver Spring (MD): US Food and Drug Administration. SCOGS (Výběrový výbor pro látky GRAS); [citováno 2018. srpna 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Kněz ND. Biologické chování a biologická dostupnost hliníku u člověka, se zvláštním odkazem na studie využívající hliník-26 jako indikátor: přehled a aktualizace studie. J Environ Monit. 2004;6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Hliník ve výrobcích pro parenterální výživu dětí: měřeno versus obsah na etiketě. J Pediatr Pharmacol Ther. 2011, 16 (2): 92-7.
- Sedman A. Toxicita hliníku v dětství. Pediatr Nephrol. 1992 (6): 4-383, červenec 93.
- US Food and Drug Administration, Department of Health and Human Services. Pravidla a regulace. Registrátor Fedu. června 2003, 68 (100): 34286.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro chlapce v grafech délky k věku a hmotnosti k věku; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centra pro kontrolu a prevenci nemocí. Washington, DC: Ministerstvo zdravotnictví a sociálních služeb USA. Národní centrum pro zdravotní statistiku: Tabulka dat pro grafy délky dívek na věk a hmotnosti na věk; [citováno 2019. dubna 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- US Food and Drug Administration, Department of Health and Human Services. Revize požadavků na základní materiály. Konečné pravidlo. Registrátor Fedu. 2011. dubna 13, 76 (71): 20513-8.
- Úřad federálního rejstříku, Národní archivy a spisová služba, Správa všeobecných služeb. Pravidla a regulace. Registrátor Fedu. 1968 leden; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím stravy a očkování. Vakcína. 2011. listopadu 28, 29 (51): 9538-43.
- Miller S, lékaři pro informovaný souhlas. Erratum v 'Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování.' In: ResearchGate. Berlín (Německo): ResearchGate GmbH; 2020. března 6 [citováno 2020. března 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Lékaři pro informovaný souhlas. Newport Beach (CA): Lékaři pro informovaný souhlas. Erratum v „Aktualizovaná farmakokinetika hliníku po expozici kojenců prostřednictvím diety a očkování“; [citováno 2020. března 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, White JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In vivo absorpce adjuvans vakcín obsahujících hliník pomocí 26Al. Vaccine 1997 srpen-září, 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Test hliníku a hodnocení lokální reakce v několika časových bodech po intramuskulárním podání vakcín obsahujících hliník u opice Cynomolgus. Vakcína. 2005. února 3, 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Hliník v plazmě a tkáních po intramuskulární injekci lidských vakcín s adjuvans u potkanů. Arch Toxicol. říjen 2019, 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritická analýza referenčních studií toxikokinetiky adjuvans na bázi hliníku. J Inorg Biochem. 2018 duben; 181: 87-95.
Článek přeložil Lékaři pro informovaný souhlas
Secondo il CDC americano, i problemi che possono derivare dopo la vaccinazione con il vaccino coniugato pneumococcico 13-valente (PCV13), vaccino pneumococcico polisaccaridico 23-valente (PPSV23) e qualsiasi altro vaccino includono:(1-2)
- Reazioni allergiche gravi che si verificano entro pochi minuti o poche ore dalla vaccinazione.
- Forte dolore alla spalla che limita i movimenti del braccio in cui è avvenuta la somministrazione.
- Svenimento o collasso dopo la vaccinazione. Può essere consigliato di rimanere seduti o sdraiati per circa 15 minuti dopo la vaccinazione per evitare svenimenti e lesioni che potrebbero derivare da una caduta. È importante informare il medico curante in caso di ronzii alle orecchie, alterazioni visive o vertigini dopo la vaccinazione.
Effetti collaterali del vaccino PCV13 (Vaccino Coniugato Pneumococcico)
Le reazioni avverse in seguito alla somministrazione del PCV13 variano in base alla dose della serie e all'età del ricevente. Nei bambini, le reazioni più comunemente segnalate sono state irritabilità, sonnolenza, perdita di appetito, arrossamento, dolore o gonfiore nel sito del vaccino e febbre lieve o moderata.
I bambini che hanno ricevuto il PCV13 contemporaneamente al vaccino antinfluenzale inattivato sono risultati a maggior rischio di convulsioni febbrili.
Negli adulti sono stati segnalati soprattutto arrossamento, gonfiore e dolore nel sito di iniezione, affaticamento, febbre, brividi, mal di testa e dolori muscolari.(3)
Reazioni avverse di Prevenar 13 (PCV13) segnalate nei neonati e nei bambini durante gli studi clinici pre-approvazione:(4) dolore nel sito di iniezione, gonfiore, arrossamento, febbre, diminuzione dell'appetito, aumento e diminuzione del sonno, irritabilità, diarrea, vomito, eruzione cutanea, orticaria, reazione di ipersensibilità che comprende broncospasmo, gonfiore del viso e respiro affannoso, convulsioni, polmonite, gastroenterite, bronchiolite, morte (segnalata come SIDS).
Reazioni avverse di Prevenar 13 (PCV13) riportate negli adulti durante gli studi clinici pre-approvazione:(5) dolore, gonfiore e arrossamento nel sito di iniezione, limitazione dei movimenti delle braccia, febbre, vomito, brividi, dolori muscolari, affaticamento, cefalea, diminuzione dell'appetito, eruzione cutanea, dolori articolari, decesso (i decessi riportati negli studi clinici pre-approvazione includevano decessi per cancro, disturbi cardiaci, peritonite, infezione polmonare da Mycobacterium avium complex e shock settico).
Reazioni avverse di Prevenar 13 (PCV13) riportate dopo la commercializzazione:(6) Cianosi, linfoadenopatia nel sito di iniezione, anafilassi, shock, ipotonia, pallore, apnea, edema angioneurotico, eritema multiforme, prurito nel sito di iniezione, orticaria ed eruzione cutanea.
Gli studi clinici pre-approvazione del primo vaccino pneumococcico coniugato, Prevenar (PCV7), hanno confrontato la sicurezza di Prevenar (PCV7) con un vaccino sperimentale contro la meningite C, compromettendo seriamente la validità scientifica della sperimentazione.
Negli studi clinici precedenti all'autorizzazione di Prevenar (PCV7), i bambini dei gruppi che hanno ricevuto il vaccino pneumococcico hanno sofferto maggiormente di convulsioni, irritabilità, febbre alta e altre reazioni. Nel gruppo Prevenar (PCV7) si sono verificati 12 decessi, tra cui 5 decessi per sindrome della morte improvvisa del lattante (SIDS). Non sono stati completati studi a lungo termine per valutare se il vaccino Prevenar (PCV7), somministrato da solo o in combinazione con altri vaccini, avesse un'associazione con malattie croniche o disabilità, come lo sviluppo di diabete, asma, disturbi convulsivi, difficoltà di apprendimento, ADHD.(7)
Gli studi clinici di sicurezza pre-approvazione di Prevenar 13 (PCV13) hanno confrontato questo vaccino di nuova generazione con il vaccino Prevenar originale (PCV7), un vaccino non adeguatamente studiato per la sicurezza, e nel 2012 sono state segnalate preoccupazioni relative a un legame tra convulsioni febbrili e Prevenar 13 (PCV13).(8-9)
Il PCV13 è risultato associato a un rischio elevato di convulsioni febbrili quando è stato somministrato indipendentemente(10) e quando è stato somministrato in combinazione con il vaccino influenzale inattivato per via parenterale (IIV).(11)
Alcuni studi hanno anche collegato il vaccino PCV alla sindrome di Guillain-Barre,(12) alla polisierosite,(13) alla spalla settica(14) e all'eritema multiforme.(15)
Effetti collaterali del vaccino PPSV23 (Pneumococco polisaccaridico)
Secondo i CDC, circa il 50% dei soggetti che ricevono il vaccino polisaccaridico pneumococcico (PPSV23) manifesta dolore e arrossamento nel sito di iniezione. Anche dolori muscolari, febbre e reazioni localizzate più gravi possono verificarsi dopo la somministrazione del PPSV23.(16)
Reazioni avverse di PNEUMOVAX23 (PPSV23) riportate negli adulti durante gli studi clinici americani pre-approvazione:(17) dolore al sito di iniezione, arrossamento, prurito, lividi e gonfiore, cefalea, brividi, febbre, diarrea, dispepsia, nausea, infezione delle vie respiratorie superiori, mal di schiena, dolore al collo, faringite, dolore muscolare, affaticamento, depressione, colite ulcerosa, dolore toracico, angina pectoris, insufficienza cardiaca, tremore, rigidità, sudorazione, ictus, radicolopatia lombare, pancreatite, infarto del miocardio, morte.
Quasi l'80% dei soggetti che hanno partecipato agli studi clinici pre-approvazione ha manifestato una reazione avversa nel sito di iniezione dopo la rivaccinazione a tre-cinque anni dal vaccino iniziale. Anche il tasso di reazioni avverse sistemiche (cefalea, affaticamento, mialgia) in seguito alla rivaccinazione con PPSV23 è stato più elevato, con il 33% degli adulti di età pari o superiore a 65 anni e il 37,5% degli adulti di età compresa tra 50 e 64 anni che hanno riportato una reazione avversa.(18)
Reazioni avverse di PNEUMOVAX23 (PPSV23) riportate dopo la commercializzazione:(19) Reazioni anafilattoidi, malessere da siero,edema angioneurotico, artrite, artralgia, vomito, nausea, diminuzione della mobilità degli arti, edema periferico nell'arto in cui è avvenuta l'iniezione, febbre, malessere, cellulite, calore nel sito di iniezione, linfoadenopatia, linfoadenite, leucocitosi, trombocitopenia in pazienti con porpora trombocitopenica idiopatica stabilizzata, anemia emolitica in pazienti che hanno avuto altri disturbi ematologici, parestesia, sindrome di Guillain-Barré, radicoloneuropatia, convulsioni febbrili, rash, eritema multiforme, orticaria, reazioni simili alla cellulite.
Sebbene il PNEUMOVAX23 (PPSV23) sia approvato per l'uso nei bambini a partire dai due anni di età con condizioni quali malattie cardiache e polmonari croniche, diabete, impianti cocleari, perdite di liquido cerebrospinale, anemia falciforme, asplenia funzionale o anatomica e immunosoppressione, non sono disponibili informazioni sulla sicurezza o sull'efficacia del vaccino nei bambini dal foglietto illustrativo del vaccino.(20)
Alcuni studi hanno collegato il PPSV23 a reazioni infiammatorie sistemiche(21) e únor.(22-23-24-25-26)
Reference (kliknutím otevřete)
- CDC Pneumococcal Conjugate (PCV13) VIS. 5. listopadu 2015
- CDC Pneumococcal Polysaccharide VIS. Dubna 24, 2015
- CDC Pneumococcal Conjugate (PCV13) VIS. 5. listopadu 2015
- FDA Prevnar 13 Package Insert Srpen 22, 2017
- Tamtéž
- Tamtéž
- FDA Pneumokoková 7-valentní konjugovaná vakcína (PREVNAR) – příloha výrobce produktu. 1. října 2002
- Hitt, E Prevnar 13 Should Be Watched for Febrile Seizure Risk, FDA Panel Says. medscape. 31
- Tse A, Tseng HF, Greene SK, et al. Signal identification and evaluation for risk of febrile seizures in children following trivalent inactivated influenza vaccine in the Vaccine Safety Datalink Project, 2010-2011. Vakcína. 2012 Mar 2;30(11):2024-31
- Baker M, Jankosky C, Yih K et al. The Risk of Febrile Seizures Following Influenza and 13-Valent Pneumococcal Conjugate Vaccines. Open Forum Infect Dis. 2017 Fall; 4(Suppl 1): S464–S465.
- CDC Childhood Vaccines and Febrile Seizures 20, 2016
- Ravishankar,N Guillain-Barre Syndrome Following PCV Vaccine. J Neurol Neurosurg 4 (1): 134
- Tawfik P, Elie Gertner E, McEvoy CE Severe polyserositis induced by the 13-valent pneumococcal conjugate vaccine: a case report J Med věc Rep. 2017; 11: 142.
- DeRogatis MJ, Parameswaran L, Lee P et al. Septic Shoulder Joint After Pneumococcal Vaccination Requiring Surgical Debridement. HSS J. 2018 Oct;14(3):299-301
- Monastirli A, Pasmatzi E, Badavanis G et al. Erythema multiforme following pneumococcal vaccination. Acta Dermatovenerol Alp Pannonica Adriat. 2017 Mar;26(1):25-26.
- CDC Pneumococcal Polysaccharide VIS. Dubna 24, 2015
- FDA Pneumovax 23 - Pneumococcal Vaccine, Polyvalent. Package Insert 30
- Tamtéž
- Tamtéž
- Tamtéž
- von Elten, KA, Duran LL, Banks TA, et al. Systemic inflammatory reaction after pneumococcal vaccine A case series Hum Vaccine Immunother. 2014 Jun 1; 10(6): 1767–1770.
- Huang DT, Chiu NC, Chi H, et al. Protracted fever with cellulitis-like reaction in pneumococcal polysaccharide-vaccinated children. Pediatr Infect Dis J. 2008 Oct;27(10):937-9.
- Yousef E, Mannan S. Systemic reaction to pneumococcal vaccine: how common in pediatrics? Allergy Asthma Proc. 2008 Jul-Aug;29(4):397-9
- Gabor EP, Seeman M. Acute febrile systemic reaction to polyvalent pneumococcal vaccine. JAMA. 1979 Nov 16;242(20):2208-9.
- Hasan S, Yousef M, Shridharani S Severe febrile systemic reaction to pneumococcal vaccine. J Natl Med Assoc. únor 2005; 97(2): 284–285.
- Lee A, Goyal R, Shan HY. Severe protracted fever following pneumococcal vaccine. Am J Med Sci. 2006 Dec;332(6):351-3.
Tento článek shrnuje a překládá Vakcína Národní informační centrum.

