Erste von Experten begutachtete Veröffentlichung zu MMRV-Impfstoffen (Priorix Tetra)

Schließlich sind wir hier - nach fast zwei Jahren - und die erste von Experten begutachtete Veröffentlichung unserer Analysen wird veröffentlicht, und viele andere werden veröffentlicht.
Ziel dieses Artikels ist es, die folgenden Themen zusammenzufassen: Was wurde veröffentlicht, was ist seine Gültigkeit und warum ist es wichtig für unsere Untersuchung von Impfstoffen. Alle diese Argumente werden auf den ersten Seiten umgangssprachlich und nicht technisch behandelt, während ab Seite 3 eine technische Studie durchgeführt wird, damit die Fachleute dieses Sektors den Artikel selbst bewerten können.
Der Artikel veröffentlicht auf "F1000 Research"1 ist das Ergebnis der ersten Studie, die von einem der Laboratorien durchgeführt wurde, die die Corvelva Association mit der Durchführung der Analysen beauftragt hat. Wir erinnern Sie daran, dass seit Beginn dieser Arbeit mehr als zwei Jahre vergangen sind und viele andere Ergebnisse zu den ersten hinzugefügt wurden Das erste große Problem, das wir untersuchen mussten, war die abnormale Menge an menschlicher DNA, die in den analysierten Impfstoffen gefunden wurde.
Die ersten Analysen zeigten, dass sowohl die analysierten vierwertigen MMRV-Impfstoffe 1 bis 2.7 Mikrogramm / Fläschchen enthielten (wie in diesem Artikel veröffentlicht), und wir beschlossen, solche Ergebnisse öffentlich und sofort zu melden, da einfach nicht erwartet wurde, dass eine solche Menge von DNA könnte in einem Impfstoff vorhanden sein.
Abgesehen von den Überlegungen und Schlussfolgerungen der Studie, die streng technisch und daher nur für diejenigen verständlich sind, die auf dem Gebiet der metagenomischen Forschung tätig sind, wird in den Grafiken festgestellt, dass die beiden Impfstoffproben einen hohen Prozentsatz menschlicher DNA-Messwerte enthalten Zusätzlich zu denen, die vom Windpockenvirus-Genom (Humanes Alphaherpes-Virus 3) erwartet wurden, wurde in dem Artikel der einzige nachweisbare unter vier als DNA-seq-Analyse-Typ vorgestellt.
Wir möchten jedoch darauf hinweisen, dass die DNA-Mengen von gefunden und bestätigt wurden die gleiche Methode, die jetzt hier validiert wird waren noch höher: bis zu 3.7 Mikrogramm pro FläschchenDies führt zu einem erheblichen Unterschied von Charge zu Charge. In unserem am 22. Dezember 2018 veröffentlichten Bericht2 Die Ergebnisse, die aus der Analyse verschiedener Chargen von den in diesem Artikel diskutierten erhalten wurden, wurden berichtet und dann durch Ringversuche bestätigt, die sich noch in der Veröffentlichung befinden.
Daher sollte in der vorliegenden Veröffentlichung als von großem Interesse angesehen werden, dass die von uns verwendete Methode validiert wird, gibt einen wichtigen Punkt zu den Diskussionen über die "Art" der durchgeführten Analyse, und als Folge es bestätigt in endgültiger Weise alle Studien, die anschließend mit der NGS-Methode durchgeführt wurden: die eingehende Analyse der Art des genetischen Materials, das Vorhandensein von zufälligen Viren, das große Fehlen abgeschwächter Viren, die vorhanden sein sollten, und die Menge an menschlicher DNA, die völlig außer Kontrolle geraten war (auch weil sie von Probe zu Probe sehr unterschiedlich war) , die mutierte Population, Phagen, DNA von anderen Spezies und so weiter. Sie finden das aAlle Ergebnisse sind auf unserer Website zusammengefasst3.
Alles, was wir in den letzten Jahren aus biologischer Sicht angeprangert haben und die Ergebnisse gründlich an die Kontrollstellen weiterleiten, nimmt eine relevantere wissenschaftliche Konnotation an (auch wenn wir es noch einmal wiederholen, waren es nicht die Peer-Reviews, die dies mussten Sorgen, aber die präsentierten Daten, sehr ernst in ihrem Inhalt und ihren möglichen Auswirkungen auf die menschliche Gesundheit). Nachdem die Veröffentlichung der Methode abgeschlossen ist, werden wir jedoch die Antworten verlangen, die uns noch nicht gegeben wurden.
Diese Ergebnisse bestätigen zweifellos das Vorhandensein von fötaler DNA in Priorix-Tetra-Impfstoffen in variablen Mengen von Charge zu Charge, was auf eine schlechte Qualitätskontrolle dieser pharmazeutischen Produkte hinweist.
Wir möchten auch an den Bericht über die gesamte MRC-5-Genomsequenzierung erinnern, der am 27. September 2019 auf der Corvelva-Website veröffentlicht wurde4 zeigt die tiefe Modifikation dieser DNA auch in Genen, die mit der Entwicklung von Tumorerkrankungen zusammenhängen (diese Daten werden ebenfalls bald veröffentlicht). Die kontaminierende fötale DNA, die in allen analysierten Proben in variablen (dh unkontrollierten) Mengen gefunden wurde, ist bis zu 300-mal höher als die von der EMA festgelegte Grenze für krebserzeugende DNA (10 ng / Dosis, entsprechend der in etwa 1000 Krebszellen enthaltenen DNA). auf der Grundlage einer statistischen Berechnung (während die Vorsichtsgrenze 100 pg / Dosis beträgt), eine Grenze, die notwendigerweise auch für fötale DNA angewendet werden muss, die den Priorix Tetra-Impfstoff zwangsläufig kontaminiert.
Infolgedessen sollte dieser Impfstoff als defekt und potenziell gefährlich für die menschliche Gesundheit angesehen werden, insbesondere für die pädiatrische Bevölkerung, die aufgrund der Unreife der Immunsysteme viel anfälliger für genetische und Autoimmunschäden ist.
Wie erwartet ist der folgende Teil des Artikels "technischer" und für Nichtfachleute schwer verständlich. Daher haben wir uns aus Gründen der Transparenz entschlossen, diesem Dokument auch das beizufügen "EMA-Dossier - NGS-Dossier Diskussion über die Ergebnisse der Impfstoffqualitätsumfrage". Wir mussten nur den Teil extrapolieren, der veröffentlicht werden konnte, dh 50 Seiten des Dossiers im Vergleich zu den 200 Seiten des NGS, da ein Großteil der Informationen, die in den Regulierungsbehörden enthalten und registriert sind, vertraulich bleiben müssen. Das strenge Gesetz der Wissenschaft schreibt vor, dass eine Information nur dann in einer Zeitschrift veröffentlicht werden kann, wenn sie original ist. Da wir andere Arbeiten in Arbeit haben, möchten wir sie nicht gefährden.
EMA - NGS Dossier Diskussion über die Ergebnisse der Impfstoffqualitätserhebung ". - https://bit.ly/342XKi7
Um Missverständnisse zu vermeiden, möchten wir abschließend den Teil der "Finanzierungserklärung" aus der oben genannten Veröffentlichung hervorheben:
"Die metagenomische Sequenzierung von B1 und B2 wurde von Corvelva (gemeinnütziger Verein, Venetien, Italien) im Rahmen eines Servicevertrags mit dem Labor finanziert. Es war kein weiterer Beitrag zur Unterstützung der Arbeit beteiligt. Die Geldgeber hatten keine Rolle bei der Gestaltung der Studie, Sammlung und Analyse von Daten, Entscheidung zur Veröffentlichung oder Erstellung des Manuskripts "
Angebracht:
- Veröffentlichung - Versteckst du mich? Auswirkung der Deckungsreduzierung auf Sequenzierungsstudien mit Metagenom-Schrotflinten
- CORVELVA-thread-NGS-EMA-eng
- Erste von Experten begutachtete Veröffentlichung zu MMRV-Impfstoffen (Priorix Tetra)
In dem Artikel „Liebst du mich? Auswirkung der Verringerung der Abdeckung auf Sequenzierungsstudien mit Metagenom-Schrotflinten "
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
Die Autoren befassen sich mit der technisch-methodologischen Frage, ob es möglich ist, einen massiv parallelen metagenomischen Ansatz mit geringer Leseabdeckung zur Charakterisierung komplexer biologischer Matrizen zu verwenden. Schätzungen der Vielfalt, des Artenreichtums und der Fähigkeit, das Metagenom zu rekonstruieren de novo In Bezug auf Länge und Vollständigkeit werden berechnet, um zu verstehen, inwieweit die Abnahme der Sequenzierungstiefe, die durch zufällige Unterabtastung der Sequenzierungswerte variiert wird, die Endergebnisse beeinflussen kann. Die Ergebnisse zeigen, dass die Diversitätsindizes komplexer prokaryotischer, eukaryotischer und viraler Gemeinschaften mit 500,000 Messwerten oder weniger genau geschätzt werden können, obwohl für besonders komplexe Proben möglicherweise 1,000,000 Messwerte erforderlich sind. Im Gegenteil, ein Projekt, das die Rekonstruktion des Metagenoms und seiner Gene umfasst enthält erfordert mehr als 1,000,000 Messwerte.
Unter den verschiedenen und sehr unterschiedlichen komplexen Matrices, die einer massiven metagenomischen Analyse unterzogen wurden, wurden zwei biologische Arzneimittel eingeschlossen, nämlich zwei verschiedene Chargen eines abgeschwächten MPRV-Lebendimpfstoffs, der zur Immunisierung gegen Masern, Mumps, Röteln und Windpocken bei Kindern verwendet wurde. DNA wurde aus den Impfstoffen extrahiert, genomische Bibliotheken wurden unter Verwendung kommerzieller Standardprotokolle erstellt und eine massive Sequenzierung wurde mit der Illumina-Technologie durchgeführt.
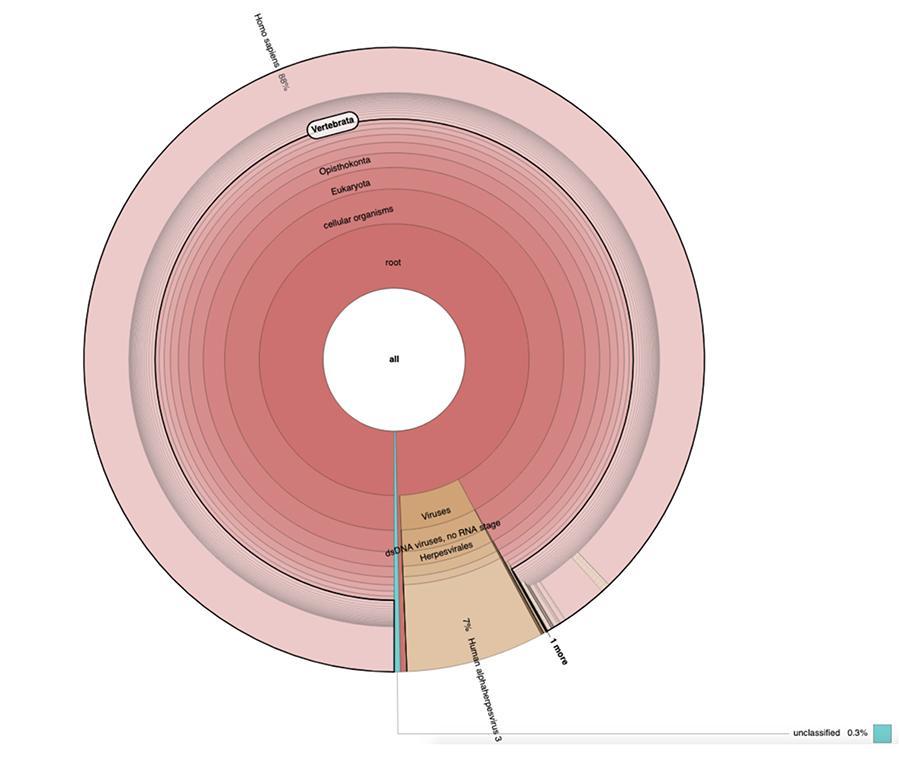
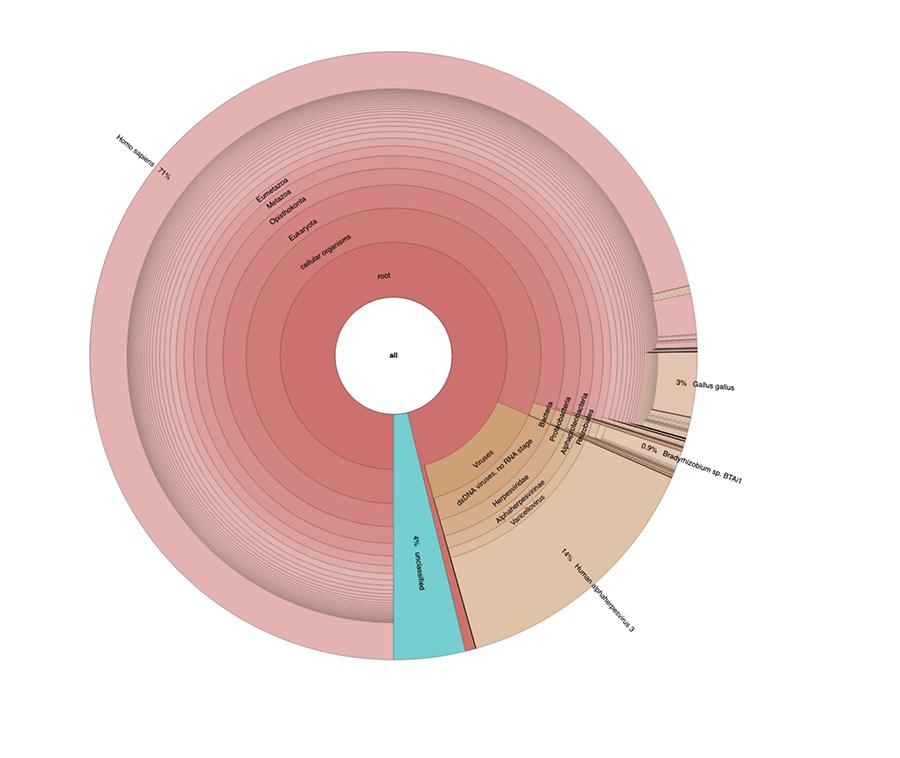
Abgesehen von den Überlegungen und Schlussfolgerungen der Arbeit, die streng technisch und daher nur für diejenigen verständlich sind, die auf dem Gebiet der Metagenomik forschen, wird in den Kreisdiagrammen in den „erweiterten Daten“ (https://osf.io/wq395/ Bei den Proben B1 und B2 wurde festgestellt, dass die beiden Impfstoffproben zusätzlich zu den vom Genom des Windpockenvirus (Human) erwarteten Werten einen hohen Prozentsatz an menschlichen DNA-Werten enthielten Alphaherpes Virus 3), der einzige, der unter den vier nachweisbar ist, da in dem Artikel eine DNA-seq-Typ-Analyse vorgestellt wurde.
71% der Messwerte in einer Charge und 88% in der anderen Charge sind menschlichen Ursprungs und stammen vermutlich aus der fetalen Zelllinie MRC-5 (denken Sie daran, dass die nachfolgende Analyse bestätigt hat, dass es sich bei der Linie um MRC5 handelt), in der lebende abgeschwächte Röteln und Windpockenviren vorkommen während der Impfstoffzubereitung gezüchtet. Darüber hinaus liegt die extrahierte DNA-Menge in der Größenordnung von Mikrogramm, wie dies bei den verschiedenen Chargen desselben von Corvelva zwischen 2017 und 2019 getesteten MPRV-Impfstoffs der Fall war.
In Impfstoffchargen, die mit denselben Protokollen und Technologien getestet wurden, die in den Materialien und Methoden des Artikels angegeben sind, lagen die nachgewiesenen Mengen zwischen 1 und fast 3 Mikrogramm pro Fläschchen, wobei die Mengen zwischen den Chargen variierten, aber immer signifikant waren.
In dem von Corvelva am 22.12.2018 veröffentlichten Bericht 5Die folgenden Ergebnisse wurden für weitere Chargen angegeben, die nach den im Artikel diskutierten Chargen analysiert wurden, was später durch eine noch im Veröffentlichungsprozess befindliche Ringanalyse bestätigt wurde.
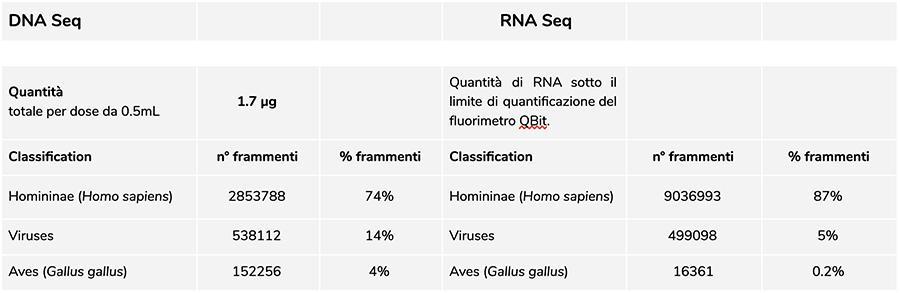
Priorix Tetra viel. A71CB205A (Juni 2018) - DNA-Analyse
Priorix Tetra viel. A71CB256A (Dezember 2018) - DNA-Analyse
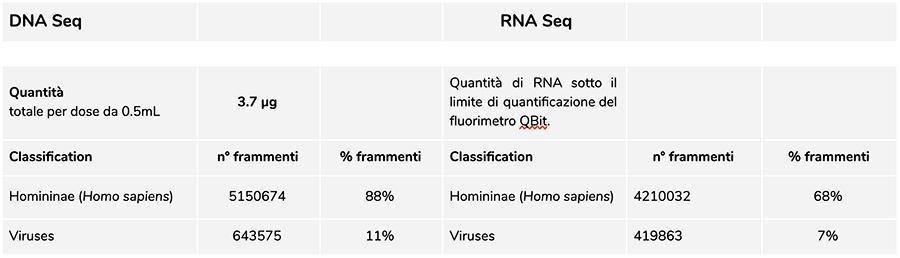
DNA-Analyse
Die Messung der DNA-Konzentration mit einem QuBit-Fluorometer zeigte, dass die A71CB205A-Charge insgesamt 1.7 µg gDNA pro 0.5-ml-Dosis enthält, berechnet wie folgt: 9.41 ng / µl (Konzentration bestimmt bei QuBit) x 45 (endgültiges Resuspensionsvolumen der DNA nach Extraktion, ausgedrückt) in Mikrolitern) x 4 (das dem Extraktionsverfahren unterworfene Ausgangsvolumen beträgt ¼ des in der gesamten Durchstechflasche enthaltenen Dosisvolumens von 0.5 ml).
Die Messung von DNA Konzentration mit QuBit Fluorometer zeigte, dass die A71CB256A Los enthält eine Summe gDNA von 3.7 ug pro 0.5 ml Dosis, berechnet wie folgt: 40.8 ng / ul (Konzentration bestimmt bei QuBit) x 55 (endgültiges Resuspensionsvolumen der DNA nach Extraktion, ausgedrückt in Mikrolitern) x 5/3 (das dem Extraktionsverfahren unterworfene Ausgangsvolumen beträgt 300 ul auf 500 ul Suspension ).
Die in dieser Charge gefundene menschliche DNA beträgt etwa 8 zu 1 relativ zu Windpocken-DNA (siehe die folgenden Ergebnisse der Klassifizierung von DNA-seq-Fragmenten, die zeigen, dass 88% der insgesamt sequenzierten DNA-Fragmente menschlichen Ursprungs sind und 11% des Windpockenvirus-Genoms).
In Anbetracht der Tatsache, dass NGS eine quantitative Technologie ist, können wir anhand der fluorimetrischen Quantifizierung der aus dem Impfstoff extrahierten Gesamt-DNA (z. B. Charge A71CB256A = 3.7 Mikrogramm pro Dosis) in Kombination mit der oben vorgenommenen relativen Quantifizierung (8: 1) sagen, dass es sich um einen Menschen handelt Die DNA könnte etwa 2.9 Mikrogramm pro Dosis betragen, verglichen mit etwa 740 Nanogramm Windpocken-DNA. Es ist auch plausibel, dass Mindestens ein Teil der auf dem Gel sichtbaren DNA mit hohem Molekulargewicht könnte menschliche DNA mit hohem Molekulargewicht sein.
RNA-Analyse
Die Menge von RNA in der Impfstoffflasche enthalten Los A71CB256A stellte sich als ca. 200 ng heraus.
Die RIN gleich 8 zeigt an ausgezeichneter Qualität RNA und eine intakte eukaryotische RNA, da sowohl die für eukaryotische RNA typischen 18S- als auch 28S-Peaks vorhanden sind.
Die Antworten auf unsere Fragen, die im Laufe der Zeit an die Aufsichtsbehörden weitergeleitet werden, sind äußerst wichtig. Derzeit haben die Agenturen die Fragen zu den Ergebnissen der vollständigen Analysen, die an die EMA und die AIFA übermittelt wurden, noch nicht beantwortet.
Auszug aus der Antwort der EMA auf unsere Frage zur Sicherheit von MRC-5-Rückständen im Priorix®-Tetra-Impfstoff (EMA-Anforderungsreferenz ask-43967, 3. August 2018) - "Basierend auf den veröffentlichten Informationen enthält Priorix® Tetra Virusstämme, die separat in Hühnerembryozellen (Mumps und Masern) oder in humanen diploiden Zellen MRC-5 (Röteln und Windpocken) produziert werden. Die für Priorix® Tetra verwendeten Zelllinien umfassen humane diploide Zelllinien, die sich nicht kontinuierlich teilen können. Beachten Sie, dass nach Angaben des Europäischen Arzneibuchs Die diploiden MRC-5-Zelllinien sind nicht tumorigen, wie durch jahrzehntelange Verwendung und Kontrolle gezeigt wurde, und daher gilt die maximale Grenze für die DNA von MRC-5-Zellen nicht. "
Bis heute wurden keine Nachweise (weder in Bezug auf Bescheinigungen über die Analyse der Produktqualität noch in Bezug auf wissenschaftliche Referenzliteratur für die EMA) für diese Kontrollen erbracht, die garantieren, dass es angemessen ist, keine Höchstgrenze anzuwenden.
In der FDA-Richtlinie "Leitfaden für die Industrie: Charakterisierung und Qualifizierung von Zellsubstraten und anderen biologischen Materialien, die bei der Herstellung von Virusimpfstoffen für Indikationen für Infektionskrankheiten verwendet werden"6 es wird angegeben, dass:
- Ein Stamm diploider Zellen sollte immer diploid bleiben. Wenn diese Eigenschaften nicht stabil sind, muss nachgewiesen werden, dass die Instabilität die Produktion oder die Konformität des Produkts nicht beeinträchtigt.
- Für weit verbreitete humane diploide Zellstämme wie MRC-5- und WI-38-Zellen ist die Messung der restlichen DNA möglicherweise nicht erforderlich, da wir die restliche DNA dieser humanen diploiden Zellen nicht als Sicherheitsbedenken betrachten
- Die restliche DNA sollte für nicht-tumorigene kontinuierliche Zellen, wie TRUE-Zellen mit geringer Anzahl von Passagen, begrenzt sein, weniger als 10 ng / Dosis für die parenterale Inokulation, wie von der WHO empfohlen
Und die WHO-Richtlinie "Anhang 3 - Empfehlungen zur Bewertung tierischer Zellkulturen als Substrate für die Herstellung biologischer Arzneimittel und zur Charakterisierung von Zellbanken. Ersetzung von Anhang 1 der WHO-Reihe technischer Berichte, n. 878 "fügt hinzu: (...) Es wurden beträchtliche Erfahrungen mit der Zytogenetik von gesammelt WI-38 und MRC-5 seit den 1960er Jahren und um diese Erfahrung zu unterstützen, werden die folgenden Artikel aufgelistet:
- Jacobs JP. Aktualisierte Ergebnisse zur Karyologie der WI-38-, MRC-5- und MRC-9-Zellstämme. Developments in Biological Standardization, 1976, 37: 155–156.
- Jacobs JP. et al. Richtlinien für die Akzeptanz, Verwaltung und Prüfung von seriell vermehrten humanen diploiden Zellen zur Herstellung von Lebendvirus-Impfstoffen zur Verwendung beim Menschen. Journal of Biological Standardization, 1981, 9: 331–342.
- Petricciani JC et al. Karyologische Standards für die diploide Rhesuszelllinie DBS-FRhL-2. Journal of Biological Standardization, 1976, 4: 43–49.
- Schollmayer et al. Hochauflösende Analyse und differentielle Kondensation in menschlichen Chromosomen mit RBA-Banden. Human Genetics, 1981, 59: 187–193.
- Rønne M. Chromosomenpräparation und hochauflösende Banding-Techniken: eine Übersicht. Journal of Dairy Science, 1989, 72: 1363–1377.
Es ist deutlich zu erkennen, dass in der Referenzliteratur, in der behauptet wird, dass die zur Herstellung von Impfstoffen verwendeten diploiden Zellen unter dem Gesichtspunkt der genetischen Stabilität sicher sind, ist veraltet. Bereits vor 40 Jahren wurden die ersten genetischen Anomalien gefunden, die für die Sicherheit von Impfstoffen als vernachlässigbar angesehen werden, und nach den Angaben in der WHO-Richtlinie wurden seitdem keine Aktualisierungen der neuen Sequenzierungstechnologien vorgenommen, insbesondere bei NGS wirtschaftlich und schnell, mit der Folge, dass in den Impfstoffen verabreicht Seit Jahrzehnten erlauben die Agenturen das Vorhandensein von immer progressiver gentechnisch veränderter DNA und in unkontrollierten Mengen. Zu diesem Thema siehe den am 5 auf der Corvelva-Website veröffentlichten Bericht über die Sequenzierung des gesamten MRC-27.09.2019-Genoms, in dem die tiefgreifende Modifikation dieser DNA auch in Genen erkennbar ist, die mit der Entwicklung von Tumorpathologien assoziiert sind. (Daten werden veröffentlicht)
Im Folgenden wird ein Auszug aus dem Brief von Dr. T. Deisher, einem Experten für die Verwendung von Stammzellen für therapeutische Zwecke und Gentherapie, beschrieben, der die Besorgnis über die Risiken hervorhebt, die mit der Verwendung von Impfstoffen verbunden sind, die mit Rückständen menschlicher fötaler Zellen kontaminiert sind :
Dr. T. DEISHER (Schreiben an die Gouverneure - 8. April 2019) - (...) Die Injektion einer menschlichen fetalen DNA-Kontamination in unsere Kinder birgt das Risiko, zwei konsolidierte Pathologien zu verursachen:
- Insertionsmutagenese: menschliche fötale DNA wird in die DNA des Kindes eingebaut und verursacht Mutationen. Gentherapie unter Verwendung homologer Rekombination kleiner Fragmente hat gezeigt, dass Mengen von nur 1.9 ng / ml DNA-Fragmenten bei 100% der injizierten Mäuse zur Insertion von Stammzellen in das Genom führen. Die Spiegel menschlicher fötaler DNA-Fragmente bei unseren Kindern nach Impfung mit MMR-, VARIVAX- (Windpocken) oder Hepatitis-A-Impfstoffen erreichen Werte über 1.9 ng / ml.
- Autoimmunerkrankung: Die fetale menschliche DNA stimuliert die Reaktion des Immunsystems, um den Körper des Kindes anzugreifen.
Unsere Ergebnisse verstärken die experimentellen Beobachtungen von Dr. Deisher erheblich, vor allem die Tatsache, dass die kontaminierende fötale DNA, die in allen in variablen Mengen analysierten Proben vorhanden ist (daher unkontrolliert), vorhanden ist bis zu 300-mal höher als die von der EMA für die krebserzeugende DNA festgelegte Grenze (10 ng / Dosis, entsprechend der in etwa 1000 Krebszellen enthaltenen DNA, die auf der Grundlage einer statistischen Berechnung erhalten wurde, während die Vorsichtsgrenze 100 pg / Dosis beträgt) Grenze, die notwendigerweise auch auf fötale DNA angewendet werden muss, die die DNA zwangsläufig kontaminiert Priorix® Tetra.
Daher muss dieser Impfstoff als defekt und potenziell gefährlich für die menschliche Gesundheit angesehen werden, insbesondere in der pädiatrischen Bevölkerung, die aufgrund von Unreife in den Reparatursystemen viel anfälliger für genetische und Autoimmunschäden ist.
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.corvelva.it/speciale-corvelva/vaccinegate.html
https://www.corvelva.it/speciale-corvelva/vaccinegate-en.html - https://www.corvelva.it/speciale-corvelva/vaccinegate/sequenziamento-del-genoma-completo-di-mrc-5-contenuto-in-priorix-tetra.html
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7059852/
- https://www.corvelva.it/speciale-corvelva/vaccinegate/analisi-metagenomiche-su-priorix-tetra.html
- https://www.federalregister.gov/documents/2010/03/04/2010-4553/guidance-for-industry-characterization-and-qualification-of-cell-substrates-and-other-biological

