سداسي Infanrix والموت المفاجئ: مراجعة لتحديث تقارير السلامة الدورية المقدمة إلى الوكالة الأوروبية للأدوية

اللقاح المعني ، "Infanrix hexa" ، الذي يجمع بين الخناق والكزاز والسعال الديكي والتهاب الكبد الوبائي وشلل الأطفال ونوع B ، تم إنتاجه بواسطة GlaxoSmithKline (GSK) وتم تقديمه في أوروبا في أكتوبر 2000.
اكتشف Puliyel و Sathyamala الإخفاء عن طريق تحليل البيانات في تقارير تحديث السلامة الدورية (PSUR) المتعلقة باللقاح الذي يجب على الشركة المصنعة GSK تقديمه بانتظام إلى الوكالة الأوروبية للأدوية (EMA).
تم تلقي تقارير السلامة السرية الخاصة بهذا اللقاح من قبل Puliyel من باحث إيطالي حصل عليها من EMA بموجب قانون حرية المعلومات - النسخة الإيطالية من الحق في المعلومات في الهند.
وفقا للتحليل ، وجد الأطباء أن أحدث تقرير لسلامة لقاح "Infanrix hexa" مقدم من GSK (2015) ألغى الوفيات ذكرت سابقا من قبل الشركة المصنعة في تقريره السادس عشر (16). لكنهم لاحظوا أنه ليس من الواضح في التقرير كيف تم إلغاء هذه الوفيات.
يلاحظ المؤلفان Puliyel و Sathyamala أنه بعد مرور عشر سنوات على نشر مقال من مركز السيطرة على الأمراض (CDC) يفحص العلاقة بين MMR والتوحد ، اعترف أحد المؤلفين William William Thompson بأنه قد قام هو ومؤلفوه المشاركون بحذف المعلومات. ذات دلالة إحصائية - أي أن الذكور الأمريكيين من أصل أفريقي الذين تلقوا لقاح MMR قبل سن 36 شهرا كانوا أكثر عرضة لمرض التوحد. بعد أن وجد طومسون وزملاؤه دليلًا على هذا الخطر المتزايد ، قاموا بحذف البيانات من الأطفال دون شهادات ميلاد جورجية (وبالتالي استبعدوا عددًا غير متناسب من الأطفال السود) وقدموا بياناتهم قائلين إنه لا يوجد زيادة خطر التوحد. من غير الواضح ما إذا كان مؤلفو PSUR 19 قد قاموا بإلغاء التأهيل بأثر رجعي مماثل للأطفال الذين وثقوا أنهم ماتوا في PSUR 16.
"إذا لم تتم إزالة هذه الوفيات ، لكانت الوفيات بعد التطعيم أعلى بكثير مما كان متوقعًا عن طريق الصدفة. كان يتعين على الشركة المصنعة أن تعترف لـ EMA بأن لقاحها هو سبب هذه الوفيات الزائدة".
يدعي بوليل و Sathyamala أن المنتج "يجب أن يفسر الأرقام المعيبة على ما يبدو التي قدمها إلى السلطات التنظيمية.
زعمت الشركة المصنعة حتى الآن أن الوفيات المبلغ عنها بعد اللقاح "مصادفة" وأنها ستحدث في هؤلاء الأطفال حتى لو لم يتلقوا التطعيمات.
ومع ذلك ، أشار بوليل وساثامالا في تعليقهما في المجلة إلى أن تحليلهما أظهر أن 83٪ من الوفيات المبلغ عنها حدثت مباشرة بعد التطعيم في الأيام العشرة الأولى و 10٪ فقط حدثت في الأيام العشرة التالية.
"لو كانت هذه الوفيات متزامنة ، فلن يتجمعوا جميعًا بعد التطعيم مباشرة ، لكنهم كانوا سيوزعون بالتساوي على مدار فترة العشرين يومًا."
كتب بولييل وساثامالا أن أي حجة تجادل بأن الوفيات المفاجئة بعد التطعيم يقابلها الأرواح التي ينقذها اللقاح غير مقبولة ، بنفس الطريقة التي يعتبر قتل شخص باستخدام أعضائه لإنقاذ خمسة أشخاص آخرين أمرًا غير قانوني. .
"يمكن أن يؤدي إخفاء الوفيات بعد التطعيم إلى منع أو تأخير تقييم ملف تعريف سلامة اللقاح ، وقد يؤدي ذلك إلى وفيات غير ضرورية ومبررة من الناحية الأخلاقية.
يشير المؤلفون إلى أن Hexavac - وهو لقاح مماثل من صنع شركة Sanofi Pasteur والذي تم طرحه أيضًا في السوق عام 2000 ، تم سحبه من السوق الأوروبية في عام 2005. وقد وجد أن وفاة الأطفال زادت خلال يومين من التطعيم.
في السياق الهندي ، يشير المؤلفون إلى أن مراقب المخدرات العام في الهند (DCGI) ينبغي أن يعيد النظر في سياسة الموافقة التلقائية الحالية لجميع الأدوية المصرح بها في الولايات المتحدة وأوروبا. "هذا الاعتماد على العناية الواجبة من قبل EMA يمكن أن يكون خاطئًا ويجب مراجعته."
يشبه "Pentavac" ، الذي ينتج عن معهد Serum Institute of India وتسويقه في الهند ، تشبيه Hexavac و Infanrix Hexa الذي تم إيقافه الآن ، باستثناء أن لقاح السعال الديكي للخلية بالكامل يستبدل بلقاح خلوي. العنصر السادس ، لقاح شلل الأطفال عن طريق الحقن. "
في ضوء تعليقاتهم ، يقترح Puliyel و Sathyamala أنه "من الضروري أن تكون DCGI على دراية بتقارير PSUR المقدمة إلى EMA والمخاوف التي أثيرت من خلال هذا التعليق."
الدراسة
المجلة الهندية لأخلاقيات مهنة الطب على الإنترنت نشرت أولاً 5 سبتمبر ، 2017
سداسي Infanrix والموت المفاجئ: مراجعة لتحديث تقارير السلامة الدورية المقدمة إلى الوكالة الأوروبية للأدوية
يعقوب بوليل ، ساثيمالا
المؤلفون: يعقوب بولييل (مؤلف مناظر -
للاستشهاد: Puliyel J ، Sathyamala C. Infanrix hexa والموت المفاجئ: مراجعة لتقارير تحديث السلامة الدورية المقدمة إلى الوكالة الأوروبية للأدوية. الهندي J ميد الأخلاق. تم النشر عبر الإنترنت في 5 سبتمبر 2017. تم تصحيحه في 9 سبتمبر 2017 *. DOI: 10.20529 / IJME.2017.079
محرر المخطوطة: مالا راماناثان © المجلة الهندية لأخلاقيات مهنة الطب 2017
ملخص
كان هناك العديد من التقارير التلقائية عن الوفاة المفاجئة غير المتوقعة بعد إعطاء إنفريكس هيكسا مباشرة (الدفتريا مجتمعة ، الكزاز ، لقاح السعال الديكي الخلوي ، إلتهاب سنجابية النخاع المعطل ، التهاب الكبد الوبائي والنوع المستدمر من النوع باء). تقدم الشركة المُصنّعة ، GlaxoSmithKline (GSK) ، تقارير دورية دورية لتحديث الأمان (PSUR) حول Infanrix Hexa إلى الوكالة الأوروبية للأدوية (EMA). الأخير هو PSUR * 19. يحتوي كل PSUR على تحليل للوفيات المفاجئة الملحوظة / المتوقعة ، مما يدل على أن عدد الوفيات التي لوحظت فور التطعيم أقل من المتوقع عن طريق الصدفة.
يركز هذا التعليق على هذا الجانب من PSUR الذي يؤثر على القرارات السياسية. لقد قمنا بتحليل البيانات المقدمة في PSUR. من الواضح أن الوفيات التي تم التعرف عليها في PSUR 16 قد تم القضاء عليها بواسطة PSUR 19. وكان عدد الوفيات التي لوحظت فور تلقيح الأطفال الذين تزيد أعمارهم عن سنة واحدة أعلى بكثير مما كان متوقعًا بمجرد حدوث الوفيات التي تم تطهيرها. المستعادة والمدرجة في التحليل.
يجب على الشركة المصنعة توضيح الأرقام التي تم تقديمها إلى السلطات التنظيمية. يجب مراجعة الإجراءات التي اتخذتها EMA لتقييم تنبيهات الشركة المصنعة في PSUR. يقبل المراقب العام للأدوية في الهند تلقائيًا العقاقير واللقاحات المعتمدة من EMA. هناك حاجة لمراجعة الثقة في الاجتهاد من قبل EMA.
مقدّمة
في 23 أكتوبر 2000 ، تم تسويق لقاحين سداسي التكافؤ ، Infanrix hexa® (GlaxoSmithKline plc-GSK) و Hexavac® (Sanofi Pasteur MSD، SNC) ، اللذين يجمعان بين الخناق والكزاز والسعال الديكي والإلتهاب الكبدي B تم ترخيص التهاب سنجابية النخاع المعطل والأنفلونزا المستدمية من النوع B في الاتحاد الأوروبي. بعد الإذن ، كانت هناك عدة تقارير عفوية عن الوفاة المفاجئة غير المتوقعة مباشرة بعد إعطاء هذه اللقاحات السداسية التكافؤ. في عام 2005 ، أجرى فون كريس وزملاؤه (1) تحليلًا مفصلاً قاموا بمقارنة الوفيات التي لوحظت فور التطعيم مع الإصابات المتوقعة. وجدوا أن نسبة الوفيات الموحدة (SMR) في غضون يومين من التطعيم Hexavac قد زادت بشكل كبير في الأطفال الذين تم تطعيمهم في السنة الثانية من العمر.
لم يكن هذا هو الحال مع Infanrix Hexa. بناءً على طلب صاحب ترخيص التسويق ، تم سحب شركة Hexavac في عام 2005 واستمرت شركة Infanrix Hexa في التسويق في أوروبا (2). وفقًا للقانون الأوروبي ، فإن وكالة الأدوية الأوروبية (EMA) مسؤولة عن حماية الصحة العامة من خلال تقييم الأدوية المعتمدة من قبلها كسلطات تنظيمية. الشركات المصنعة مسؤولة عن فعالية وجودة وسلامة عقاقيرهم (3).
أتاحت محكمة القاضي الإيطالية نيكولا دي ليو للجمهور تقارير التحديث الأمني الدوري السري (PSUR) 15 و 16a من 2009 إلى 2011 لشركة GlaxoSmithKline (4). تم الحصول على PSUR 19 (الذي يتضمن PSUR 17 و 18 و 19 ، بتاريخ 15 يناير 2015) من قبل باحث إيطالي من EMA وفقًا للمادة 3 من قواعد EMA (EMA 110196/2006 المؤرخ 30 نوفمبر 2010) (5 ). أرسل الطبيب الإيطالي هذا PSUR إلى المؤلف الأول (JP) ، وطلب منه كتابة تقرير لتقديمه إلى البرلمان الأوروبي. ويستند هذا التعليق على كل هذه PSURs. في سياق جانب الأمان الذي تم تسليط الضوء عليه سابقًا بواسطة von Kries (1) ، يفحص هذا التعليق الموت المفاجئ بعد استخدام لقاح Infanrix Hexa. لا يتم فحص الجوانب الأخرى المشمولة في PSUR.
PSUR 15 - تجمع الموتى بعد التطعيم
معظم الوفيات التي تحدث في فترة ما بعد الولادة هي بسبب الالتهابات أو العيوب الخلقية أو الأورام الخبيثة أو الحوادث. نادراً ما يموت الأطفال بدون سبب واضح ، وبالتالي يتم تصنيف الوفيات على أنها (15) متلازمة الموت المفاجئ (SIDS) ، والمعروفة في PSUR بأنها الوفاة التي تحدث في السنة الأولى من العمر وتبقى غير معروفة بعد التشريح ، أو (ii) الموت المفاجئ غير المتوقع (SOUTH) ، والمعروف باسم الموت الذي يحدث خلال العامين الأولين من العمر ، والذي لا يزال غير مفسر بعد التاريخ السريري والنهائي للأحداث ، ولكن دون تشريح معًا ، يعتبر هذان الاثنان موتًا مفاجئًا (SD) في PSUR 2. يتم إعطاء عدد معين من اللقاحات للأطفال دون سن عامين في يوم معين ، وعدد الأطفال الذين تم تلقيحهم في جميع أنحاء العالم كبير جدًا. من المحتمل أن يموت بعض الأطفال الذين تم تلقيحهم عن طريق الخطأ بسبب SIDS / SUD بالمناسبة ، فإن مثل هذه الأحداث قد تحدث حتى لو لم يتم تحصين هؤلاء الأطفال في ذلك اليوم. للتأكد مما إذا كانت هذه الوفاة ناجمة عن التطعيم أو كان حدثًا عارضًا ، يتم إجراء تحليل SD متوقع / متوقع. يقيم التحليل ما إذا كان عدد الوفيات التي لوحظت بعد التطعيم يتجاوز ما يمكن التنبؤ به عن طريق الصدفة.
الوفيات المفاجئة: لوحظ نحو التوقعات
يشرح PSUR 15 كيفية إجراء هذا التحليل (4: p 782): "قام المجتمع بتقييم ما إذا كان عدد الوفيات المفاجئة المبلغ عنها في هذه الفئة العمرية والتي تجاوزت الرقم الأول يمكن أن تحدث بشكل عشوائي. منذ التوزيع العمري في حالة عدم معرفة الأشخاص الذين تم تطعيمهم ، افترضت الشركة أن نسبة الأحداث الضائرة حسب العمر تمثل التوزيع العمري الفعلي عند التطعيم.وبالتالي يمكن تقدير أن 90,6٪ من جميع متلقي Infanrix كانت Hexa في السنة الأولى من العمر ، و 9,4٪ كانت في السنة الثانية من العمر ، ومن ثم قُدِّر عدد الجرعات (منذ الإطلاق) بـ 54.927.729 و 5,698,904 على التوالي. البلد الرئيسي حيث يتم توزيع جرعات Infanrix Hexa (حوالي 30 ٪ في ألمانيا وحدها) ، كان من المفترض أن يكون معدل حدوث الموت المفاجئ الذي لوحظ في ألمانيا ممثلاً لجميع السكان المتلقين لـ Infanrix Hexa (المكتب الفيدرالي)إحصائي ألماني ، Statistisches Bundesamt ؛ معدل الحدوث في السنة الأولى من العمر: 0,454 / 1000 ولادة حية ؛ السنة الثانية: 0.062 لكل 1000 مولود حي ، بيانات عام 2008).
"تقوم PSUR بتوثيق الوفاة المبلغ عنها خلال 20 يومًا من التطعيم. وكان عدد الوفيات المرصودة أقل من المتوقع (الجدول 1).
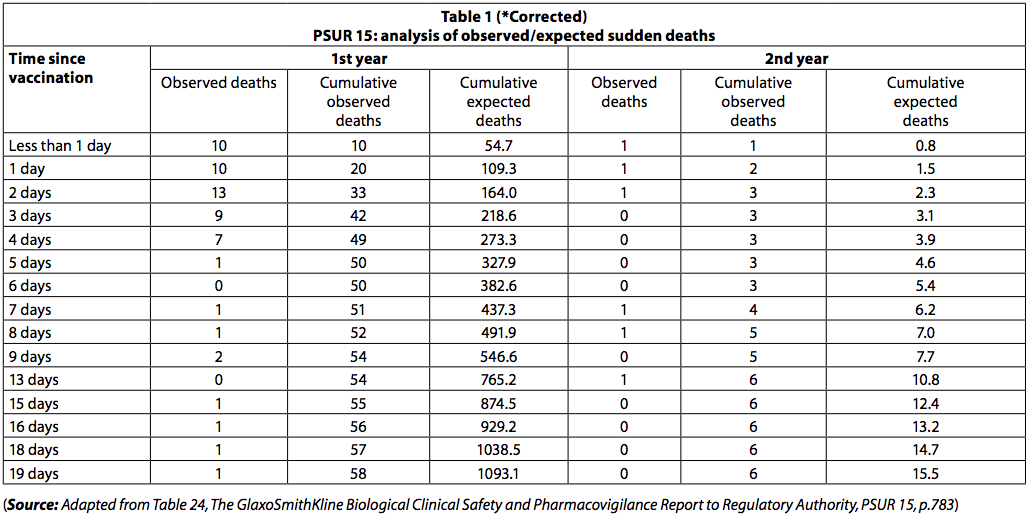
ومع ذلك ، بين الأطفال حديثي الولادة ، كانت هناك مجموعة من الوفيات بعد التطعيم مباشرة ، حيث حدثت 42 حالة وفاة في الأيام الثلاثة الأولى بعد التطعيم و 8 فقط في الأيام الثلاثة التالية. من بين أولئك الذين تقل أعمارهم عن عام واحد ، حدثت 3 حالة وفاة (54٪) في الأيام العشرة الأولى و 93 (4٪) في الأيام العشرة التالية. إذا كانت الوفيات عبارة عن "وفيات عشوائية من الدول الجزرية الصغيرة النامية" ، فإن هذا التفاوت في عدد الوفيات خلال الفترتين الزمنيتين لن يتم ملاحظته.
كانت الوفيات الناجمة عن SIDS قد وزعت بالتساوي على مدار 20 يومًا.
حقيقة أن معدل الوفيات ينخفض بسرعة مع مرور الوقت بعد التحصين يشير إلى أن الوفيات قد تكون ذات صلة بالتطعيم.
وبالمثل ، حدثت 5 وفيات (83,3٪) بين الأطفال فوق سن سنة واحدة في الأيام العشرة الأولى وحدثت وفاة واحدة (10٪) في الأيام العشرة التالية. ولوحظ أيضًا تجميع الوفيات المبلغ عنها في PSUR 17 في PSUR 10 ، وقد تم التعليق على هذا في وقت سابق (15).
إجابة GlaxoSmithKline
ردًا على هذا النقد (7) ، اقترح الرئيس التنفيذي لشركة GlaxoSmithKline (GSK) (الرئيس التنفيذي) السير أندرو ويتي ، من خلال الدكتور نورمان بيج ، الرئيس الطبي للشركة ، في رسالة أن هناك احتمالية أكبر بكثير للتفكير في ارتباط سببي محتمل ثم إبلاغ شركة GSK عن حدث ضار إذا حدث بعد وقت قصير من التطعيم وليس بعد أسابيع. وكتب أيضًا: "في ضوء ما سبق ، نظل واثقين من الاستنتاجات التي توصلت إليها شركة GSK سابقًا ومشاركتها مع الهيئات التنظيمية والسلطات الصحية حول العالم ، والتي تفيد بأن البيانات المتاحة حاليًا لا تشير إلى زيادة خطر الموت المفاجئ للرضع بعد التطعيم باستخدام Infanrix hexa. إذا تغيرت البيانات والمعلومات المتاحة وتشير إلى وجود مخاطر متزايدة ، فإننا نظل ملتزمين بإخطار السلطات على الفور واتخاذ الإجراءات اللازمة لإيصال هذه البيانات والمعلومات إلى المتخصصين في الرعاية الصحية. "
تحتوي هذه الاستجابة على إقرار ضمني بأنه لم يكن هناك يقظة نشطة خلال فترة ما بعد التطعيم وأن الوفيات التي تم الإبلاغ عنها تلقائيًا لـ GSK فقط كانت مدرجة تحت عنوان "الوفيات الملحوظة". هذا يمكن أن يسبب التقليل من الوفيات بعد التطعيم. تجدر الإشارة إلى أن عدد جرعات اللقاح الموزعة يستخدم في "الوفيات المتوقعة". يعترف التقرير بأن جميع جرعات اللقاح الموزع لم تستخدم بالضرورة. بهذه الطريقة ، تضخمت أعداد "الوفيات المتوقعة".
ومع ذلك ، نظرًا لتفسير الرئيس التنفيذي وتأكيده أن GSK قد التزمت بإخطار السلطات وأخصائيي الرعاية الصحية على الفور بأي مخاطر متزايدة مع Infanrix Hexa ، فإن قضية تجميع الوفيات لم تخضع لمزيد من الدراسة.
PSUR 16: مضاعفة عدد الوفيات المتوقعة
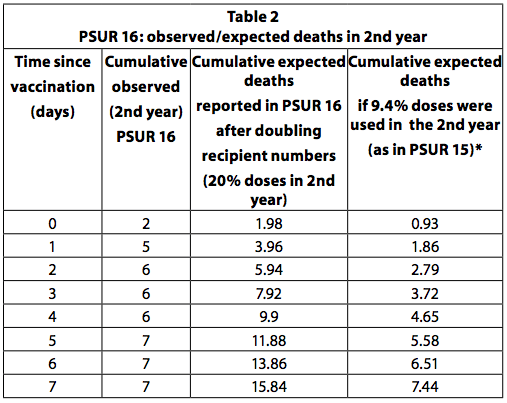
إذا تلقى جميع الأطفال الذين تلقوا الجرعة الأولى من اللقاح ما مجموعه أربع جرعات وتم إعطاء آخر جرعة في السنة الثانية من العمر ، فيمكن تقدير أن ربع (25٪) الجرعات تُعطى للأطفال الأكبر سناً إلى سنة. هذا هو جدول التطعيم الموصى به في ألمانيا. ومع ذلك ، فإن بعض الدول ، مثل إيطاليا ، توصي بثلاث جرعات فقط ، جميعها في السنة الأولى ، ولا يوجد في الثانية. بالإضافة إلى ذلك ، لا يتلقى جميع الأطفال جميع الجرعات الموصى بها. حتى 20-25 ٪ من الجرعات من غير المرجح أن تستخدم في السنة الثانية. في PSUR 15 ، تم تقدير أن 90,6 ٪ من الجرعات المباعة استخدمت في الأطفال دون سن سنة واحدة و 9,4 ٪ للذين تزيد أعمارهم عن سنة واحدة. في PSUR 16 ، ارتفع تقدير الجرعات المستلمة في السنة الثانية بأكثر من الضعف (من 9,4 ٪ إلى 20 ٪) ، وبالتالي تضاعف تقدير الوفيات المتوقعة. على الرغم من مضاعفة الوفيات المتوقعة ، كان عدد الوفيات التي لوحظت في السنة الثانية أعلى من المتوقع في الأيام الثلاثة الأولى بعد التطعيم (الجدول 3 ، صفحة 36). إذا كانت التقديرات في PSUR 249 بأن 15٪ من الجرعات تستخدم في السنة الثانية صحيحة ، فإن هذا ينطبق أيضًا على PSUR 9,4 ، وبالتالي فإن الوفيات المرصودة أعلى من الوفيات المتوقعة في الأيام السبعة الأولى.
PSUR 19: الوفيات المتوقعة حسب البلد والنسبة السنوية للجرعات
في PSUR 19 ، تم حساب المتوسط المرجح للتقويم لمعدلات حدوث الوفيات المفاجئة من ألمانيا وفرنسا وهولندا للوصول إلى الحدوث المتوقع للوفيات المفاجئة.
بعبارات بسيطة جدا ، هذا يعني أنه إذا تم توزيع 60 ٪ من الجرعات في ألمانيا في سنة معينة ، فإن معدل SD (الموت المفاجئ) في ألمانيا قد حصل على وزن 60 ٪ عند حساب معدل SD. عموما لتلك السنة ؛ إذا تم توزيع 30 ٪ في فرنسا ، فإن معدل SD في فرنسا ساهم بنسبة 30 ٪ ، وتم إعطاء وزن 10 ٪ لمعدل SD الهولندي. أخيرًا ، تم حساب معدل SD العالمي لجميع السنوات معًا.
تم حساب معدل SD الإجمالي على أنه 0.0102 / 1000 مولود حي للسنة الثانية. هذا الرقم هو سدس التردد المتوقع المستخدم في PSUR 15 و 16 (الذي يحسب الوفيات المفاجئة عند 0,062 / 1000 مولود حي ، باستخدام البيانات الألمانية).
تم الإبلاغ عن فاصل الثقة Poisson (CI) من 95 ٪ من الوفيات لوحظ في السنة الثانية في الجدول 8 ap 447 من PSUR 19. ويذكر أنه بالنسبة للسنة الثانية من العمر ، كان عدد الوفيات التي لوحظت أعلى ، أيضا إن لم يكن بشكل ملحوظ ، من تلك الوفيات المتوقعة خلال فترة خطر من 1-4 أيام بعد التطعيم.
وفيات مفقودة في PSUR 19
من PSUR 16 إلى PSUR 19 ، زاد إجمالي جرعات اللقاح من 69 إلى 112 مليون. وفقًا لـ PSUR 19 ، كان من المفترض أن 20,2٪ من الجرعات الموزعة كانت تُعطى للأطفال في السنة الثانية من العمر (PSUR 19 ، ص 436-448). استبعدت حالات الوفاة التي لم يُعرف فيها سن التطعيم أو تاريخ الوفاة أو تجاوز وقت الوفاة 19 يومًا من التطعيم.
ال تبلغ PSUR 19 (الوفيات حتى 22 أكتوبر 2014) عن الوفيات المفاجئة المذكورة في PSUR 16 (حالات الوفاة التي حدثت حتى 22 أكتوبر 2011). تجدر الإشارة إلى أنه في PSUR 16 تم تسجيل عمر الطفل الذي توفي بعد التطعيم ووقت الوفاة (خلال 14 يومًا من التطعيم).
الوفيات التراكمية المُبلغ عنها أقل في PSUR 19 عنها في PSUR 16. أما بالنسبة للأطفال الذين تزيد أعمارهم عن سنة واحدة ، فإن PSUR 19 يسجل حدوث 5 وفيات فقط في أول 19 يومًا بعد التطعيم ، في حين يبلغ PSUR 16 8 الأرقام ليست متسقة مع بعضها البعض. نتساءل لماذا هذا هو الحال.
بعد عشر سنوات من نشر مقال CDC (مركز السيطرة على الأمراض) الذي يفحص العلاقة بين لقاح الحصبة والنكاف والحصبة الألمانية (MMR) والتوحد (8) ، اعترف أحد المؤلفين ، William Thompson ، بأن فشل هو وزملاؤه في تقديم معلومات ذات دلالة إحصائية بأن الذكور الأمريكيين من أصل أفريقي الذين تلقوا MMR قبل سن 36 شهرًا كانوا أكثر عرضة للإصابة بالتوحد (9). حذف المؤلفون بيانات الأطفال الذين ليس لديهم شهادات ميلاد في جورجيا (10) ، من أجل استبعاد عدد غير متناسب من الأطفال السود ، وقدموا بياناتهم من أجل إظهار أنه لم تكن هناك زيادة في خطر.
من غير الواضح ما إذا كان مؤلفو PSUR 19 قد استبعدوا بالمثل الأطفال الموتى والموثقين في PSUR 16.
يعرض الجدول 3 الوفيات المرصودة والمتوقعة المبلغ عنها في PSUR 19 والوفيات التي لوحظت بعد استعادة الوفيات المبلغ عنها في PSUR 16.
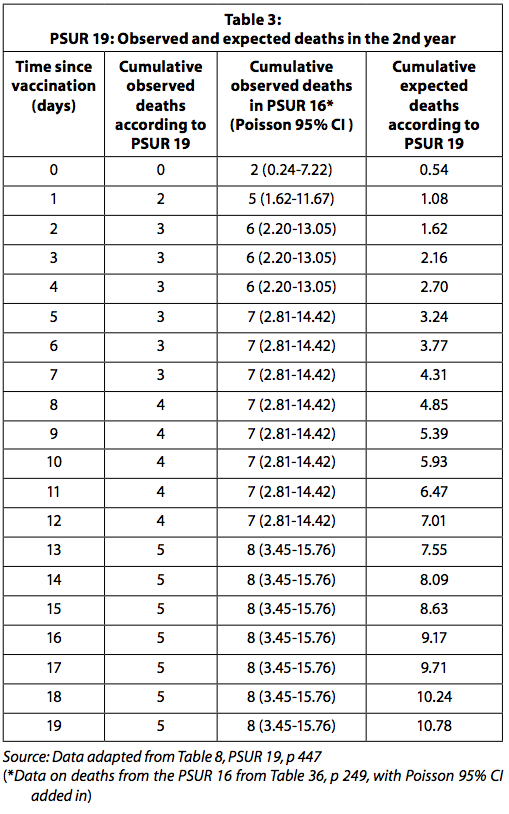
عند استخدام بيانات الوفيات المرصودة في PSUR 16 ، يكون عدد الوفيات المرصودة أعلى بكثير من المتوقع في الأيام الأربعة الأولى بعد التطعيم. يجب أن يؤخذ في الاعتبار ، كما هو موضح أعلاه ، أنه نظرًا لأن عدد الوفيات المرصودة يتم جمعه بشكل سلبي ، فمن المحتمل أن يتم التقليل من شأنه. من ناحية أخرى ، من المحتمل المبالغة في تقدير الوفيات المتوقعة حيث يتم حسابها بافتراض أن جميع الجرعات الموزعة قد تم استخدامها دون أي خسارة ولم يتم تجاهل أي لقاح بسبب انتهاء صلاحيته. كان من المتوقع أن تقوم شركة GSK بالإبلاغ عن زيادة خطر الوفاة ذات الدلالة الإحصائية في الأيام الأربعة بعد التطعيم للسلطة التنظيمية والأطباء.
الجرعات المستخدمة في السنة الثانية
PSUR 19 يفترض أن 20,2 ٪ من الجرعات قد استخدمت في السنة الثانية. ينص على أن توزيع العمر الذي يتم فيه تلقيح الأشخاص غير معروف ، وقد توقعت الشركة أن نسبة الأحداث الضائرة (بما في ذلك الوفاة) حسب العمر تمثل التوزيع الفعلي للعمر عند التطعيم. وبالتالي ، نظرًا لأن 20,2٪ من الأحداث السلبية حدثت في الأطفال الذين تزيد أعمارهم عن سنة واحدة ، افترضت الشركة أن 20,2٪ من الجرعات قد استخدمت لهذه الفئة العمرية.
من السهل تقدير عدد الجرعات المستخدمة في السنة الثانية بناءً على الأحداث الضارة الملحوظة (بما في ذلك الوفاة) ، ثم استخدم تقدير الجرعة هذا لحساب عدد الوفيات المتوقعة ، وأخيراً قارنها بعدد الوفيات المرصودة - بالنظر إلى أن يتم حساب تقدير الوفيات المتوقعة بشكل أساسي من الأحداث السلبية الملحوظة (بما في ذلك الوفاة).
على افتراض أن جميع الوفيات بعد التطعيم متزامنة وغير متسببة في لقاح SIDS / SOUTHS ، وبالنظر إلى أنه (وفقًا لـ PSUR 19) ، فإن التواتر الطبيعي للموت المفاجئ في السنة الأولى أعلى 44 مرة من السنة الثانية (0.441) / 1000 في السنة الأولى و 0.0102 / 1000 في السنة الثانية) ، يجب تحصين 44 مرة أكثر من الأطفال في السنة الثانية للوصول إلى نفس عدد الوفيات كما في السنة الأولى.
في مجموعة من 100 حالة وفاة ، إذا حدثت 20٪ من الوفيات المفاجئة في السنة الثانية و 80٪ في السنة الأولى ، فيجب تطعيم 880 طفلاً في السنة الثانية مقابل كل 20 حالة تطعيم في السنة الأولى. في هذه الحالة ، سيكون من المفترض أن 44٪ من جميع جرعات Infanrix hexa قد استخدمت في السنة الثانية و 80٪ فقط في السنة الأولى (بدلاً من العكس). هذا يعكس سخافة حساب توزيع الجرعة حسب العمر ، بناءً على التوزيع العمري للأحداث السلبية ، كما هو الحال في وثيقة GSK.
الطريقة الوحيدة لتقييم عدد الجرعات المستخدمة في السنة الثانية هي النظر في جداول التطعيم في مختلف البلدان - النظر في البلدان التي توصي بالجرعة الرابعة في السنة الثانية وتلك التي لا توصي الجرعات في السنة الثانية. يمكن تخصيص وزن لعدد الجرعات الموزعة في هذه البلدان. يجب مراعاة معدل التسرب (الأطفال الذين يتركون برنامج التطعيم بعد تلقي جرعات اللقاح الأولى) في الحساب النهائي للنسبة المئوية للجرعات المستخدمة في السنة الثانية. يبدو أن التقدير المعقول للجرعات المستخدمة في السنة الثانية هو 9,4 ٪ من إجمالي الجرعات وهذا هو الرقم المستخدم في PSUR 15.
المعضلة الأخلاقية - مشكلة العربة
لا يحاول هذا التعليق فحص ما إذا كانت هذه الوفيات المفرطة بعد التطعيم (التي يُفترض أنها ناجمة عن اللقاح) يمكن تعويضها بالأرواح التي أنقذها المرض عن طريق الوقاية التي تم الحصول عليها باستخدام اللقاح. في تجربته العقلية الكلاسيكية ، التي تسمى معضلة العربة ، يسأل Philippa Foot ما إذا كان من الأخلاقي إعادة توجيه العربة التي هربت من مسار السكك الحديدية الذي كان من شأنه أن يقتل خمسة أشخاص على مسار آخر حيث مات واحد فقط (11). . في متغير من معضلة العربة ، يكون الشخص الوحيد على المسار البديل هو طفل الشخص الذي يمكنه تبديل المقطوعات.[2] تفترض جوديث طومسون أنه يمكن إنقاذ حياة خمسة أشخاص عن طريق زرع أعضاء من متبرع سليم ، وتتساءل عما إذا كان من الأخلاقي قتل شخص عن قصد لإنقاذ الخمسة الآخرين (12). يجادل الأخلاقيون أن الغاية لا تبرر الوسيلة. إذا قمت بإخفاء الوفاة بعد التطعيم ، يمكنك منع / تأخير تقييم ملف تعريف سلامة اللقاح وهذا له القدرة على التسبب في وفيات غير ضرورية ، يصعب تبريرها أخلاقياً.
الصلة بالهند
السلطة التنظيمية لحكومة الهند هي مراقب المخدرات العام في الهند (DCGI). وفقًا لقواعد DCGI ، يتم اعتماد الأدوية المعتمدة في بلد واحد أو أكثر ، مثل الولايات المتحدة والمملكة المتحدة وكندا واليابان وأستراليا ودول الاتحاد الأوروبي ، في الهند (13). هناك حاجة فقط إلى دراسات إضافية لتقييم تأثير العوامل العرقية على فعالية وسلامة وجرعة وأنظمة الدواء من المخدرات (14).
في الآونة الأخيرة ، تم نشر دراسات تبحث في مناعة وسلامة اللقاح المركب سداسي التكافؤ في تجارب صغيرة في الهند (15,16،17). بالإضافة إلى ذلك ، نشر قسم طب الأطفال الهندي افتتاحية بعنوان "اللقاحات السداسية التكافؤ: مستقبل التحصين الروتيني؟" (XNUMX) ، الذي اقترح أنه سيتم الترويج لهذا اللقاح المركب في الهند. من المهم أن تدرك السلطة التنظيمية في الهند المخاوف التي أثيرت في هذا التعليق على تقارير PSUR ، خاصة وأن أنظمة المراقبة في الهند ضعيفة.
ملخص وخاتمة
أبلغ Von Kries (1) عن زيادة ملحوظة إحصائيا في SMR في الأطفال في السنة الثانية من حياتهم ، في غضون يومين من التطعيم مع Hexavac® (واحد من اثنين من لقاح سداسي التكافؤ المأذون به ، تم سحبها الآن).
في تقارير تحديث السلامة الدورية ، تقوم GSK ، شركة إنتاج Infanrix hexa ، بتقييم ما إذا كان عدد الوفيات المفاجئة التي تم الإبلاغ عنها بعد تلقيح عقاقيرهم قد تجاوز العدد الذي يمكن توقعه عن طريق الصدفة. يوحي تجميع الوفيات بعد التطعيم مباشرة أن الوفاة قد تكون ناجمة عن اللقاح.
علاوة على ذلك ، يوضح تحليلنا أن الوفيات التي تم التعرف عليها في PSUR 16 قد تم القضاء عليها من PSUR 19. يتم الإبلاغ عن الوفيات التي تمت ملاحظتها تلقائيًا لـ GSK ومن المحتمل أن يتم التقليل من قيمتها. بإضافة الوفيات التي تم تطهيرها من PSUR 16 ، هناك زيادة ذات دلالة إحصائية في خطر الوفاة في الأيام الأربعة الأولى بعد التطعيم ، مقارنةً بالوفيات المتوقعة. سيحتاج المصنعون إلى توضيح سبب عدم إدراج هذه الوفيات في PSUR 19. ولم يتم الكشف عن زيادة خطر الوفاة إلى السلطة التنظيمية أو موظفي الرعاية الصحية الذين يديرون هذا اللقاح.
بالنظر إلى ما تقدم ، من الصعب فهم كيف قبلت EMA PSUR 19 على أساس رمزي. يمكن القول أن العناية الواجبة لم تمارس ، بحيث تعرض العديد من الأطفال دون داع لخطر الموت.
يجب أن تكون DCGI على دراية بالقيود في Infanrix Hexa PSUR.

