Ocena skuteczności i wydajności szczepionek przeciw grypie u zdrowych dzieci: przegląd systematyczny

Lancet
T Jefferson, S Smith, V Demicheli, A Harnden, A Rivetti, C Di Pietrantonj
2005
Abstrakcyjny
Kontekst Naszym celem była ocena dowodów skuteczności i skuteczności żywych atenuowanych i inaktywowanych szczepionek przeciw grypie u dzieci w wieku do 16 lat.
Metody Przeglądaliśmy Cochrane Library, MEDLINE, EMBASE Biological Abstracts i Science Citation Index od czerwca 2004 r., W dowolnym języku, i skontaktowaliśmy się z odpowiednimi producentami szczepionek i autorami badań w celu zidentyfikowania dodatkowych danych. Uwzględniliśmy randomizowane, kohortowe i kontrolne przypadki porównujące skuteczność szczepionek przeciw grypie (redukcja przypadków potwierdzonych laboratoryjnie), skuteczność szczepionek przeciw grypie podobnych (redukcja objawów objawowych) lub oba , z placebo lub bez interwencji. Przeanalizowaliśmy następujące wyniki: grypa, choroba grypopodobna, hospitalizacje, nieobecności w szkole, powikłania i wtórne przenoszenie.
Wyniki Uwzględniono 14 randomizowanych kontrolowanych badań, osiem badań kohortowych, jedno badanie kontrolne i jedno randomizowane kontrolowane badanie dotyczące stosowania szczepionki wewnątrz epidemicznej. Żywe atenuowane szczepionki przeciw grypie są skuteczne w 79% i 38% u dzieci w wieku powyżej 2 lat w porównaniu z placebo lub immunizacją. Szczepionki inaktywowane miały niższą skuteczność (65%) niż żywe szczepionki atenuowane, a u dzieci w wieku 2 lat lub mniej miały podobny wpływ na placebo. Skuteczność szczepionek inaktywowanych wynosiła około 28% u dzieci w wieku powyżej 2 lat.
Szczepionki skutecznie zmniejszały długie nieobecności w szkole (ryzyko względne 0-14 [95% CI 0-07]). Badania oceniające wpływ szczepionek na wtórne przypadki, chorobę dolnych dróg oddechowych, ostre zapalenie ucha środkowego i pobyt w szpitalu nie sugerowały żadnej różnicy w porównaniu z placebo lub standardowym leczeniem, ale brakowało mocy statystycznej.
Interpretacja Szczepionki przeciw grypie (szczególnie żywe szczepionki atenuowane dwudawkowe) są skuteczne u dzieci w wieku powyżej 2 lat. Skuteczność i skuteczność szczepionek znacznie się różnią. Tylko dwa małe badania oceniały wpływ szczepionek przeciw grypie na przyjęcia do szpitala i żadne z nich nie oceniało zmniejszenia śmiertelności, poważnych powikłań i przenoszenia grypy w społeczności.
Jeśli szczepienie przeciwko grypie u dzieci ma być zalecane jako polityka zdrowia publicznego, pilnie potrzebne są szeroko zakrojone badania oceniające tak ważne wyniki i dokonujące bezpośrednich porównań szczepionek.
wprowadzenie
Wysiłki mające na celu zapobieganie rocznemu rozprzestrzenianiu się grypy koncentrowały się na stosowaniu szczepionek. Do tej pory kampanie szczepień i ubezpieczenia były skierowane do osób w wieku 65 lat lub starszych. W sytuacji niepandemicznej wybór strategii zapobiegawczej polega na uodpornieniu niektórych kategorii populacji, na przykład dzieci, osób starszych, osób z chorobami przewlekłymi, pracowników służby zdrowia lub całej populacji.
Komitet Doradczy ds. Praktyk Szczepienia Amerykańskiej Akademii Pediatrii i Amerykańskich Centrów Kontroli i Prewencji Chorób1 (Komitet Konsultacyjny ds. Szczepień Centrów Kontroli i Zapobiegania Chorobom Stanów Zjednoczonych) zalecił, aby szczepienie przeciw grypie dzieci w wieku od 6 do 23 miesięcy było wprowadzane jako środek ochrony zdrowia publicznego począwszy od sezonu grypowego 2004-05. Deklaracja Komitetu Doradczego ds. Szczepień z maja 2004 r. Zatytułowana Zapobieganie i kontrola grypy 2 (Zapobieganie i kontrola grypy) zaleca również szczepienie osób pozostających w bliskim kontakcie z niemowlętami w wieku od 0 do 23 miesięcy.
W Kanadzie Krajowy Komitet Doradczy ds. Szczepień3 (Krajowy Komitet Doradczy ds. Szczepień) poszedł w tym samym kierunku w lutym 2004 r. Główne tematy rozszerzenia szczepień na zdrowe dzieci w wieku od 6 do 23 miesięcy4-6 i ci, którzy uczęszczają do szkoły6,7 obejmują zmniejszenie: liczby pacjentów z grypą; liczba nadwyżek przyjęć; śmiertelność osób starszych w rodzinach z dziećmi; kontakty w służbie zdrowia (np. lekarze rodzinni); liczba recept na antybiotyki; oraz nieobecności w pracy dla dzieci i konkubentów.
Logiczny proces decyzyjny dotyczący zapobiegania grypie jest skomplikowany z powodu braku wiarygodnych prognoz dotyczących działania wirusa i niepewności co do działania szczepionek w różnych grupach wiekowych.
W przeglądzie Cochrane szczepionek przeciw grypie u zdrowych osób dorosłych 8zauważono zauważalną różnicę między skutecznością szczepionek przeciwko grypie (redukcja przypadków potwierdzonych laboratoryjnie) a skutecznością przeciwko chorobom podobnym do grypy (redukcja przypadków objawowych). Dokładna ocena skuteczności i wydajności szczepionek przeciw grypie jest niezbędna, aby umożliwić uzasadniony wybór między alternatywnymi strategiami.
Naszym celem było zidentyfikowanie i ocena badań porównawczych oceniających skuteczność i skuteczność szczepionek przeciw grypie u zdrowych dzieci w wieku poniżej 16 lat.
Nasz artykuł jest częścią nadchodzącego większego przeglądu Cochrane, który obejmuje testy bezpieczeństwa szczepionek.9
Metody i badania
Aby zidentyfikować raporty z badań i przeglądy systematyczne, do końca maja 2004 r. Przeszukaliśmy następujące elektroniczne bazy danych: Bibliotekę Cochrane, w tym bazę danych przeglądów systematycznych Cochrane, bazę danych streszczeń recenzji skuteczności NHS oraz Centralny rejestr Cochrane kontrolowanych prób (CENTRAL); MEDLINE (OVID, od stycznia 1966); EMBASE (Dialog, 1974–79; SilverPlatter, od 1980); Biological Abstracts (SilverPlatter, od 1969); oraz Science Citation Index (Web of Science, od 1974).
Podjęliśmy badania w dowolnym języku.
Szczegółowy opis strategii wyszukiwania znajduje się w dodatku internetowym 1 (http://image.thelancet.com/extras/04art9306webappendix1.pdf).
Aby zidentyfikować dodatkowe opublikowane i niepublikowane badania, przeszukaliśmy indeks cytowań naukowych w celu znalezienia artykułów powołujących się na odpowiednie badania. Uwzględniliśmy również te badania w PubMed i skorzystaliśmy z funkcji Powiązane artykuły. Oceniliśmy bibliografie wszystkich uzyskanych odpowiednich artykułów oraz wszelkie recenzje opublikowane do dalszych badań. W celu uzyskania wyjaśnień skontaktowaliśmy się z producentami szczepionek lub z autorami odpowiednich badań.
wybór
Wybraliśmy randomizowane badania kliniczne, badania kohortowe i badania kontrolne przypadków (załącznik internetowy 2; http://image.thelancet.com/extras/04art9306webappendix2.pdf) w celu oceny immunizacji dzieci w wieku 16 lat i poniżej w dowolnym położeniu geograficznym za pomocą dowolnej szczepionki przeciw grypie podanej niezależnie, w dowolnej dawce, preparacie lub harmonogramie, w porównaniu z placebo lub bez interwencji.
Zdecydowaliśmy się dołączyć dowody z nierandomizowanych badań porównawczych, aby poprawić trafność przeglądu.
Wybierając badania, wzięliśmy pod uwagę następujące podstawowe miary wyniku: skuteczność i skuteczność zapobiegawcza; przypadki grypy potwierdzone przez izolację wirusa, wsparcie serologiczne, każdy inny rodzaj testu laboratoryjnego w celu identyfikacji wirusa (przypadki grypy) lub ich kombinacja; przypadki chorób grypopodobnych w ciągu 1 roku po zaszczepieniu; hospitalizacje z powodu grypopodobnej choroby lub grypy; zgony (z powodu choroby grypopodobnej lub grypy); oraz wszelkie inne bezpośrednie lub pośrednie wskaźniki wpływu choroby. Nie wzięliśmy pod uwagę danych dotyczących wyników serologicznych, ponieważ naszym celem była ocena dowodów wpływu szczepień na zdrowie publiczne.
Ekstrakcja danych i ocena ważności badania
Dwóch z nas (SS i AR) niezależnie zastosowało kryteria włączenia do wszystkich zidentyfikowanych i odzyskanych przedmiotów, a następnie wyodrębniło dane z włączonych badań na standardowych formularzach Pola Szczepionek Cochrane. Procedura była nadzorowana i arbitrażowana przez TJ i VD.
Oceniliśmy jakość metodologiczną dla randomizowanych badań kontrolowanych na podstawie kryteriów z podręcznika recenzenta Cochrane.10 Ocenialiśmy badania według losowości, generowania sekwencji i ukrywania alokacji, badań ślepych i kolejnych badań. Oceniliśmy jakość badań nierandomizowanych w odniesieniu do obecności możliwych czynników zakłócających. Do oceny badań wykorzystaliśmy schody Newcastle-Ottawa.11
Ze względu na brak dowodów empirycznych na wpływ jakości metodologicznej na wyniki badań nierandomizowanych, zastosowaliśmy jakość w fazie analizy jako sposób interpretacji wyników poprzez stopniową analizę wrażliwości. Pełne informacje na temat oceny jakości są dostępne od odpowiedniego autora.
Wprowadziliśmy wyodrębnione dane do oprogramowania Cochrane RevMan (wersja 4.2, Cochrane Collaboration, Oxford, Wielka Brytania). Agregacja danych zależała od czułości i jednorodności użytych definicji narażenia, populacji i wyników. Gdy badania były jednorodne, przeprowadziliśmy metaanalizę w ramach każdej kategorii projektu. Podsumowaliśmy szacunki wydajności i skuteczności jako ryzyko względne z 95% CI. Skuteczność absolutnej szczepionki obliczono jako 1 minus ryzyko względne i wyrażono jako procent.
Rozpoczęliśmy stopniową analizę sensoryczną, wyłączając badania wykonane w byłym Związku Radzieckim z naszej metaanalizy. Przeprowadziliśmy również analizę podgrup, gdy dostępne były dane według rodzaju podanej szczepionki, wieku osób i specyfiki definicji wyników.
Stratyfikacja wieku (≤2 lata, ≤6 lat i> 6 lat) wskazuje na najczęstszą stratyfikację opisywaną w włączonych badaniach. Aby ocenić wpływ na niejednorodność statystyczną, obliczyliśmy I2 dla każdego oszacowania zagregowanego.12 Statystyka ta może być interpretowana jako proporcja całkowitej zmienności między szacunkami efektu, która wynika raczej z niejednorodności niż z błędu próbkowania i jest wewnętrznie niezależna od liczby badań. Kiedy ja2 wynosi mniej niż 30%, nie ma obaw dotyczących heterogeniczności statystycznej.12-14 Zastosowaliśmy modele efektów losowych, aby wyjaśnić wariancję badania w naszych ustaleniach.15
Rola źródła finansowania
Sponsor nie brał udziału w projektowaniu badania, gromadzeniu danych, analizie danych, interpretacji danych ani pisaniu raportów. Autor miał pełny dostęp do wszystkich danych z badań i ostatecznie był odpowiedzialny za decyzję o przedłożeniu do publikacji.
wyniki
Spośród 1204 tytułów zidentyfikowanych w naszych badaniach wybraliśmy i uzyskaliśmy 125 raportów z badań, które mogą spełniać kryteria włączenia (ryc. 1). 100 raportów zostało wykluczonych. Najczęstszą przyczyną wykluczenia był brak niezależnych kontroli (n = 29) i model nieporównawczy (n = 15). Pełna lista z podstawami wykluczenia jest dostępna na żądanie autora.
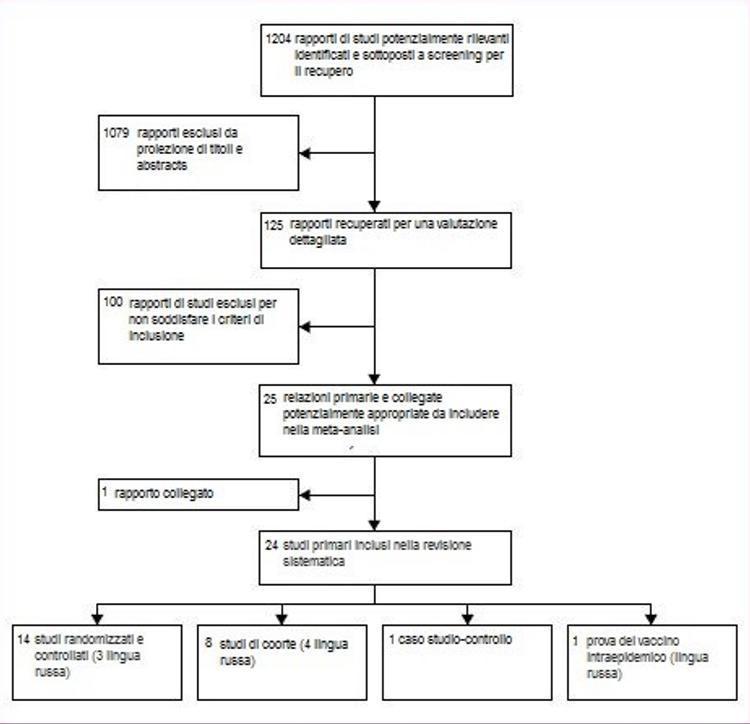
Rycina 1: przepływ analizowanych badań
Tabela 1 zawiera streszczenie uwzględnionych badań. Spośród 25 uwzględnionych raportów 14 pochodziło z randomizowanych badań kontrolowanych;16-29 Trybunał zidentyfikował także randomizowane badanie dotyczące stosowania wewnątrzpidemicznego żywej szczepionki podawanej doustnie.30 Dziewięć raportów pochodzi z ośmiu badań kohortowych:31-39 związek32 była to ponowna analiza poprzedniego badania31 z dalszymi danymi, dlatego rozważaliśmy publikacje dwa raporty z tego samego badania. Jeden raport obejmował badanie kliniczne.40 Trzy randomizowane próby22,29,30 oraz pięć raportów z badań kohortowych31-34,39 zostały przetłumaczone z rosyjskiego. Dwa z nich31-33 sklasyfikowano je jako badania kohortowe, ponieważ w tekście nie wspomniano o randomizacji.
W sześciu randomizowanych badaniach kontrolowanych placebo grypę zgłoszono jako miarę wyniku (łączny mianownik 5052) 17-20,23,24 Inne ustalenia dotyczyły choroby podobnej do grypy w czterech raportach (93 023), 16,20,23,28 objawy infekcji górnych dróg oddechowych u czterech innych (29 498), 20,22,23,28 przypadki wtórne (zakażone kontaktami) w jednym (123), 23 nieobecności w szkole w innym (550), 25 dwie choroby dolnych dróg oddechowych (1550), 18,20 ostre zapalenie ucha środkowego w trzech (2298), 18,20,24 i konsekwencje ostrego zapalenia ucha środkowego w jednym (765).24 Żadne z trzech randomizowanych kontrolowanych badań z grupą bez interwencji nie miało wpływu jako miara wyniku. Choroba grypopodobna była wynikiem dwóch doniesień (łączny mianownik 67 324), 21,29 nieobecności w szkole przez ponad 4 dni i ostre zapalenie ucha środkowego doprowadziły do jednego badania (344), 21 a wpływ społeczno-gospodarczy (gorączkowa choroba układu oddechowego, liczba dni szpitalnych i liczba utraconych dni szkolnych) była wynikiem innego raportu (303).26 Wpływ był miarą wyniku czterech badań kohortowych (łączny mianownik 1912) 33,36-38 a grypopodobna choroba była jednym na sześć badań (8593).31-36,39 W ocenie ważności dwa badania uzyskały wysoką ocenę pod względem wszystkich kryteriów.17,24 Dziewięć prób miało odpowiednią randomizację17-19,21,24-26,28,30 a w pozostałych sześciu randomizacja była nieodpowiednia lub niejasna. Alokacja została odpowiednio ukryta w sześciu badaniach kontrolowanych placebo.16,17,19,23,24,27 Osiem badań udokumentowało straty następcze17,19,20,23-25,28,30 w tych raportach podano wystarczające dane, aby umożliwić nam przeprowadzenie analizy zamiaru leczenia (ITT - analiza wyników eksperymentu, która jest oparta na początkowym przypisaniu leczenia, a nie na ostatecznie otrzymanym leczeniu). Dwa badania kohortowe uzyskały wysoką ocenę wszystkich przedmiotów.33,37 Badanie kliniczno-kontrolne zostało odpowiednio przeprowadzone i przedstawione, ale iloraz szans nie został podany (iloraz szans jest miarą związku między dwoma czynnikami, na przykład między czynnikiem ryzyka a chorobą).40
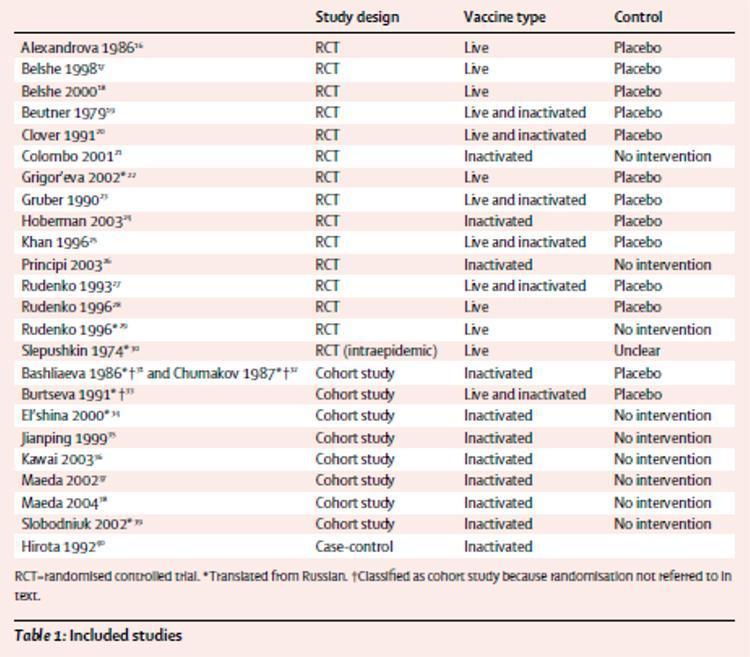
Tabela 1: przeanalizowane badania
W naszej metaanalizie przeprowadziliśmy pięć głównych porównań: trzy próby z randomizowanych badań kontrolowanych (porównania 1-3) i dwa dane z badań kohortowych. Porównania 1 i 4 obejmowały wyniki dla żywych atenuowanych szczepionek, podczas gdy porównania 2 i 5 wykorzystywały dane dla szczepionek inaktywowanych. Wszystkie komparatory były placebo lub bez interwencji, a porównania 1, 2, 4 i 5 zostały stratyfikowane według dostępnych grup wiekowych) i rodzaju wyniku (grypa, porównania 1, 2, 4, 5; choroba grypopodobna, porównania 1a, 2, 4, 5). Porównanie 3 obejmowało dane dotyczące wyników oddziaływania (przypadki wtórne, nieobecności w szkole, choroba dolnych dróg oddechowych, ostre zapalenie ucha środkowego i jego konsekwencje oraz pobyt w szpitalu). Ze względu na brak danych (większość wyników zgłoszono tylko z jednego lub dwóch badań), nie było możliwe ustalenie wieku lub stratyfikacji dla porównania 3. Rycina 2 ilustruje ocenę skuteczności szczepionki , Dla porównania 1, żywe atenuowane szczepionki miały ogólną skuteczność 79%, chociaż nie odnotowano żadnych użytecznych danych u dzieci w wieku 2 lat lub mniej. W badaniu z udziałem 1602 dzieci w wieku 15–71 miesięcy szacunki skuteczności szczepionki zgłoszono w części do dyskusji na temat 86% (95% CI 65-94) u dzieci w wieku 1 roku i 96% (86-99 ) w wieku 2 lat 1.17 Bez podziału według wieku dane te nie mogą zostać uwzględnione w metaanalizie. Porównanie 2 wykazało, że szczepionki inaktywowane były skuteczne w 65%, czyli mniej niż szczepionki żywe atenuowane, chociaż różnica nie jest znacząca. U dzieci w wieku 2 lat i młodszych inaktywowane szczepionki nie były bardziej skuteczne niż placebo (24%), chociaż obserwację tę oparto na niewielkim badaniu.24 Dla porównania 4, żywe atenuowane szczepionki były skuteczne w 44%, chociaż obserwacja ta była ponownie oparta na wynikach małego badania.33 Porównanie 5 wykazało, że szczepionki inaktywowane miały skuteczność 64% u dzieci w wieku powyżej 6 lat, 66% u dzieci w wieku 6 lat lub młodszych i nie były lepsze niż placebo (37%) u dzieci w wieku 2 lat lat lub młodszych.
Rycina 2 przedstawia także ocenę skuteczności szczepionki. Dla porównania 1a, żywe atenuowane szczepionki miały 38% ogólnej skuteczności, ale nie znaleźliśmy żadnych dowodów u dzieci w wieku 2 lat lub młodszych. Porównanie 2a wykazało, że szczepionki inaktywowane miały ogólną skuteczność 28%; ponownie, nie znaleźliśmy żadnych dowodów u dzieci w wieku 2 lat lub młodszych. Dla porównania 4a, żywe atenuowane szczepionki nie były skuteczne u dzieci w wieku powyżej 6 lat, chociaż obserwację tę oparto na badaniu.33 Nie znaleziono dowodów na to porównanie w innych grupach wiekowych. Porównanie 5a wykazało, że ogólna skuteczność szczepionek inaktywowanych wynosi 57%, ale po raz kolejny nie byliśmy w stanie znaleźć danych dotyczących dzieci w wieku 2 lat lub młodszych. Szczepionki te nie są skuteczne u dzieci w wieku 6 lat lub młodszych, ale u dzieci w wieku powyżej 6 lat były skuteczne w 58%.
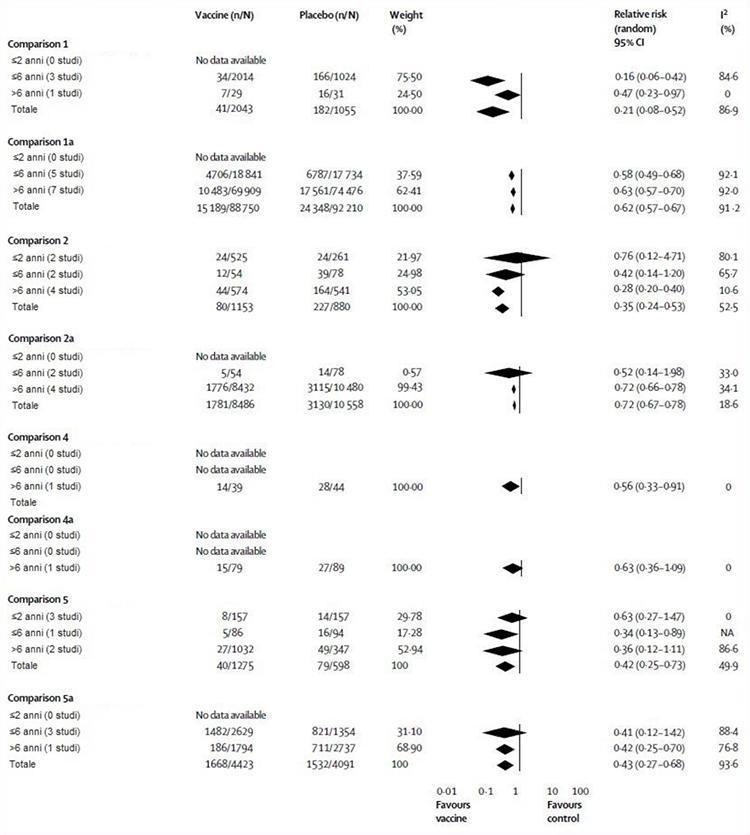
Rycina 2: Żywa atenuowana i inaktywowana szczepionka przeciw grypie w porównaniu z placebo lub bez interwencji według wieku i planu badań
NA = nie dotyczy.
W badaniu klinicznym sprawdzono skuteczność szczepionki inaktywowanej przeciwko chorobie grypopodobnej podczas epidemii u 803 dzieci w wieku od 6 do 12 lat.40 Szczepionka była dobrze zrównoważona antygenowo z krążącym szczepem, a jej podanie było odwrotnie związane z ryzykiem poważnej, ale nie łagodnej choroby podobnej do grypy.
Rycina 3 ilustruje ocenę dowodów z randomizowanych kontrolowanych badań skuteczności szczepionki pod kątem wyników oddziaływania. Szczepionki były znacznie bardziej skuteczne niż placebo lub brak interwencji w ograniczanie nieobecności w szkole, ale obie obserwacje były oparte na badaniu.21,25 W trzecim badaniu 26 odnotowano znaczny spadek liczby opuszczonych dni szkolnych przez dzieci szczepione w porównaniu do dzieci nieleczonych. Wpływ szczepionek na wszystkie inne wyniki (przypadki wtórne, choroba dolnych dróg oddechowych, ostre zapalenie ucha środkowego i jego konsekwencje oraz pobyt w szpitalu) nie różnił się znacząco od placebo lub jakiejkolwiek interwencji (ryc. 3).
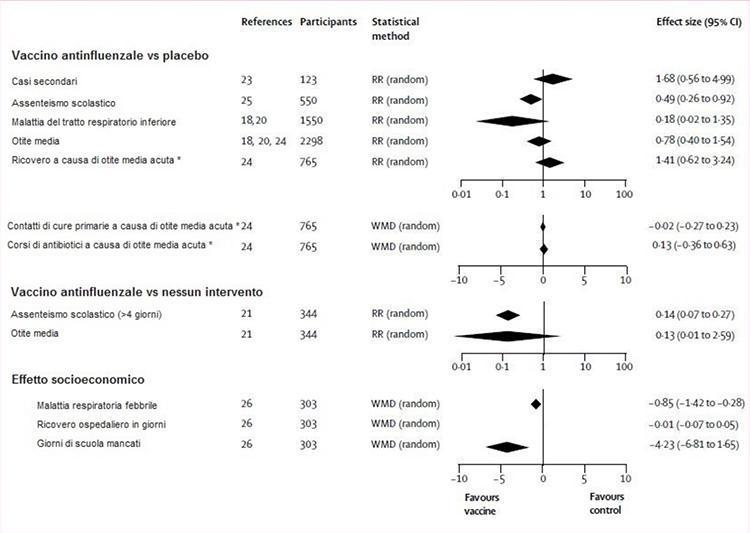
Rycina 3: Szczepionka przeciw grypie vs. placebo lub brak interwencji
RR (losowy) = ryzyko względne (model efektu losowego). WMD (losowo) = średnia różnica wagi (model z efektem losowym). * Inaktywowana szczepionka, dwie dawki.
Porównanie skuteczności modeli z pojedynczą dawką i dwoma dawkami żywych atenuowanych szczepionek w porównaniu z placebo faworyzowało program dwóch dawek (skuteczność 73% 17,18,20,23 w porównaniu z 93% 17), chociaż szacunek dla programu dwóch dawek opiera się tylko na jednym badaniu. We wszystkich badaniach inaktywowanych szczepionek zastosowano program z pojedynczą dawką.19,20,23,24, Dane grupujące dla wszystkich grup wiekowych nie wpłynęły na nasze wnioski.
Tabela 2 pokazuje wyniki progresywnej czułości analizy. Wszystkie porównania, z wyjątkiem porównań 1 i 2, były wrażliwe na wykluczenie dowodów z badań wykonanych w byłym ZSRR. Dla porównania 1a, wykluczenie sześciu niezależnych zestawów danych sprawiło, że oszacowanie skuteczności było nieznaczne u dzieci w wieku powyżej 6 lat, ale zwiększyło całkowitą skuteczność z 38% do 67%. Dla porównania 2a szacunki skuteczności dla dzieci w wieku powyżej 6 lat nie zostały znacząco zmienione, ale wzrosły z 28% do 76%. Porównania 4 i 4a zostały wyludnione przez usunięcie zestawu danych w każdej warstwie. W porównaniu 5, nieistotne szacunki 64% dla dzieci powyżej 6 lat stały się znaczące (80%), podczas gdy w porównaniu 5a szacunki dla dzieci powyżej 6 lat (58%) pozostały znaczące ale wzrost wielkości (90%).
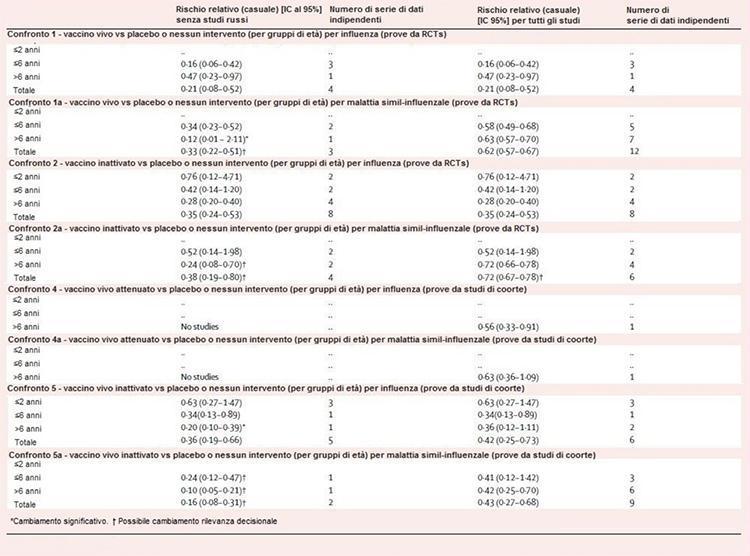
Tabela 2: czułość analizy
Discussione
Wykazaliśmy, że żywe atenuowane szczepionki przeciw grypie mają dobrą skuteczność, ale niską skuteczność u dzieci w wieku powyżej 2 lat. Te szczepionki mogą być odpowiednie do kontrolowania wybuchu szkoły; nie są one jednak dopuszczone do stosowania u dzieci w wieku poniżej 2 lat. Szczepionki inaktywowane miały mniejszą skuteczność niż żywe szczepionki atenuowane, a u dzieci w wieku 2 lat lub mniej miały działanie podobne do placebo. Ich skuteczność była niska u dzieci w wieku powyżej 2 lat; nie znaleźliśmy dowodów od 2 lat lub młodszych. Nasze wnioski dotyczące szczepionek inaktywowanych opierają się na ponad 18 000 obserwacji z randomizowanych badań. Wyniki badań kohortowych (5910 obserwacji) sugerują, że szczepionki inaktywowane miały wysoką skuteczność i skuteczność u dzieci w wieku powyżej 6 lat, ale u dzieci w wieku poniżej 2 lat skuteczność nie była lepsza niż placebo i nie było dowodów na ich skuteczność. Różnice między skutecznością i skutecznością szczepionki nie są zaskakujące, ponieważ szczepionki przeciw grypie są specjalnie ukierunkowane na wirusy grypy i nie zostały zaprojektowane w celu zapobiegania innym przyczynom chorób grypopodobnych.
Znaleźliśmy niewiele dowodów na inne wyniki. Szczepionki były nieco skuteczne w zmniejszaniu nieobecności w szkole, ale miały niewielki wpływ na inne wyniki (przypadki wtórne, choroba dolnych dróg oddechowych, ostre zapalenie ucha środkowego i jego konsekwencje oraz pobyt w szpitalu) w porównaniu z placebo lub bez interwencji. Jednak wnioski te opierają się na kilku badaniach.
Badania z Rosji rzadko były włączane do dyskusji na ten temat. Nasz raport obejmował siedem badań przetłumaczonych z rosyjskiego. Wyłączenie tych badań z byłego ZSRR nie wpłynęło znacząco na nasze wnioski, ale sprawiło, że nasze szacunki były bardziej niestabilne. Nie mamy powodu, aby sądzić, że szczepionki produkowane w byłym Związku Radzieckim działają inaczej niż ich zachodnie odpowiedniki. Jedyne badanie kontrolowane placebo, które bezpośrednio porównuje skuteczność inaktywowanej trójwartościowej szczepionki przeciw podzielonemu wirusowi z żywą atenuowaną, przystosowaną do zimna trójwartościową szczepionką przeciw grypie pod nieobecność w szkole, nie wykazało żadnej różnicy w wydajności.25
Nasza analiza ma kilka potencjalnych ograniczeń. Po pierwsze, nie byliśmy w stanie znaleźć wystarczających danych, które pozwoliłyby nam wyciągnąć ostateczne wnioski na temat ścieżek immunizacji (domięśniowej lub donosowej) lub na temat programów szczepionek inaktywowanych z jedną lub dwiema dawkami. Po drugie, nasza metaanaliza wykazała znaczną niejednorodność, którą można przypisać kilku czynnikom. Na przykład różnice między okresami obserwacji (im dłuższy okres obserwacji, tym mniejszy potencjał identyfikacji przypadków osłabionej szczepionki, takiej jak krążenie wirusowe), definicje przypadków chorób grypopodobnych (nasza analiza wrażliwości nie wykazała różnic w szczegółowości definicji przypadku), wydajność żywych szczepionek, wyszukiwanie przypadków i jakość badania oraz stężenia krążenia wirusa mogły spowodować heterogeniczność. Wreszcie, uwzględnione badania dostarczyły niewystarczających danych do stratyfikacji krążenia wirusowego lub czasu obserwacji, ale nie uważamy, że heterogeniczność wpłynęła na nasze wnioski, ponieważ nasze szacunki są jednoznaczne i wszystkie wskazują na wysoką skuteczność i słaba skuteczność szczepionek.
Ogólna jakość metodologiczna uwzględnionych badań była rozsądna, chociaż zauważyliśmy, że opis zawartości szczepionki był zmienny i nie zgłoszono żadnych środków konserwujących ani zaróbek. Możemy znaleźć kilka uwag na temat jakości miary między szczepionkami stosowanymi w badaniach, krążącym szczepem i składem szczepionek zalecanych przez WHO. U zdrowych osób dorosłych skład antygenowy jest ważnym predyktorem skuteczności szczepionki.8 Względny niedobór bezpośrednich porównań szczepionek zapobiega istotnym rozważaniom na temat ich względnej skuteczności i ustanawia bezwzględny wymóg dla dalszych bezpośrednich badań porównawczych.
Podsumowując, zidentyfikowaliśmy duży zestaw danych pokazujący dowody na rozsądną jakość skuteczności szczepionek przeciw grypie u dzieci w wieku 2 lat lub starszych, szczególnie w przypadku żywych szczepionek atenuowanych o dwóch dawkach. Zauważyliśmy jednak zauważalną różnicę między skutecznością szczepionki a skutecznością ze względu na duży odsetek chorób grypopodobnych spowodowanych przez czynniki inne niż wirusy grypy, co jest zgodne z przeglądem szczepionek przeciw grypie u Cochrane u zdrowych osób dorosłych.8
Ten punkt jest ważny przy podejmowaniu decyzji o szczepieniu całych populacji. Nasze ustalenia nie potwierdzają szczepień bardzo małych dzieci. Chociaż coraz więcej dowodów wskazuje na wpływ grypy na liczbę hospitalizacji i zgonów dzieci, nie znaleźliśmy przekonujących dowodów na to, że szczepionki mogą zmniejszyć śmiertelność, liczbę hospitalizacji, poważne komplikacje i przenoszenie grypy w społeczności dziecięcej.
Rifestions
1. Komitet Amerykańskiej Akademii Pediatrii ds. Chorób Zakaźnych. Zalecenia dotyczące immunizacji grypy u dzieci. Pediatria 2004; 113: 1441-47.
2. Harper SA, Fukuda K, Uyeki TM, Cox NJ, Bridges CB. Zapobieganie i kontrola grypy: zalecenia Komitetu Doradczego ds. Praktyk Szczepienia (ACIP). MMWR zalecany Rep 2004; 53 (RR-6): 1-40.
3. Orr P. Oświadczenie w sprawie szczepień przeciwko grypie w sezonie 2004–2005. Czy Wspólny Dis Rep , , , , , , , , ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, , 2004; 30: 1-32.
4. Neuzil KM, Mellen BG, Wright PF, Mitchel EF Jr, Griffin MR. Wpływ grypy na hospitalizacje, wizyty ambulatoryjne i kursy antybiotyków u dzieci. N angielski J. Med 2000; 342: 225-31.
5. Izurieta HS, Thompson WW, Kramarz P, i in. Wpływ i odsetek hospitalizacji z powodu chorób układu oddechowego u niemowląt i małych dzieci. N angielski J. Med 2000; 342: 232-39.
6. Zasady N, Esposito S. Czy jesteśmy gotowi na powszechne szczepienia przeciw grypie w pediatrii? Lancet Infect Dis 2004; 4: 75-83.
7. Reichert TA, Sugaya N, Fedson DS, Glezen WP, Simonsen L, Tashiro M. Japońskie doświadczenia ze szczepieniem dzieci w wieku szkolnym przeciwko grypie. N angielski J. Med 2001; 344: 889-96.
8. Demicheli V, Nity D, Deeks JJ, Jefferson TO. Szczepionki do zapobiegania grypie u zdrowych osób dorosłych (Cochrane Review). Baza danych Cochrane Syst Obrót silnika 2004; 3: CD001269.
9. Smith S, Demicheli V, Jefferson T, Harnden A, Matheson N, Di Pietrantonj C. Szczepionki do zapobiegania grypie u zdrowych dzieci (Protokół do przeglądu Cochrane). Baza danych Cochrane Syst Obrót silnika 2004; 3: CD004879.
10. Alderson P, Green S, Higgins JPT. Sekcja 6, ocena jakości badania - podręcznik recenzentów Cochrane, 4.2.2 [zaktualizowany marzec 2004]. http://www.cochrane.org/cochrane/handbook/hbook.htm (dostęp 18 stycznia 2005).
11. Wells GA, Shea B, O'Connell D i in. Skala Newcastle-Ottawa (NOS) do oceny jakości badań niezandomizowanych w metaanalizach. http://www.ohri.ca/programs/clinical_epidemiology/ oxford.htm (dostęp 18 stycznia 2005).
12. Higgins JP, Thompson SG. Ilościowa heterogeniczność w metaanalizie. Stat Med 2002; 21: 1539-58.
13. Higgins JP, Thompson SG, Deeks JJ, Altman DG. Pomiar niespójności w metaanalizach. BMJ 2003; 327: 557-60.
14. Deeks JJ, Higgins JPT, Altman DG. Sekcja 8, analiza i prezentacja wyników. W: Alderson P, Green S, Higgins J, red. Podręcznik recenzenta Cochrane 4.2.2 [zaktualizowany marzec 2004]. http://www.cochrane.org/cochrane/handbook/hbook.htm (dostęp 18 stycznia 2005).
15. DerSimonian R, Laird N. Metaanaliza w badaniach klinicznych. Control Klinika Próby 1986; 7: 177-88.
16. Alexandrova GI, Budilovsky GN, Koval TA i in. Badanie żywej rekombinowanej przystosowanej na zimno dwuwartościowej szczepionki przeciw grypie typu A do stosowania u dzieci: badanie epidemiologiczne. Szczepionka 1986; 4: 114-18.
17. Belshe RB, Mendelman PM, Treanor J i in. Skuteczność żywej atenuowanej, przystosowanej na zimno, trójwartościowej, donosowej szczepionki przeciw grypie u dzieci. N angielski J. Med 1998; 338: 1405-12.
18. Belshe RB, Gruber WC, Mendelman PM, i in. Skuteczność szczepienia żywą atenuowaną, przystosowaną do zimna, trójwartościową, donosową szczepionką przeciw wirusowi grypy przeciwko wariantowi (A / Sydney) nie zawartemu w szczepionce. J Pediatra 2000; 136: 168-75.
19. Beutner KR, Chow T, Rubi E, Strussenberg J, Clement J, Ogra PL. Ocena szczepionki przeciw wirusowi grypy A swoistej dla neuraminidazy u dzieci: odpowiedzi przeciwciał i wpływ na dwa kolejne wybuchy naturalnego zakażenia. J Infect Dis 1979; 140: 844-50.
20. Clover RD, Crawford S, Glezen WP, Taber LH, Matson CC, Couch RB. Porównanie ochrony heterotypowej przeciwko grypie A / Tajwan / 86 (H1N1) przez atenuowane i inaktywowane szczepionki do wirusów podobnych do A / Chile / 83. J Infect Dis 1991; 163: 300-04.
21. Szczepionka Colombo C, Argiolas L, La Vecchia C, Negri E, Meloni G, Meloni T. Grypa u zdrowych dzieci w wieku przedszkolnym. Obrót silnika Epidemiol Sante publiczny 2001; 49: 157-62.
22. EP Grigor'eva, Desheva I, Donina SA i in. Porównawcza charakterystyka bezpieczeństwa, aktywności immunogennej i siły profilaktycznej dorosłych i dzieci rodzajów żywej szczepionki przeciw grypie u dzieci w wieku 7–14 lat [w języku rosyjskim]. Wrz Wirusol 2002; 47: 24-27.
23. Gruber WC, Taber LH, Glezen WP, i in. Żywe atenuowane i inaktywowane szczepionki przeciw grypie u dzieci w wieku szkolnym. Am J Dis Child 1990; 144: 595-600.
24. Hoberman A, Greenberg DP, Paradise JL i in. Skuteczność inaktywowanej szczepionki przeciw grypie w zapobieganiu ostremu zapaleniu ucha środkowego u małych dzieci: randomizowane badanie kontrolowane. JAMA 2003; 290:1608-16.
25. Khan AS, Polezhaev F, Vasiljeva R, i in. Porównanie inaktywowanych w USA wirusów typu split i rosyjskich żywych atenuowanych, przystosowanych na zimno trójwartościowych szczepionek przeciw grypie u rosyjskich uczniów. J Infect Dis 1996; 173: 453-56.
26. Principi N, Esposito S, Marchisio P, Gasparini R, Crovari P. Społeczno-gospodarczy wpływ grypy na zdrowe dzieci i ich rodziny. Pediatra Infekuj Dis J 2003; 22 (suplement 10): S207 – 10.
27. Rudenko LG, Slepushkin AN, Monto AS i in. Skuteczność żywych atenuowanych i inaktywowanych szczepionek przeciw grypie u dzieci w wieku szkolnym i ich nieszczepionych kontaktów w Nowogrodzie w Rosji. J Infect Dis 1993; 168: 881-87.
28. Rudenko LG, Lonskaya NI, Klimov AI, Vasilieva RI, Ramirez A. Ocena kliniczna i epidemiologiczna żywej, przystosowanej do przeziębienia szczepionki przeciw grypie dla osób w wieku 3–14 lat. Bull Światowy Organ Zdrowia 1996; 74: 77-84.
29. Rudenko LG, Vasil'eva RI, Ismagulov AT i in. Profilaktyczna skuteczność żywej rekombinowanej szczepionki przeciw grypie typu A w immunizacji dzieci w wieku 3-14 lat [po rosyjsku]. Wrz Wirusol 1996; 41: 37-39.
30. Slepushkin AN, Dukova VS, Kalegaeva VA, Kagan AN, Temriuk EE. Wyniki badań skuteczności żywej szczepionki przeciw grypie do stosowania w okresie okołozabiegowym u dzieci w wieku przedszkolnym i szkolnym [w języku rosyjskim]. Zh Mikrobiolo Epidemiol Immunobiolo 1974; 12: 24-29.
31. Bashliaeva ZA, Sumarokov AA, Nefedova LA, Iaroshevskaia II, Ozeretskovskaia NA. Podstawowe wyniki badania komitetowego nowej szczepionki Grippovac SE-AZh [po rosyjsku]. Zh Mikrobiolo Epidemiol Immunobiolo 1986; 2: 49-54.
32. Chumakov MP, Boiko VM, Malyshkina LP, Mel'nikova SK, Rodin VI. Wyniki zakodowanych prób działania trójwartościowej podjednostkowej szczepionki przeciw grypie Grippovak w moskiewskich przedszkolach w grudniu 1983 r. Do 1. kwartału 1984 r. [W języku rosyjskim]. Wrz Wirusol 1987; 32: 175-83.
33. Burtseva EI, Obrosova-Serova NP, Govorkova EA i in. Badanie porównawcze właściwości ochronnych żywych rekombinowanych i inaktywowanych szczepionek przeciw grypie wykonanych ze szczepu A / Filipiny / 2/82 (H3N2) u dzieci w wieku 8–15 lat [w języku rosyjskim]. Wrz Wirusol 1991; 36: 375-77.
34. El'shina GA, Gorbunov MA, Bektimirov TA i in. Ocena reaktywności, nieszkodliwości i skuteczności profilaktycznej trójwartościowej szczepionki przeciw grypie Grippol z polimerową podjednostką podanej uczniom [w języku rosyjskim]. Zh Mikrobiolo Epidemiol Immunobiolo 2000; 2: 50-54.
35. Jianping H, Xin F, Changshun L i in. Ocena skuteczności Vaxigrip. Szczepionka 1999; 17 (suplement 1): S57 – 58.
36. Kawai N, Ikematsu H, Iwaki N i in. Prospektywne, internetowe badanie skuteczności i bezpieczeństwa szczepień przeciw grypie w sezonie 2001–2002. Szczepionka 2003; 21: 4507-13.
37. Maeda T, Shintani Y, Miyamoto H, i in. Profilaktyczny efekt inaktywowanej szczepionki przeciw grypie na małe dzieci. Pediatra Int 2002; 44: 43-46.
38. Maeda T, Shintani Y, Nakano K, Terashima K, Yamada Y. Niepowodzenie szczepionki przeciwko inaktywowanej grypie A w celu ochrony zdrowych dzieci w wieku 6–24 miesięcy. Pediatra Int 2004; 46: 122-25.
39. Slobodniuk AV, Romanenko VV, Utnitskaia OS, Motus TM, Pereverzev AV. Wpływ różnorodności immunizacji dzieci szczepionką przeciw inaktywowanej grypie na odpowiedź immunologiczną i skuteczność ochrony [po rosyjsku]. Zh Mikrobiolo Epidemiol Immunobiolo 2002; 4: 36-39.
40. Hirota Y, Takeshita S, Ide S i in. Różne czynniki związane z manifestacją choroby podobnej do grypy. Int J Epidemiol 1992; 21:574-82.
źródło: www.ncbi.nlm.nih.gov/pubmed/15733718
Tłumaczenie Valentina Sbrana, Cliva Toskania

