Czy szczepionka przeciwko wirusowemu zapaleniu wątroby typu B może spowodować obrażenia i/lub śmierć?

WAŻNA UWAGA: Corvelva zaprasza do uzyskania szczegółowych informacji poprzez przeczytanie wszystkich sekcji i linków, a także ulotek producenta i kart technicznych oraz do rozmowy z jednym lub kilkoma zaufanymi specjalistami przed podjęciem decyzji o zaszczepieniu siebie lub dziecka. Informacje te służą wyłącznie celom informacyjnym i nie stanowią porady medycznej.
Problem wielu szczepionek (kliknij, aby otworzyć)
Problem wielu szczepionek

Obecne kalendarze szczepień, zwłaszcza dla wieku pediatrycznego, przewidują podanie wielu antygenów i szczepionek w jednej sesji, sprzyjając wygodzie kosztem bezpieczeństwa. Aby móc wygłosić konkretną wypowiedź na temat bezpieczeństwa szczepionek, musimy koniecznie wziąć pod uwagę złożoność zjawiska, doradzając wszystkim czytelnikom odpowiednie zapoznanie się ze wszystkimi aspektami szczepień, zaletami i wadami.
Dr Russell Blaylock, adiunkt kliniczny neurochirurgii w Centrum Medycznym Uniwersytetu Mississippi, przez lata badał „toksyczną synergię” i był w stanie zaobserwować, że kiedy dwa słabo toksyczne pestycydy, z których żaden nie jest w stanie wywołać zespołu Parkinsona u zwierząt doświadczalnych, są ze sobą łączone, mogą wywołać chorobę nawet szybko i porównuje to zjawisko do wielu szczepionek podawanych jednocześnie: „Szczepionki, jeśli są zbyt liczne i zbyt blisko siebie, zachowują się jak choroba przewlekła”.(A). Inne Dwa badania potwierdziły, że po zaszczepieniu wieloma szczepionkami w jednym podaniu może wystąpić nagła śmierć niemowląt.(pne)
Badanie opublikowane w Human and Experimental Toxicology wykazało, że kraje, które przepisują więcej szczepionek dzieciom, mają zwykle wyższy wskaźnik śmiertelności niemowląt.(D) Na przykład w Stanach Zjednoczonych, gdzie dzieci otrzymują 26 szczepionek, umiera ponad 6 dzieci na 1000 żywych urodzeń, podczas gdy w Szwecji i Japonii, gdzie podaje się 12 szczepionek pediatrycznych, zgłaszane są 3 zgony na każde 1000 żywych urodzeń. We wspomnianym badaniu rozważany jest również związek między szczepionkami a SIDS.
Ze szwajcarskiego badania opublikowanego w 2005 roku w European Journal of Pediatrics(E) wynika z tego, że jeśli chodzi o wpływ na wcześniaki, częstość nawracających lub nasilających się bezdechów i bradykardii po podaniu szczepionek sześciowartościowych wynosi 13%. W tym samym roku w tym samym czasopiśmie opublikowano niemieckie badanie, w którym zbadano nagłe zgony niemowląt po sześciowartościowym. Autorzy piszą: „Wyniki te, oparte na doniesieniach spontanicznych, nie dowodzą związku przyczynowego między szczepieniem a nagłą śmiercią niemowląt, ale stanowią sygnał dotyczący jednego z dwóch dostępnych sześciowartościowych; sygnał, który powinien skłonić do zintensyfikowania nadzoru nad nagłymi zgonami niemowląt po szczepieniu”.(fa)
W 2006 roku został opublikowany w czasopiśmie medycznym Vaccine(G) list od zespołu naukowców z Uniwersytetu w Monachium, który zgłosił „sześć przypadków nagłej śmierci niemowląt po szczepieniu sześciowartościowym. Wszystkie znalezione martwe bez wyjaśnienia 1-2 dni po szczepieniu”. Zostały one sklasyfikowane jako typowe przypadki nagłej śmierci niemowląt, ale autoptyczna weryfikacja wykazała nieprawidłowości neuropatologiczne i histologiczne, a wszystkie dzieci wykazywały znaczny obrzęk mózgu, co czyniło je wyjątkiem w porównaniu z innymi przypadkami SIDS (zespół nagłej śmierci niemowląt). Badacze napisali, że „Przed wprowadzeniem szczepionki sześciowartościowej (w latach 1994-2000) obserwowaliśmy przypadek tylko jednego na 198 dzieci z nagłą śmiercią łóżeczkową, które zmarło wkrótce po szczepieniu DTP. Ale w latach 2001-2004 zidentyfikowali pięć podobnych przypadków z 74 z SIDS. Oznaczałoby to trzynastokrotny wzrost”.
Również w 2006 roku w Archiwum Virchowa(H), zespół z Instytutu Patologii Uniwersytetu w Mediolanie napisał: „Eksperci z Europejskiej Agencji ds. Oceny Produktów Medycznych przeanalizowali możliwość istnienia związku między sześciowartościowymi szczepionkami a niektórymi przypadkami śmierci. Wśród uczestników byli patolodzy z doświadczeniem w szczepionkach i zespołach nagłej śmierci niemowląt, którzy prowadzili sekcje zwłok, ale, o ile nam wiadomo, niewiele uwagi poświęcono badaniu pnia mózgu i serca krwi na skrawkach seryjnych i nie było możliwości ustalenia roli wyzwalającej szczepionki na te zgony. W pracy przedstawiono przypadek 3-miesięcznej dziewczynki, która zmarła nagle po szczepieniu szczepionką sześciowartościową. Badanie pnia mózgu na seryjnych skrawkach wykazało obustronną hipoplazję jąder łukowatych. Układ przewodzący serca miał uporczywe rozproszenie i zwyrodnienie płodu. Ten przypadek oferuje wyjątkowe zrozumienie możliwej roli szczepionki sześciowartościowej w wywoływaniu śmiertelnych konsekwencji u wrażliwego dziecka. Każdy przypadek nagłej i nieoczekiwanej śmierci, który ma miejsce wkrótce po urodzeniu lub we wczesnym dzieciństwie, zwłaszcza po szczepieniu, powinien zawsze zostać poddany pełnej sekcji zwłok, zgodnie z wytycznymi.
Referencje
- Blaylock R, „Szczepienia: ukryte niebezpieczeństwa”, The Blaylock Wellness Report, maj 2004, s. 1-9
- Ottaviani G. i wsp., „Zespół nagłej śmierci łóżeczkowej (SIDS) wkrótce po szczepieniu sześciowartościowym: inna patologia w podejrzeniu SIDS?”, Virchowa Archiwum, 2006, 448, s. 100-104.
- Zinka B. i in., „Niewyjaśnione przypadki nagłej śmierci niemowląt wkrótce po szczepieniu sześciowartościowym”, Vaccine, lipiec 2006, 24 (31-32), s. 5779-5780.
- Miller NZ i in.1. , "Wskaźniki śmiertelności niemowląt regresowały w stosunku do liczby rutynowo podawanych dawek szczepionki: czy istnieje toksyczność biochemiczna lub synergistyczna?”, Hum. Exp. Toxicol., maj 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Kwestia aluminium (kliknij, aby otworzyć)
Aluminium w szczepionkach: co rodzice powinni wiedzieć

1. Co to jest aluminium?
Aluminium to srebrzystobiały lekki metal, plastyczny i odporny. Te cechy sprawiają, że jest on przydatny w wielu branżach i produktach, m.in. maszynowej, budowlanej, magazynowej, kuchennej, przyborów kuchennych, tekstyliów, barwników i kosmetyków. Aluminium jest również metalem najobficiej występującym w skorupie ziemskiej, a praktycznie cały glin ze środowiska znajduje się w glebie. Jednak glin nie występuje naturalnie w znacznych ilościach w organizmach żywych (takich jak rośliny i zwierzęta) i nie ma żadnej znanej funkcji biologicznej. W ciągu ostatniego stulecia stosowanie aluminium w niektórych produktach doprowadziło do zwiększonego narażenia ludzi. Głównymi źródłami narażenia są żywność zawierająca glin (np. proszek do pieczenia, żywność przetworzona, odżywki dla niemowląt itp.), produkty medyczne (np. antyperspiranty, środki zobojętniające kwasy itp.), zastrzyki przeciwalergiczne i szczepionki .1-3
2. Dlaczego aluminium jest obecne w szczepionkach?
Niektóre szczepionki wykorzystują związki glinu (wodorotlenek glinu i fosforan glinu) jako adiuwanty, które są składnikami, które zwiększają odpowiedź immunologiczną na antygen (substancję obcą).4-5 Amerykańska Agencja ds. Żywności i Leków (FDA) twierdzi, że gdyby niektóre szczepionki nie zawierały aluminium, wywołana przez nie odpowiedź immunologiczna mogłaby się zmniejszyć.6
3. Jakie szczepionki zawierają aluminium?
Następujące szczepionki zawierają glin i są podawane niemowlętom, dzieciom i młodzieży (ryc. 1):
- Wirusowe zapalenie wątroby typu B (HepB)
- sześciowartościowego
- Błonica, tężec i krztusiec (DTaP i Tdap)
- Haemophilus influenzae typu b (PedvaxHIB)
- Pneumokoki (PCV)
- Wirusowe zapalenie wątroby typu A (HepA)
- Wirus brodawczaka ludzkiego (HPV)
- Meningokoki B (MenB)
Rycina 1: Od urodzenia do 18 roku życia podaje się do 22 dawek szczepionek zawierających glin7-8
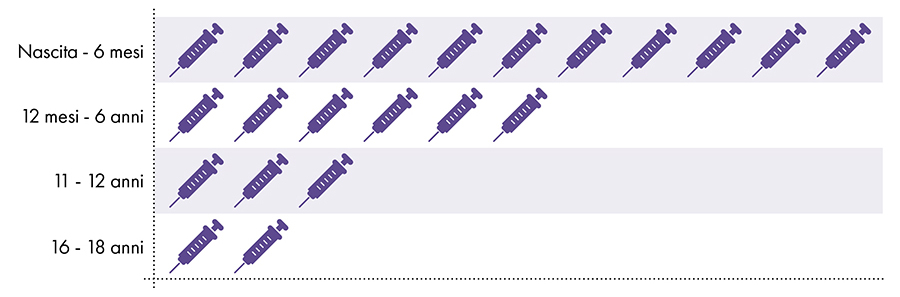
4. Czy narażenie na aluminium jest bezpieczne?
FDA uważa aluminium powszechnie uznawane za bezpieczne (GRAS) od 1975 roku.9 Jednak przed 1990 r. nie było technologii umożliwiającej dokładne wykrywanie niewielkich ilości glinu podawanego badanym w badaniach naukowych.10 W konsekwencji nie była znana ilość glinu, która mogłaby zostać wchłonięta przed wystąpieniem działań niepożądanych.
Od lat 1990. XX wieku, dzięki postępowi technologicznemu, zaobserwowano, że niewielkie ilości aluminium pozostające w organizmie człowieka zakłócają szereg procesów komórkowych i metabolicznych w układzie nerwowym oraz tkankach innych części ciała.1-10-11 Największe negatywne skutki aluminium zaobserwowano w układzie nerwowym i obejmują zarówno upośledzenie zdolności motorycznych, jak i encefalopatię (zmiany stanu psychicznego, zmiany osobowości, trudności w myśleniu, utrata pamięci, drgawki, śpiączka i inne).2-12
Departament Zdrowia i Opieki Społecznej Stanów Zjednoczonych (HHS) uznaje aluminium za znaną neurotoksynę.2 Ponadto FDA ostrzega przed ryzykiem toksyczności aluminium u niemowląt i dzieci.13
REJESTR FEDERALNY: Codzienna gazeta rządu Stanów Zjednoczonych„Nawet urodzone w terminie niemowlęta z prawidłową czynnością nerek mogą być zagrożone z powodu szybkiego wzrostu i niedojrzałości mózgu i szkieletu, a także niedojrzałości bariery krew-mózg. Do 1 lub 2 roku życia niemowlęta mają niższą współczynnik filtracji kłębuszkowej niż u dorosłych, co wpływa na czynność nerek. Agencja obawia się, że małe dzieci i osoby z niedojrzałą czynnością nerek są bardziej narażone na ekspozycję na glin. |
5. Ile doustnego aluminium nie jest bezpieczne?
W 2008 roku Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR), oddział HHS, wykorzystała badania nad neurotoksycznym działaniem glinu w celu ustalenia, że nie więcej niż 1 miligram (1.000 mikrogramów) glinu na kilogram masy ciała dziennie do unikaj negatywnych skutków aluminium.2
6. Ile wtryskiwanego aluminium nie jest bezpieczne?
Aby określić ilość glinu, którą można bezpiecznie wstrzyknąć, konieczne jest przeliczenie doustnego limitu glinu ATSDR. Limit ATSDR dla glinu podawanego doustnie (1.000 mikrogramów glinu na kilogram masy ciała na dzień) opiera się na 0,1% glinu podawanego doustnie, który jest wchłaniany do krwiobiegu, ponieważ przewód pokarmowy blokuje prawie całość glinu podawanego doustnie.2 W przeciwieństwie do tego, glin wstrzykiwany domięśniowo omija przewód pokarmowy i 100% glinu może z czasem zostać wchłonięte do krwiobiegu (tj. proporcja wchłoniętego glinu jest 1.000 razy większa). Aby uwzględnić te różne ilości wchłaniania, doustny limit glinu ATSDR należy podzielić przez 1000. Ta konwersja prowadzi do limitu glinu we krwi pochodzącego z ATSDR wynoszącego 1 mikrogram glinu (0,1% z 1.000 mikrogramów) na kilogram masy ciała na dzień. W związku z tym, aby uniknąć neurotoksycznego działania glinu, nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien dostawać się do krwiobiegu dziennie. Rycina 3 przedstawia limit glinu we krwi pochodzący z ATSDR dla niemowląt w różnym wieku w oparciu o ich wagę.
7. Ile glinu jest w szczepionkach?
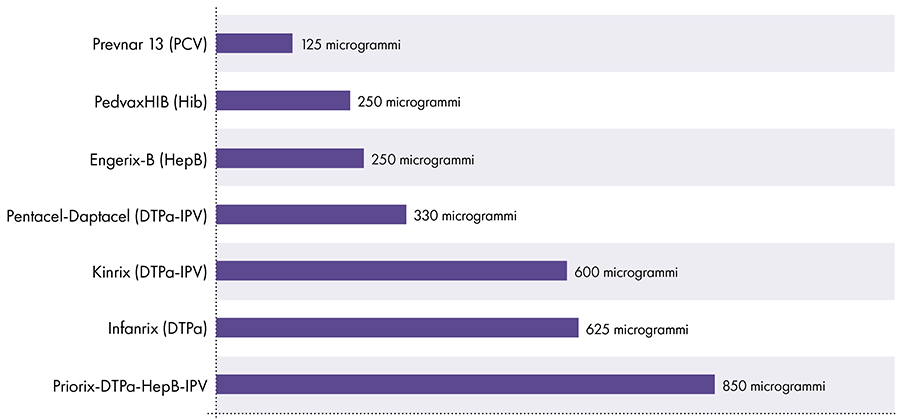
Ilość glinu w szczepionkach jest różna.16 W 1968 r. rząd federalny USA ustanowił limit ilości glinu w szczepionkach na 850 mikrogramów na dawkę, w oparciu o ilość glinu potrzebną do uczynienia niektórych szczepionek skutecznymi.6-17 W konsekwencji ilość glinu w zawierających glin szczepionkach dla niemowląt waha się od 125 do 850 mikrogramów na dawkę. Rysunek 4 przedstawia zawartość glinu w jednej dawce różnych szczepionek podawanych dzieciom.
8. Czy w jakichś badaniach porównywano ilość glinu w szczepionkach z limitem ustalonym przez Agencję ds. Rejestru Substancji Toksycznych i Chorób (ATSDR)?
W 2011 roku opublikowano badanie, którego celem było porównanie ilości glinu w szczepionkach z limitem przepływu krwi określonym przez ATSDR.18 Jednak to badanie błędnie oparło swoje obliczenia na 0,78% glinu doustnego wchłoniętego do krwiobiegu, a nie na wartości 0,1% stosowanej przez ATSDR w swoich obliczeniach.19-20 W rezultacie w badaniu z 2011 r. postawiono hipotezę, że prawie 8 razy (0,78% / 0,1%) aluminium może bezpiecznie dostać się do krwioobiegu, co doprowadziło do błędnego wniosku.
9. Czy ekspozycja na aluminium ze szczepionek jest bezpieczna?
Szczepionki są wstrzykiwane domięśniowo, a szybkość migracji glinu ze szczepionek z ludzkich mięśni do krwiobiegu jest nieznana. Badania na zwierzętach sugerują, że aluminium ze szczepionek może dostać się do krwiobiegu od kilku miesięcy do ponad roku, ze względu na wiele zmiennych.21-23 Ponieważ skumulowana ekspozycja na glin ze szczepionek u dzieci poniżej pierwszego roku życia przekracza dzienny limit ustalony przez ATSDR o kilkaset (ryc. 3 i 4), limit ten nadal byłby przekroczony, gdyby glin ze szczepionek dostał się do krwiobiegu w trakcie około roku. Ponadto badania wykazały, że glin ze szczepionek jest wchłaniany przez komórki odpornościowe i dociera do części ciała znajdujących się daleko od miejsca wstrzyknięcia, w tym do mózgu.24
Zakres działań niepożądanych glinu w szczepionkach nie jest znany, ponieważ nie przeprowadzono badań bezpieczeństwa porównujących populację zaszczepioną szczepionkami zawierającymi glin z populacją nieszczepioną takimi szczepionkami.
Ograniczenie przepływu krwi przez glin pochodzące z ATSDR2-14-15
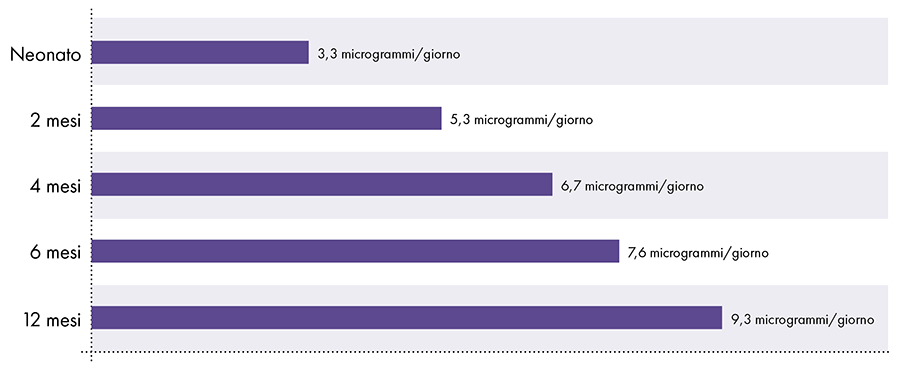 Rysunek 3: Ten wykres przedstawia limit glinu dla dzieci w różnym wieku, zgodnie z rejestrem substancji toksycznych i chorób, oddziału Departamentu Zdrowia i Opieki Społecznej Stanów Zjednoczonych. Limit wskazuje, że nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien codziennie dostawać się do krwiobiegu, aby uniknąć neurotoksycznego działania glinu.
Rysunek 3: Ten wykres przedstawia limit glinu dla dzieci w różnym wieku, zgodnie z rejestrem substancji toksycznych i chorób, oddziału Departamentu Zdrowia i Opieki Społecznej Stanów Zjednoczonych. Limit wskazuje, że nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien codziennie dostawać się do krwiobiegu, aby uniknąć neurotoksycznego działania glinu.
Ilość glinu w szczepionkach
Referencje
- Amerykańska Akademia Pediatrii, Komitet ds. Żywienia. Toksyczność glinu u niemowląt i dzieci. Pediatria. 1996 marzec; 97 (3): 413.
- Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR). Profil toksykologiczny dla aluminium. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA; 2008.3, 13-24, 145, 171-7, 208.
- Jokel RA. Aluminium w żywności — charakter i udział dodatków do żywności. W: El-Samragy Y, redaktor. Dodatek do żywności. Rijeka (Chorwacja): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. W kierunku zrozumienia działania adiuwantowego aluminium. Nat Rev Immunol. 2009 kwiecień; 9 (4): 287.
- Volk VK, Bunney WE. Uodpornienie na błonicę toksoidem płynnym i toksoidem strącanym ałunem. Am J Zdrowie publiczne Zdrowie Narodów. 1942 VII; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Sole glinu w szczepionkach — perspektywa USA. Szczepionka. 2002 31 maja; 20 dodatek 3: S18-22.
- Amerykańska Agencja ds. Żywności i Leków. Silver Spring (MD): Amerykańska Agencja ds. Żywności i Leków. Szczepionki licencjonowane do użytku w Stanach Zjednoczonych; [aktualizacja 2018 lutego 14; cytowany 2018 lutego 27 r.]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. Zalecany harmonogram szczepień dla dzieci i młodzieży w wieku 18 lat lub młodszych, Stany Zjednoczone, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Amerykańska Agencja ds. Żywności i Leków. Silver Spring (MD): Amerykańska Agencja ds. Żywności i Leków. SCOGS (Komitet Specjalny ds. Substancji GRAS); [cytowano 2018]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Ks. ND. Zachowanie biologiczne i biodostępność glinu u człowieka, ze szczególnym uwzględnieniem badań z wykorzystaniem glinu-26 jako znacznika: przegląd i aktualizacja badania. J Monitorowanie środowiska. 2004; 6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Glin w pediatrycznych produktach do żywienia pozajelitowego: zawartość zmierzona w porównaniu z zawartością oznaczoną. J Pediatr Pharmacol Ther. 2011; 16 (2): 92-7.
- Sedman A. Toksyczność glinu w dzieciństwie. Pediatr Nefrol. 1992 lipiec; 6 (4): 383-93.
- Amerykańska Agencja ds. Żywności i Leków, Departament Zdrowia i Opieki Społecznej. Zasady i przepisy. Rejestr Fed. 2003 czerwiec; 68 (100): 34286.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. National Center for Health Statistics: Tabela danych dla wykresów długości i wieku chłopców w zależności od wieku; [cyt. 2019 kwietnia 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. National Center for Health Statistics: Tabela danych dla wykresów długości i wagi dziewcząt w zależności od wieku; [cyt. 2019 kwietnia 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Amerykańska Agencja ds. Żywności i Leków, Departament Zdrowia i Opieki Społecznej. Rewizja wymagań dotyczących materiałów składowych. Ostateczna zasada. Rejestr Fed. 2011 kwietnia 13; 76 (71): 20513-8.
- Biuro Rejestru Federalnego, Krajowa Służba Archiwów i Rejestrów, Administracja Usług Ogólnych. Zasady i przepisy. Rejestr Fed. 1968 styczeń; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Zaktualizowana farmakokinetyka glinu po narażeniu niemowląt poprzez dietę i szczepienia. Szczepionka. 2011 listopada 28; 29 (51): 9538-43.
- Miller S, lekarze za świadomą zgodę. Errata w „Zaktualizowanej farmakokinetyce glinu w następstwie narażenia niemowląt poprzez dietę i szczepienia”. W: Brama Badań. Berlin (Niemcy): ResearchGate GmbH; 2020 marca 6 [cytowano 2020 marca 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Lekarze za świadomą zgodę. Newport Beach (Kalifornia): Lekarze za świadomą zgodę. Errata w „Zaktualizowanej farmakokinetyce glinu w następstwie narażenia niemowląt poprzez dietę i szczepienia”; [cytowano 2020 marca 6 r.]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, Biały JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorpcja in vivo adiuwantów szczepionkowych zawierających glin przy użyciu 26A1997. Szczepionka 15 sierpień-wrzesień; 12 (13-1314): 8-XNUMX.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Oznaczenie aluminium i ocena reakcji miejscowej w kilku punktach czasowych po domięśniowym podaniu szczepionek zawierających aluminium u małpy Cynomolgus. Szczepionka. 2005 lutego 3; 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanisławski B. Aluminium w osoczu i tkankach po wstrzyknięciu domięśniowym adiuwantów ludzkich szczepionek u szczurów. Arch toksykol. 2019 październik; 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Analiza krytyczna badań referencyjnych dotyczących toksykokinetyki adiuwantów na bazie glinu. J Inorg Biochem. 2018 kwiecień 181: 87-95.
Artykuł przetłumaczony przez Lekarze dla świadomej zgody
W 1981 roku amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B pochodzącą z osocza, zawierającą antygeny pobrane od zakażonych osób. Szczepionka ta została później wycofana z rynku, ponieważ, jak wszystkie szczepionki produkowane z ludzkiej krwi, była zdolna do przenoszenia niepożądanych i potencjalnie niebezpiecznych wirusów. W 1986 r. zatwierdzono pierwszą z serii szczepionek modyfikowanych genetycznie (rekombinowanego DNA).
W licznych badaniach sprawdzano prawdopodobieństwo, że osoby, które otrzymały szczepionkę pochodzącą z osocza, mogły również zarazić się niechcianymi wirusami, zwłaszcza wirusem HIV, prekursorem AIDS.(1-2) Co więcej, badania kliniczne potwierdzające bezpieczeństwo aktualnej szczepionki przeciwko wirusowemu zapaleniu wątroby typu B przeprowadzono jedynie na 147 zdrowych dzieciach, które monitorowano przez zaledwie 5 dni po podaniu(3) Nie jest to wystarczająco duża próba ani wystarczająco długi okres, aby określić rzeczywistą częstość występowania zdarzeń niepożądanych. Same firmy produkcyjne przyznały, że „powszechne stosowanie szczepionki może prowadzić do pojawienia się działań niepożądanych nieobserwowanych w badaniach klinicznych”.(4)
Nawet dorośli pacjenci byli monitorowani tylko przez pięć dni po szczepieniu i pomimo tego nadal zgłaszano skutki ogólnoustrojowe, takie jak bóle stawów, bóle mięśni, parestezje, bóle pleców i szyi, powiększenie węzłów chłonnych, ból głowy, gorączka, złe samopoczucie, dreszcze, wymioty. , biegunka, bóle brzucha ból, infekcje górnych dróg oddechowych, ból ucha i niedociśnienie.(5)
Pomimo oficjalnych kart danych technicznych i innych dokumentów, które propagują(6) szczepionki przeciw wirusowemu zapaleniu wątroby typu B, minimalizują lub zaprzeczają poważnym działaniom niepożądanym, liczne badania opublikowane w czasopismach medycznych i naukowych na całym świecie oraz raporty przekazywane do VAERS(7) potwierdzić różne patologie w wyniku szczepienia. Poniżej podsumowano niektóre z tych badań.
Artretyzm
W 1990 roku, wkrótce po wprowadzeniu szczepionki przeciwko wirusowemu zapaleniu wątroby typu B, British Medical Journal udokumentował związek pomiędzy szczepionką a zapaleniem wielostawowym, bolesnym zapaleniem pięciu lub więcej stawów.(8) W tym samym roku w czasopiśmie Journal of Rheumatology opublikowano artykuł na temat reaktywnego zapalenia stawów po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(9)
W 1994 roku British Journal of Rheumatology opublikował dane dokumentujące reumatoidalne zapalenie stawów po zaszczepieniu(10) a BMJ opublikowało trzy kolejne raporty potwierdzające związek między szczepionką a reaktywnym zapaleniem stawów.(11-12) W 1995 roku w „Scandian Journal of Rheumatology” opublikowano dwa badania potwierdzające przypadki poszczepiennego zapalenia stawów(13-14) w tym samym roku Irish Medical Journal udokumentował związek z artropatią.(15) W 1997 r. w British Journal of Rheumatology opublikowano dwa inne badania dokumentujące kilka przypadków zapalenia wielostawowego po podaniu szczepionki(16-17) aw 1998 r. Journal of Rheumatology ponownie potwierdził reumatoidalne zapalenie stawów.(18) Również w tym samym roku francuski magazyn Revue de Médecine Interne opublikował badanie dotyczące choroby Stilla rozpoczynającej się w wieku dorosłym – rzadkiego i bolesnego rodzaju zapalenia stawów – po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu A i B.(19) W 1999 roku Reumatologia udokumentowała zaburzenia reumatologiczne po szczepieniu(20) a w 2000 r. American College of Rheumatology opublikowało badania w recenzowanym czasopiśmie Arthritis & Rheumatology, które udokumentowały zespół Sjogrena – rzadką postać przewlekłego zapalenia stawów – po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(21)
Choroby autoimmunologiczne i neurologiczne, w tym stwardnienie rozsiane
W 1983 roku w czasopiśmie New England Journal of Medicine opublikowano badanie wykazujące wystąpienie polineuropatii – jednoczesnego zaburzenia wielu nerwów – po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(22) W 1988 roku w czasopiśmie American Journal of Epidemiology opisano wiele „neurologicznych zdarzeń niepożądanych” po szczepionce, w tym liczne przypadki zespołu Guillain-Barré, radikulopatii lędźwiowej, neuropatii splotu ramiennego, zapalenia nerwu wzrokowego i poprzecznego zapalenia rdzenia kręgowego.(23) W tym samym roku czasopismo Archives of Internal Medicine udokumentowało miastenię – ciężką przewlekłą autoimmunologiczną chorobę nerwowo-mięśniową – ponownie po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(24)
W 1991 roku The Lancet opublikował raport dokumentujący demielinizację ośrodkowego układu nerwowego po szczepionce(25) aw 1992 r. firma Nephron opublikowała dane łączące szczepienia z toczniem rumieniowatym układowym, przewlekłą chorobą autoimmunologiczną atakującą wiele narządów.(26) Również w 1992 r. w czasopiśmie Clinical Infectious Diseases opublikowano badanie łączące zespół Evansa – rzadką chorobę autoimmunologiczną i krwi o wysokiej śmiertelności – ze szczepionką.(27) a francuski magazyn Thérapie ponownie opublikował badanie dotyczące „porażenia obwodowego twarzy” po podaniu leku.(28) Ponadto Infectious Disease News opublikowało raport stwierdzający liczne przypadki uszkodzeń neurologicznych przypominających stwardnienie rozsiane(29) aw 1993 r. w Journal of Hepatology ukazał się artykuł na temat poprzecznego zapalenia rdzenia kręgowego – zapalenia rdzenia kręgowego – po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(30) W tym samym roku francuska gazeta La Nouvelle Presse Médicale opublikowała dane potwierdzające wystąpienie poszczepiennego „ostrego zapalenia rdzenia kręgowego”(31) i Kliniczne Choroby Zakaźne udokumentowały „klasyczne stwardnienie rozsiane”.(32) W 1994 roku Archives of Pediatrics and Adolescent Medicine opublikowało dane łączące toczeń ze szczepionką(33) oraz w czasopiśmie Acta Neurologica Scandinavica opublikowano raport dotyczący ostrej ataksji móżdżkowej – poważnej utraty równowagi i koordynacji ruchowej – po wspomnianym szczepieniu.(34)
W 1995 roku w czasopiśmie Journal of Neurology, Neurosurgery and Psychiatry opisano demielinizację ośrodkowego układu nerwowego.(35) oraz w American Journal of Neuroradiology zapalenie rdzenia kręgowego. Autorzy tego ostatniego badania zauważyli, że zdarzenia niepożądane tego rodzaju mogą być niedostatecznie zgłaszane ze względu na późne wystąpienie objawów.(36) W 1996 roku zarówno Nephron, jak i francuskie czasopismo Annales de Dermatologie et de Vénéréologie opublikowały badania potwierdzające korelację pomiędzy toczniem rumieniowatym a szczepionką przeciwko wirusowemu zapaleniu wątroby typu B.(37-38) W tym samym roku Journal of Hepatology opublikował raport na temat związku z leukoencephalitis, zapaleniem istoty białej mózgu.(39) W 1996 roku w czasopiśmie New England Journal of Medicine udokumentowano krioglobulinemię poszczepienną – rzadką chorobę autoimmunologiczną, która upośledza krążenie, powoduje krwawienie i inne problemy.(40)
Autoimmunizacja wywołana szczepionką została potwierdzona w czasopiśmie Journal of Autoimmunity(41) a w 1997 r. w Indian Journal of Pediatrics opublikowano badanie łączące zespół Guillain-Barré – chorobę autoimmunologiczną powodującą uszkodzenie nerwów, osłabienie mięśni i paraliż – ze szczepionką.(42) W tym samym roku Journal of Korean Medical Science udokumentował ostre zapalenie rdzenia kręgowego(43) pojawiło się również powiązanie z „nuropatią nerwu psychicznego”.(44)
Następnie w JAMA pojawiły się dane dotyczące 46 osób – głównie kobiet – które utraciły włosy po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(45)
W 1998 roku u zaszczepionych osób udokumentowano zarówno toczeń rumieniowaty, jak i małopłytkowość(46) aw 1999 r. więcej łysienia w American Journal of Gastroenterology.(47) W tym samym roku w czasopiśmie Autoimmunology udokumentowano polineuropatię demielinizacyjną, natomiast w czasopiśmie Neurology opublikowano dane łączące stwardnienie rozsiane i zapalenie mózgu ze szczepionką.(48-49) Również w 1999 r. La Nouvelle Presse Médicale napisała o poszczepiennym zapaleniu rdzenia szyjnego(50) aw 2000 roku w Neurology omówiono stwardnienie rozsiane.(51) Również w 2000 roku w czasopiśmie Journal of the Medical Association of Tajlandii opisano zespół Guillain-Barré po zastosowaniu szczepionki przeciwko wirusowemu zapaleniu wątroby typu B z rekombinowanym DNA(52) aw 2001 r. w Klinicznym Chorób Zakaźnych udokumentowano leukoencefalopatia.(53) W 2004 roku czasopismo Neurology opublikowało badanie wykazujące związek pomiędzy szczepionką a statystycznie istotnym ryzykiem zachorowania na stwardnienie rozsiane;(54) w 2006 roku Chinese Medical Journal również udokumentował stwardnienie rozsiane.(55) W 2008 roku firma Neurology opublikowała dwa badania wykazujące statystycznie istotną korelację pomiędzy szczepieniem dzieci przeciwko wirusowemu zapaleniu wątroby typu B a rozwojem stwardnienia rozsianego u dzieci (demielinizacji ośrodkowego układu nerwowego) ponad trzy lata później.(56-57)
Zaburzenia sensoryczne
W licznych publikacjach medycznych i naukowych udokumentowano zaburzenia wzroku i słuchu po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. Na przykład w 1987 r. w czasopiśmie The Lancet opublikowano artykuł na temat zapalenia błony naczyniowej oka – zapalenia wewnętrznej wyściółki oka, które często prowadzi do ślepoty – po szczepieniu.(58) W 1993 r. ponownie w czasopiśmie The Lancet pojawiły się dalsze dane dokumentujące utratę wzroku i eozynofilię – alergiczną chorobę krwi – ponownie po szczepieniu.(59) W 1994 roku Optometry and Vision Science udokumentowały poszczepienne zapalenie nerwu wzrokowego(50) a w 1995 r. w Archiwum Okulistyki omówiono epiteliopatię – rzadką chorobę oczu powodującą pogorszenie widzenia.(61) W 1996 r. The Lancet opublikował raport dokumentujący „zamknięcie żyły środkowej siatkówki” po szczepionce,(62) natomiast w American Journal of Ophtalmology wspomniano o obustronnym zespole białej plamki – który powoduje utratę wzroku w obu oczach.(63) Również w 1996 r. La Nouvelle Presse Médicale udokumentowała zapalenie nerwu wzrokowego – zapalenie i uszkodzenie nerwu wzrokowego – po podaniu szczepionki(64) a inne francuskie czasopismo, Annales d'Otolaryngologie et de Chirurgie Cervico-Faciale, wspomniało o utracie słuchu.(65) W 1997 r. La Nouvelle Presse Médicale opublikowała następnie dwa różne badania dokumentujące poważne przypadki niedrożności żyły środkowej siatkówki po szczepieniu.(66-67) W tym samym roku Nefrologia Dializa Transplantacyjna potwierdziła początek zapalenia nerwu wzrokowego po szczepionce(68) oraz Międzynarodowa Okulistyka certyfikowana jako „powikłania okulistyczne” u zaszczepionych osób.(69) Również w 1997 r. Annals of the New York Academy of Sciences i międzynarodowe czasopismo Auris, Nasus, Larynx odnotowały utratę słuchu po szczepieniu,(70-71) natomiast w 1998 r. w czasopiśmie Journal of French Ophtalmology opublikowano dane dotyczące epiteliopatii.(72) W 1999 roku BMJ potwierdziło zapalenie nerwu wzrokowego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B(73) i Acta Ophtalmologica Scandinavica papilledema - obrzęk tarczy wzrokowej.(74) W 2001 roku niemieckie czasopismo Klinische Monatsblätter Für Augenheilkunde również potwierdziło występowanie poszczepiennego zapalenia nerwu wzrokowego.(75)
Choroby krwi
W 1990 r., wkrótce po masowym wprowadzeniu na rynek szczepionki przeciwko wirusowemu zapaleniu wątroby typu B, BMJ udokumentowało zapalenie naczyń, czyli zapalenie naczyń krwionośnych, po podaniu leku.(76) W 1993 roku angielski magazyn Thorax potwierdził tę tezę(77) oraz The Lancet opublikowali badanie dotyczące eozynofilii, alergicznej choroby krwi, ponownie po szczepieniu.(78) W 1994 i 1995 r. „The Lancet” również udokumentował trombocytopenię – poważną chorobę powodującą nadmierne krwawienie, powstawanie siniaków i problemy z krzepnięciem krwi.(79-80) W 1998 roku u wielu niedawno zaszczepionych pacjentów potwierdzono początek trombocytopenii(81) potwierdziły także dane ze skandynawskiego dziennika chorób zakaźnych i Archives of Disease in Children, które potwierdzają, że choroba ta jest zdarzeniem niepożądanym szczepionki.(82) W 1999 r. w European Journal of Pediatrics po raz kolejny potwierdzono małopłytkowość po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B i szczepionce MMR(83) w tym samym roku w czasopiśmie Journal of Rheumatology opublikowano dwa ważne badania, z których pierwsze wykazało korelację między szczepionką a zapaleniem naczyń(84) i druga erytermalgia, skurcze naczyń w dłoniach i stopach, które powodują ból i pieczenie.(85) W 2000 roku Reumatologia Kliniczna i Doświadczalna badała przypadki guzkowego zapalenia wielostawowego(86) - rzadki, ogólnoustrojowy, martwiczy (uszkadzający komórki) rodzaj zapalenia naczyń - a British Journal of Hematology udokumentowało ciężką pancytopenię - niebezpieczne zmniejszenie liczby czerwonych krwinek.(87) W 2001 roku w czasopiśmie Journal of Rheumatology opublikowano dodatkowe dane potwierdzające możliwość wystąpienia zapalenia naczyń po zastosowaniu rekombinowanej szczepionki przeciw wirusowemu zapaleniu wątroby typu B(88) a włoski dziennik „Haematologica” potwierdził, że małopłytkowość jest zdarzeniem niepożądanym.(89)
Choroby skórne
W 1989 roku w czasopiśmie New England Journal of Medicine opisano rumień guzowaty – bolesne zapalenie skóry z miękkimi guzkami – po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B.(90) W 1993 roku w czasopiśmie Journal of Rheumatology opisano przypadki zarówno rumienia guzowatego, jak i zapalenia stawów typu Takayasu – rzadkiej postaci zapalenia naczyń.(91) W tym samym roku szwedzkie czasopismo Acta Dermato-Venereologica napisało o liszaju ruberowym płaskim po szczepieniu(92) - swędząca wysypka na skórze charakteryzująca się grubymi, twardymi zmianami położonymi blisko siebie, przypominającymi algi lub grzyby rosnące na skałach. W 1994 roku Archiwum Dermatologiczne udokumentowało również liszaj płaski po szczepieniu(93) i Dermatologia Dziecięca wykazały związek z rumieniem wielopostaciowym.(94) W 1997 r. w Australasian Journal of Dermatology potwierdzono wystąpienie „reakcji liszajowatej” (liszaj płaski) po podaniu szczepionki(95) a Journal of the American Academy of Dermatology napisał o anetodermii(96) - miejscowe zmarszczki, utrata elastyczności i zanik skóry - po szczepieniu. W 1998 roku w British Journal of Dermatology opublikowano dwa badania dokumentujące choroby skóry poszczepienne: jedno dotyczyło liszaja płaskiego(97) a drugi na pokrzywkę i obrzęk naczynioruchowy,(98) patologie o podłożu alergicznym charakteryzujące się pieczeniem, kłuciem i bolesnym obrzękiem. W 1999 roku o liszaju płaskim wspomniano także w International Journal of Dermatology(99) aw 2000 roku w czasopiśmie Clinical and Experimental Dermatology opublikowano dane potwierdzające występowanie rumienia wielopostaciowego poszczepiennego.(100) W tym samym roku Nepal Journal of Dermatology ponownie napisał o liszaju płaskim po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B(101) w 2001 roku wzmianka pojawiła się w czasopiśmie Journal of the American Academy of Dermatology(102) podczas gdy dermatologia dziecięca mówiła o erupcji liszajowatych.(103)
Cukrzyca, choroby wątroby i nerek
W 1994 roku „The Lancet” udokumentował dysfunkcję wątroby po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B(104) aw 1995 Clinical Nephrology opublikowało badanie dotyczące zespołu nerczycowego – uszkodzenia nerek – ponownie po szczepieniu.(105) W 1996 New Zealand Medical Journal opublikował dwa dokumenty, które korelowały wirusowe zapalenie wątroby typu B z epidemią cukrzycy insulinozależnej (IDDM). Autorzy ustalili, że w ciągu trzech lat po nowo wprowadzonej i bardzo szeroko zakrojonej kampanii masowych szczepień nastąpił 60% wzrost liczby przypadków IDDM.(106-107) W 1997 r. Intensive Care Medicine napisało o zapaleniu wątroby i ostrych chorobach układu oddechowego po szczepieniu (108). W 2000 roku Nefrologia Dziecięca potwierdziła możliwość wystąpienia zespołu nerczycowego po zaszczepieniu.(109) Inne publikacje również dokumentowały działania niepożądane tej szczepionki.(110-111-112-113-114-115-116-117-118-119)
Francja wyeliminowała wirusowe zapalenie wątroby typu B z kalendarza szczepień pediatrycznych
W lipcu 1998 r. około 15.000 XNUMX obywateli francuskich należących do piętnastu stowarzyszeń złożyło pozew przeciwko rządowi francuskiemu, zarzucając mu wprowadzenie w błąd opinii publicznej co do ryzyka i korzyści związanych ze szczepionką przeciwko wirusowemu zapaleniu wątroby typu B. Setki, a może tysiące – osób cierpiało na choroby autoimmunologiczne i zaburzenia neurologiczne, w tym stwardnienie rozsiane, po szczepieniu.(120) W rezultacie w październiku 1998 r. Francja jako pierwszy kraj zniosła obowiązek przyjmowania tej szczepionki do szkół.(121)
Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B
W 1978 roku New York Blood Center na Manhattanie w stanie Nowy Jork wstrzyknęło homoseksualnym mężczyznom eksperymentalną szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B, wyprodukowaną przez firmę Merck, do przygotowania której wykorzystano szympansy. Wkrótce potem homoseksualni mężczyźni w San Francisco, Los Angeles, Denver, Chicago i St. Louis również otrzymali 3 dawki leku w ciągu trzech miesięcy.
W 1980 r. 20% homoseksualistów, którzy zgłosili się na ochotnika do eksperymentu na Manhattanie, uzyskało pozytywny wynik testu na obecność wirusa HIV – jest to najwyższa liczba przypadków na świecie, w tym w Afryce. W 1981 roku oficjalnie ogłoszono epidemię AIDS. Chociaż nie ma dowodów na to, że eksperymentalna szczepionka przeciwko wirusowemu zapaleniu wątroby typu B zastosowana u tych homoseksualnych ochotników spowodowała AIDS, nie ma wątpliwości, że choroba osiągnęła szczyt wkrótce po zastrzyku.(122)
Jak skuteczna jest szczepionka przeciwko wirusowemu zapaleniu wątroby typu B?
Skuteczność szczepionki przeciwko wirusowemu zapaleniu wątroby typu B określono poprzez wstrzyknięcie leku osobom, u których następnie zmierzono specyficzne przeciwciała wytwarzane we krwi. Przeciwciała te muszą spełniać lub przekraczać pewne poziomy ustalone przez ekspertów i które, jak się przypuszcza, zapewniają ochronę. Naukowcy nazywają to „seroprotekcją”. Zgodnie z tą definicją szczepionkę uważa się za „wysoce immunogenną”, jeśli poziom przeciwciał można zmierzyć w krótkim czasie po ostatniej dawce cyklu składającego się z trzech dawek przypominających.(123) Jednak według branż produkcyjnych czas trwania efektu ochronnego u zdrowych zaszczepionych osób nie jest znany. Badania kontrolne przeprowadzone już pięć do dziewięciu lat później wykazały, że około połowa wszystkich zaszczepionych osób nie ma już ochronnego poziomu przeciwciał.(124-125)
Na przykład badanie opublikowane w New England Journal of Medicine wykazało, że po pięciu latach poziom przeciwciał (przypuszczalnie powiązany z odpornością) dramatycznie spadł lub nie był już wykrywalny u 42% zaszczepionych. Ponadto 34 z 773 osób (4,4%) zostało zakażonych wirusem.(126-127) W innym badaniu mniej niż 40% zaszczepionych miało przeciwciała ochronne po pięciu latach.(128)
Podobne badania wykazały, że u 48% zaszczepionych osób poziom przeciwciał był niewystarczający już po czterech latach.(129) Według WHO aż „60% dorosłych utraci wszystkie mierzalne przeciwciała wywołane szczepionką przeciwko wirusowemu zapaleniu wątroby typu B w ciągu sześciu do dziesięciu lat”.(130) a literatura medyczna jest pełna danych potwierdzających niepowodzenie szczepień.(131-132)
Referencje
- Jacobson IM i wsp., „Brak efektu szczepionki przeciwko wirusowemu zapaleniu wątroby typu B na fenotypy komórek T”, NEJM, 1984, 311 (16), s. 1030-1032.
- Instytut Medycyny, Zdarzenia niepożądane związane ze szczepionkami dla dzieci: dowody dotyczące przyczynowości, National Academy Press, Waszyngton, DC, 1994.
- Merck & Co., Inc. Recombivax HB Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B (rekombinowana), ulotka dołączona do opakowania, stan na czerwiec 2005 r.
- Tamże.
- Tamże.
- Tan LJ, „Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B”, Amerykańskie Stowarzyszenie Medyczne, AMA pomagająca lekarzom pomagać pacjentom, www.arna-assn.org, 9 grudnia 2004 r.
- System zgłaszania zdarzeń niepożądanych szczepionek VAERS. Rockville, Maryland
- Rogers ton SJ i in. , „Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B związanemu z rumieniem guzowatym i zapaleniem wielostawowym”, BMJ, 1990, 301, s. 345. XNUMX.
- Hachulla E. i wsp., „Reaktywne zapalenie stawów po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B Journal of Rheumatology”, 1990, 17, s. 1250-1251.
- Vautier G. i wsp., „Ostre seropozytywne reumatoidalne zapalenie stawów występujące po szczepieniu przeciwko wirusowemu zapaleniu wątroby”, Br. J. Rheumatol., październik 1994, 33 (10), s. 991-XNUMX. XNUMX.
- Hassan W. i wsp., „Zespół Reitera i reaktywne zapalenie stawów u pracowników służby zdrowia po szczepieniu”, BMJ, 9 lipca 1994, 309 (6967), s. 94-XNUMX. XNUMX.
- Birley HD i wsp., „Immunizacja zapalenia wątroby typu B i reaktywne zapalenie stawów”, BMJ, grudzień 1994, 309 (6967), s. 1514. XNUMX.
- Gross i wsp., „Zapalenie stawów po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. Opis trzech przypadków”, Scand. J. Rheumatol., 1995, 24(1), s. 50-52.
- Biasi D. i wsp., „Objawy reumatologiczne po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. Opis trzech przypadków”, Scand. J. Rheumatol., 1995, 24, s. 50-52.
- Aherne P. i wsp., „Artropatia łuszczycowa”, Irish Medical Journal, marzec-kwiecień 1995, 88 (2), s. 72. XNUMX.
- Harrison BJ i wsp., „Pacjenci, u których rozwinęło się zapalenie wielostawowe (PH) po immunizacji, są klinicznie nie do odróżnienia od innych pacjentów z PH”, Br. J. Rheum., marzec 1997, 36 (3), s. 366-369.
- Bracci M. i wsp., „Zapalenie wielostawowe związane ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, Br. J. Rheumatol., luty 1997, 36(2), s. 300-301.
- Pope JE i wsp., „Rozwój reumatoidalnego zapalenia stawów po szczepieniu rekombinowanym wirusem zapalenia wątroby typu B”, J. Rheum., wrzesień 1998, 25 (9), s. 1687-1693.
- Grasland A i wsp., „Choroba Stilla o początku w wieku dorosłym po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu A i B?”, Rev. Internal Med., luty 1998, 19 (2), s. 134-136.
- Maillefert JF i wsp., „Zaburzenia reumatyczne rozwinięte po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Rheumatol. (Oxford), październik 1999, 38 (10), s. 978-983.
- Toussirot E. i wsp., „Zespół Sjogrena występujący po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Arthritis Rheuma, wrzesień 2000, 43 (9), s. 2139-2140.
- Ribera ER i wsp., „Polineuropatia związana z podawaniem szczepionki przeciwko wirusowemu zapaleniu wątroby typu B”, N. Engl. J. Med., 8 września 1983, 309(10), s. 614-615.
- Shaw FE Jr. i wsp., „Nadzór po wprowadzeniu na rynek neurologicznych zdarzeń niepożądanych zgłoszonych po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. Doświadczenia z pierwszych trzech lat”, Am. J. Epidemiol., luty 1988, 27 (s), s. 337-352 .
- Biron P. i wsp., „Myasthenia gravis po znieczuleniu ogólnym i szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, arch. stażysta. Med., grudzień 1988, 148(12), s. 2685-XNUMX. XNUMX.
- Herroelen L. i in. „Demielinizacja ośrodkowego układu nerwowego po immunizacji rekombinowaną szczepionką przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, 9 listopada 1991, 338 (8776), s. 1174-1175.
- Tudela P. i wsp., „Toczeń rumieniowaty układowy i szczepienia przeciwko wirusowemu zapaleniu wątroby typu B”, Nephron, 1992, 62 (2), s. 236-XNUMX. XNUMX.
- Martinez E. i wsp., „Zespół Evana wywołany rekombinowaną szczepionką przeciwko wirusowemu zapaleniu wątroby typu B”, Clin. Infect. Dis., 1992, 15, str. 1051.
- Ganry 0. i wsp., „Obwodowe porażenie twarzy po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. A propos przypadku”, Therapie, 1992, 47, s. 437-438.
- Waisbren BA, „Druga strona medalu (litera)”, Inf Dis. Wiadomości, 1992, 5, s. 2. XNUMX.
- Trevisani F. i wsp., „Poprzeczne zapalenie rdzenia kręgowego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”,]. Hepatologii, wrzesień 1993, 19(2), s. 317-318.
- Mahassin F. i in. , „Ostre zapalenie rdzenia kręgowego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Presse Med., grudzień 1993, 22 (40), s. 1997-1998.
- Nadler JP, „Szczepienia na stwardnienie rozsiane i wirusowe zapalenie wątroby typu B”, Clin. Infekować. Dis., listopad 1993, 17 (5), s. 928-929.
- Mamoux V. i wsp., „Lupus erthymatosus disseminatus i szczepienie przeciwko wirusowi zapalenia wątroby typu B”, Arch. Pediatr., 1994, 1, s. 307-309.
- Deisenhammer F. i wsp., „Ostra ataksja móżdżkowa po immunizacji rekombinowaną szczepionką przeciwko wirusowemu zapaleniu wątroby typu B”, Acta Neurol. Scand., czerwiec 1994, 89(6), s. 462-463.
- Kaplanski G. i wsp., „Demielinizacja ośrodkowego układu nerwowego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B i haplotypowi HLA”, J. Neurol. Neurochirurg. Psychiatria, czerwiec 1995, 58(6), s. 758-759.
- Tartaglino LM i wsp., „Obrazowanie MR w przypadku zapalenia szpiku po szczepieniu”, Am. J. Neuroradiol., 1995, 16 (3), s. 581-582. XNUMX-XNUMX.
- Guiserix J., „Toczeń rumieniowaty układowy po szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, Nephron, 1996, 74 (2), s. 441. XNUMX.
- Grezard P. i wsp., „Toczeń rumieniowaty skórny i aftoza policzkowa po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B u 6-letniego dziecka”, Ann. Dermatol. Venereal., 1996, 123(10), s. 657-659.
- Manna R. i wsp., „Leukoencephalitis after recombinant hepatitis B szczepionka”, J. of Hepatology, czerwiec 1996, 24 (6), s. 764-765.
- Mathieu E. i wsp., „Krioglobulinemia po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Nowa Anglia]. Med., sierpień 1996, 335(5), s.335.
- Cohen AD. i wsp., „Vaccine- duced autoimmunity”, J. Autoimmunity, grudzień 1996, 9 (6), s. 699-703.
- Kakar A. i wsp., „Zespół Guillaina Barre’a związany ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, Ind. J. Ped., wrzesień-październik 1997, 64 (5), 710-712.
- Song HK i wsp., „Ostre zapalenie rdzenia kręgowego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, J. Koreański Med. Sci., czerwiec 1997, 12 (3), s. 249-251.
- Maillefert JF i wsp., „Mental nerw neuropatia jako wynik szczepienia przeciwko wirusowemu zapaleniu wątroby typu B”, Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontology, czerwiec 1997, 83 (6), s. 663-664.
- Wise RP i wsp., „Wypadanie włosów po rutynowych szczepieniach”, JAMA, 8 października 1997, 278 (14), s. 1176-1178.
- Finielz P. i wsp., „Toczeń rumieniowaty układowy i plamica małopłytkowa u dwóch członków tej samej rodziny po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Nephrol. Wybierz. Transplant., 1998, 13(9), s. 2420-2421.
- Flemrner M. i wsp., „The bald prawda”, Am. J. Gastroenterol., kwiecień 1999, 94 (4), s. 1104-XNUMX. XNUMX.
- Creange A i wsp., „Ostra polineuropatia demielinizacyjna lędźwiowo-krzyżowa po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Autoimmunity, 1999, 30, s. 143-146.
- Tourbah A. i wsp., „Zapalenie mózgu po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B: nawracające rozsiane zapalenie mózgu lub stwardnienie rozsiane?”, Neurology, 22 lipca 1999, 53 (2), s. 396-401.
- Renard JL i wsp., „Ostre poprzeczne zapalenie rdzenia szyjnego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B. Ewolucja przeciwciał anty-HBs”, Presse Med., 3-10 lipca 1999, 28 (24), s. 1290-1292.
- Gran B. i wsp., „Martin R. Rozwój stwardnienia rozsianego po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Neurol., 2000, 54 (suppl 3), A164.
- Sinsawaiwong S. i wsp., „Zespół Guillain-Barre po rekombinowanej szczepionce przeciwko wirusowemu zapaleniu wątroby typu B i przegląd literatury”, J. Med. Assoc. Thai., wrzesień 2000, 83 (9), s. 1124-1126.
- Konstantinou D. i wsp., „Dwa epizody leukoencephalitis związane z rekombinowanym szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B u jednego pacjenta”, Clin. Inf. Dis., 15 listopada 2001, 33, s. 1772-1773.
- Heman MA i wsp., „Rekombinowana szczepionka przeciwko wirusowemu zapaleniu wątroby typu B a ryzyko stwardnienia rozsianego: badanie prospektywne”, Neurology, 2004, 63, s. 838-842.
- Terney D. i wsp., „Stwardnienie rozsiane po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B u 16-letniego pacjenta”, Chinese Medical Journal, 2006, 119 (1), s. 77-79.
- Yann M. i wsp., „Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B i ryzyko demielinizacji zapalnej OUN w dzieciństwie”, Neurology, 8 października 2008 r. [opublikowano w Internecie].
- Ness JM i wsp. „Szczepionki przeciwko wirusowemu zapaleniu wątroby i stwardnieniu rozsianemu u dzieci. Czy liczy się czas czy rodzaj?”, Neurology, 17 grudnia 2008 (opublikowane w Internecie).
- Fried Met wsp., „Zapalenie błony naczyniowej oka po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, 12 września 1987, s. 631-632.
- Brezin A. i wsp., „Utrata wzroku i eozynofilia po szczepionce rekombinowanej przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, 28 sierpnia 1993, 342 (8870), s. 563-564.
- Achiron LR i wsp., „Postinfekcyjne zapalenie nerwu wzrokowego typu B”, Optom. Pogląd Sci., 1994, 71, s. 53-56.
- Brezin AP i wsp., „Ostra tylna wieloogniskowa epiteliopatia placoidalna po szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, Arch. Ophtalmol., marzec 1995, 113 (3), s. 297-300.
- Devin F. i wsp., „Occlusion of central siatkówki żyły po szczepieniu przeciw wirusowemu zapaleniu wątroby typu B”, The Lancet, czerwiec 1996, 347 (9015), s. 1626-XNUMX. XNUMX.
- Baglivo E. i wsp., „Zespół wielu zanikających białych kropek po szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, Am. J. Ophtalmol., wrzesień 1996, 122 (3), s. 431-432.
- Berkman N. i wsp., „Obustronne zapalenie nerwów brodawkowatych po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Presse Med., 28 września 1996, 25 (28), s. 1301-XNUMX. XNUMX (francuski).
- Bonfils P. i wsp., „Zmienna percepcja utraty słuchu po szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, Ann. Otolaryngol. Chir. Cervicofac., 1996, 113 (6), s. 359-361 (francuski).
- Granel B. i wsp., „Zamknięcie żyły środkowej siatkówki po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B szczepionkami rekombinowanymi. 4 przypadki”, Presse Med., 1 lutego 1997, 26 (2), s. 62-65 [francuski].
- Berkman N., „Przypadek segmentowej jednostronnej niedrożności żyły środkowej siatkówki po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Presse Med., 26 kwietnia 1997, 26 (14), s. 670-XNUMX. XNUMX [francuski].
- Albitar S. i wsp., „Obustronne pozagałkowe zapalenie nerwu wzrokowego ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, Nephrol. Wybierz. Transplant, październik 1997, 12 (10), s. 2169-2170.
- Arya SC, „Powikłania okulistyczne po szczepionkach przeciwko wirusowi zapalenia wątroby typu B”, Int. Ophth., 1997, 21 (3), s. 177-178.
- Orlando MP i wsp., „Nagła utrata słuchu w wyniku szczepienia przeciwko wirusowemu zapaleniu wątroby typu B: opis przypadku”, Annals of the New York Academy of Sciences, 29 grudnia 1997, 830, s. 319-321.
- Biacabe B. i wsp., „A case report of fluctuant odbiorczo-nerwowy ubytek słuchu po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Auris, Nasus, Larynx, październik 1997, 24, (4), s. 357-360.
- Bourges JL i wsp., „Wieloogniskowa epiteliopatia placoidalna i szczepienie przeciwko wirusowemu zapaleniu wątroby typu B”, J. Fr. Ophtalmol., listopad 1998, 21(9), s. 696-700 [w języku francuskim].
- Stewart O. i wsp., „Jednoczesne podawanie szczepionek przeciwko wirusowemu zapaleniu wątroby typu B i polio związane z obustronnym zapaleniem nerwu wzrokowego”, Br. J. Ophtalmol., październik 1999, 83 (10), str. 1200-1201.
- Fledelius HC, „Jednostronny obrzęk brodawek po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B u pacjenta z migreną. Opis przypadku uwzględniający aspekty kryminalistyczne”, Acta Ophtalmol. Scand., grudzień 1999, 77 (6), s. 722-724.
- Voigt u. i wsp., „Zapalenie nerwu wzrokowego po szczepieniach przeciwko wirusowemu zapaleniu wątroby typu A, zapaleniu wątroby typu B i żółtej febrze”, Klin. Monatsbl. Augenheilkd., październik 2001, 218 (10), s. 688-690 (niemiecki).
- Cockwell P. i wsp., „Zapalenie naczyń związane ze szczepionką przeciwko wirusowemu zapaleniu wątroby typu B”, BMJ, 1 grudnia 1990, 301 (6763) str. 1281.
- Allen MB i wsp., „Zapalenie naczyń płucnych i skóry po szczepieniu przeciwko wirusowi hep B”, Thorax, maj 1993, 48 (5), s. 580-581.
- Nagafuchi S. i wsp., „Eozynofilia po śródskórnym szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, 1993, 342, s. 998. XNUMX.
- Poullin P. i wsp., „Plamica małopłytkowa po szczepionce rekombinowanej przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, listopad 1994, 344 (8932), s. 1293. XNUMX.
- Meyboom RH i wsp., „Trombocytopenia zgłaszana w związku ze szczepionkami przeciwko wirusowemu zapaleniu wątroby typu B i A”, The Lancet, czerwiec 1995, 345 (8965), s. 1638-XNUMX. XNUMX.
- Neau D. i wsp., „Immunologiczna plamica małopłytkowa po szczepionce rekombinowanej przeciwko wirusowemu zapaleniu wątroby typu B: retrospektywne badanie siedmiu przypadków”, Scan J. Infect Dis., 1998, 30 (2), s. 115-118.
- Ronchi F. i wsp., „Plamica małopłytkowa jako reakcja niepożądana na rekombinowaną szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B”, Arch. Dis. Child., marzec 1998, 78(3), s. 273-274.
- Muller A. i wsp., „Plamica małopłytkowa: reakcja niepożądana na skojarzoną immunizację (rekombinowaną szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B i odrze-śwince-różyczce) i po leczeniu ko-trimoksazolem”, Eur.]. Pediatr., grudzień 1999, 158 Suppi. 3, S209-10.
- Le Hello C. i wsp., „Podejrzane zapalenie naczyń związane ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, J. of Rheumatology, styczeń 1999, 26 (1), s. 191-194.
- Rabaud C. i wsp., „Pierwszy przypadek erytermalgii związanej ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, J. of Rheum., styczeń 1999, 26 (1), s. 233-234.
- De Keyser F. i wsp., „Patologia o podłożu immunologicznym po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”. Dwa przypadki guzkowego zapalenia tętnic i jeden przypadek wysypki polekowej przypominającej łupież różowy”, Clin. Exp. Rheumatol., styczeń-luty 2000, 18 (1), s. 81-85.
- Viallard JF i wsp., „Severe pancytopenia wyzwalana przez rekombinowaną szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B”, Br. J. Haematol., lipiec 2000, 110 (1), s. 230-233.
- Zaas A. i wsp., uZapalenie naczyń dużych tętnic po szczepieniu rekombinowanym wirusowym zapaleniem wątroby typu B. 2 przypadki”, J. Rheumatol., maj 2001, 28 (S), s. 1116-11120.
- Conesa V. i wsp., „Plamica małopłytkowa po szczepionce Recombinant Hepatitis B. Arzadkie stowarzyszenie”, Haematologica, marzec 2001, 86 (3), E09 [włoski].
- Goolsby PL, „Rumień guzowaty po szczepionce Recombivax HB przeciwko wirusowemu zapaleniu wątroby typu B”, N. Engl. J. Med., październik 1989, 321, 1198-1199.
- Castresana-Isla CJ i wsp., „Rumień guzowaty i zapalenie tętnic Talkayasu po immunizacji szczepionką przeciwko wirusowemu zapaleniu wątroby typu B pochodzącą z osocza”, J. Rheumatol., sierpień 1993, 20(8), s. 1417-1418.
- 109. Trevisian G. i wsp., „Liszaj ruber płaski po szczepieniu przeciwko HBV”. Acta Dermato-Venereotogica, luty 1993, 73 (1), s. 73. XNUMX.
- Aubin F. i wsp., „Liszaj płaski po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Archives of Dermatology, październik 1994; 130 (10), s. 1329-1330.
- Di Lernia V. i wsp., „Bisighini G. Rumień wielopostaciowy po szczepionce przeciwko wirusowemu zapaleniu wątroby typu B”, Ped. Derma., grudzień 1994, 11 (4), s. 363-364.
- Saywell Kalifornia. i wsp., „Kossard S. Lichenoid reakcja na szczepienie przeciwko wirusowemu zapaleniu wątroby typu B”, Australasian J. Derm., sierpień 1997, 38 (3), s. 152-154.
- Dauod MS i wsp., „Anetoderma po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B u dwójki rodzeństwa”,/. Amera. Acad. Dermatol., maj 1997, 36 (5 pkt 1), s. 779-780.
- Ferrando MF i wsp., „Liszaj płaski po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, br. J. Dermatol., sierpień 1998, 139 (2) s. 350.
- Barbaud A. i wsp., „Mechanizmy alergiczne i pokrzywka/obrzęk naczynioruchowy po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Bt. J. Dermatot, listopad 1998, 139 (5), s. 925-926.
- Schupp P. i wsp., „Liszaj płaski po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Inter. J. of Dermat., październik 1999, 38 (10), s. 799-800.
- Loche F. i wsp., „Rumień wielopostaciowy związany ze szczepieniem przeciwko wirusowemu zapaleniu wątroby typu B”, Cfin. Exp. Dermatol., marzec 2000, 25 (2), s. 167-168.
- Agrawal S. i wsp., „Liszaj płaski po szczepieniu HBV u dziecka: opis przypadku z Nepalu”, J. Dermatol., wrzesień 2000, 27(9), s. 618-620.
- Al-Khenaizan S., „Liszaj płaski występujący po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B: nowy przypadek”, J. Am. Acad. Dermatol., październik 2001, 4S (4), s. 614-615.
- Usman A. i wsp., „Erupcja liszajowata po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B: pierwszy opis przypadku z Ameryki Północnej”. Pediatr. Dermato J., marzec-kwiecień 2001, 18 (2) s. 123-126.
- Lilic D. i wsp., „Dysfunkcja wątroby i przeciwciała DNA po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, The Lancet, listopad 1994, 344 (8932), s. 1292-1293.
- Macario F. i wsp., „Zespół nerczycowy po szczepionce rekombinowanej przeciwko wirusowemu zapaleniu wątroby typu B”, Clin. Nephrol., maj 1995, 43 (5), s. 349.
- Classen John Barthelow, „Szczepienia u dzieci i cukrzyca”, New Zealand Med. J., 24 maja 1996, s. 195-XNUMX. XNUMX.
- Classen John Barthelow, „Epidemia cukrzycy i szczepionka przeciwko wirusowemu zapaleniu wątroby typu B”, New Z. Med. J., 24 maja 1996, s. 366.
- Ranieri VM i wsp., „Zapalenie wątroby i zespół ostrej niewydolności oddechowej u pacjenta otrzymującego szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B: możliwy związek?”, Intensive Care Medicine, styczeń 1997, 23 (1), s. 119-121.
- Islek I. i wsp., „Zespół nerczycowy po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Pediatr. Nephrol., styczeń 2000, 14, s. 89-90.
- Snider GB i wsp., „A możliwa ogólnoustrojowa reakcja na szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B”, JAMA. 1 marca 1985, 253(9), s. 1260-1261.
- AADRAC, „Australijski Komitet Doradczy ds. Niepożądanych Reakcji Leków: Reakcje na szczepionki przeciwko wirusowemu zapaleniu wątroby typu B”, Australijski Biuletyn ds. Niepożądanych Reakcji Leków, sierpień 1990.
- Germanaud J. i wsp., „Przypadek ciężkiej cytolizy po szczepieniu przeciwko wirusowemu zapaleniu wątroby typu B”, Amer. J. Med., czerwiec 1995, 98(6), s. 595-S96.
- Fisher BL, wyd., „Szczepionka przeciwko wirusowemu zapaleniu wątroby typu B: nieopowiedziana historia”, The Vaccine Reaction, Krajowe Centrum Informacji o Szczepionkach, wrzesień 1998.
- Belkin Michael, „Talidomid na zlecenie rządu dla niemowląt”, WorldNetDaily, 25 stycznia 1999, worldnetdaily.com
- Howd A., „Uncja zapobiegania, funt niedoli”, Magazyn Insight, 12 marca 1999 r.,
- Bethell T., „Strzały w ciemno”. Amerykański widz. Maj 1999.
- Wallstin B., „Immune to Reason”, The Houston Press, 3 czerwca 1999, www.houstonpress.com
- Shaw FE, „Wrzawa wokół mało znanego środka konserwującego, tiomersalu, zakłóca politykę Stanów Zjednoczonych dotyczącą szczepionek przeciwko wirusowemu zapaleniu wątroby typu B”, Raport dotyczący kontroli zapalenia wątroby typu B, raport dotyczący kontroli zapalenia wątroby, lato 1999, tom 4, nr 2. XNUMX.
- Spalding BJ, „Cud czy morderstwo? Kontrowersje dotyczące szczepionki przeciwko wirusowemu zapaleniu wątroby typu B”, Biospace.com, 11 listopada 1999, www.biospace.com
- Nauka, 31 lipca 1998 r.
- „Francja zawiesza stosowanie szczepionki przeciwko wirusowemu zapaleniu wątroby typu B”. https://www.bmj.com/content/317/7165/1034.2
- Cantwell A., „Eksperyment gejowski, który zapoczątkował AIDS w Ameryce”, Not Aids, 13 stycznia 2006 r., obecnie w http://rense.com/general68/gayex.htm
- Merck & Co.t Inc., Recombivax HB szczepionka przeciwko wirusowemu zapaleniu wątroby typu B (rekombinowana), ulotka dołączona do opakowania, stan na czerwiec 2005 r.; GlaxoSmithKline Biologicals, Engerix-B (szczepionka przeciwko wirusowemu zapaleniu wątroby typu B (rekombinowana), ulotka dołączona do opakowania, stan na grudzień 2005 r.
- Wainwright RB i wsp., „Czas trwania immunogenności i skuteczność szczepionki przeciwko wirusowemu zapaleniu wątroby typu B w populacji Yupik Eskimo, wstępne wyniki 8-letniego badania”, w „Viral hepatitis and wątroby choroba”, Hollinger FB i wsp. (red.) , Williams & Wilkins, 1990, s. 762-766.
- Hadler SC i wsp., „Ocena długoterminowej ochrony przez szczepionkę przeciwko wirusowemu zapaleniu wątroby typu B przez 7 do 9 lat u mężczyzn homoseksualnych”. w Wirusowym zapaleniu wątroby i chorobach wątroby, Hollinger FB i in. (red..), Williams i Wilkinst 1990, s. 766-768.
- Hadler SC i wsp., „Long-term immunogenność i skuteczność szczepionki przeciwko wirusowemu zapaleniu wątroby typu B u homoseksualnych mężczyzn”, NEJM, 24 lipca 1986, 315, s. 209-214.
- Stevens CE i wsp., „Perspektywy kontroli zakażenia wirusem zapalenia wątroby typu B: implikacje szczepień u dzieci i długoterminowej ochrony”, Pediatrics, 1992, 90, s. 170-173.
- Street AC i wsp., „Trwałość przeciwciał u pracowników służby zdrowia zaszczepionych przeciwko wirusowemu zapaleniu wątroby typu B”, Infec. Kontrola Hosp. Epidem., 1990, 11, s. 525-530.
- Pasko MT i wsp., „Persistence of anty-HBs wśród personelu medycznego zaszczepionego szczepionką przeciwko wirusowemu zapaleniu wątroby typu B”, American Journal of Public Health, 1990, 80, s. 590-593.
- Światowa Organizacja Zdrowia, ccSzczepionki przeciwko wirusowemu zapaleniu wątroby typu B: ponowna ocena immunogenności, WHO Drug Infor., 1994, 8 (2).
- Ballinger, AB i wsp., „Severe ostre zakażenie wirusem zapalenia wątroby typu B po szczepieniu”, The Lancet, 1994, 344, s. 1292–1293
- Goffin E. i wsp., „Ostre zakażenie wirusem zapalenia wątroby typu B po szczepieniu”, The Lancet, 1995, 345, s. 263. XNUMX.
Szczepionki: przewodnik po świadomym wyborze autorstwa Neila Z. Millera (autor) i Claudii Benatti (tłumacz)
Wydania Terra Nuova, 2018

