Czy szczepionka przeciw tężcowi może spowodować obrażenia i/lub śmierć?

Poniższy artykuł stara się rzucić światło na rozległy świat reakcji niepożądanych, ze szczególnym spojrzeniem na reakcję przeciwko tężcowi, ale zachęcamy do przeczytania wszystkich przedstawionych poniżej zagadnień, aby zrozumieć inne powiązane kwestie, takie jak problem wielu szczepionek , nadwrażliwość na jeden lub więcej składników szczepionek, problem SIDS i adiuwantów. Większość szczepionek dostępnych na rynku jest produkowana do celów komercyjnych, często w wielu postaciach, co sprawia, że temat uszkodzeń szczepionek jest znacznie szerszy.
Problem wielu szczepionek (kliknij, aby otworzyć)
Problem wielu szczepionek

Obecne kalendarze szczepień, zwłaszcza dla wieku pediatrycznego, przewidują podanie wielu antygenów i szczepionek w jednej sesji, sprzyjając wygodzie kosztem bezpieczeństwa. Aby móc wygłosić konkretną wypowiedź na temat bezpieczeństwa szczepionek, musimy koniecznie wziąć pod uwagę złożoność zjawiska, doradzając wszystkim czytelnikom odpowiednie zapoznanie się ze wszystkimi aspektami szczepień, zaletami i wadami.
Dr Russell Blaylock, adiunkt kliniczny neurochirurgii w Centrum Medycznym Uniwersytetu Mississippi, przez lata badał „toksyczną synergię” i był w stanie zaobserwować, że kiedy dwa słabo toksyczne pestycydy, z których żaden nie jest w stanie wywołać zespołu Parkinsona u zwierząt doświadczalnych, są ze sobą łączone, mogą wywołać chorobę nawet szybko i porównuje to zjawisko do wielu szczepionek podawanych jednocześnie: „Szczepionki, jeśli są zbyt liczne i zbyt blisko siebie, zachowują się jak choroba przewlekła”.(A). Inne Dwa badania potwierdziły, że po zaszczepieniu wieloma szczepionkami w jednym podaniu może wystąpić nagła śmierć niemowląt.(pne)
Badanie opublikowane w Human and Experimental Toxicology wykazało, że kraje, które przepisują więcej szczepionek dzieciom, mają zwykle wyższy wskaźnik śmiertelności niemowląt.(D) Na przykład w Stanach Zjednoczonych, gdzie dzieci otrzymują 26 szczepionek, umiera ponad 6 dzieci na 1000 żywych urodzeń, podczas gdy w Szwecji i Japonii, gdzie podaje się 12 szczepionek pediatrycznych, zgłaszane są 3 zgony na każde 1000 żywych urodzeń. We wspomnianym badaniu rozważany jest również związek między szczepionkami a SIDS.
Ze szwajcarskiego badania opublikowanego w 2005 roku w European Journal of Pediatrics(E) wynika z tego, że jeśli chodzi o wpływ na wcześniaki, częstość nawracających lub nasilających się bezdechów i bradykardii po podaniu szczepionek sześciowartościowych wynosi 13%. W tym samym roku w tym samym czasopiśmie opublikowano niemieckie badanie, w którym zbadano nagłe zgony niemowląt po sześciowartościowym. Autorzy piszą: „Wyniki te, oparte na doniesieniach spontanicznych, nie dowodzą związku przyczynowego między szczepieniem a nagłą śmiercią niemowląt, ale stanowią sygnał dotyczący jednego z dwóch dostępnych sześciowartościowych; sygnał, który powinien skłonić do zintensyfikowania nadzoru nad nagłymi zgonami niemowląt po szczepieniu”.(fa)
W 2006 roku został opublikowany w czasopiśmie medycznym Vaccine(G) list od zespołu naukowców z Uniwersytetu w Monachium, który zgłosił „sześć przypadków nagłej śmierci niemowląt po szczepieniu sześciowartościowym. Wszystkie znalezione martwe bez wyjaśnienia 1-2 dni po szczepieniu”. Zostały one sklasyfikowane jako typowe przypadki nagłej śmierci niemowląt, ale autoptyczna weryfikacja wykazała nieprawidłowości neuropatologiczne i histologiczne, a wszystkie dzieci wykazywały znaczny obrzęk mózgu, co czyniło je wyjątkiem w porównaniu z innymi przypadkami SIDS (zespół nagłej śmierci niemowląt). Badacze napisali, że „Przed wprowadzeniem szczepionki sześciowartościowej (w latach 1994-2000) obserwowaliśmy przypadek tylko jednego na 198 dzieci z nagłą śmiercią łóżeczkową, które zmarło wkrótce po szczepieniu DTP. Ale w latach 2001-2004 zidentyfikowali pięć podobnych przypadków z 74 z SIDS. Oznaczałoby to trzynastokrotny wzrost”.
Również w 2006 roku w Archiwum Virchowa(H), zespół z Instytutu Patologii Uniwersytetu w Mediolanie napisał: „Eksperci z Europejskiej Agencji ds. Oceny Produktów Medycznych przeanalizowali możliwość istnienia związku między sześciowartościowymi szczepionkami a niektórymi przypadkami śmierci. Wśród uczestników byli patolodzy z doświadczeniem w szczepionkach i zespołach nagłej śmierci niemowląt, którzy prowadzili sekcje zwłok, ale, o ile nam wiadomo, niewiele uwagi poświęcono badaniu pnia mózgu i serca krwi na skrawkach seryjnych i nie było możliwości ustalenia roli wyzwalającej szczepionki na te zgony. W pracy przedstawiono przypadek 3-miesięcznej dziewczynki, która zmarła nagle po szczepieniu szczepionką sześciowartościową. Badanie pnia mózgu na seryjnych skrawkach wykazało obustronną hipoplazję jąder łukowatych. Układ przewodzący serca miał uporczywe rozproszenie i zwyrodnienie płodu. Ten przypadek oferuje wyjątkowe zrozumienie możliwej roli szczepionki sześciowartościowej w wywoływaniu śmiertelnych konsekwencji u wrażliwego dziecka. Każdy przypadek nagłej i nieoczekiwanej śmierci, który ma miejsce wkrótce po urodzeniu lub we wczesnym dzieciństwie, zwłaszcza po szczepieniu, powinien zawsze zostać poddany pełnej sekcji zwłok, zgodnie z wytycznymi.
Referencje
- Blaylock R, „Szczepienia: ukryte niebezpieczeństwa”, The Blaylock Wellness Report, maj 2004, s. 1-9
- Ottaviani G. i wsp., „Zespół nagłej śmierci łóżeczkowej (SIDS) wkrótce po szczepieniu sześciowartościowym: inna patologia w podejrzeniu SIDS?”, Virchowa Archiwum, 2006, 448, s. 100-104.
- Zinka B. i in., „Niewyjaśnione przypadki nagłej śmierci niemowląt wkrótce po szczepieniu sześciowartościowym”, Vaccine, lipiec 2006, 24 (31-32), s. 5779-5780.
- Miller NZ i in.1. , "Wskaźniki śmiertelności niemowląt regresowały w stosunku do liczby rutynowo podawanych dawek szczepionki: czy istnieje toksyczność biochemiczna lub synergistyczna?”, Hum. Exp. Toxicol., maj 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Kwestia aluminium (kliknij, aby otworzyć)
Aluminium w szczepionkach: co rodzice powinni wiedzieć

1. Co to jest aluminium?
Aluminium to srebrzystobiały lekki metal, plastyczny i odporny. Te cechy sprawiają, że jest on przydatny w wielu branżach i produktach, m.in. maszynowej, budowlanej, magazynowej, kuchennej, przyborów kuchennych, tekstyliów, barwników i kosmetyków. Aluminium jest również metalem najobficiej występującym w skorupie ziemskiej, a praktycznie cały glin ze środowiska znajduje się w glebie. Jednak glin nie występuje naturalnie w znacznych ilościach w organizmach żywych (takich jak rośliny i zwierzęta) i nie ma żadnej znanej funkcji biologicznej. W ciągu ostatniego stulecia stosowanie aluminium w niektórych produktach doprowadziło do zwiększonego narażenia ludzi. Głównymi źródłami narażenia są żywność zawierająca glin (np. proszek do pieczenia, żywność przetworzona, odżywki dla niemowląt itp.), produkty medyczne (np. antyperspiranty, środki zobojętniające kwasy itp.), zastrzyki przeciwalergiczne i szczepionki .1-3
2. Dlaczego aluminium jest obecne w szczepionkach?
Niektóre szczepionki wykorzystują związki glinu (wodorotlenek glinu i fosforan glinu) jako adiuwanty, które są składnikami, które zwiększają odpowiedź immunologiczną na antygen (substancję obcą).4-5 Amerykańska Agencja ds. Żywności i Leków (FDA) twierdzi, że gdyby niektóre szczepionki nie zawierały aluminium, wywołana przez nie odpowiedź immunologiczna mogłaby się zmniejszyć.6
3. Jakie szczepionki zawierają aluminium?
Następujące szczepionki zawierają glin i są podawane niemowlętom, dzieciom i młodzieży (ryc. 1):
- Wirusowe zapalenie wątroby typu B (HepB)
- sześciowartościowego
- Błonica, tężec i krztusiec (DTaP i Tdap)
- Haemophilus influenzae typu b (PedvaxHIB)
- Pneumokoki (PCV)
- Wirusowe zapalenie wątroby typu A (HepA)
- Wirus brodawczaka ludzkiego (HPV)
- Meningokoki B (MenB)
Rycina 1: Od urodzenia do 18 roku życia podaje się do 22 dawek szczepionek zawierających glin7-8
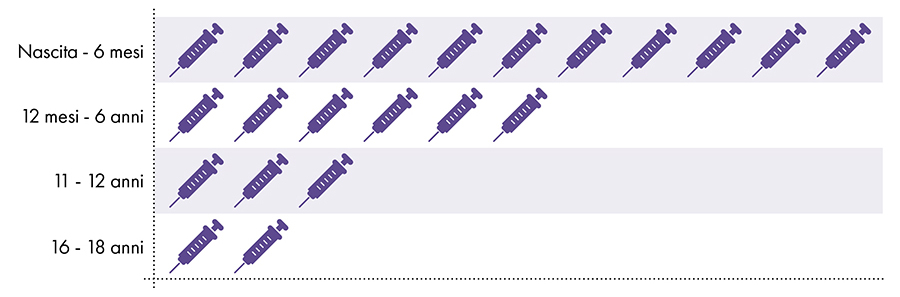
4. Czy narażenie na aluminium jest bezpieczne?
FDA uważa aluminium powszechnie uznawane za bezpieczne (GRAS) od 1975 roku.9 Jednak przed 1990 r. nie było technologii umożliwiającej dokładne wykrywanie niewielkich ilości glinu podawanego badanym w badaniach naukowych.10 W konsekwencji nie była znana ilość glinu, która mogłaby zostać wchłonięta przed wystąpieniem działań niepożądanych.
Od lat 1990. XX wieku, dzięki postępowi technologicznemu, zaobserwowano, że niewielkie ilości aluminium pozostające w organizmie człowieka zakłócają szereg procesów komórkowych i metabolicznych w układzie nerwowym oraz tkankach innych części ciała.1-10-11 Największe negatywne skutki aluminium zaobserwowano w układzie nerwowym i obejmują zarówno upośledzenie zdolności motorycznych, jak i encefalopatię (zmiany stanu psychicznego, zmiany osobowości, trudności w myśleniu, utrata pamięci, drgawki, śpiączka i inne).2-12
Departament Zdrowia i Opieki Społecznej Stanów Zjednoczonych (HHS) uznaje aluminium za znaną neurotoksynę.2 Ponadto FDA ostrzega przed ryzykiem toksyczności aluminium u niemowląt i dzieci.13
REJESTR FEDERALNY: Codzienna gazeta rządu Stanów Zjednoczonych„Nawet urodzone w terminie niemowlęta z prawidłową czynnością nerek mogą być zagrożone z powodu szybkiego wzrostu i niedojrzałości mózgu i szkieletu, a także niedojrzałości bariery krew-mózg. Do 1 lub 2 roku życia niemowlęta mają niższą współczynnik filtracji kłębuszkowej niż u dorosłych, co wpływa na czynność nerek. Agencja obawia się, że małe dzieci i osoby z niedojrzałą czynnością nerek są bardziej narażone na ekspozycję na glin. |
5. Ile doustnego aluminium nie jest bezpieczne?
W 2008 roku Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR), oddział HHS, wykorzystała badania nad neurotoksycznym działaniem glinu w celu ustalenia, że nie więcej niż 1 miligram (1.000 mikrogramów) glinu na kilogram masy ciała dziennie do unikaj negatywnych skutków aluminium.2
6. Ile wtryskiwanego aluminium nie jest bezpieczne?
Aby określić ilość glinu, którą można bezpiecznie wstrzyknąć, konieczne jest przeliczenie doustnego limitu glinu ATSDR. Limit ATSDR dla glinu podawanego doustnie (1.000 mikrogramów glinu na kilogram masy ciała na dzień) opiera się na 0,1% glinu podawanego doustnie, który jest wchłaniany do krwiobiegu, ponieważ przewód pokarmowy blokuje prawie całość glinu podawanego doustnie.2 W przeciwieństwie do tego, glin wstrzykiwany domięśniowo omija przewód pokarmowy i 100% glinu może z czasem zostać wchłonięte do krwiobiegu (tj. proporcja wchłoniętego glinu jest 1.000 razy większa). Aby uwzględnić te różne ilości wchłaniania, doustny limit glinu ATSDR należy podzielić przez 1000. Ta konwersja prowadzi do limitu glinu we krwi pochodzącego z ATSDR wynoszącego 1 mikrogram glinu (0,1% z 1.000 mikrogramów) na kilogram masy ciała na dzień. W związku z tym, aby uniknąć neurotoksycznego działania glinu, nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien dostawać się do krwiobiegu dziennie. Rycina 3 przedstawia limit glinu we krwi pochodzący z ATSDR dla niemowląt w różnym wieku w oparciu o ich wagę.
7. Ile glinu jest w szczepionkach?
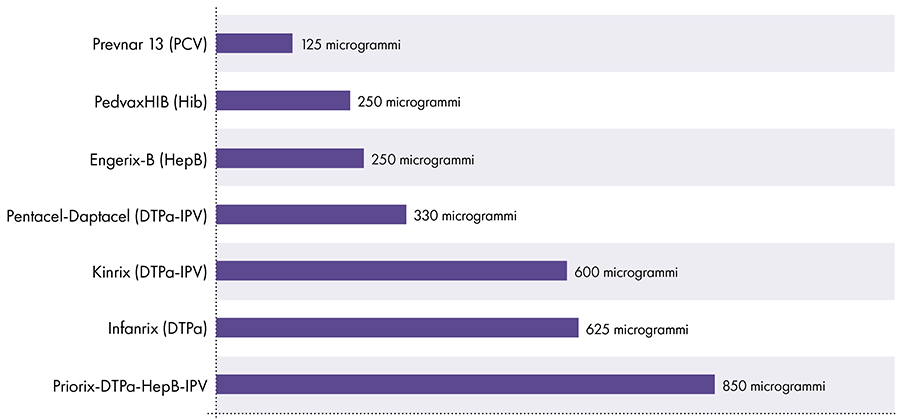
Ilość glinu w szczepionkach jest różna.16 W 1968 r. rząd federalny USA ustanowił limit ilości glinu w szczepionkach na 850 mikrogramów na dawkę, w oparciu o ilość glinu potrzebną do uczynienia niektórych szczepionek skutecznymi.6-17 W konsekwencji ilość glinu w zawierających glin szczepionkach dla niemowląt waha się od 125 do 850 mikrogramów na dawkę. Rysunek 4 przedstawia zawartość glinu w jednej dawce różnych szczepionek podawanych dzieciom.
8. Czy w jakichś badaniach porównywano ilość glinu w szczepionkach z limitem ustalonym przez Agencję ds. Rejestru Substancji Toksycznych i Chorób (ATSDR)?
W 2011 roku opublikowano badanie, którego celem było porównanie ilości glinu w szczepionkach z limitem przepływu krwi określonym przez ATSDR.18 Jednak to badanie błędnie oparło swoje obliczenia na 0,78% glinu doustnego wchłoniętego do krwiobiegu, a nie na wartości 0,1% stosowanej przez ATSDR w swoich obliczeniach.19-20 W rezultacie w badaniu z 2011 r. postawiono hipotezę, że prawie 8 razy (0,78% / 0,1%) aluminium może bezpiecznie dostać się do krwioobiegu, co doprowadziło do błędnego wniosku.
9. Czy ekspozycja na aluminium ze szczepionek jest bezpieczna?
Szczepionki są wstrzykiwane domięśniowo, a szybkość migracji glinu ze szczepionek z ludzkich mięśni do krwiobiegu jest nieznana. Badania na zwierzętach sugerują, że aluminium ze szczepionek może dostać się do krwiobiegu od kilku miesięcy do ponad roku, ze względu na wiele zmiennych.21-23 Ponieważ skumulowana ekspozycja na glin ze szczepionek u dzieci poniżej pierwszego roku życia przekracza dzienny limit ustalony przez ATSDR o kilkaset (ryc. 3 i 4), limit ten nadal byłby przekroczony, gdyby glin ze szczepionek dostał się do krwiobiegu w trakcie około roku. Ponadto badania wykazały, że glin ze szczepionek jest wchłaniany przez komórki odpornościowe i dociera do części ciała znajdujących się daleko od miejsca wstrzyknięcia, w tym do mózgu.24
Zakres działań niepożądanych glinu w szczepionkach nie jest znany, ponieważ nie przeprowadzono badań bezpieczeństwa porównujących populację zaszczepioną szczepionkami zawierającymi glin z populacją nieszczepioną takimi szczepionkami.
Ograniczenie przepływu krwi przez glin pochodzące z ATSDR2-14-15
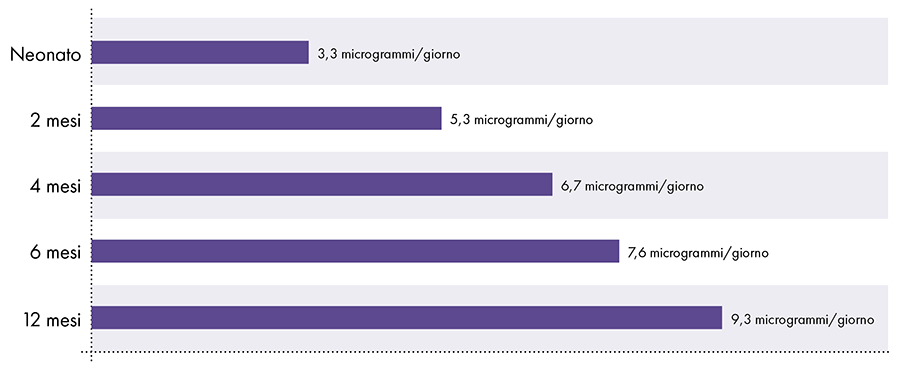 Rysunek 3: Ten wykres przedstawia limit glinu dla dzieci w różnym wieku, zgodnie z rejestrem substancji toksycznych i chorób, oddziału Departamentu Zdrowia i Opieki Społecznej Stanów Zjednoczonych. Limit wskazuje, że nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien codziennie dostawać się do krwiobiegu, aby uniknąć neurotoksycznego działania glinu.
Rysunek 3: Ten wykres przedstawia limit glinu dla dzieci w różnym wieku, zgodnie z rejestrem substancji toksycznych i chorób, oddziału Departamentu Zdrowia i Opieki Społecznej Stanów Zjednoczonych. Limit wskazuje, że nie więcej niż 1 mikrogram glinu na kilogram masy ciała powinien codziennie dostawać się do krwiobiegu, aby uniknąć neurotoksycznego działania glinu.
Ilość glinu w szczepionkach
Referencje
- Amerykańska Akademia Pediatrii, Komitet ds. Żywienia. Toksyczność glinu u niemowląt i dzieci. Pediatria. 1996 marzec; 97 (3): 413.
- Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR). Profil toksykologiczny dla aluminium. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA; 2008.3, 13-24, 145, 171-7, 208.
- Jokel RA. Aluminium w żywności — charakter i udział dodatków do żywności. W: El-Samragy Y, redaktor. Dodatek do żywności. Rijeka (Chorwacja): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. W kierunku zrozumienia działania adiuwantowego aluminium. Nat Rev Immunol. 2009 kwiecień; 9 (4): 287.
- Volk VK, Bunney WE. Uodpornienie na błonicę toksoidem płynnym i toksoidem strącanym ałunem. Am J Zdrowie publiczne Zdrowie Narodów. 1942 VII; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Sole glinu w szczepionkach — perspektywa USA. Szczepionka. 2002 31 maja; 20 dodatek 3: S18-22.
- Amerykańska Agencja ds. Żywności i Leków. Silver Spring (MD): Amerykańska Agencja ds. Żywności i Leków. Szczepionki licencjonowane do użytku w Stanach Zjednoczonych; [aktualizacja 2018 lutego 14; cytowany 2018 lutego 27 r.]. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. Zalecany harmonogram szczepień dla dzieci i młodzieży w wieku 18 lat lub młodszych, Stany Zjednoczone, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Amerykańska Agencja ds. Żywności i Leków. Silver Spring (MD): Amerykańska Agencja ds. Żywności i Leków. SCOGS (Komitet Specjalny ds. Substancji GRAS); [cytowano 2018]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Ks. ND. Zachowanie biologiczne i biodostępność glinu u człowieka, ze szczególnym uwzględnieniem badań z wykorzystaniem glinu-26 jako znacznika: przegląd i aktualizacja badania. J Monitorowanie środowiska. 2004; 6: 376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Glin w pediatrycznych produktach do żywienia pozajelitowego: zawartość zmierzona w porównaniu z zawartością oznaczoną. J Pediatr Pharmacol Ther. 2011; 16 (2): 92-7.
- Sedman A. Toksyczność glinu w dzieciństwie. Pediatr Nefrol. 1992 lipiec; 6 (4): 383-93.
- Amerykańska Agencja ds. Żywności i Leków, Departament Zdrowia i Opieki Społecznej. Zasady i przepisy. Rejestr Fed. 2003 czerwiec; 68 (100): 34286.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. National Center for Health Statistics: Tabela danych dla wykresów długości i wieku chłopców w zależności od wieku; [cyt. 2019 kwietnia 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centra Kontroli i Zapobiegania Chorobom. Waszyngton, DC: Departament Zdrowia i Opieki Społecznej USA. National Center for Health Statistics: Tabela danych dla wykresów długości i wagi dziewcząt w zależności od wieku; [cyt. 2019 kwietnia 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Amerykańska Agencja ds. Żywności i Leków, Departament Zdrowia i Opieki Społecznej. Rewizja wymagań dotyczących materiałów składowych. Ostateczna zasada. Rejestr Fed. 2011 kwietnia 13; 76 (71): 20513-8.
- Biuro Rejestru Federalnego, Krajowa Służba Archiwów i Rejestrów, Administracja Usług Ogólnych. Zasady i przepisy. Rejestr Fed. 1968 styczeń; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Zaktualizowana farmakokinetyka glinu po narażeniu niemowląt poprzez dietę i szczepienia. Szczepionka. 2011 listopada 28; 29 (51): 9538-43.
- Miller S, lekarze za świadomą zgodę. Errata w „Zaktualizowanej farmakokinetyce glinu w następstwie narażenia niemowląt poprzez dietę i szczepienia”. W: Brama Badań. Berlin (Niemcy): ResearchGate GmbH; 2020 marca 6 [cytowano 2020 marca 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Lekarze za świadomą zgodę. Newport Beach (Kalifornia): Lekarze za świadomą zgodę. Errata w „Zaktualizowanej farmakokinetyce glinu w następstwie narażenia niemowląt poprzez dietę i szczepienia”; [cytowano 2020 marca 6 r.]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, Biały JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. Absorpcja in vivo adiuwantów szczepionkowych zawierających glin przy użyciu 26A1997. Szczepionka 15 sierpień-wrzesień; 12 (13-1314): 8-XNUMX.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Oznaczenie aluminium i ocena reakcji miejscowej w kilku punktach czasowych po domięśniowym podaniu szczepionek zawierających aluminium u małpy Cynomolgus. Szczepionka. 2005 lutego 3; 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanisławski B. Aluminium w osoczu i tkankach po wstrzyknięciu domięśniowym adiuwantów ludzkich szczepionek u szczurów. Arch toksykol. 2019 październik; 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Analiza krytyczna badań referencyjnych dotyczących toksykokinetyki adiuwantów na bazie glinu. J Inorg Biochem. 2018 kwiecień 181: 87-95.
Artykuł przetłumaczony przez Lekarze dla świadomej zgody
W wielu opublikowanych badaniach opisano poważne działania niepożądane po szczepieniu toksoidem tężcowym. Zdarzenia niepożądane obejmują anafilaksję,(1-2) zapalenie nerwu ramiennego,(3) pemfigoid pęcherzowy(4-5-6) zespół Guillain-Barre (GBS),(7-8) ostre rozsiane zapalenie mózgu i rdzenia (ADEM),(9) rumień wielopostaciowy,(10-11-12) zapalenie mięśnia sercowego,(13-14-15-16-17) artretyzm,(18-19) zapalenie nerwu wzrokowego,(20-21) i inne choroby autoimmunologiczne.(22-23)
Działania niepożądane zgłaszane po szczepieniu przeciw tężcowi zostały zebrane przez niemieckiego autora(24) oraz przez System Monitorowania Zdarzeń Niepożądanych Po Szczepieniu(25) i można je podzielić na dwie grupy: miejscowe działania niepożądane i ogólnoustrojowe działania niepożądane.
Można powiedzieć, że efekty te zależą od różnych czynników:
- wiek biorcy szczepionki;
- warunki fizjologiczne i patologiczne biorcy szczepionki;
- liczba przyjętych dawek szczepionki;
- ilość podanej toksyny tężcowej;
- obecność innych antygenów bakteryjnych i/lub wirusowych związanych z toksyną tężcową;
- obecność adiuwantów lub innych powiązanych substancji toksycznych.
Uważa się, że działania niepożądane wywołane pierwszym podaniem szczepionki przeciw tężcowi nakładają się na te, które mogą wystąpić po dawkach przypominających, a przy zbyt częstym podawaniu tworzą stan hiperimmunizacji, który znacznie zwiększa ryzyko uszkodzenia szczepionki iz tego powodu wiele badań naukowcy zalecają, aby nie podawać dawek przypominających tej szczepionki w odstępach krótszych niż 10 lat.(26) Do tego dochodzi fakt, że anatoksyna tężca pediatrycznego zawarta w szczepionkach skojarzonych jest większa niż ta stosowana u dorosłych, ponieważ z powodu niedojrzałości układu odpornościowego konieczna jest nadmierna stymulacja noworodka w celu uzyskania odpowiedniej odpowiedzi przeciwciał.
Najczęstsze, zwykle łagodniejsze i przejściowe miejscowe skutki uboczne szczepienia przeciw tężcowi(32) są one spowodowane szczególną nadwrażliwością na toksynę tężca i objawiają się bólem (50-85% przypadków), zaczerwienieniem, stwardnieniem i obrzękiem (25-30% przypadków) aż do ropnia.(27) W niektórych przypadkach miejscowe reakcje były szczególnie poważne, takie jak zespół Lyella (lub zespół oparzonej skóry), który charakteryzuje się śmiertelnością 50% u dorosłych i 25% u dzieci.(28)
Wszystkie miejscowe działania niepożądane występują częściej, jeśli szczepionka jest podawana podskórnie, a nie domięśniowo. Efekty te nasilają się wraz ze wzrostem ilości zaszczepionej toksyny tężcowej(29) a dzieje się tak zwłaszcza u osób, które otrzymały kilka i częstych zastrzyków szczepionki przeciw tężcowi.(30-27)
Badanie z 2017 roku wykazało, że wśród dzieci z rozległymi obrzękami kończyn po otrzymaniu czwartej dawki bezkomórkowej szczepionki przeciw błonicy, tężcowi i krztuścowi nawrót odczynu miejscowego był szczególnie częsty po podaniu piątej dawki szczepionki (78% zaszczepionych).(31)
Skutki uboczne zwiększają się również, jeśli szczepionka przeciw tężcowi jest łączona z innymi szczepionkami, a nie stosowana samodzielnie.(32)
W 1994 roku Instytut Medycyny Stanów Zjednoczonych (IOM) poinformował, że istnieją przekonujące dowody naukowe, które pozwalają stwierdzić, że szczepionki przeciw tężcowi, DT i Td mogą powodować zespół Guillain-Barre (GBS), w tym śmierć, zapalenie nerwu ramiennego i zgon z powodu anafilaksji (wstrząsu). ).(33) IOM uznała również, że istnieje indywidualna podatność na reakcje poszczepienne z powodów genetycznych, biologicznych i środowiskowych, ale dostawcy szczepionek nie mogą dokładnie przewidzieć, kto dozna powikłań, obrażeń lub śmierci przed podaniem szczepionki w wyniku szczepienia.(34)
W 2017 r. naukowcy z Gwinei Bissau porównali wskaźniki śmiertelności niemowląt zaszczepionych przeciwko błonicy, tężcowi i krztuścowi pełnokomórkowemu (DTP) w wieku od 3 do 5 miesięcy ze śmiertelnością niemowląt, które nie zostały jeszcze zaszczepione szczepionką DTP. śmiertelność była znacznie wyższa wśród niemowląt zaszczepionych DTP niż wśród tych, które jeszcze nie były szczepione. Naukowcy zauważyli również, że jeśli doustna szczepionka przeciwko polio (OPV) została podana w tym samym czasie co szczepionka DTP, śmiertelność z jakiejkolwiek przyczyny spadła, ale nadal pozostawała znacznie wyższa niż u dzieci nieszczepionych.(35)
Ważnym miejscowym działaniem niepożądanym, które można zaobserwować ze względną częstością u dorosłych, jest neuropatia splotu ramiennego,(36) jeśli inokulacja jest wykonywana w ramieniu i pojawia się kilka dni lub tygodni po szczepieniu(37). Ta neuropatia charakteryzuje się bólem mięśni, osłabieniem i zanikiem mięśni. Oprócz neuropatii zlokalizowanych w obszarze, w którym zaszczepiono szczepionkę, w literaturze znajdujemy również różne inne doniesienia o zlokalizowanych neuropatiach spowodowanych podaniem leków przeciwtężcowych,(38-39) takie jak zajęcie różnych nerwów czaszkowych(40-41) lub nerwy oka(42) lub nerw krtaniowy wsteczny.(43)
Najczęstsze ogólnoustrojowe skutki szczepienia przeciw tężcowi(32) Można podzielić na:
- niespecyficzne objawy, takie jak gorączka, ból głowy (który jest dość częstym działaniem niepożądanym po szczepieniu), bóle mięśni, pokrzywka, nudności, wymioty,(44) astenia, jadłowstręt, drażliwość, senność,
- specyficzne skutki, takie jak wstrząs anafilaktyczny, uogólnione neuropatie, silne bóle brzucha z biegunką, różne formy zapalne, nawet ciężkie, aw rzadkich przypadkach nawet śmierć.
Wśród wszystkich najczęstszych i licznych skutków ogólnoustrojowych znajdują się uszkodzenia neurologiczne(45) a wśród nich na pewno na pierwszym miejscu należy umieścić polineuropatię dotyczącą obwodowego układu nerwowego, która występuje częściej niż zajęcie ośrodkowego układu nerwowego i może pojawić się zarówno po pierwszej dawce szczepionki, jak i po trzeciej.(46) Polineuropatia zwykle występuje w ciągu kilku minut do kilku godzin (w przypadku ostrych reakcji alergicznych) lub w ciągu 12-48 godzin (w przypadku opóźnionych reakcji alergicznych) lub co najwyżej w ciągu 4-14 dni od zaszczepienia (w przypadku zapalenie nerwu).(47) Polineuropatia może dotyczyć kilku nerwów lub dużych obszarów ciała, aż do rdzenia i kory mózgowej i może być spowodowana wyłącznie szczepionką przeciw tężcowi(48) lub z podania innych szczepionek połączonych ze szczepionką przeciw tężcowi.(36-49)
Wśród różnych postaci polineuropatii opisano następujące: polineuropatię demielinizacyjną;(50) asymetryczna polineuropatia; zapalenie wielokorzeniowe z niedowładem pęcherza moczowego i odbytnicy;(51) wysypka bliznowata,(40) ostre reakcje pokrzywkowe,(44) porażenie nerwów oddechowych (porażenie Landry'ego), które również może prowadzić do śmierci;(52-53) skurcze tężcowe;(44) poprzeczne zapalenie rdzenia kręgowego;(54) sindrom di Guillain-Barré;(55-56) obwodowa afazja ruchowa;(57) i śmierć.(28)
Referencje (kliknij, aby otworzyć)
- Mayorga C, Torres MJ, Corzo JL i in. Natychmiastowa alergia na szczepionkę z anatoksyną tężcową: oznaczanie przeciwciał immunoglobulin E i immunoglobulin G na białka alergenne. Ann Allergy Astma Immunol. 2003 Feb;90(2):238-43.
- Martín-Muñoz MF, Pereira MJ, Posadas S i in. Reakcja anafilaktyczna na szczepionkę przeciw błonicy i tężcowi u dziecka: oznaczenia swoistych IgE/IgG i badania reaktywności krzyżowej. Szczepionka. 2002 Sep 10;20(27-28):3409-12.
- Hamati-Haddad A, Fenichel GM. Zapalenie nerwu ramiennego po rutynowej szczepieniu dzieci przeciwko błonicy, tężcowi i krztuścowi (DTP): opis dwóch przypadków i przegląd literatury. Pediatria. 1997 Apr;99(4):602-3.
- Fournier B, Descamps V, Bouscarat F i in. Pemfigoid pęcherzowy wywołany szczepieniem. Br J. Dermatol. 1996 Jul;135(1):153-4.
- Venning VA, Wojnarowska F. Indukowany gwałtowny pemfigoid. Br J. Dermatol. 1995 May;132(5):831-2.
- Sezin T, Egozi E, Hillou W i in. Pemfigoid błony śluzowej przeciw lamininie-332 rozwijający się po szczepieniu przeciw błonicy tężcowi. JAMA Dermatol. 2013 Jul;149(7):858-62.
- Bakshi R., Graves MC. Zespół Guillaina-Barrégo po skojarzonym szczepieniu przeciw tężcowi i toksoidowi błoniczemu. J. Neurol Sci. 1997 Apr 15;147(2):201-2.
- Newton N Jr, Janati A. Zespół Guillain-Barré po szczepieniu oczyszczonym toksoidem tężcowym. Południe Med J. 1987 Aug;80(8):1053-4.
- Hamidon BB, Raymond AA. Ostre rozsiane zapalenie mózgu i rdzenia (ADEM) objawiające się drgawkami wtórnymi do szczepienia toksyną przeciwtężcową. Med J Malezja. 2003 Dec;58(5):780-2.
- Griffith RD, Miller III Rumień wielopostaciowy po szczepieniu przeciw błonicy i toksoidowi tężcowi. J Am Acad Dermatol. 1988 Oct;19(4):758-9.
- Frederiksen MS, Brenøe E, Trier J. Rumień wielopostaciowy mniejszy po szczepieniu szczepionkami pediatrycznymi. Scand J Zainfekować Dis. 2004;36(2):154-5.
- Kaur S., Handa S. Rumień wielopostaciowy po szczepieniu u niemowlęcia. Indyjski J Dermatol Venereol Leprol. 2008 May-Jun;74(3):251-3.
- Kumar V, Sidhu N, Roy S, Gaurav K. Zapalenie mięśnia sercowego po szczepieniu przeciwko błonicy, krztuścowi pełnokomórkowemu i toksoidowi tężcowemu u małego niemowlęcia. Ann Pediatr Cardiol. 2018 May-Aug;11(2):224-226
- Yamamoto H, Hashimoto T, Ohta-Ogo K i in. Przypadek potwierdzonego biopsją eozynofilowego zapalenia mięśnia sercowego związanego ze szczepieniem toksoidem tężcowym. Patol sercowo-naczyniowy. 2018 listopad - grudzień;37:54-57
- Wu SJ, Sun S, Li JY i in. Ostre piorunujące zapalenie mięśnia sercowego po szczepieniu przeciw błonicy, polio i tężcowi. Azjatycka Cardiovasc Thorac Ann. 2006 Dec;14(6):e111-2.
- Dilber E, Karagöz T, Aytemir K i in. Ostre zapalenie mięśnia sercowego związane ze szczepieniem przeciw tężcowi. Mayo Clin Proc. 2003 Nov;78(11):1431-3.
- Amsel SG, Hanukoglu A, Fried D, Wolyvovics M Zapalenie mięśnia sercowego po potrójnej immunizacji. Arch Dis dziecko. Kwi 1986; 61 (4): 403–405.
- Jawad AS, Scott DG Szczepienia wywołujące reumatoidalne zapalenie stawów? Ann Rheum Dis. luty 1989; 48(2):174.
- Kaul A, Adler M, Alokaily F, Jawad A Nawrót reaktywnego zapalenia stawów po dawce przypominającej toksoidu tężcowego Ann Rheum Dis. luty 2002; 61(2):185.
- O'Brien P, Wong RW Zapalenie nerwu wzrokowego po skojarzonym szczepieniu przeciw błonicy, tężcowi, krztuścowi i inaktywowanemu wirusowi polio: opis przypadku. J Med Case Rep. 2018 Nov 30;12(1):356
- Cabrera-Maqueda JM, Hernández-Clares R, Baidez-Guerrero AE i in. Zapalenie nerwu wzrokowego w ciąży po szczepieniu Tdap: opis dwóch przypadków. Clin Neurol Neurochirurg. 2017 wrzesień;160:116-118.
- Ruhrman-Shahar N, Torres-Ruiz J, Rotman-Pikielny P, Levy Y. Reakcja autoimmunologiczna po szczepieniu przeciwtężcowym – opis czterech przypadków i przegląd piśmiennictwa. Immunol Res. 2017 Feb;65(1):157-163.
- Shoenfeld Y., Aron-Maor A. Szczepienia i autoimmunizacja - „szczepionka”: niebezpieczny związek? J Autoimmunologiczny. 2000 Feb;14(1):1-10.
- Roczne skutki uboczne leków. Tom 12. (Elsevier, 988).
- Roczne skutki uboczne leków. Tom 13. (Elsevier, 1989).
- Adebahr, G. [Śmierć przez wstrząs w pierwszym zapobiegawczym podskórnym wstrzyknięciu surowicy tężcowej]. Dtsch. Z. Gesamte Gerichtl. Med. 41, 405-8 (1952).
- Skutki uboczne leków roczne. Tom 11. (Elsevier, 1987).
- Frank, K.-H. Todliche Imptkomplikationen (zespół Lyella) nach Tetatoxoid. Dt. Gesundh.wes. 29, 1430-4 (1974).
- Relihan, M. Reakcje na anatoksynę tężcową. dr med. J. Jr. 62, 430-4 (1969).
- Levine, L., Ipsen, J. & McComb, J. Szczepienia dorosłych. Przygotowanie i ocena połączonych płynnych toksoidów tężca i błonicy do stosowania u dorosłych. Am. J. Hyg. 73, 20 (1961).
- Zafack, JG i in. Ryzyko nawrotu działań niepożądanych po szczepieniu: przegląd systematyczny. Pediatria 140, (2017).
- Cody, CL, Baraff, LJ, Cherry, JD, Marcy, SM i Manclark, CR Charakter i wskaźniki działań niepożądanych związanych ze szczepieniami DTP i DT u niemowląt i dzieci. Pediatrics 68, 650-60 (1981).
- Komitet Instytutu Medycyny do przeglądu działań niepożądanych szczepionek. Niekorzystne skutki szczepionek: dowody i przyczynowość. (Ocena mechanizmów biologicznych zdarzeń niepożądanych: zwiększona podatność). Waszyngton.: National Academies Press. 1994. Rozdział 5 Toksoidy błonicze i tężcowe str. 67 - 117
- Komitet Instytutu Medycyny do przeglądu działań niepożądanych szczepionek. Niekorzystne skutki szczepionek: dowody i przyczynowość. (Ocena mechanizmów biologicznych zdarzeń niepożądanych: zwiększona podatność). Waszyngton.: National Academies Press. 2012
- Mogensen SW, Andersen A, Rodrigues A i in. Wprowadzenie szczepionki przeciw błonicy, tężcowi, krztuścowi i doustnej szczepionce przeciw polio wśród młodych niemowląt w miejskiej społeczności afrykańskiej: naturalny eksperyment. EBioMedycyna. 2017 Mar; 17: 192-198.
- Tsairis, P., Dyck, PJ & Mulder, DW Historia naturalna neuropatii splotu ramiennego. Zgłoś 99 pacjentów. Arch. Neuro/. 27, 09-17 (1972).
- Blumstein, GI & Kreithen, H. Neuropatia obwodowa po podaniu toksoidu tężcowego. JAMA 198, I 030-1 (1966)
- Gersbach, P. & Waridel, D. [Paraliż po zapobieganiu tężcowi]. Szwajcaria. Med Wochenschr. 106, 150-3 (1976).
- Baust, W., Meyer, D. i Wachsmuth, W. Neuropatia obwodowa po podaniu anatoksyny tężcowej. J. Neuro/. 222, 131-33 (1979).
- Cutter, R. Zajęcie nerwu słuchowego po antytoksynie tężcowej: pierwszy zgłoszony przypadek. J Am Med Ass 106, I006-7 (I 936).
- Wirth, G. Reversibele kochlearisschadigung nach zastrzyk tężcowy. Munch Med Wschr 101, 349-81 (1965).
- Harrer, G., Melnizky, V. & Wendt, H. Akkomodationsparese und Schlucklahmung nach Tetanus-Toxoid-Auffrlschungsimpfung. Wien Med Wochenschr 15, 296-7 (1971)
- Basek, M. Jednostronny! porażenie strun głosowych po podaniu antytoksyny tężcowej (TAT). Laryngoskop 68, 805-807 (1958).
- Cunningham, AA Anafilaksja po wstrzyknięciu toksoidu tężcowego. Br Med J. 2, 522-3 (1940).
- Jeźdźca. Plexuslahmung nach Schutzimpfung mit Tetanusserum. Chrupać. med. Wsch. 81, 1035 (1934).
- Holliday, PL & Bauer, RB Poliradiculoneuritis wtórne do immunizacji anatoksyną tężca i błonicy. Arch Neuro/40, 56-57 (1983).
- Ehrengut, W. Reaktionen der Wundstarrrkrampfimpfung. Dtsch Med Wochenschr 95, 1799-1800 (1970).
- 1 Woolling, KR i Rushton, JG Zapalenie nerwu w surowicy; opis dwóch przypadków i krótki przegląd zespołu. Arch. Neuro/. Psychiatria 64, 568-73 (1950).
- Martin, GI & Weintraub, MI Zapalenie nerwu ramiennego i porażenie siódmego nerwu: rzadkie zagrożenie związane ze szczepieniem DPT. Clin. Pediatra. (fila). 12, 506-507 (1973).
- Pollard, JD & Selby, G. Nawracająca neuropatia spowodowana anatoksyną tężcową. Sprawozdanie ze sprawy. J. Neuro/. Sci 37, 113-125 (1978).
- Skutki uboczne leków rok/. Tom 09. (Elsevier, 1985).
- Harrfeldt, HP [Śmierć po czynnej i biernej immunizacji przeciw tężcowi]. Monatsschr. Unfallheilkd. Versicherungsmed. 66, 36-7 (1963).
- Elsasser, G. Zur Entstehung, Lokalizacja und Verhiitung der Serumpolyneuritis. Nervenarzt 15, 280 (1942).
- Whittle, E. & Robertson, NR Poprzeczne zapalenie rdzenia kręgowego po immunizacji błonicy, tężca i polio. Br Med J. 1, 1450 (1977).
- Skutki uboczne leków rok/. Tom 14. (Elsevier, 1990).
- Hopf, HC [zespół Guillain-Barré po podaniu toksoidu tężcowego. Ankieta i relacja z przypadku]. Aktualny Neuro/. 7, 195-200 (1980).
- Palfty, GF & Merei, T. Bez tytułu. Orw. Hetil. 102, 2321 (1961).
Ten artykuł został podsumowany i przetłumaczony przez Krajowe Centrum Informacji Vaccine.

