Infanrix hexa i nagła śmierć: przegląd aktualizacji okresowych raportów bezpieczeństwa przedkładanych Europejskiej Agencji Leków

Przedmiotowa szczepionka „Infanrix hexa”, która łączy szczepionki przeciw błonicy, tężcowi, krztuścowi, wirusowemu zapaleniu wątroby typu B, polio i grypie typu B, jest wytwarzana przez GlaxoSmithKline (GSK) i została wprowadzona w Europie w październiku 2000 r.
Puliyel i Sathyamala odkryli to ukrywanie, analizując dane w okresowych raportach o bezpieczeństwie (PSUR) związanych ze szczepionką, które jego producent GSK musi regularnie przekazywać Europejskiej Agencji Leków (EMA).
Te poufne raporty bezpieczeństwa dotyczące tej szczepionki zostały otrzymane przez Puliyela od włoskiego badacza, który uzyskał je od EMA na mocy Ustawy o wolności informacji - włoskiej wersji prawa do informacji w Indiach.
Według analizy lekarze stwierdzili, że ostatni raport bezpieczeństwa szczepionki „Infanrix hexa” przedłożony przez GSK (2015) odwołał zgony wcześniej zgłoszone przez producenta w jego 16. raporcie (2012). Zauważają jednak, że w raporcie nie jest jasne, w jaki sposób te zgony zostały anulowane.
Autorzy Puliyel i Sathyamala zauważają, że dziesięć lat po opublikowaniu artykułu z Centrum Kontroli Chorób (CDC) badającego związek między MMR a autyzmem, jeden z autorów William Thompson przyznał, że on i jego współautorzy pominęli informacje. istotne statystycznie - tzn. że mężczyźni z Ameryki Południowej, którzy otrzymali szczepionkę MMR przed 36 miesiącem życia, byli narażeni na zwiększone ryzyko autyzmu. Po tym, jak Thompson i jego koledzy znaleźli dowody na to zwiększone ryzyko, usunęli dane od dzieci bez gruzińskich świadectw urodzenia (a zatem zdyskwalifikowali nieproporcjonalną liczbę czarnych dzieci) i przedstawili swoje dane, mówiąc, że nie ma zwiększone ryzyko autyzmu. Nie jest jasne, czy autorzy PSUR 19 dokonali podobnej retroaktywnej dyskwalifikacji dzieci udokumentowanych jako zmarłe w PSUR 16.
„Gdyby te zgony nie zostały usunięte, zgony po szczepieniu byłyby znacznie wyższe niż oczekiwane przez przypadek. Producent musiałby przyznać EMA, że ich szczepionka była przyczyną tych nadmiernych zgonów”.
Puliyel i Sathyamala twierdzą, że producent „musi wyjaśnić pozornie błędne dane, które przedłożył organom regulacyjnym.
Do tej pory producent twierdził, że zgony zgłoszone po szczepionce są „zbieżne” i że miałyby miejsce u tych dzieci, nawet gdyby nie otrzymały szczepień.
Jednak w komentarzu do czasopisma Puliyel i Sathyamala wskazują, że ich analiza wykazała, że 83% zgłoszonych zgonów nastąpiło natychmiast po szczepieniu w ciągu pierwszych 10 dni, a tylko 17% nastąpiło w ciągu następnych dziesięciu dni.
„Gdyby to były przypadkowe zgony, nie wszystkie zgrupowałyby się natychmiast po szczepieniu, ale byłyby równomiernie rozmieszczone w ciągu 20 dni”.
Puliyel i Sathyamala piszą, że jakikolwiek argument twierdzący, że nagłe zgony po szczepieniu są równoważone przez życie uratowane przez szczepionkę, jest nie do przyjęcia, tak samo, jak byłoby uważane za nielegalne zabicie osoby w celu wykorzystania jej narządów do uratowania pięciu innych osób. .
„Ukrywanie zgonów po szczepieniu może uniemożliwić lub opóźnić ocenę profilu bezpieczeństwa szczepionki, a to może prowadzić do niepotrzebnych i uzasadnionych etycznie zgonów.
Autorzy podkreślają, że Hexavac - podobna szczepionka wyprodukowana przez Sanofi Pasteur, a także wprowadzona na rynek w 2000 r., Została wycofana z rynku europejskiego w 2005 r. Stwierdzono, że śmierć dzieci wzrosła w ciągu dwóch dni po szczepieniu.
W kontekście indyjskim autorzy zwracają uwagę, że Generalny Kontroler Narkotyków (DCGI) powinien ponownie rozważyć obecną politykę automatycznej akceptacji wszystkich leków dopuszczonych w Stanach Zjednoczonych i Europie. „Ta zależność oparta na należytej staranności EMA może być błędna i należy ją zweryfikować”.
„Pentavac”, produkowany przez Serum Institute of India i sprzedawany w Indiach, jest podobny do wycofanego obecnie produktu Hexavac i Infanrix Hexa, z tym wyjątkiem, że szczepionkę przeciw krztuścowi na całą komórkę zastąpiono szczepionką bezkomórkową szósty składnik, wstrzykiwana szczepionka przeciw polio. ”
W świetle informacji zwrotnych Puliyel i Sathyamala sugerują, że „konieczne jest, aby DCGI była świadoma raportów PSUR przekazanych EMA i obaw wyrażonych w tym komentarzu”.
Firma
Indian Journal of Medical Ethics Online po raz pierwszy opublikowany 5 września 2017 r
Infanrix hexa i nagła śmierć: przegląd aktualizacji okresowych raportów bezpieczeństwa przedkładanych Europejskiej Agencji Leków
JACOB PULIYEL, C. SATHYAMALA
Autorzy: Jacob Puliyel (autor korespondent -
Cytowanie: Puliyel J, Sathyamala C. Infanrix hexa i nagła śmierć: przegląd okresowych raportów o bezpieczeństwie przekazywanych do Europejskiej Agencji Leków. Indian J Med Ethics. Publikacja internetowa z 5 września 2017 r. Poprawiona 9 września 2017 r. *. DOI: 10.20529 / IJME.2017.079
Redaktor manuskryptu: Mala Ramanathan © Indian Journal of Medical Ethics 2017
Abstrakcyjny
Odnotowano kilka spontanicznych doniesień o nieoczekiwanej nagłej śmierci natychmiast po podaniu szczepionki Infanrix hexa (skojarzona szczepionka przeciw błonicy, tężcowi, bezkomórkowym krztuścowi, inaktywowane zapalenie polio, wirusowe zapalenie wątroby typu B i Haemophilus influenzae typu B). Producent, GlaxoSmithKline (GSK), przedkłada okresowe poufne raporty o bezpieczeństwie (PSUR) dotyczące Infanrix Hexa Europejskiej Agencji Leków (EMA). Ostatni to PSUR * 19. Każdy PSUR zawiera analizę zaobserwowanych / oczekiwanych nagłych zgonów, która pokazuje, że liczba zgonów zaobserwowanych natychmiast po immunizacji jest mniejsza niż oczekiwana przypadkowo.
Ten komentarz koncentruje się na tym aspekcie PSUR, który wpływa na decyzje polityczne. Przeanalizowaliśmy dane przedstawione w raporcie PSUR. Oczywiste jest, że zgony rozpoznane w PSUR 16 zostały wyeliminowane przez PSUR 19. Liczba zgonów zaobserwowanych bezpośrednio po szczepieniu u dzieci w wieku powyżej jednego roku była znacznie wyższa niż oczekiwano przypadkowo po usunięciu zgonów przywrócone i uwzględnione w analizie.
Producent musi wyjaśnić liczby, które zostały przedłożone organom regulacyjnym. Procedury podjęte przez EMA w celu oceny ostrzeżeń producenta w raporcie PSUR wymagają przeglądu. Generalny kontroler leków w Indiach prawie automatycznie przyjmuje leki i szczepionki zatwierdzone przez EMA. EMA musi zweryfikować zaufanie do staranności.
wprowadzenie
W dniu 23 października 2000 r. Wprowadzono do obrotu dwie szczepionki sześciowartościowe, Infanrix hexa® (GlaxoSmithKline plc-GSK) i Hexavac® (Sanofi Pasteur MSD, SNC), które łączą błonicę, tężec, bezkomórkowe krztusiec, zapalenie wątroby typu B, la inaktywowane zapalenie polio i grypa Haemophilus typu B zostało dopuszczone do obrotu w Unii Europejskiej. Po autoryzacji pojawiło się kilka spontanicznych doniesień o nieoczekiwanej nagłej śmierci natychmiast po podaniu tych sześciowartościowych szczepionek. W 2005 r. Von Kries i współpracownicy (1) przeprowadzili szczegółową analizę, w której porównali zgony zaobserwowane natychmiast po szczepieniu z oczekiwanymi ofiarami. Stwierdzili, że ustandaryzowany współczynnik umieralności (SMR) w ciągu dwóch dni po szczepieniu szczepionką Hexavac znacznie wzrósł u dzieci szczepionych w drugim roku życia.
Nie było tak w przypadku Infanrix Hexa. Na wniosek posiadacza pozwolenia na dopuszczenie do obrotu Hexavac został wycofany w 2005 r., A Infanrix Hexa nadal był sprzedawany w Europie (2). Zgodnie z prawem europejskim Europejska Agencja Leków (EMA) odpowiada za ochronę zdrowia publicznego poprzez ocenę leków zatwierdzonych przez nią jako organy regulacyjne. Producenci są odpowiedzialni za skuteczność, jakość i bezpieczeństwo swoich leków (3).
Włoski sąd sędziego Nicola Di Leo podał do publicznej wiadomości okresowe raporty o poufnych aktualizacjach bezpieczeństwa (PSUR) 15 i 16a od 2009 do 2011 r. GlaxoSmithKline (4). PSUR 19 (który obejmuje PSUR 17, 18 i 19, z dnia 15 stycznia 2015 r.) Został uzyskany przez włoskiego naukowca z EMA zgodnie z art. 3 zasad EMA (EMA 110196/2006 z 30 listopada 2010 r.) (5). ). Włoski lekarz wysłał ten raport PSUR do pierwszego autora (JP), prosząc go o napisanie raportu, który zostanie przedstawiony Parlamentowi Europejskiemu. Ten komentarz jest oparty na wszystkich tych raportach PSUR. W kontekście aspektu bezpieczeństwa poprzednio podkreślonego przez von Kriesa (1), ten komentarz analizuje nagłą śmierć po zastosowaniu szczepionki Infanrix Hexa. Inne aspekty objęte PSUR nie są badane.
PSUR 15 - grupowanie zmarłych po szczepieniu
Większość zgonów, które mają miejsce po okresie noworodkowym, jest spowodowana infekcjami, wadami wrodzonymi, nowotworami złośliwymi lub wypadkami. Dzieci rzadko umierają bez wyraźnej przyczyny, dlatego zgony są klasyfikowane jako (i) zespół nagłej śmierci (SIDS), zdefiniowany w PSUR jako śmierć, która ma miejsce w pierwszym roku życia i pozostaje niewyjaśniona po sekcji zwłok lub ) nieoczekiwana nagła śmierć (POŁUDNIE), zdefiniowana jako śmierć, która ma miejsce w ciągu pierwszych dwóch lat życia i która pozostaje niewyjaśniona po klinicznej i końcowej historii zdarzeń, ale bez sekcji zwłok. Razem te dwa są uważane za nagłą śmierć (SD) w PSUR 15. Pewną liczbę szczepionek podaje się dzieciom poniżej 2 lat w danym dniu, a liczba dzieci zaszczepionych na całym świecie jest bardzo duża. Możliwe jest, że niektóre zaszczepione dzieci przypadkowo umrą z powodu SIDS / POŁUDNIOWE, zdarzenia takie miałyby miejsce, nawet gdyby te dzieci nie zostały zaszczepione tego dnia. Aby ustalić, czy taka śmierć była spowodowana szczepieniem, czy była incydentem, wykonuje się obserwowaną / oczekiwaną analizę SD. Analiza ocenia, czy liczba zgonów zaobserwowanych po szczepieniu przekracza to, co można przewidzieć przypadkowo.
Nagłe zgony: obserwowane w kierunku oczekiwań
PSUR 15 wyjaśnia, w jaki sposób przeprowadzono tę analizę (4: p 782): „Towarzystwo oceniło, czy liczba nagłych zgonów zgłoszonych w tej grupie wiekowej przekraczająca liczbę jeden może wystąpić losowo. Od czasu rozkładu wieku u których osoby zaszczepione są nieznane, firma założyła, że odsetek zdarzeń niepożądanych według wieku jest reprezentatywny dla rzeczywistego rozkładu wieku w momencie szczepienia. Można zatem oszacować, że 90,6% wszystkich osób zaszczepionych szczepionką Infanrix Hexa były w pierwszym roku życia, a 9,4% w drugim, stąd liczbę dawek (od momentu wprowadzenia) oszacowano na odpowiednio 54.927.729 i 5,698,904. w głównym kraju, w którym rozprowadzane są dawki Infanrix Hexa (prawie 30% w samych Niemczech), przyjęto, że częstość nagłych zgonów obserwowana w Niemczech była reprezentatywna dla całej populacji biorców Infanrix Hexa (Federalne BiuroNiemiecki statystyka, Statistisches Bundesamt; zapadalność w pierwszym roku życia: 0,454 / 1000 żywych urodzeń; drugi rok: 0.062 / 1000 urodzeń żywych, dane z 2008 r.).
„PSUR dokumentuje zgłoszoną śmierć w ciągu 20 dni po szczepieniu. Obserwowana liczba ofiar śmiertelnych była niższa niż oczekiwano (tabela 1).
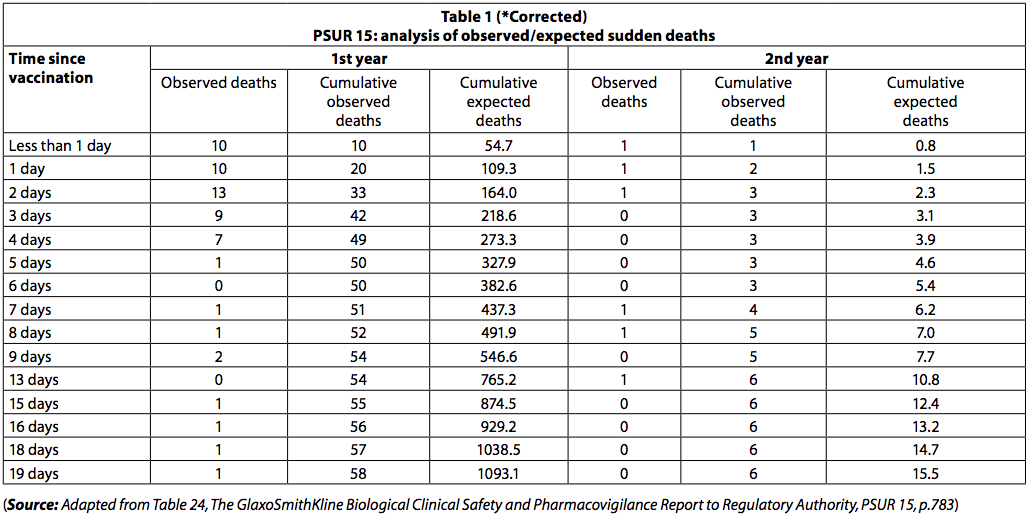
Jednak wśród noworodków odnotowano nagromadzenie zgonów bezpośrednio po szczepieniu, z 42 zgonami w pierwszych trzech dniach po szczepieniu i tylko 8 w ciągu następnych 3 dni. Wśród osób poniżej jednego roku życia 54 zgony (93%) wystąpiły w ciągu pierwszych dziesięciu dni, a 4 (7%) w ciągu następnych 10 dni. Gdyby zgony były „przypadkowymi zgonami z SIDS”, ta różnica w liczbie zgonów w dwóch okresach czasu nie zostałaby zaobserwowana.
Zgony z powodu SIDS byłyby równomiernie rozłożone w okresie 20 dni.
Fakt, że śmiertelność gwałtownie spada wraz z upływem czasu po immunizacji, sugeruje, że zgony mogą być związane ze szczepieniem.
Podobnie wśród dzieci w wieku powyżej jednego roku 5 zgonów (83,3%) miało miejsce w ciągu pierwszych 10 dni, a jedna śmierć (17%) nastąpiła w ciągu następnych 10 dni. Grupowanie zgonów zgłoszone w raporcie PSUR 15 odnotowano również w raporcie PSUR 16, o czym skomentowano wcześniej (6).
Odpowiedź GlaxoSmithKline
W odpowiedzi na tę krytykę (7), dyrektor generalny GlaxoSmithKline (GSK) (CEO) Sir Andrew Witty, za pośrednictwem dr Normana Begga, dyrektora medycznego firmy, zasugerował w liście, że istnieje znacznie większe prawdopodobieństwo wymyślenie potencjalnego związku przyczynowego, a następnie zgłoszenie zdarzenia niepożądanego do GSK, jeśli wystąpi ono krótko po szczepieniu, a nie tygodnie później. Następnie napisał: „W świetle powyższego, jesteśmy pewni wniosków, do których doszedł wcześniej GSK i przekazaliśmy agencjom regulacyjnym i organom zdrowia na całym świecie, że obecnie dostępne dane nie wskazują na zwiększone ryzyko nagłej śmierci niemowląt po szczepienie preparatem Infanrix hexa. Jeżeli dostępne dane i informacje zmienią się i zasugerują, że istnieje zwiększone ryzyko, nadal jesteśmy zobowiązani do niezwłocznego powiadomienia władz i podjęcia niezbędnych działań w celu przekazania takich danych i informacji pracownikom służby zdrowia ”.
Ta odpowiedź zawiera milczące przyznanie, że nie było aktywnej czujności w okresie po szczepieniu i tylko zgony spontanicznie zgłaszane GSK zostały uwzględnione w tytule „obserwowane zgony”. Może to spowodować niedoszacowanie liczby zgonów po szczepieniu. Należy zauważyć, że liczba dystrybuowanych dawek szczepionki jest wykorzystywana do „spodziewanych zgonów”. Raport potwierdza, że niekoniecznie zastosowano wszystkie dawki szczepionki dystrybuowanej. W ten sposób liczba „oczekiwanych zgonów” została zawyżona.
Biorąc jednak pod uwagę wyjaśnienie CEO i zapewnienie, że GSK zobowiązało się do niezwłocznego powiadomienia władz i pracowników służby zdrowia o zwiększonym ryzyku związanym z Infanrix Hexa, kwestia grupowania zgonów nie była dalej badana.
PSUR 16: podwojenie oczekiwanych zgonów
Jeśli wszystkie dzieci, które otrzymały pierwszą dawkę szczepionki, otrzymały łącznie cztery dawki, a ostatnia dawka została podana w drugim roku życia, wówczas można oszacować, że jedna czwarta (25%) dawek jest podawana starszym dzieciom do roku. Jest to zalecany harmonogram szczepień w Niemczech. Jednak niektóre kraje, takie jak Włochy, zalecają tylko trzy dawki, wszystkie w pierwszym roku i żadne w drugim. Ponadto nie wszystkie dzieci otrzymują wszystkie zalecane dawki. Tak więc prawdopodobnie nie będzie 20-25% dawek w drugim roku. W raporcie PSUR 15 oszacowano, że 90,6% sprzedawanych dawek stosowano u niemowląt w wieku poniżej jednego roku i 9,4% w przypadku dzieci w wieku powyżej jednego roku. W raporcie PSUR 16 szacunkowe dawki otrzymane w drugim roku wzrosły ponad dwukrotnie (z 9,4% do 20%), a zatem szacowana liczba zgonów podwoiła się. Pomimo podwojenia oczekiwanych zgonów liczba zgonów zaobserwowanych w drugim roku była wyższa niż oczekiwano w pierwszych 3 dniach po szczepieniu (Tabela 36, str. 249). Jeżeli oszacowanie w PSUR 15, że 9,4% dawek zostanie zastosowane w drugim roku, jest prawidłowe, dotyczy to również PSUR 16, a zatem zaobserwowane zgony są wyższe niż spodziewane zgony w ciągu pierwszych 7 dni.
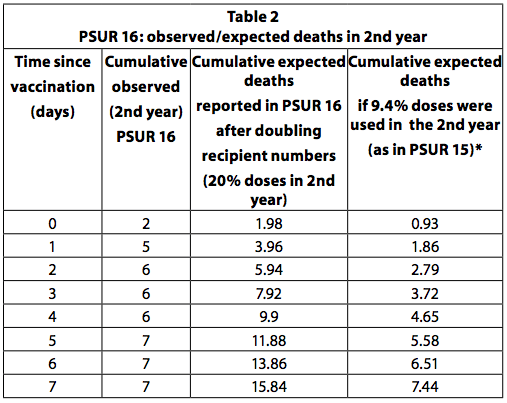
PSUR 19: przewidywane zgony ważone według kraju i rocznego odsetka dawek
W PSUR 19 obliczono średnią ważoną kalendarzową wskaźników częstości nagłych zgonów z Niemiec, Francji i Holandii, aby uzyskać oczekiwaną częstość występowania nagłych zgonów.
Mówiąc bardzo prosto, oznacza to, że jeśli 60% dawek rozłożono w Niemczech w danym roku, wskaźnik SD (nagłej śmierci) w Niemczech otrzymał 60% wagi przy obliczaniu wskaźnika SD. ogólnie za ten rok; jeśli 30% było dystrybuowane we Francji, wskaźnik SD we Francji przyczyniał się do 30%, a waga 10% została przypisana do holenderskiego wskaźnika SD. Na koniec obliczono globalną stawkę SD dla wszystkich lat łącznie.
Ogólny wskaźnik SD obliczono jako 0.0102 / 1000 urodzeń żywych dla drugiego roku. Liczba ta stanowi jedną szóstą oczekiwanej częstotliwości stosowanej w PSUR 15 i 16 (która oblicza nagłe zgony przy 0,062 / 1000 urodzeń żywych, na podstawie danych niemieckich).
Przedział ufności Poissona (CI) dla 95% zgonów zaobserwowanych w drugim roku podano w tabeli 8 ap 447 PSUR 19. Podano, że w drugim roku życia liczba zaobserwowanych zgonów była wyższa, również jeśli nie znacząco, niż przewidywana liczba zgonów w okresie ryzyka 1-4 dni po szczepieniu.
Brak zgonów w PSUR 19
Od PSUR 16 do PSUR 19 łączne dawki szczepionek wzrosły z 69 do 112 milionów. Zgodnie z PSUR 19 przyjęto, że 20,2% rozdzielonych dawek podawano dzieciom w drugim roku życia (PSUR 19, str. 436-448). Wykluczono przypadki zgonów, w których wiek szczepienia nie był znany, data zgonu nie została odnotowana lub czas zgonu przekroczył 19 dni od szczepienia.
PSUR 19 (zgony do 22 października 2014 r.) Nie zgłasza nagłych zgonów wymienionych w PSUR 16 (przypadki zgonów, które miały miejsce do 22 października 2011 r.). Należy zauważyć, że w PSUR 16 odnotowano zarówno wiek dziecka, które zmarło po szczepieniu, jak i czas śmierci (w ciągu 14 dni od szczepienia).
Zgłoszone skumulowane zgony są niższe w PSUR 19 niż w PSUR 16. Jeśli chodzi o dzieci powyżej jednego roku, PSUR 19 odnotowuje występowanie tylko 5 zgonów w ciągu pierwszych 19 dni po szczepieniu, podczas gdy PSUR 16 zgłasza 8 Liczby nie są ze sobą zgodne. Zastanawiamy się, dlaczego tak jest.
Dziesięć lat po publikacji artykułu CDC (Center for Disease Control) badającego związek między szczepionką przeciwko odrze, śwince i różyczce (MMR) a autyzmem (8), jeden z autorów, William Thompson, przyznał, że on i jego współautorzy nie przedstawili istotnych statystycznie informacji, że mężczyźni pochodzenia afroamerykańskiego, którzy otrzymali MMR przed 36 miesiącem życia, mieli zwiększone ryzyko autyzmu (9). Autorzy wykreślili dane dzieci, które nie posiadały aktów urodzenia w Gruzji (10), aby wykluczyć nieproporcjonalną liczbę dzieci czarnoskórych, oraz przedstawili ich dane, aby wykazać, że nie nastąpił wzrost liczby dzieci. ryzyko.
Nie jest jasne, czy autorzy PSUR 19 podobnie wykluczyli martwe i udokumentowane dzieci w PSUR 16.
Tabela 3 przedstawia zaobserwowane i oczekiwane zgony zgłoszone w PSUR 19 oraz zgony zaobserwowane po przywróceniu zgonów zgłoszonych w PSUR 16.
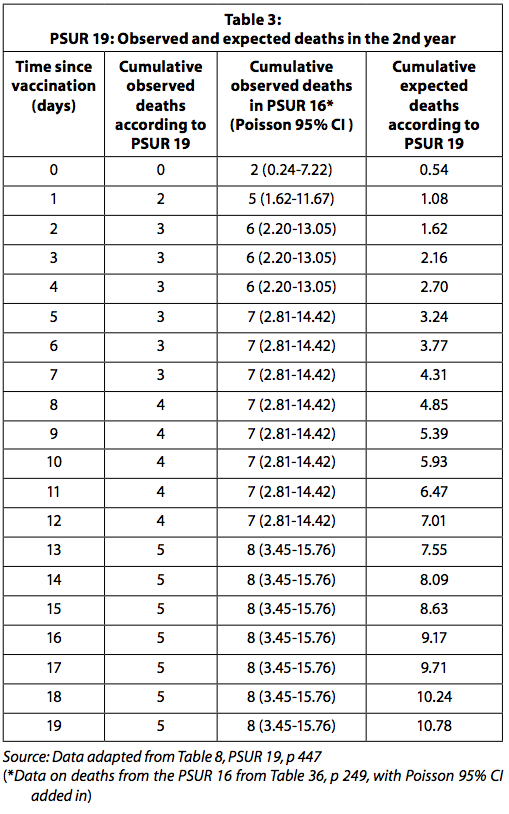
Gdy stosuje się dane dotyczące zaobserwowanych zgonów w PSUR 16, liczba zaobserwowanych zgonów jest znacznie wyższa niż oczekiwana w ciągu pierwszych czterech dni po szczepieniu. Należy pamiętać, jak wyjaśniono powyżej, że skoro liczba zaobserwowanych zgonów jest gromadzona w sposób bierny, prawdopodobnie zostanie ona niedoszacowana. Z drugiej strony, spodziewane zgony są prawdopodobnie przeszacowane, ponieważ są obliczane przy założeniu, że wszystkie rozdane dawki zostały użyte bez strat i żadna szczepionka nie została odrzucona, ponieważ wygasła. Oczekiwano, że GSK poinformuje organ nadzorujący i lekarzy o statystycznie istotnym zwiększonym ryzyku zgonu w ciągu czterech dni po szczepieniu.
Dawki stosowane w drugim roku
PSUR 19 zakłada, że w drugim roku wykorzystano 20,2% dawek. Stwierdzono, że rozkład wieku, w którym osoby są szczepione, jest nieznany, a firma spekuluje, że odsetek zdarzeń niepożądanych (w tym zgonów) według wieku jest reprezentatywny dla faktycznego rozkładu wieku przy szczepieniu. W związku z tym, ponieważ 20,2% zdarzeń niepożądanych wystąpiło u dzieci w wieku powyżej jednego roku, firma przyjęła, że w tej grupie wiekowej zastosowano 20,2% dawek.
Łatwo jest oszacować liczbę dawek zastosowanych w drugim roku w oparciu o zaobserwowane zdarzenia niepożądane (w tym zgon), a następnie użyć tego oszacowania dawki, aby obliczyć liczbę oczekiwanych zgonów, a na koniec porównać je z liczbą zaobserwowanych zgonów - biorąc pod uwagę, że oszacowanie oczekiwanych zgonów oblicza się przede wszystkim na podstawie zaobserwowanych zdarzeń negatywnych (w tym śmierci).
Zakładając, że wszystkie zgony po szczepieniu są zbieżne i SIDS / SUD niezwiązane z przyczynami związanymi ze szczepionką oraz biorąc pod uwagę, że (zgodnie z PSUR 19) naturalna częstotliwość nagłych zgonów w pierwszym roku jest 44 razy wyższa niż w drugim roku (0.441 / 1000 w pierwszym roku i 0.0102 / 1000 w drugim roku), w drugim roku należy zaszczepić 44 razy więcej dzieci, aby osiągnąć taką samą liczbę zgonów, jak w pierwszym roku.
W kohorcie 100 zgonów, jeśli 20% nagłych zgonów nastąpi w drugim roku i 80% w pierwszym roku, 880 dzieci musi zostać zaszczepionych w drugim roku na każde 20 zaszczepionych w pierwszym roku. W takim przypadku należy założyć, że 44% wszystkich dawek Infanrix hexa zostało zastosowanych w drugim roku, a tylko 80% w pierwszym roku (zamiast na odwrót). Odzwierciedla to absurdalność obliczania rozkładu dawki według wieku, w oparciu o rozkład wieku zdarzeń niepożądanych, jak to opisano w dokumencie GSK.
Jedynym sposobem oceny liczby dawek zastosowanych w drugim roku jest sprawdzenie harmonogramów szczepień w różnych krajach - sprawdzenie, które kraje zalecają czwartą dawkę w drugim roku, a które nie zalecają dawek w drugim roku. Można przypisać wagę liczbie dawek dystrybuowanych w tych krajach. Wskaźnik rezygnacji (dzieci, które opuszczają program szczepień po otrzymaniu pierwszych dawek szczepionki) należy również uwzględnić w końcowym obliczeniu odsetka dawek zastosowanych w drugim roku. Wydaje się, że rozsądne oszacowanie dawek zastosowanych w drugim roku wynosi 9,4% dawek całkowitych i jest to liczba zastosowana w PSUR 15.
Dylemat etyczny - problem z wózkiem
Ten komentarz nie próbuje zbadać, czy nadmierną liczbę zgonów po szczepieniu (prawdopodobnie spowodowanych przez szczepionkę) można zrównoważyć życiem ocalonym przez chorobę dzięki profilaktyce uzyskanej dzięki szczepionce. W swoim klasycznym eksperymencie mentalnym, zwanym dylematem dotyczącym wózka, Philippa Foot pyta, czy etyczne jest przekierowanie wózka uciekającego z toru kolejowego, który zabiłby pięć osób na innym torze, na którym zginęłaby tylko jedna osoba (11) , W wariancie dylematu wózka samotna osoba na alternatywnym torze jest dzieckiem osoby, która może przełączać tory.[2] Judith Thomson zakłada, że przeszczepy narządów od zdrowego dawcy mogą uratować pięć istnień ludzkich i pyta, czy celowe zabicie jednej osoby byłoby uratowaniem pozostałych pięciu (12). Etyka twierdzi, że cel nie może usprawiedliwić środków. Jeśli ukryjesz śmierć po szczepieniu, możesz zapobiec / opóźnić ocenę profilu bezpieczeństwa szczepionki, co może potencjalnie spowodować więcej niepotrzebnych zgonów, co jest trudne do uzasadnienia etycznego.
Znaczenie dla Indii
Organem regulacyjnym rządu Indii jest General Controller India (DCGI). Zgodnie z zasadami DCGI leki zatwierdzone w co najmniej jednym kraju, takim jak Stany Zjednoczone, Wielka Brytania, Kanada, Japonia, Australia i kraje Unii Europejskiej, są również zatwierdzone w Indiach (13). Potrzebne są tylko dodatkowe badania, aby ocenić wpływ czynników etnicznych na skuteczność, bezpieczeństwo, dawkowanie i schematy dawkowania leków (14).
Niedawno w Indiach opublikowano badania oceniające immunogenność i bezpieczeństwo sześciowartościowej szczepionki skojarzonej w niewielkich badaniach (15,16). Dodatkowo Indian Pediatrics opublikowało artykuł redakcyjny zatytułowany „Szczepienia sześciowartościowe: przyszłość rutynowych szczepień?” (17), którzy zasugerowali, że ta szczepionka skojarzona będzie promowana w Indiach. Istotne jest, aby organ regulacyjny w Indiach był świadomy obaw poruszonych w tym komentarzu do raportów PSUR, zwłaszcza że systemy nadzoru w Indiach są słabe.
Podsumowanie i wnioski
Von Kries (1) odnotował statystycznie istotny wzrost SMR u dzieci w drugim roku życia, w ciągu dwóch dni po szczepieniu szczepionką Hexavac® (jedna z dwóch zatwierdzonych szczepionek sześciowartościowych, obecnie wycofanych).
W okresowych raportach o bezpieczeństwie GSK, firma produkująca Infanrix hexa, ocenia, czy liczba nagłych zgonów zgłoszonych po szczepieniu ich lekiem przekroczyła liczbę, której można by się spodziewać przypadkowo. Grupowanie zgonów bezpośrednio po szczepieniu sugeruje, że śmierć mogła być spowodowana szczepionką.
Ponadto nasza analiza pokazuje, że zgony rozpoznane w PSUR 16 zostały wyeliminowane z PSUR 19. Obserwowane zgony zgłaszane są spontanicznie do GSK i prawdopodobnie zostaną niedoszacowane. Po dodaniu zgonów usuniętych z PSUR 16 istnieje statystycznie istotny wzrost ryzyka zgonu w ciągu pierwszych czterech dni po szczepieniu, w porównaniu do oczekiwanych zgonów. Producenci będą musieli wyjaśnić, dlaczego zgony te nie zostały uwzględnione w PSUR 19. Zwiększone ryzyko śmierci nie zostało ujawnione organowi regulacyjnemu ani personelowi medycznemu podającemu szczepionkę.
Biorąc powyższe pod uwagę, trudno jest zrozumieć, w jaki sposób EMA mogła zaakceptować PSUR 19 w ujęciu nominalnym. Można argumentować, że nie dochowano należytej staranności, tak że wiele dzieci niepotrzebnie zostało narażonych na ryzyko śmierci.
DCGI musi zostać poinformowany o ograniczeniach zawartych w PSUR Infanrix Hexa.

