Końcowy raport techniczny - Analiza profilu molekularnego szczepionek

Przedmowa
Przede wszystkim chcielibyśmy podziękować za bardzo przydatne uwagi przedstawione przez osoby, które dokonały przeglądu wyników analiz przeprowadzonych w kontekście badań naukowych dotyczących produktów Priorix tetra i Infanrix Hexa. Przedstawione kwestie krytyczne były rzeczywiście bardzo przydatne w celu dodania integracji techniczno-naukowych mogących wyjaśnić wykonane prace. Uważamy, że tylko dzięki zdrowej komunii wizji naukowych można wyciągnąć wnioski na temat uzyskanych danych, które mogą być przydatne dla całej społeczności naukowej i osób, które się nią zajmują.
1. Stan techniki
Wstępne badania (badanie przesiewowe nie wymaga potwierdzenia) profilu biomolekularnego, metabolomicznego i proteomicznego przeprowadzone na produktach Priorix Tetra i Infanrix Hexa doprowadziły do opracowania struktury składu podsumowanej w następujących punktach:
- Obecność różnych sygnałów analitycznych, których nie można powiązać ze znanymi związkami poprzez badania w bazach danych Metlin 1-2 i KEGG3. Dlatego pojawił się obraz związany ze znaczną złożonością składu produktów handlowych.
- Obecność białek niezadeklarowanych w ulotce w produkcie Priorix Tetra. Te ostatnie mogą być potencjalnie związane z pozostałościami z procesu produkcyjnego
- Niewykrycie antygenów zadeklarowanych w produkcie Infanrix Hexa. Technika analizy polegała na trawieniu enzymatycznym trypsyną związaną z technikami spektrometrii mas. 4-5
Dane te wzbudziły szereg uwag, szczególnie w odniesieniu do punktu C - Wykrywanie białka jest w rzeczywistości przeprowadzane przy użyciu standardowego podejścia, uznawanego na całym świecie przez ponad 10 lat 4, trawienia za pomocą enzymu trypsyny 4. Tak uzyskane peptydy są chromatograficznie rozdzielane i analizowane za pomocą spektrometrii mas 4-5. Główna obserwacja nieodłącznie wiąże się z faktem, że w szczepionkach znajdują się adiuwanty na bazie glinu, które mogą potencjalnie hamować proces trawienia enzymatycznego. Zebrane dane umożliwiły następnie udzielenie istotnych wyjaśnień, zwłaszcza w odniesieniu do skargi wyrażonej w pkt C.
2. Nowe spostrzeżenia i analizy
2.1 Informacje dotyczące analizy produktu Infanrix Hexa
Przed przystąpieniem do zilustrowania nowych uzyskanych danych dotyczących szczepionek Hexyon i Gardas 9 należy odpowiedzieć na pytanie dotyczące wątpliwości dotyczących hamowania aktywności proteolitycznej trypsyny spowodowanej obecnością adiuwantów na bazie glinu w Infanrix Hexa szczepionka. W związku z tym należy sprecyzować, że kontrola trawienia jest zawsze obecna w trawieniu tryptycznym. W rzeczywistości trypsyna stosowana do przeprowadzania trawienia, chociaż opracowana w celu zapobiegania autolizy, ma niewielki procent tej ostatniej, co w przypadku aktywności enzymatycznej prowadzi do uzyskania fragmentu m / z 842 i następującej sekwencji peptydowej: VATVSLPR. Wspomniany fragment został faktycznie wykryty w trakcie trawienia tryptycznego produktu Infanrix Hexa, co można zweryfikować za pomocą chromatogramu ekstrakcji jonowej (ryc. 1).
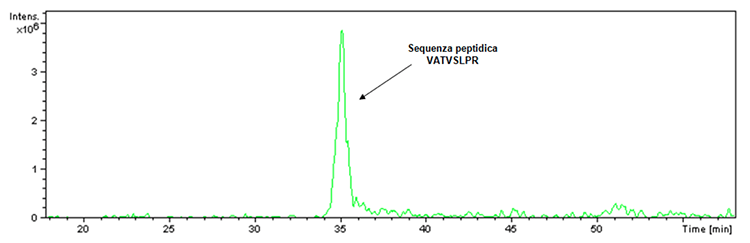
Rycina 1: Chromatogram jonowy ekstrakcyjny związany ze stosunkiem m / z 842 znaleziony w próbce partii produktu Infanrix Hexa (nr partii A21CD072D).
Ponadto przeprowadza się kontrolę zewnętrzną poprzez trawienie hemoglobiny w celu dalszej weryfikacji dobroczynności zastosowanej partii trypsyny. Hemoglobina, analizowana w części analitycznej, w której monitorowano produkt, została rozpoznana z istotnym wynikiem statystycznym (loge <- 100). Dane te potwierdziły fakt, że aktywność enzymatyczna była obecna.
2.2 Nowe analizy dotyczące produktów Hexyon i Gardasil
Analiza produktów Hexyon i Gardas 9 doprowadziła do wykrycia złożonych profili molekularnych. W tym przypadku wykryto jednak obecność większości antygenów podanych w ulotce informacyjnej. Wykryto je przez trawienie tryptyczne i w obecności adiuwantów.
Fakt ten dodatkowo wzmacnia dowody, że reakcja trawienia tryptycznego nie jest hamowana w obecności adiuwantów. W przypadku szczepionek Hexyon i Gardas 9 złożoność profilu molekularnego przypisywano głównie obecności wielu gatunków o niskiej masie cząsteczkowej, których nie można zidentyfikować w referencyjnych bazach danych Metlin 1-2- i KEGG 3.
3. Wnioski i uwagi końcowe
Przeprowadzone analizy doprowadziły do następujących wniosków:
- Profil molekularny analizowanych szczepionek jest na ogół złożony i w dużej mierze nieznany.
- Istnieją zanieczyszczenia białkowe, niezadeklarowane w ulotce, których skład jest zmienny.
- W kilku przypadkach antygeny zadeklarowane w ulotce nie zostały wykryte. Fakt ten można przypisać kilku czynnikom. Wśród tych ostatnich możemy rozważyć czułość zastosowanej metody. Uważamy jednak, że możemy wykluczyć zjawisko hamowania trawienia ze względu na obecność adiuwantów w formulacji szczepionki. W rzeczywistości aktywność enzymatyczną potwierdza głównie obecność fragmentów autolizy tryptycznej w roztworach strawionych szczepionek (kontrola wewnętrzna).
4. Przyszłe studia
Dalsze badania zostaną przeprowadzone w ramach działań badawczo-rozwojowych mających na celu zbadanie następujących aspektów:
- kompozycja makrocząsteczkowa związana ze stałymi resztkami obecnymi w szczepionkach (analiza MALDI TOF MS); 5
- ocena stężenia metali obecnych w produktach.
- Analiza drugiego poziomu w celu potwierdzenia obecności toksycznych związków wykrytych w fazie przesiewowej. Ich stężenie będzie wówczas związane z jego toksycznością zgodnie z danymi zawartymi w międzynarodowych kartach charakterystyki. Analizy drugiego poziomu zostaną przeprowadzone zgodnie z europejską dyrektywą UE 2002/657 / WE, przydatną do zagwarantowania wysokich standardów jakości w sektorze spektrometrii mas. 6
Lorettę Bolgan
5. Literatura bibliograficzna
- Autenhahn R, Cho K, Uritboonthai W, Zhu Z, Patti G, Siuzdak G (wrzesień 2012). „Przyspieszony przepływ pracy dla nieukierunkowanej metabolomiki przy użyciu bazy danych METLIN”. Nature Biotechnology. 30: 826–828. DOI: 10.1038 / nbt.2348. PMC 3666346. PMID 22965049.
- Smith CA, I'Maille G, Want EJ, Qin C, Trauger SA, Brandon TR, Custodio DE, Abagyan R, Siuzdak G (grudzień 2005). „METLIN: baza danych spektrometrii masowej metabolitów” (PDF). Ther Drug Monit. 27 (6): 747–51. DOI: 10.1097 / 01.ftd.0000179845.53213.39. PMID 16404815.
- Kanehisa M. (2013). „Ewolucja chemiczna i genomowa sieci katalizowanych enzymami”. FEBS Lett. 587 (17): 2731–7.
- Cristoni S, Bernardi LR. „Bioinformatyka w analizie danych spektrometrii mas dla badań proteomicznych”. Expert Rev Proteomics. Grudzień 2004; 1 (4): 469–83.
- Cristoni S, Bernardi LR. „Opracowanie nowych metodologii badań spektrometrii mas bioorganicznych makrocząsteczek”. Mass Spectrom Rev. 2003 listopad-grudzień; 22 (6): 369-406.
- Cristoni S, Dusi G, Brambilla P, Albini A, Conti M, Brambilla M, Bruno A, Di Gaudio F, Ferlin L, Tazzari V, Mengozzi S, Barera S, Sialer C, Trenti T, Cantu M, Rossi Bernardi L, Noonan DM. „SANIST: optymalizacja technologii identyfikacji związków na podstawie dyrektywy Unii Europejskiej z zastosowaniami w analizach kryminalistycznych, farmaceutycznych i spożywczych”. J. Mass Spectrom. 2017 stycznia; 52 (1): 16–21. doi: 10.1002 / jms.3895.
Download: CORVELVA-końcowy-techniczne-report.pdf
Przetłumaczone przez zespół CLiVa - www.clivatoscana.com

