Szczepionka: pełne sekwencjonowanie genomu MRC-5 zawartego w Priorix Tetra

Te ostatnie analizy były możliwe dzięki aktywnemu wkładowi francuskich stowarzyszeń Stowarzyszenie Liberté Informations Santé (ALIS) Ligue nationale pour la liberté des Vaccinations (LNPLV) i stowarzyszenie australijskie Australijska Sieć Ryzyka Szczepień (AVN) za co dziękujemy.
Sekwencery nowej generacji stały się instrumentem z wyboru do dogłębnych analiz w dziedzinie biologii i medycyny, zwłaszcza precyzyjnej. Narzędzia te umożliwiają nowe i bardziej globalne podejście do szeregu zastosowań, takich jak sekwencjonowanie de novo, badania metagenomiczne, epigenomika, sekwencjonowanie transkryptomu i ponowne sekwencjonowanie genomu.
To ostatnie zastosowanie (ponowne sekwencjonowanie) jest bardzo rozpowszechnione w dziedzinie ludzkiej zarówno do celów badawczych, jak i diagnostycznych i polega na sekwencjonowaniu technologii NGS (sekwencjonowanie nowej generacji) całego pojedynczego genomu w celu zmapowania pojedynczych mutacji nukleotydowych (SNP, wymowa „wycinanie”), wstawianie i usuwanie mniej lub bardziej długich sekwencji występowało w niektórych pozycjach genomu i różnice w liczbie kopii części genomu / genów (CNV, warianty liczby kopii).
Ta procedura jest przydatna do zrozumienia mechanizmów rozwoju niektórych patologii w celu określenia kierunków przyszłego leczenia klinicznego, na przykład w przypadku raka. Dzięki tej metodzie dziedzictwo genetyczne pacjenta z rakiem może zostać całkowicie zdekodowane w tkance normalnej i nowotworowej, co pozwala zrozumieć, co zmieniło się w genomie i, jeśli to możliwe, interweniować za pomocą ukierunkowanych protokołów.
Procedura ponownego sekwencjonowania wymaga mechanicznego rozbicia DNA osobnika na małe fragmenty (400-500 par zasad) i fragmentów związanych ze sztucznymi odcinkami DNA zwanymi adapterami, które umożliwiają wiązanie fragmentów Ludzkie DNA na szklanej powierzchni, na której następnie odczytywane są zasady (A, C, G, T). Zasady DNA odczytuje się poprzez włączenie reakcji chemicznych nukleotydów znakowanych cząsteczkami fluorescencyjnymi. Miliony sekwencji (odczytów) uzyskanych z sekwencjonowania na szklanej powierzchni są następnie mapowane na ludzkim genomie referencyjnym za pomocą odpowiedniego oprogramowania, a zatem wszystkie warianty obecne w analizowanym genomie są identyfikowane w odniesieniu do referencji.
Tę samą procedurę przeprowadzono na ludzkim genomie obecnym w partii Priorix Tetra. N. A71CB256A, genom należący do linii komórkowej MRC-5 (pochodzenia płodowego); prace przeprowadzono w firmie z siedzibą w USA, która rutynowo zajmuje się analizą ludzkich genomów poprzez sekwencjonowanie. *
* Nazwa laboratorium, które wykonało tę analizę, zostanie zamieszczona w następnym oświadczeniu, że złożymy depozyt w Prokuraturze w Rzymie, a także we włoskich i europejskich organach kontrolnych. Rzeczywistości, które deponują wyniki analiz finansowanych przez Corvelvę, również zostaną natychmiast zaktualizowane o te zagadkowe wyniki. Nie zaprzeczamy, że jako rodzice przede wszystkim niepokoją nas wyniki, które przedstawiamy poniżej - jeśli to, co odkryliśmy do tej pory, nie wystarczyło.
wyniki
Stwierdzono, że ludzki genom referencyjny jest objęty odczytami pochodzącymi z DNA szczepionki w 99.76%, a więc prawie w całości. Ludzki DNA płodu reprezentowany w tej szczepionce jest zatem kompletnym indywidualnym genomem lub jest obecny w szczepionce genomowego DNA wszystkich chromosomów osobnika męskiego (i faktycznie płód, z którego pochodzi linia komórkowa MRC-5, jest płci męskiej).
Poniżej znajdują się wyniki analizy różnych rodzajów wariantów w odniesieniu do ludzkiego genomu referencyjnego.
Warianty pojedynczego nukleotydu (SNP) i krótkie insercje / delecje (InDels)
Warianty poszczególnych zasad DNA (SNP, wymawiane „wycinanie”) są polimorfizmami, to znaczy odmianami materiału genetycznego przenoszonego przez pojedynczy nukleotyd. Z drugiej strony „InDels” to małe insercje i delecje o długości mniejszej niż 50 pb i stanowią kolejną klasę wariantów genomowych w ludzkim genomie.
W genomie ludzkiej szczepionki zidentyfikowano ogółem około 3.6 miliona SNP (z czego 98.31% zgłoszono już w publicznej bazie danych dbSNP i 61.805 804 nowych lub oryginalnych tego DNA) oraz około 89.42 tysięcy InDels (z czego 85.106% już zgłoszone w dbSNP i XNUMX XNUMX nowych).
Ilość SNP jest zgodna z tym, co opisano w literaturze w „typowym ludzkim genomie”, podczas gdy indele są w większej ilości niż podano w „Konsorcjum Projektu 1000 Genomes” lub 800 tys. W porównaniu do 600 tys.
CNV (warianty numerów kopii) i SV (warianty strukturalne)
Warianty liczby kopii (CNV) są wariantami genomowymi z powodu zmian liczby kopii stosunkowo dużych fragmentów (dłuższych niż 50 pz) między poszczególnymi genomami. Istnieją dwa rodzaje CNV: typ „zysk” (wzrost liczby kopii) i typ „utrata” (utrata kopii). W genomie ludzkiej szczepionki wykryto 218 CNV, z których 82 są typu „wzmocnienia” (obejmującego część genomu równą około 6.9 miliona par zasad) i 136 CNV „tracących” (które pokrywają część genomu około 70 milionów zasad).
Jak opisano w Konsorcjum Projektu 1000 Genomes w „Globalnym źródle ludzkiej zmienności genetycznej (Nature, vol. 526, 10 października 2015)” typowy ludzki genom zawiera od 2.100 do 2.500 dużych wariantów, w tym:
- 1.000 dużych usunięć
- 160 zmian liczby kopii (CNV)
- 10 inwersji
które wpływają ogólnie, uwzględniając także insercje, na 20 milionów zasad sekwencji.
Jak zaobserwowano w przypadku krótkich INDEL, nawet w przypadku dużych insercji i delecji genom szczepionkowy nie jest zatem zgodny z „normalnym” ludzkim genomem, ponieważ jest znacznie bardziej „przestawiony” niż genom zwykłego osobnika.
Kołowa wizualizacja genomu (wykres cyrkowy)
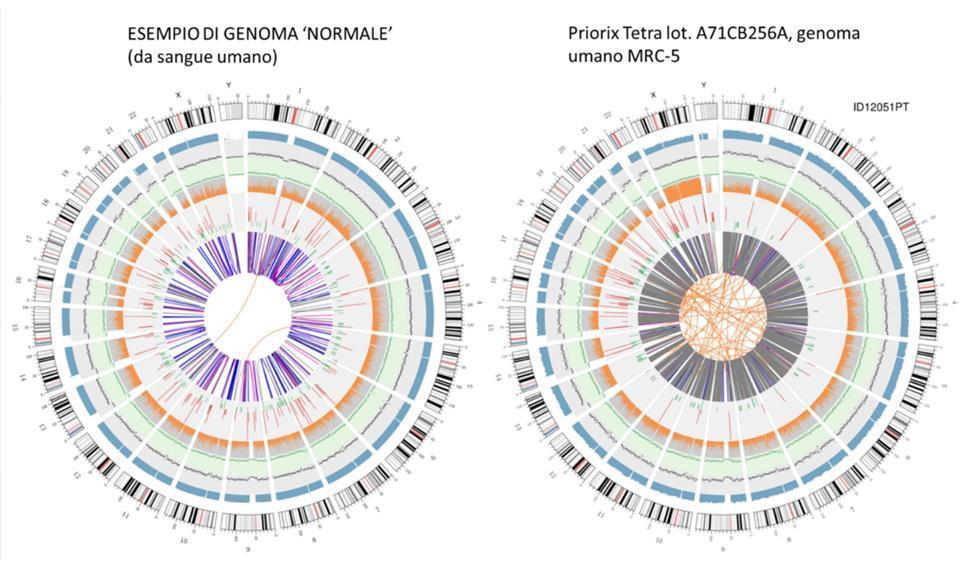
Graficzna reprezentacja genomu szczepionki zwanego „polem okrężnym” (który jest powszechnie używany do reprezentowania ponownie zsekwencjonowanego genomu), jest pokazana poniżej, obok innego, który reprezentuje ponownie zsekwencjonowany genom zaczynający się od DNA ekstrahowanego z krwi zdrowego osobnika - genom „normalny”:
Znaczenie różnych koncentrycznych kół
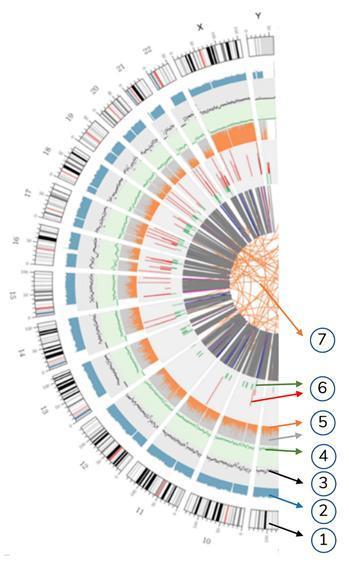
7) Najbardziej centralny pierścień reprezentuje wnioskowanie SV (warianty strukturalne) w obszarach egzonicznych i splicingowych. MIĘDZY (pomarańczowy, translokacje), INS (zielony, wstawki), DEL (skreślenia, szary), DUP (duplikacje, różowy) i INV (inwersje, niebieski).
6) Szósty pierścień reprezentuje wnioskowanie CNV (warianty w liczbie kopii). Czerwony oznacza zdobycie kawałków DNA, a zielony oznacza utratę.
5) Piąty pierścień reprezentuje proporcję SNP w homozygotyczności (pomarańczowy) i heterozygotyczności (szary) w stylu histogramu.
4) Czwarty pierścień (zielony) reprezentuje snp gęstości w stylu „wykresu dyspersji”.
3) Trzeci pierścień (czarny) reprezentuje gęstość INDELI w stylu „wykresu dyspersji”.
2) Drugi pierścień (niebieski) reprezentuje zasięg odczytów w stylu histogramu.
1) Zewnętrzne koło (pierwsze koło) to liczba chromosomów.
Można również z grubsza porównać DNA płodu i DNA komórki HeLa, unieśmiertelnioną linię komórkową stosowaną również do produkcji szczepionki przeciw polio.
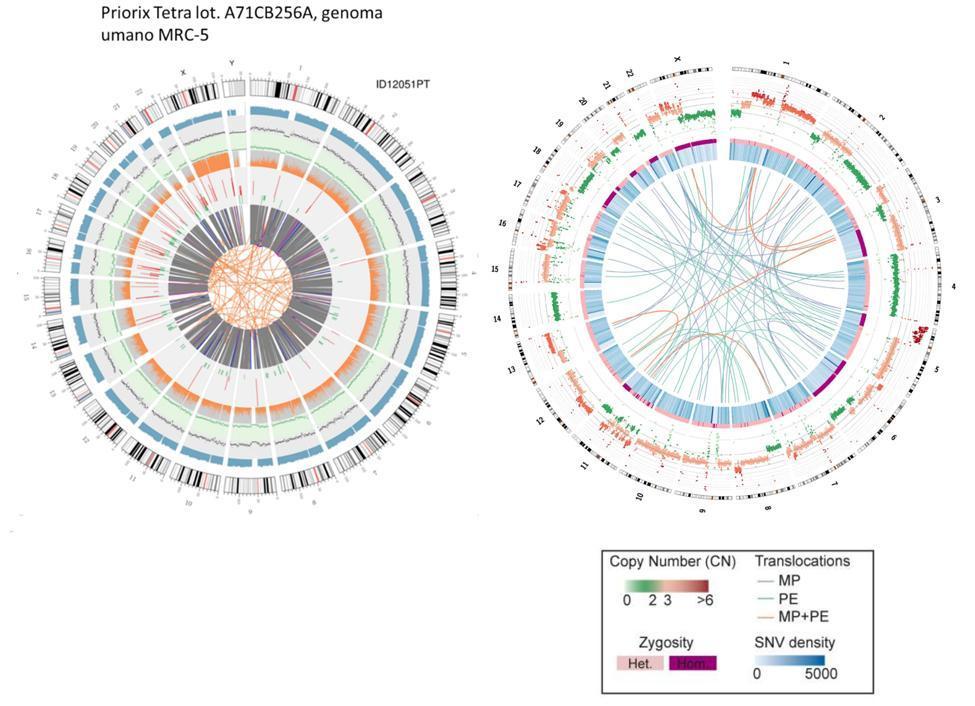
Należy podkreślić, że translokacje komórek HeLa reprezentowane na wykresie woskowym przez linie jądra odnoszą się do całego genomu (a więc części kodującej i niekodującej), podczas gdy w przypadku komórek szczepionki płodowej odnoszą się tylko do genów kodujących.
Nie trzeba być naukowcem, aby po prostu na pierwszy rzut oka zrozumieć, że genom szczepionki nie jest genomem, który można określić jako „normalny”. Pomarańczowe linie przeplatające się w środku Circos, nieobecne tak liczne w odpowiednim pierścieniu „normalnego” genomu, już każą nam odgadnąć anomalię tego genomu.
wnioski
Ludzki genomowy DNA zawarty w szczepionce serii Prorix. N. A71CB256A jest ewidentnie anomalny, wykazując istotne niespójności w odniesieniu do typowego ludzkiego genomu, to znaczy zdrowego osobnika. Istnieje wiele nieznanych wariantów (nie odnotowanych w publicznych bazach danych), a kilka z nich znajduje się w genach zaangażowanych w raka. Ewidentnie anomalny jest także nadmiar genomu, który pokazuje zmiany liczby kopii (CNV) i wariantów strukturalnych (SV), takich jak translokacje, insercje, delecje, duplikacje i inwersje, z których wiele obejmuje geny.
Potencjalny udział wielu wariantów (nieobecnych w literaturze naukowej i publicznych bazach danych) w fenotypie komórek wykorzystywanych do wzrostu wirusów szczepionkowych nie jest znany.
W pliku PDF znajdziesz wszystkie spostrzeżenia związane również z implikacjami dla zdrowia i korespondencją z EMA.
Download: CORVELVA-Ri-sekwencjonowanie genomu ludzkim Priorix-Tetra.pdf

