Covid-19 Vaccinverplichtingen: 20 wetenschappelijke feiten die hen uitdagen

HYPOTHESE: COVID-19-vaccins verminderen de verspreiding van COVID-19 aanzienlijk, dus hoge universele vaccinatiepercentages zullen uitbraken voorkomen en de pandemie beëindigen |
GEDAAN #1: uit een onderzoek naar een uitbraak van COVID-19 in juli 2021, gepubliceerd in Eurosurveillance, bleek dat: "Alle overdrachten tussen patiënten en personeel vonden plaats tussen gemaskerde en gevaccineerde personen, zoals gebeurde bij een uitbraak in Finland". De auteurs stellen dat de studie "daagt de hypothese uit dat hoge universele vaccinatiepercentages leiden tot kudde-immuniteit en uitbraken van COVID-19 voorkomen".1
GEDAAN #2: een studie van de Centers for Disease Control and Prevention naar een andere COVID-19-uitbraak in juli 2021 wees uit dat 74 procent van de gevallen volledig was gevaccineerd.2
GEDAAN #3: Een Harvard-studie die COVID-19-gevallen in 68 landen en 2.947 Amerikaanse provincies analyseerde, vond geen "geen significante tekenen van een afname van COVID-19-gevallen in aanwezigheid van hogere percentages van de volledig gevaccineerde bevolking ".3
HYPOTHESE: COVID-19-vaccins voorkomen overlijden door COVID-19 |
GEDAAN #4: Klinische onderzoeken hebben tienduizenden proefpersonen geobserveerd en zijn de enige die een controlegroep omvatten en waarin alle proefpersonen werden gecontroleerd en getest op COVID-19, ongeacht de vaccinatiestatus. Deze studies vonden echter niet een voldoende aantal sterfgevallen als gevolg van COVID-19 om een significant verschil in mortaliteit tussen gevaccineerde en niet-gevaccineerde patiënten te meten.4-7 De Amerikaanse Food and Drug Administration (FDA) stelt dat: "Er zouden meer personen met een hoog risico op COVID-19 en hogere aanvalspercentages nodig zijn om de effectiviteit van het vaccin tegen sterfte te bevestigen.".4-7
GEDAAN #5: Uit een onderzoek naar een uitbraak van COVID-19 in juli 2021, gepubliceerd in Eurosurveillance, bleek dat 100% van de ernstige, kritieke en dodelijke gevallen van COVID-19 zich voordeed bij gevaccineerde personen.1
GEDAAN #6: Uit CDC-gegevens blijkt dat massale vaccinatie met het COVID-19-vaccin geen meetbare impact had op het sterftecijfer door COVID-19 in de Verenigde Staten. In de negen maanden voorafgaand aan de introductie van massale vaccinatie (april 2020 tot december 2020), waren er ongeveer 356.000 sterfgevallen als gevolg van COVID-19, of 39.500 sterfgevallen per maand - een sterftecijfer van 0,120 per 1.000 mensen. In de negen maanden na de introductie van massavaccinatie (januari 2021 tot september 2021) waren er 342.000 sterfgevallen als gevolg van COVID-19 of 38.000 sterfgevallen per maand - een sterftecijfer van 0,115 per 1.000 mensen. In de volgende vijf maanden (van oktober 2021 tot februari 2022) waren er nog eens 249.000 sterfgevallen als gevolg van COVID-19, of 49.800 sterfgevallen per maand, met een sterftecijfer van 0,151 per 1.000 mensen.7
HYPOTHESE: Voor kinderen is een injectie met het COVID-19-vaccin veiliger dan een SARS-CoV-2-infectie. |
GEDAAN #7: In de klinische studie van Pfizer waren er geen gevallen van ernstige COVID-19 bij kinderen die het vaccin niet kregen.8-9 Voor kinderen van 5 jaar of ouder bleek daarentegen uit de klinische studie van Pfizer naar het COVID-19-vaccin dat het vaccin ernstige (graad 3) systemische reacties veroorzaakt, waaronder koorts boven 39 ° C, braken waarvoor hydratatie via intraveneuze weg nodig is, 24- uur diarree en ernstige vermoeidheid, ernstige hoofdpijn, ernstige spierpijn of ernstige gewrichtspijn die dagelijkse activiteit verhinderen.9-12
GEDAAN #8: In de klinische studie kreeg 1 op 59 tot 1 op 143 gevaccineerde kinderen van 5 tot 11 jaar ernstige systemische reacties binnen zeven dagen na de tweede dosis. In de gevaccineerde groep werden 3 tot 8 gevallen van ernstige systemische reacties waargenomen voor elke 10 niet-ernstige COVID-19-gevallen in de niet-gevaccineerde groep.9
GEDAAN #9: In de klinische studie kreeg 1 op de 9 gevaccineerde adolescenten tussen 12 en 15 jaar ernstige systemische reacties binnen zeven dagen na ontvangst van de tweede dosis. Ernstige systemische reacties waargenomen in de gevaccineerde groep waren 7 keer groter dan niet-ernstige gevallen van COVID-19 in de niet-gevaccineerde groep.10-12
GEDAAN #10: Uit de klinische studie bleek ook dat 1 op de ongeveer 1.100 gevaccineerde kinderen van 12 tot 15 jaar na de eerste dosis een systemische reactie van graad 4 (koorts boven 39 ° C) had, waarvoor een bezoek aan de eerste hulp en het staken van de studie nodig waren.10-13
HYPOTHESE: De klinische proef met het COVID-19-vaccin was groot genoeg om de veiligheid bij kinderen aan te tonen.
|
FEIT # 11: De klinische studie van Pfizer had niet voldoende statistische power om aan te tonen dat het vaccin veilig is bij kinderen onder de 18 jaar, aangezien de studie niet voldoende proefpersonen omvatte om de veiligheid vast te stellen (d.w.z. de klinische studie omvatte slechts ongeveer 2.600 gevaccineerde kinderen tussen de 5 en 15 jaar).9-14 Ter vergelijking: het is bekend dat sterfgevallen als gevolg van COVID-19 zeldzaam zijn bij kinderen. Vanaf 3 november 2021 was de kans dat een 17-jarige of jonger SARS-CoV-2 krijgt en sterft aan COVID-19 1 op 126.000 of 0,0008%.15
De klinische proef met het COVID-19-vaccin is onvoldoende om de veiligheid bij kinderen aan te tonen
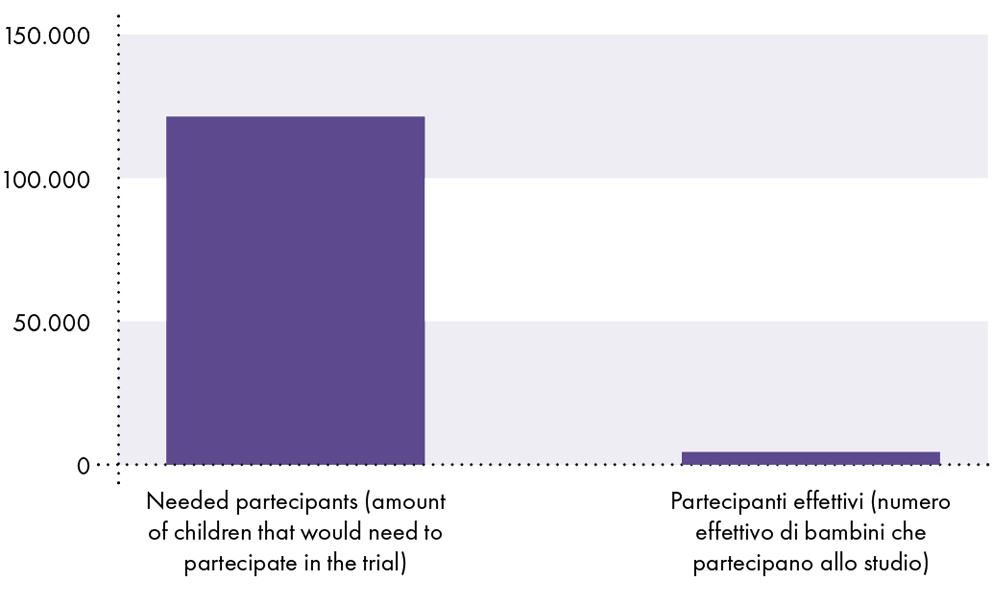
Omdat de kans dat een kind SARS-CoV-2 oploopt en sterft aan COVID-19 0,0008% of 1 op 126.000 is, zijn er minstens 126.000 kinderen nodig om een overlijden door COVID-19 te detecteren. Daarom moeten er ten minste 126.000 gevaccineerde deelnemers zijn ingeschreven voor de klinische proef om het risico op overlijden door COVID-19 te vergelijken met het risico op overlijden door vaccins. Aan de klinische studie namen echter slechts ongeveer 2.600 gevaccineerde kinderen deel.
HYPOTHESE: Van COVID-19-vaccins is bekend dat ze geen bijwerkingen op de lange termijn hebben.
|
FEIT #12: Aangezien alle proefpersonen in klinische onderzoeken slechts twee tot zes maanden werden geobserveerd, is de veiligheid op lange termijn van COVID-19-vaccins voor elke leeftijdsgroep onbekend. Volgens de FDA zijn er momenteel onvoldoende gegevens om conclusies te trekken over de veiligheid van Pfizer-, Moderna- en Johnson & Johnson-vaccins in subpopulaties zoals zwangere en zogende personen en immuungecompromitteerde personen.4-8-16 Voor Pfizer, het vaccin "is niet geëvalueerd op potentieel om carcinogeniteit, genotoxiciteit of aantasting van de mannelijke vruchtbaarheid te veroorzaken".17
FEIT # 13: Veiligheidsbewakingsrapporten identificeerden ernstige risico's van myocarditis en pericarditis bij personen jonger dan 40 jaar, binnen zeven dagen na vaccinatie. Bij 16- of 17-jarige jongens heeft de FDA een verhoogd risico op myocarditis of pericarditis van 1 op 5.000 gemeld na de tweede dosis Pfizer COVID-19.18-vaccin EN bij jongens van 12 tot 17 jaar, opnieuw na een tweede dosis dosis van het Pfizer COVID-19-vaccin, vond een studie in Hong Kong een verhoogd risico op myocarditis of pericarditis van 1 op 2.700.19
HYPOTHESE: De boosters zullen het probleem van de daling van de vaccinimmuniteit oplossen.
|
FEIT #14: Klinische studies hebben aangetoond dat de immuniteit van vaccins in korte tijd aanzienlijk afneemt. Zo daalde de effectiviteit van het Pfizer-vaccin in slechts zes maanden van 8% naar 18% en daalde de effectiviteit van het Johnson & Johnson-vaccin in slechts zes maanden van 25% naar 29%.20-21 Bovendien was de werkzaamheid gemeten in klinische onderzoeken tegen de oorspronkelijke Wuhan-stam, niet tegen de nieuwe varianten.
FEIT # 15: In klinische onderzoeken werd een derde dosis van het Pfizer- of Moderna-vaccin of een tweede dosis van het Johnson & Johnson-vaccin niet geëvalueerd op werkzaamheid tegen de ziekte, maar werden bij een klein aantal gevaccineerde personen slechts een maand lang antilichaamtellingen waargenomen.18-21-22
HYPOTHESE: Er zijn geen effectieve behandelings- of preventiemogelijkheden voor COVID-19 bekend, behalve voor vaccins.
|
FEIT # 16Behandelingen voor COVID-19 zijn aanzienlijk verbeterd sinds het begin van de pandemie begin 2020, wat heeft geleid tot verbeterde overlevingspercentages in gehospitaliseerde gevallen.23-24 Voor mensen die niet in een verpleeghuis wonen, is het totale overlevingspercentage van COVID-19 99,8% in de Verenigde Staten en 99,999% in het bijzonder voor kinderen.25-26
FEIT # 17: Honderden studies hebben gekeken naar de effectiviteit van verschillende behandelingen, waarvan de meest bestudeerde ivermectine, vitamine D, hydroxychloroquine (HCQ) en monoklonale antilichamen zijn.27-30 Deze behandelingen kunnen ook nuttig zijn voor profylaxe (d.w.z. preventie vóór of na blootstelling van symptomatische COVID-19-infecties).31-35
HYPOTHESE: Mensen die eerder met SARS-CoV-2 zijn geïnfecteerd, moeten zich laten vaccineren omdat de natuurlijke immuniteit onvoldoende is. |
FEIT # 18Het is aangetoond dat eerdere SARS-CoV-2-infectie effectiever is in het voorkomen van SARS-CoV-2-infectie dan COVID-19-vaccins. De klinische proef met het COVID-19-vaccin van Johnson & Johnson omvatte meer dan 2.000 proefpersonen die voorafgaand aan het onderzoek SARS-CoV-2 hadden opgelopen. De studie, die consequent niet-gevaccineerde en gevaccineerde mensen testte, registreerde de incidentie van COVID-19 in de niet-gevaccineerde groep ten minste 28 dagen na vaccinatie van de andere proefpersonen. De incidentie van COVID-19 in de niet-gevaccineerde groep met eerdere SARS-CoV-2-infectie was 0,1% (2/2.021), terwijl de incidentie van COVID-19 bij de gevaccineerde proefpersonen 0,59% was (113/19.306). Deze gegevens suggereren dat COVID-19-gevallen bij gevaccineerde personen 6 keer hoger zijn dan bij niet-gevaccineerde personen die eerder met SARS-CoV-2 waren geïnfecteerd.36
FEIT # 19Gegevens uit de klinische studie van Johnson & Johnson geven ook aan dat een niet-gevaccineerde persoon die eerder met SARS-CoV-2 is geïnfecteerd, 99,9% kans heeft om beschermd te worden tegen een nieuwe infectie. Opgemerkt moet worden dat op 1 juli 2021 177,4 miljoen SARS-CoV-2-infecties werden geregistreerd in de Verenigde Staten, wat overeenkomt met 53,8% van de Amerikaanse bevolking.26-36
HYPOTHESE: Van verplichte vaccins is aangetoond dat ze een veiligere omgeving creëren. |
FEIT # 20: Infectie en overdracht van SARS-CoV-2 komen in hoge mate voor bij volledig gevaccineerde populaties, en een aanzienlijk percentage van ernstige, kritieke en fatale gevallen van COVID-19 komt voor bij volledig gevaccineerde personen. Uit gegevens van de CDC blijkt dat massale vaccinatie met COVID-19-vaccins geen meetbare impact had op de COVID-19-sterfte in de Verenigde Staten. Bovendien geven gegevens van klinische onderzoeken op korte termijn aan dat 1 op de 6 tot 1 op de 9 mensen van 12 tot 55 jaar die het op mRNA gebaseerde COVID-19-vaccin krijgen, last heeft van ernstige (graad 3) systemische reacties.) en geen veiligheid op de lange termijn. onderzoeken zijn gedaan.13-37 Daarom tonen wetenschappelijke gegevens aan dat verplichte vaccinatie geen veiligere omgeving kan creëren.
Referenties
- Shitrit P, Zuckerman NS, Mor O, Gottesman BS, Chowers M. Nosocomiale uitbraak veroorzaakt door de SARS-CoV-2 Delta-variant in een sterk gevaccineerde populatie, Israël, juli 2021. Euro Surveill. 2021 sept; 26 (39). https://pubmed.ncbi.nlm.nih.gov/34596015/.
- Brown CM, Vostok J, Johnson H, Burns M, Gharpure R, Sami S, Sabo RT, Hall N, Foreman A, Schubert PL, Gallagher GR, Fink T, Madoff LC, Gabriel SB, MacInnis B, Park DJ, Siddle KJ , Harik V, Arvidson D, Brock-Fisher T, Dunn M, Kearns A, Laney AS. Uitbraak van SARS-CoV-2-infecties, waaronder doorbraakinfecties door COVID-19-vaccins, geassocieerd met grote openbare bijeenkomsten – Barnstable County, Massachusetts, juli 2021. MMWR Morb Mortal Wkly Rep. 2021 6 aug. 70 (31): 1059-62. https://www.cdc.gov/mmwr/volumes/70/wr/mm7031e2.htm?s_cid=mm7031e2_w.
- Subramanian SV, Kumar A. Verhogingen van COVID-19 houden geen verband met vaccinatieniveaus in 68 landen en 2947 provincies in de Verenigde Staten. Eur J Epidemiol. 2021 30 september: 1-4. https://pubmed.ncbi.nlm.nih.gov/34591202/.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Modern COVID-19-vaccin. Bijeenkomst van de adviescommissie voor vaccins en gerelateerde biologische producten: 17 december 2020. https://www.fda.gov/media/144434/download.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Janssen Ad26.COV2.S-vaccin voor de preventie van COVID-19. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 26 februari 2021. Tabel 22: werkzaamheid van het vaccin bij het eerste optreden van matige tot ernstige/kritieke en ernstige/kritieke COVID-19, inclusief niet-centraal bevestigde gevallen met aanvang van ten minste 14 of ten minste 28 dagen na vaccinatie, per land van deelname, per protocolset, studie 3001; 37. https://www.fda.gov/media/146217/download.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Pfizer-BioNTech COVID-19-vaccin. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 10 december 2020. https://www.fda.gov/media/144245/download.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. COVID-datatracker: trends in aantal COVID-19-gevallen en sterfgevallen in de VS gemeld aan CDC, per staat / territorium; [geciteerd 2022 april 2]. https://covid.cdc.gov/covid-data-tracker/#trends_totaldeaths.
- Amerikaanse Food and Drug Administration, Center for Biologics Evaluation and Research (CBER) Office of Vaccines Research and Review (OVRR). Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Wijziging toelating tot gebruik in noodgevallen (EUA) voor een niet-goedgekeurd product: beoordelingsmemorandum; 2021 9 april: 23, 39. https://www.fda.gov/media/148542/download.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: EUA-wijzigingsverzoek voor Pfizer-BioNTech COVID-19-vaccin voor gebruik bij kinderen van 5 tot en met 11 jaar. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 26 oktober 2021. https://www.fda.gov/media/153447/download.
- Wallace M. Beoordeling van aanbevelingen, beoordeling, ontwikkeling en evaluatie (GRADE): Pfizer-BioNTech COVID-19-vaccin. Werkgroep COVID-19 Vaccins van het Adviescomité voor immunisatiepraktijken (ACIP). Centrum voor ziektecontrole en Preventie. 2021 12 mei: 24, 25. https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-05-12/03-COVID-Wallace-508.pdf.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Beoordeling van aanbevelingen, beoordeling, ontwikkeling en evaluatie (GRADE): Pfizer-BioNTech COVID-19-vaccin voor personen van 12-15 jaar; [geciteerd op 2021 mei 14]. https://www.cdc.gov/vaccines/acip/recs/grade/covid-19-pfizer-biontech-vaccine-12-15-years.html#table03d.
- Pfizer. New York (NY): Pfizer Inc. Factsheet voor zorgverleners die vaccins toedienen (vaccinatieaanbieders); herzien 2022 jan. 3. Tabel 11: werkzaamheid van het vaccin - eerste optreden van COVID-19 vanaf 7 dagen na dosis 2: zonder bewijs van infectie en met of zonder bewijs van infectie vóór 7 dagen na dosis 2 - geblindeerde placebogecontroleerde follow-upperiode , adolescenten van 12 tot 15 jaar evalueerbare werkzaamheid (7 dagen) populatie; 48. https://www.fda.gov/media/153713/download.
- Artsen voor geïnformeerde toestemming. Pfizer COVID-19-vaccin: gegevens over werkzaamheid en veiligheid op korte termijn. december 2021. https://www.physiciansforinformedconsent.org/COVID-19-vaccines.
- Pfizer. New York (NY): Pfizer Inc. Factsheet voor zorgverleners die vaccins toedienen (vaccinatieaanbieders); herzien 2022 3 jan. 48. https://www.fda.gov/media/153713/download.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Wekelijkse updates op basis van geselecteerde demografische en geografische kenmerken: voorlopige sterftecijfers voor coronavirusziekte (COVID-19); [geciteerd nov 2021 3]. https://www.cdc.gov/nchs/nvss/vsrr/covid_weekly/index.htm#AgeAndSex.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Janssen Ad26.COV2.S-vaccin voor de preventie van COVID-19. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 26 februari 2021. https://www.fda.gov/media/146217/download.
- Pfizer. New York (NY): Pfizer Inc. Comirnaty (COVID-19-vaccin, mRNA) suspensie voor injectie, voor intramusculair gebruik; herzien 2021 dec. https://www.fda.gov/media/151707/download.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Aanvraag voor licentieverlening van een boosterdosis voor Comirnaty (COVID-19-vaccin, mRNA). Bijeenkomst van de adviescommissie voor vaccins en gerelateerde biologische producten: 17 september 2021. https://www.fda.gov/media/152176/download.
- Chua GT, Kwan MYW, Chui CSL, Smith RD, Cheung EC, Tian T, Leung MTY, Tsao SSL, Kan E, Ng WKC, Man Chan VC, Tai SM, Yu TC, Lee KP, Wong JSC, Lin YK, Shek CC, Leung ASY, Chow CK, Li KW, Ma J, Fung WY, Lee D, Ng MY, Wong WHS, Tsang HW, Kwok J, Leung D, Chung KL, Chow CB, Chan GCF, Leung WH, naar KKW, Yuen KY, Lau YL, Wong ICK, Ip P. Epidemiologie van acute myocarditis / pericarditis bij adolescenten in Hong Kong na vaccinatie met Comirnaty. Clin Infect Dis. 2021 28 nov: ciab989. https://pubmed.ncbi.nlm.nih.gov/34849657.
- Thomas SJ, Moreira ED Jr, Kitchin N, Absalon J, Gurtman A, Lockhart S, Perez JL, Pérez Marc G, Polack FP, Zerbini C, Bailey R, Swanson KA, Xu X, Roychoudhury S, Koury K, Bouguermouh S, Kalina WV, Cooper D, Frenck RW Jr, Hammitt LL, Türeci Ö, Nell H, Schaefer A, Ünal S, Yang Q, Liberator P, Tresnan DB, Mather S, Dormitzer PR, Şahin U, Gruber WC, Jansen KU; C4591001 Klinische proefgroep. Veiligheid en werkzaamheid van het BNT162b2-mRNA covid-19-vaccin gedurende 6 maanden. N Engl J Med. 2021 november 4; 385 (19): 1761-73. https://pubmed.ncbi.nlm.nih.gov/34525277.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: EUA-wijzigingsverzoek voor een boosterdosis voor het Janssen COVID-19-vaccin. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 15 oktober 2021, 21, 39. https://www.fda.gov/media/153037/download.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: EUA-wijzigingsverzoek voor een boosterdosis voor het Moderna COVID-19-vaccin. Bijeenkomst van de adviescommissie voor vaccins en gerelateerde biologische producten: 14 oktober 2021. https://www.fda.gov/media/152991/download.
- Horwitz LI, Jones SA, Cerfolio RJ, Francois F, Greco J, Rudy B, Petrilli CM. Trends in risicogecorrigeerde sterftecijfers voor COVID-19. J Hosp Med. 2021 februari, 16 (2): 90-2. https://www.journalofhospitalmedicine.com/jhospmed/article/230561/hospital-medicine/trends-covid-19-risk-adjusted-mortality-rates.
- Dennis JM, McGovern AP, Vollmer SJ, Mateen BA. Verbetering van de overleving van intensive care-patiënten met coronavirusziekte 2019 in Engeland: een nationale cohortstudie, maart tot juni 2020. Crit Care Med. 2021 februari 1; 49 (2): 209-14. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7803441/.
- Ioannidis, JPA. Verzoening van schattingen van wereldwijde verspreiding en sterftecijfers van COVID-19: een overzicht van systematische evaluaties. Eur J Clin Invest. 2021; 51: e13554. https://onlinelibrary.wiley.com/doi/epdf/10.1111/eci.13554.
- Artsen voor geïnformeerde toestemming. COVID-19 - Ziekte-informatieverklaring (DIS). Augustus 2021. https://physiciansforinformedconsent.org/covid-19/.
- C19early.com. Vroegtijdige behandeling van COVID-19: realtime analyse van 1,298 onderzoeken; [geciteerd 2022 januari 11]. https://c19early.com/.
- Regeneron. Tarrytown, (NY): Regeneron Pharmaceuticals, Inc. Factsheet voor zorgverleners: autorisatie voor noodgevallen (EUA) van REGEN-COV (casirivimab en imdevimab); herzien 2021 dec. https://www.regeneron.com/downloads/treatment-covid19-eua-fact-sheet-for-hcp.pdf.
- Lilly. Indianapolis (IN): Eli Lilly en Bedrijf. Neutraliserende antilichamen voor COVID-19; [geciteerd 2022 februari 9]. https://www.lilly.com/news/media/media-kits/bamlanivimab-covid19.
- GSK. Londen (VK): GlaxoSmithKline plc. GSK en Vir Biotechnology kondigen de Amerikaanse regeringsovereenkomst aan voor de aankoop van aanvullende leveringen van sotrovimab, goedgekeurd voor de vroege behandeling van COVID-19; 2022 11 januari [geciteerd 2022 februari 9]. https://www.gsk.com/en-gb/media/press-releases/gsk-and-vir-biotechnology-announce-united-states-government-agreement-to-purchase-additional-supply-of-sotrovimab.
- C19early.com. COVID-19-onderzoeken: ivermectine; [geciteerd 2022 februari 12]. https://c19ivermectin.com.
- Bryant A, Lawrie TA, Dowswell T, Fordham EJ, Mitchell S, Hill SR, Tham TC. Ivermectine voor preventie en behandeling van COVID-19-infectie: een systematische review, meta-analyse en sequentiële analyse van onderzoeken om klinische richtlijnen te informeren. Ben J Ther. 2021 juni 21;28 (4): e434-60. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8248252/.
- C19early.com. COVID-19-onderzoeken: vitamine D; [geciteerd 2022 februari 12]. https://c19vitamind.com.
- Ilie PC, Stefanescu S, Smith L. De rol van vitamine D bij de preventie van infectie en sterfte door coronavirusziekte 2019. Veroudering Clin Exp Res. 2020 juli; 32 (7): 1195-8. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7202265/.
- C19early.com. HCQ voor COVID-19: realtime meta-analyse van 303 onderzoeken; [geciteerd op 2022 januari 10]. https://hcqmeta.com.
- Raadgevend Comité van de Amerikaanse Food and Drug Administration, Vaccins en gerelateerde biologische producten. FDA-briefingdocument: Janssen Ad26.COV2.S-vaccin voor de preventie van COVID-19. Bijeenkomst van het Adviescomité voor vaccins en gerelateerde biologische producten: 26 februari 2021. Tabel 14: werkzaamheid van het vaccin bij het eerste optreden van matige tot ernstige/kritieke COVID-19, inclusief niet-centraal bevestigde gevallen, met aanvang ten minste 14 of ten minste 28 dagen na vaccinatie, op baseline SARS-CoV-2-status, per protocolset; 30. https://www.fda.gov/media/146217/download.
- El Sahly HM, Baden LR, Essink B, Doblecki-Lewis S, Martin JM, Anderson EJ, Campbell TB, Clark J, Jackson LA, Fichtenbaum CJ, Zervos M, Rankin B, Eder F, Feldman G, Kennelly C, Han- Conrad L, Levin M, Neuzil KM, Corey L, Gilbert P, Janes H, Follmann D, Marovich M, Polakowski L, Mascola JR, Ledgerwood JE, Graham BS, Augustus A, Clouting H, Deng W, Han S, Leav B , Manzo D, Pajon R, Schödel F, Tomassini JE, Zhou H, Miller J; COVE-studiegroep. Werkzaamheid van het mRNA-1273 SARS-CoV-2-vaccin na voltooiing van de geblindeerde fase. N Engl J Med. 2021 november 4; 385 (19): 1774-85. Aanvullende bijlage; 36-7. https://www.nejm.org/doi/suppl/10.1056/NEJMoa2113017/suppl_file/nejmoa2113017_appendix.pdf.
Artikel vertaald door Artsen voor geïnformeerde toestemming

