Kan het tetanusvaccin letsel en/of de dood veroorzaken?

Het volgende artikel probeert een licht te werpen op de enorme wereld van bijwerkingen, met een specifieke blik op die tegen tetanus, maar we raden u aan alle onderstaande aandachtspunten te lezen om de andere gerelateerde problemen te begrijpen, zoals het probleem van meerdere vaccins , de overgevoeligheid voor een of meer vaccinverbindingen, het wiegendoodprobleem en dat van adjuvantia. De meeste vaccins op de markt worden voor commerciële doeleinden geproduceerd in vaak meerdere formuleringen en dit maakt het onderwerp vaccinschade veel breder.
Het probleem van meerdere vaccins (klik om te openen)
Het probleem van meerdere vaccins

De huidige vaccinatiekalenders, vooral voor de pediatrische leeftijd, voorzien in de toediening van meerdere antigenen en vaccins in één enkele sessie, wat het comfort bevordert ten koste van de veiligheid. Om een specifieke toespraak te kunnen houden over de veiligheid van vaccins, moeten we noodzakelijkerwijs rekening houden met de complexiteit van het fenomeen en alle lezers adviseren om zich voldoende te informeren over alle aspecten van vaccinatie, voor- en nadelen.
Dr. Russell Blaylock, klinisch assistent-professor neurochirurgie aan het University of Mississippi Medical Center, heeft jarenlang "toxische synergie" bestudeerd en was in staat om te observeren dat wanneer twee zwak giftige pesticiden, waar geen van beide het syndroom van Parkinson kan veroorzaken bij proefdieren, met elkaar worden gecombineerd, kunnen de ziekte zelfs snel veroorzaken en vergelijkt dit fenomeen met dat van meerdere vaccins die tegelijkertijd worden toegediend: "Vaccinaties, als ze te talrijk en te dicht bij elkaar liggen, gedragen zich als een chronische ziekte".(A). Overige Twee onderzoeken hebben bevestigd dat plotselinge kindersterfte kan optreden na inenting van meerdere vaccins in een enkele toediening.(bc)
Een studie gepubliceerd in Human and Experimental Toxicology toonde aan dat landen die meer vaccins voorschrijven aan kinderen, een hogere kindersterfte hebben.(D) In de Verenigde Staten, waar kinderen 26 vaccins krijgen, sterven bijvoorbeeld meer dan 6 kinderen per 1000 levendgeborenen, terwijl in Zweden en Japan, waar 12 pediatrische vaccins worden toegediend, 3 sterfgevallen worden gemeld voor elke 1000 levendgeborenen. In de bovengenoemde studie wordt ook gekeken naar de link tussen vaccins en wiegendood.
Uit een Zwitserse studie gepubliceerd in 2005 in het European Journal of Pediatrics(E) we verkrijgen dat, met betrekking tot de effecten op te vroeg geboren baby's, de incidentie van recidiverende of verhoogde apneu en bradycardie na toediening van hexavalente vaccins 13% is. Datzelfde jaar publiceerde hetzelfde tijdschrift een Duitse studie die de plotselinge kindersterfte na hexavalent had onderzocht. De auteurs schrijven: «Deze resultaten, gebaseerd op spontane rapporten, bewijzen geen causaal verband tussen vaccinatie en wiegendood, maar vormen een signaal met betrekking tot een van de twee beschikbare hexavalenten; signaal dat moet leiden tot een intensivering van het toezicht op wiegendood na vaccinatie".(F)
In 2006 werd het gepubliceerd in het medische tijdschrift Vaccine(G) de brief van een team van onderzoekers van de Universiteit van München die melding maakten van «zes gevallen van plotselinge kindersterfte na hexavalente vaccinatie. Allen dood aangetroffen zonder uitleg 1-2 dagen na vaccinatie». Ze waren geclassificeerd als typische gevallen van wiegendood, maar de autoptische verificatie had neuropathologische en histologische afwijkingen aan het licht gebracht en alle kinderen vertoonden een significant hersenoedeem, waardoor ze een uitzondering vormden in vergelijking met de andere wiegendoodgevallen (Wiegendood). De onderzoekers schreven: “Voor de introductie van het hexavalente vaccin (in de jaren 1994-2000) hadden we het geval waargenomen van slechts één op de 198 kinderen met wiegendood die kort na de DTP-vaccinatie stierf. Maar tussen 2001 en 2004 hadden ze vijf van de 74 soortgelijke gevallen met wiegendood geïdentificeerd. Dat zou duiden op een dertienvoudige toename."
Ook in 2006 op Virchows Archief(H), schreef het team van het Instituut voor Pathologie van de Universiteit van Milaan: “Deskundigen van het Europees Agentschap voor de Evaluatie van Medische Producten hebben de mogelijkheid geanalyseerd dat er een verband bestaat tussen zeswaardige vaccins en sommige gevallen van overlijden. Onder de deelnemers bevonden zich pathologen met ervaring in vaccins en wiegendood die de autopsies uitvoerden, maar voor zover bekend werd er weinig aandacht besteed aan onderzoek van de hersenstam en het bloedhart op seriële secties en was er geen mogelijkheid om een triggerrol vast te stellen van het vaccin voor deze sterfgevallen. Hier rapporteren we het geval van een 3 maanden oud meisje dat plotseling stierf na hexavalente vaccinatie. Onderzoek van de hersenstam op seriële secties onthulde bilaterale arcuate nucleus hypoplasie. Het geleidingssysteem van het hart had aanhoudende foetale dispersie en degeneratie. Deze casus biedt een uniek inzicht in de mogelijke rol van het zeswaardige vaccin bij het veroorzaken van een dodelijk gevolg bij een kwetsbaar kind. Elk geval van plotseling en onverwacht overlijden dat zich kort na de geboorte of in de vroege kinderjaren voordoet, vooral na een vaccinatie, moet volgens de richtlijnen altijd een volledige autopsie ondergaan.
Referenties
- Blaylock R, "Vaccinaties: de verborgen gevaren", The Blaylock Wellness Report, mei 2004, pp.1-9
- Ottaviani G. et al., "Sudden infant death syndrome (SIDS) kort na hexavalente vaccinatie: een andere pathologie bij vermoedelijke wiegendood?", Virchows Archief, 2006, 448, blz. 100-104.
- Zinka B. et al., "Onverklaarde gevallen van plotselinge kindersterfte kort na zeswaardige vaccinatie", Vaccine, juli 2006, 24 (31-32), pp. 5779-5780.
- Miller NZ et al1. , "Kindersterfte daalde ten opzichte van het aantal routinematig toegediende vaccindoses: is er een biochemische of synergetische toxiciteit?", Hum. Exp. Toxicol., mei 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Het aluminium probleem (klik om te openen)
Aluminium in vaccins: wat ouders moeten weten

1. Wat is aluminium?
Aluminium is een zilverwit licht metaal, kneedbaar en resistent. Deze eigenschappen maken het bruikbaar in tal van industrieën en producten, waaronder machines, bouw, magazijnen, kookgerei, keukengerei, textiel, kleurstoffen en cosmetica. Aluminium is ook het meest voorkomende metaal in de aardkorst en vrijwel al het aluminium in de omgeving wordt in de bodem aangetroffen. Aluminium wordt echter van nature niet in significante hoeveelheden aangetroffen in levende organismen (zoals planten en dieren) en heeft geen bekende biologische functie. In de afgelopen eeuw heeft het gebruik van aluminium in sommige producten geleid tot een verhoogde blootstelling van de mens. De belangrijkste bronnen van blootstelling zijn aluminiumbevattende voedingsmiddelen (bijv. bakpoeder, bewerkte voedingsmiddelen, babyvoeding, enz.), medische producten (bijv. anti-transpiranten, maagzuurremmers, enz.), allergie-injecties en vaccins.1-3
2. Waarom is aluminium aanwezig in vaccins?
Sommige vaccins gebruiken aluminiumverbindingen (aluminiumhydroxide en aluminiumfosfaat) als hulpstoffen, dit zijn ingrediënten die de immuunrespons op een antigeen (vreemde stof) versterken.4-5 De Amerikaanse Food and Drug Administration (FDA) zegt dat als sommige vaccins geen aluminium bevatten, de immuunrespons die ze veroorzaken zou kunnen afnemen.6
3. Welke vaccins bevatten aluminium?
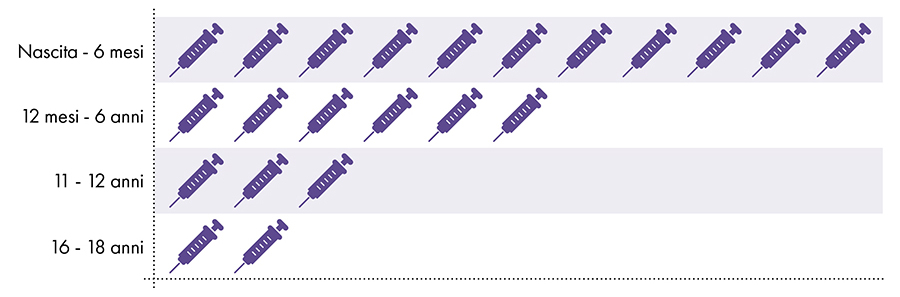
De volgende vaccins bevatten aluminium en worden gegeven aan zuigelingen, kinderen en adolescenten (Fig. 1):
- Hepatitis B (HepB)
- zeswaardig
- Difterie, tetanus en kinkhoest (DTaP en Tdap)
- Haemophilus influenzae type b (PedvaxHIB)
- Pneumokokken (PCV)
- Hepatitis A (HepA)
- Humaan papillomavirus (HPV)
- Meningokokken B (MenB)
Figuur 1: Er worden tot 18 doses aluminiumbevattende vaccins gegeven vanaf de geboorte tot 22 jaar7-8
4. Is blootstelling aan aluminium veilig?
De FDA beschouwt aluminium sinds 1975 als algemeen erkend als veilig (GRAS).9 Vóór 1990 was er echter geen technologie om nauwkeurig kleine hoeveelheden aluminium te detecteren die aan proefpersonen werden toegediend in wetenschappelijke studies.10 Bijgevolg was de hoeveelheid aluminium die kon worden geabsorbeerd voordat de bijwerkingen optreden, niet bekend.
Sinds de jaren negentig is dankzij technologische vooruitgang waargenomen dat de kleine hoeveelheden aluminium die in het menselijk lichaam achterblijven een aantal cellulaire en metabolische processen in het zenuwstelsel en weefsels van andere delen van het lichaam verstoren.1-10-11 De grootste negatieve effecten van aluminium zijn waargenomen in het zenuwstelsel en variëren van verminderde motoriek tot encefalopathie (veranderde mentale toestand, persoonlijkheidsveranderingen, denkproblemen, geheugenverlies, toevallen, coma en meer).2-12
Het Amerikaanse ministerie van Volksgezondheid en Human Services (HHS) erkent aluminium als een bekend neurotoxine.2 Bovendien heeft de FDA gewaarschuwd voor de risico's van aluminiumtoxiciteit bij zuigelingen en kinderen.13
FEDERAAL REGISTER: Het dagblad van de regering van de Verenigde Staten"Zelfs voldragen zuigelingen met een normale nierfunctie lopen mogelijk risico vanwege de snelle groei en onvolgroeidheid van de hersenen en het skelet, evenals onvolgroeidheid van de bloed-hersenbarrière. Tot de leeftijd van 1 of 2 hebben zuigelingen een lagere glomerulaire filtratiesnelheid dan volwassenen, wat hun nierfunctie beïnvloedt. Het bureau vreest dat jonge kinderen en mensen met een onvolgroeide nierfunctie een verhoogd risico lopen op blootstelling aan aluminium. " |
5. Hoeveel oraal aluminium is niet veilig?
In 2008 gebruikte het Agency for Toxic Substances and Disease Registry (ATSDR), een afdeling van HHS, onderzoeken naar de neurotoxische effecten van aluminium om vast te stellen dat niet meer dan 1 milligram (1.000 microgram) aluminium per kilogram lichaamsgewicht per dag vermijd de negatieve effecten van aluminium.2
6. Hoeveel aluminium geïnjecteerd is niet veilig?
Om de hoeveelheid aluminium te bepalen die veilig kan worden geïnjecteerd, is het noodzakelijk om de orale aluminiumlimiet van de ATSDR om te rekenen. De ATSDR-limiet voor oraal aluminium (1.000 microgram aluminium per kilogram lichaamsgewicht per dag) is gebaseerd op 0,1% van het orale aluminium dat in de bloedbaan wordt opgenomen, aangezien het spijsverteringskanaal bijna al het orale aluminium blokkeert.2 Omgekeerd, intramusculair geïnjecteerd aluminium omzeilt het spijsverteringskanaal en 100% van het aluminium kan in de loop van de tijd in de bloedbaan worden opgenomen (d.w.z. het geabsorbeerde aandeel aluminium is 1.000 keer groter). Om rekening te houden met deze verschillende hoeveelheden absorptie, moet de orale aluminiumlimiet van de ATSDR worden gedeeld door 1000. Deze conversie leidt tot een ATSDR-afgeleide bloedaluminiumlimiet van 1 microgram aluminium (0,1% van 1.000 microgram) per kilogram lichaamsgewicht per dag. Om de neurotoxische effecten van aluminium te voorkomen, mag daarom dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan terechtkomen. Figuur 3 toont de ATSDR-afgeleide bloedaluminiumlimiet voor zuigelingen van verschillende leeftijden op basis van hun gewicht.
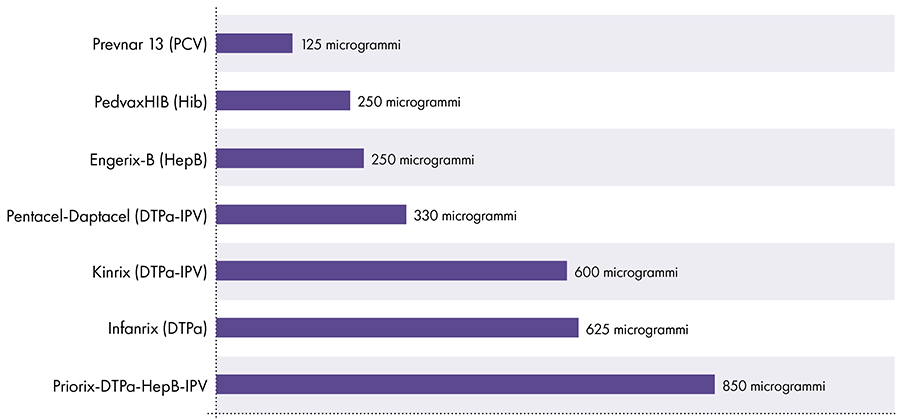
7. Hoeveel aluminium zit er in vaccins?
De hoeveelheid aluminium in vaccins varieert.16 In 1968 stelde de Amerikaanse federale overheid de limiet voor de hoeveelheid aluminium in vaccins op 850 microgram per dosis, gebaseerd op de hoeveelheid aluminium die nodig is om sommige vaccins effectief te maken.6-17 Bijgevolg varieert de hoeveelheid aluminium in aluminiumbevattende zuigelingenvaccins van 125 tot 850 microgram per dosis. Figuur 4 toont het aluminiumgehalte van één dosis van verschillende vaccins die aan kinderen worden gegeven.
8. Zijn er onderzoeken die de hoeveelheid aluminium in vaccins hebben vergeleken met de limiet die is afgeleid van de Agency for Toxic Substances and Disease Registry (ATSDR)?
In 2011 werd een studie gepubliceerd die tot doel had de hoeveelheid aluminium in vaccins te vergelijken met de door de ATSDR vastgestelde bloedstroomlimiet.18 Deze studie baseerde zijn berekeningen echter ten onrechte op 0,78% oraal aluminium dat in de bloedbaan werd opgenomen, in plaats van de 0,1% waarde die door de ATSDR in zijn berekeningen werd gebruikt.19-20 Als gevolg hiervan veronderstelde de studie van 2011 dat bijna 8 keer (0,78% / 0,1%) aluminium veilig in de bloedbaan kan komen, en dit heeft tot een onjuiste conclusie geleid.
9. Is blootstelling aan aluminium door vaccins veilig?
Vaccins worden intramusculair geïnjecteerd en de snelheid waarmee aluminium uit vaccins migreert van menselijke spieren naar de bloedbaan is onbekend. Dierstudies suggereren dat het een paar maanden tot meer dan een jaar kan duren voordat aluminium uit vaccins in de bloedbaan terechtkomt, vanwege meerdere variabelen.21-23 Aangezien de cumulatieve blootstelling aan aluminium uit vaccins bij kinderen jonger dan één jaar de door de ATSDR vastgestelde dagelijkse limiet met enkele honderden overschrijdt (Fig. 3 en 4), zou de limiet nog steeds worden overschreden als aluminium uit vaccins in de loop van de tijd in de bloedstroom zou komen van ongeveer een jaar. Bovendien hebben sommige onderzoeken aangetoond dat aluminium uit vaccins wordt geabsorbeerd door immuuncellen en delen van het lichaam bereikt die ver van de injectieplaats verwijderd zijn, inclusief de hersenen.24
De omvang van de bijwerkingen van aluminium in vaccins is niet bekend, aangezien er geen veiligheidsonderzoeken zijn uitgevoerd waarin een populatie die is gevaccineerd met aluminiumbevattende vaccins is vergeleken met een populatie die niet met dergelijke vaccins is gevaccineerd.
Aluminiumbeperking van de bloedstroom afgeleid van de ATSDR2-14-15
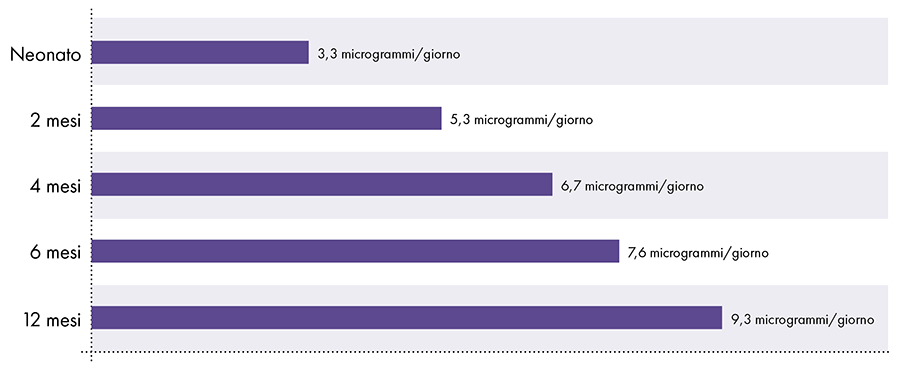 Afbeelding 3: Deze grafiek toont de aluminiumlimiet voor kinderen van verschillende leeftijden, zoals afgeleid van de Toxic Substances and Disease Registry, een afdeling van het Amerikaanse ministerie van Volksgezondheid en Human Services. De limiet geeft aan dat er dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan mag komen om de neurotoxische effecten van aluminium te voorkomen.
Afbeelding 3: Deze grafiek toont de aluminiumlimiet voor kinderen van verschillende leeftijden, zoals afgeleid van de Toxic Substances and Disease Registry, een afdeling van het Amerikaanse ministerie van Volksgezondheid en Human Services. De limiet geeft aan dat er dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan mag komen om de neurotoxische effecten van aluminium te voorkomen.
Hoeveelheid aluminium in vaccins
Referenties
- American Academy of Pediatrics, Comité voor voeding. Aluminiumtoxiciteit bij zuigelingen en kinderen. Kindergeneeskunde. 1996 maart; 97 (3): 413.
- Agentschap voor Toxic Substances and Disease Registry (ATSDR). Toxicologisch profiel voor aluminium. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Aluminium in voedsel — de aard en bijdrage van levensmiddelenadditieven. In: El-Samragy Y, redacteur. Additief voor levensmiddelen. Rijeka (Kroatië): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Naar een begrip van de adjuvante werking van aluminium. Nat Rev Immunol. april 2009; 9 (4): 287.
- Volk VK, Bunney WE. Difterie-immunisatie met vloeibaar toxoïde en met aluin neergeslagen toxoïde. Am J Volksgezondheid Volksgezondheid. juli 1942; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Aluminiumzouten in vaccins - Amerikaans perspectief. Vaccin. 2002 31 mei 20 Suppl 3: S18-22.
- Amerikaanse Food and Drug Administration. Silver Spring (MD): Amerikaanse Food and Drug Administration. Vaccins waarvoor een vergunning is verleend voor gebruik in de Verenigde Staten; [bijgewerkt 2018 februari 14; geciteerd 2018 februari 27. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Aanbevolen immunisatieschema voor kinderen en adolescenten van 18 jaar of jonger, Verenigde Staten, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Amerikaanse Food and Drug Administration. Silver Spring (MD): Amerikaanse Food and Drug Administration. SCOGS (Select Committee on GRAS Substances); [geciteerd 2018 aug. 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Priester N.D. Het biologische gedrag en de biologische beschikbaarheid van aluminium bij de mens, met speciale aandacht voor onderzoeken waarbij aluminium-26 als tracer wordt gebruikt: beoordeling en studie-update. J Omgeving Monit. 2004;6:376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminium in parenterale voedingsproducten voor kinderen: gemeten versus gelabelde inhoud. J Pediatr Pharmacol Ther. 2011;16 (2):92-7.
- Sedman A. Aluminiumtoxiciteit in de kindertijd. Pediatr Nephrol. 1992 juli;6 (4): 383-93.
- Amerikaanse Food and Drug Administration, ministerie van Volksgezondheid en Human Services. Regels en voorschriften. Fed-register. juni 2003; 68 (100): 34286.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Nationaal centrum voor gezondheidsstatistieken: gegevenstabel voor grafieken van lengte-naar-leeftijd en gewicht-naar-leeftijd voor jongens; [geciteerd op 2019 april 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. National Center for Health Statistics: gegevenstabel voor grafieken van lengte-naar-leeftijd en gewicht-naar-leeftijd van meisjes; [geciteerd op 2019 april 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Amerikaanse Food and Drug Administration, ministerie van Volksgezondheid en Human Services. Herziening van de eisen voor samenstellende materialen. Laatste regel. Fed-register. 2011 april 13; 76 (71): 20513-8.
- Bureau van de Federal Register, National Archives and Records Service, General Services Administration. Regels en voorschriften. Fed-register. 1968 jan; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie. Vaccin. 2011 november 28; 29 (51): 9538-43.
- Miller S, artsen voor geïnformeerde toestemming. Erratum in 'Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie.' In: ResearchGate. Berlijn (Duitsland): ResearchGate GmbH; 2020 maart 6 [geciteerd 2020 maart 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Artsen voor geïnformeerde toestemming. Newport Beach (CA): artsen voor geïnformeerde toestemming. Erratum in 'Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie'; [geciteerd 2020 maart 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, Witte JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In vivo absorptie van aluminiumbevattende vaccinadjuvantia met 26Al. Vaccin 1997 aug-sept; 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminiumtest en evaluatie van de lokale reactie op verschillende tijdstippen na intramusculaire toediening van aluminiumbevattende vaccins bij de Cynomolgus-aap. Vaccin. 2005 februari 3; 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminium in plasma en weefsels na intramusculaire injectie van menselijke vaccins met adjuvans bij ratten. Boog toxicol. 2019 okt; 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritische analyse van referentieonderzoeken naar de toxicokinetiek van op aluminium gebaseerde hulpstoffen. J Inorg Biochem. 2018 april 181: 87-95.
Artikel vertaald door Artsen voor geïnformeerde toestemming
Veel gepubliceerde onderzoeken hebben ernstige bijwerkingen gemeld na vaccinatie met tetanustoxoïd. Bijwerkingen zijn onder meer anafylaxie,(1-2) brachiale neuritis,(3) bulleus pemfigoïd(4-5-6) Guillain-Barre-syndroom (GBS),(7-8) acute gedissemineerde encefalomyelitis (ADEM),(9) erythema multiforme,(10-11-12) myocarditis,(13-14-15-16-17) artritis,(18-19) oogzenuwontsteking,(20-21) en andere auto-immuunziekten.(22-23)
De bijwerkingen gemeld na tetanusvaccinatie werden verzameld door een Duitse auteur(24) en door het monitoringsysteem voor bijwerkingen na immunisatie(25) en kan worden onderverdeeld in twee groepen: lokale bijwerkingen en systemische bijwerkingen.
We kunnen zeggen dat deze effecten afhankelijk zijn van verschillende factoren:
- leeftijd van de ontvanger van het vaccin;
- fysiologische en pathologische omstandigheden van de ontvanger van het vaccin;
- aantal ingenomen vaccindoses;
- hoeveelheid toegediend tetanustoxine;
- aanwezigheid van andere bacteriële en/of virale antigenen geassocieerd met tetanustoxine;
- aanwezigheid van hulpstoffen of andere bijbehorende toxische stoffen.
Er wordt aangenomen dat de ongewenste effecten die worden veroorzaakt door de eerste toediening van het tetanusvaccin, kunnen worden toegevoegd aan de bijwerkingen die kunnen optreden bij boosterdoses en als ze te vaak worden toegediend, een staat van hyperimmunisatie creëren die het risico op vaccinschade aanzienlijk verhoogt en om deze reden zijn er veel onderzoeken wetenschappers raden aan om geen boosters van dit vaccin toe te dienen met tussenpozen van minder dan 10 jaar.(26) Daarbij komt nog dat de pediatrische tetanusanatoxine in de gecombineerde vaccins groter is dan die gebruikt voor volwassenen, omdat het vanwege de onrijpheid van het immuunsysteem noodzakelijk is om de pasgeborene te overstimuleren om een adequate antilichaamrespons te verkrijgen.
De meest voorkomende en meestal mildere en voorbijgaande lokale bijwerkingen van tetanusvaccinatie(32) ze worden veroorzaakt door een bepaalde overgevoeligheid voor tetanustoxine en worden vertegenwoordigd door: pijn (50-85% van de gevallen), roodheid, verharding en zwelling (25-30% van de gevallen) zelfs tot abces.(27) In sommige gevallen waren de lokale reacties bijzonder ernstig, zoals het syndroom van Lyell (of scalded skin syndrome) met een sterftecijfer van 50% bij volwassenen en 25% bij kinderen.(28)
Alle lokale bijwerkingen komen vaker voor als het vaccin subcutaan wordt toegediend in plaats van intramusculair. Deze effecten nemen toe met toenemende hoeveelheid geïnoculeerd tetanustoxine(29) en dit komt vooral voor bij proefpersonen die meerdere en frequente injecties met tetanusvaccin hebben gehad.(30-27)
Een onderzoek uit 2017 toont aan dat bij kinderen met uitgebreide zwelling van de ledematen na ontvangst van de vierde dosis van het acellulaire difterie-tetanus-pertussis-vaccin, herhaling van de lokale reactie bijzonder vaak voorkwam na de vijfde dosis van het vaccin (78% van de gevaccineerden).(31)
Bijwerkingen nemen ook toe als het tetanusvaccin wordt gecombineerd met andere vaccins, in plaats van alleen te worden gebruikt.(32)
In 1994 rapporteerde het Amerikaanse Institute of Medicine (IOM) dat er overtuigend wetenschappelijk bewijs was om te concluderen dat tetanus-, DT- en Td-vaccins het Guillain-Barre-syndroom (GBS) kunnen veroorzaken, met inbegrip van overlijden, brachiale neuritis en overleden aan anafylaxie (shock). ).(33) De IOM erkende ook dat er een individuele gevoeligheid is voor vaccinreacties om genetische, biologische en omgevingsredenen, maar dat vaccinleveranciers niet nauwkeurig kunnen voorspellen wie door vaccinatie complicaties, verwondingen of overlijden zal oplopen voordat een vaccin wordt toegediend.(34)
In 2017 vergeleken Guinee-Bissau-onderzoekers de sterftecijfers van baby's die tussen 3 en 5 maanden oud waren gevaccineerd tegen difterie, tetanus en hele cellen pertussis (DTP) met die van baby's die nog niet waren gevaccineerd met het DTP-vaccin. sterftecijfers waren significant hoger bij zuigelingen die met de DTP waren gevaccineerd dan bij degenen die nog niet waren gevaccineerd. De onderzoekers merkten ook op dat als het orale poliovaccin (OPV) tegelijkertijd met het DTP-vaccin werd gegeven, de sterftecijfers door alle oorzaken daalden, maar nog steeds aanzienlijk hoger bleven dan bij niet-gevaccineerde kinderen.(35)
Een belangrijke lokale bijwerking die relatief vaak voorkomt bij volwassenen is neuropathie van de plexus brachialis,(36) als de inenting in de arm wordt uitgevoerd en enkele dagen of weken na vaccinatie verschijnt(37). Deze neuropathie wordt gekenmerkt door spierpijn, zwakte en spierafbraak. Naast de neuropathieën gelokaliseerd in het gebied waar het vaccin werd geïnoculeerd, vinden we in de literatuur ook diverse andere meldingen van gelokaliseerde neuropathieën veroorzaakt door de anti-tetanustoediening,(38-39) zoals de betrokkenheid van verschillende hersenzenuwen(40-41) of oogzenuwen(42) of de terugkerende larynxzenuw.(43)
De meest voorkomende systemische effecten van tetanusvaccinatie(32) kan worden onderverdeeld in:
- niet-specifieke effecten, zoals koorts, hoofdpijn (een vrij vaak voorkomende bijwerking na vaccinatie), spierpijn, netelroos, misselijkheid, braken,(44) asthenie, anorexia, prikkelbaarheid, slaperigheid,
- specifieke effecten, zoals anafylactische shock, gegeneraliseerde neuropathie, intense buikpijn met diarree, verschillende ontstekingsvormen, zelfs ernstige, en in sommige zeldzame gevallen zelfs de dood.
Onder alle meest voorkomende en talrijke systemische effecten vinden we neurologische schade(45) en onder deze moet polyneuropathie die het perifere zenuwstelsel aantast zeker op de eerste plaats komen.Het komt vaker voor dan de betrokkenheid van het centrale zenuwstelsel en kan zowel na de eerste dosis van het vaccin als na de derde dosis optreden.(46) Polyneuropathie treedt meestal op binnen enkele minuten tot enkele uren (in het geval van acute allergische reacties) of binnen 12-48 uur (in het geval van vertraagde allergische reacties) of hoogstens binnen 4-14 dagen na inenting (in het geval van neuritis).(47) Polyneuropathie kan enkele zenuwen of grote delen van het lichaam aantasten tot aan de medulla en de hersenschors en kan alleen worden veroorzaakt door het tetanusvaccin(48) of door de toediening van andere vaccins in combinatie met die van tetanus.(36-49)
Van de verschillende vormen van polyneuropathie zijn de volgende gerapporteerd: demyeliniserende polyneuropathie;(50) asymmetrische polyneuropathie; polyradiculoneuritis met blaas- en rectale parese;(51) scarlatiniforme uitslag,(40) acute urticariële reacties,(44) verlamming van de ademhalingszenuwen (Landry's palsy), die ook tot de dood kan leiden;(52-53) tetanische spasmen;(44) transversale myelitis;(54) sindroom van Guillain-Barré;(55-56) perifere motorische afasie;(57) en dood.(28)
Referenties (klik om te openen)
- Mayorga C, Torres MJ, Corzo JL et al. Onmiddellijke allergie voor tetanustoxoïdvaccin: bepaling van immunoglobuline E- en immunoglobuline G-antilichamen tegen allergene eiwitten. Ann Allergie Astma Immunol. 2003 Feb;90(2):238-43.
- Martín-Muñoz MF, Pereira MJ, Posadas S et al. Anafylactische reactie op het difterie-tetanusvaccin bij een kind: specifieke IgE/IgG-bepalingen en kruisreactiviteitsonderzoeken. Vaccin. 2002 Sep 10;20(27-28):3409-12.
- Hamati-Haddad A, Fenichel GM. Brachiale neuritis na routinematige kinderimmunisatie voor difterie, tetanus en kinkhoest (DTP): rapport van twee gevallen en overzicht van de literatuur. Kindergeneeskunde. 1997 Apr;99(4):602-3.
- Fournier B, Descamps V, Bouscarat F et al. Bulleus pemfigoïd geïnduceerd door vaccinatie. Br J Dermatol. 1996 Jul;135(1):153-4.
- Venning VA, Wojnarowska F. Geïnduceerd gewelddadig pemfigoïd. Br J Dermatol. 1995 May;132(5):831-2.
- Sezin T, Egozi E, Hillou W et al. Anti-laminine-332 slijmvliespemfigoïd ontwikkelt zich na een vaccinatie tegen difterie en tetanus. JAMA-dermatol. 2013 Jul;149(7):858-62.
- Bakshi R., Graves MC. Guillain-Barré-syndroom na gecombineerde tetanus-difterietoxoïdvaccinatie. J Neurol Wetenschap. 1997 Apr 15;147(2):201-2.
- Newton N Jr., Janati A. Guillain-Barré-syndroom na vaccinatie met gezuiverd tetanustoxoïd. Zuid Med J. 1987 Aug;80(8):1053-4.
- Hamidon BB, Raymond AA. Acute gedissemineerde encefalomyelitis (ADEM) die zich presenteert met epileptische aanvallen secundair aan vaccinatie tegen tetanustoxine. Med J Maleisië. 2003 Dec;58(5):780-2.
- Griffith RD, molenaar van III Erythema multiforme na difterie- en tetanustoxoïdvaccinatie. J Ben Acad Dermatol. 1988 Oct;19(4):758-9.
- Frederiksen MS, Brenøe E, Trier J. Erythema multiforme minor na vaccinatie met pediatrische vaccins. Scan J Infect Dis. 2004;36(2):154-5.
- Kaur S, Handa S. Erythema multiforme na vaccinatie bij een zuigeling. Indiase J Dermatol Venereol Leprol. 2008 May-Jun;74(3):251-3.
- Kumar V, Sidhu N, Roy S, Gaurav K. Myocarditis na vaccinatie tegen difterie, kinkhoest met hele cellen en tetanustoxoïdvaccinatie bij een jonge baby. Ann Pediatr Cardio. 2018 May-Aug;11(2):224-226
- Yamamoto H, Hashimoto T, Ohta-Ogo K, et al. Een geval van door biopsie bewezen eosinofiele myocarditis gerelateerd aan tetanustoxoïd-immunisatie. Cardiovasculaire Pathol. 2018 nov - dec;37:54-57
- Wu SJ, Sun S, Li JY et al. Acute fulminante myocarditis na vaccinatie tegen difterie, polio en tetanus. Aziatische cardiovasculaire thorax Ann. 2006 Dec;14(6):e111-2.
- Dilber E, Karagöz T, Aytemir K et al. Acute myocarditis geassocieerd met tetanusvaccinatie. Mayo Clin Proc. 2003 Nov;78(11):1431-3.
- Amsel SG, Hanukoglu A, Fried D, Wolyvovics M Myocarditis na drievoudige immunisatie. Aarts Dis Kind. 1986 april; 61 (4): 403-405.
- Jawad AS, Scott DG Immunisatie die reumatoïde artritis veroorzaakt? Ann Reum Dis. februari 1989; 48(2):174.
- Kaul A, Adler M, Alokaily F, Jawad A Herhaling van reactieve artritis na een boosterdosis tetanustoxoïd Ann Reum Dis. februari 2002; 61(2):185.
- O'Brien P, Wong RW Optische neuritis na difterie, tetanus, kinkhoest en geïnactiveerd poliovirus gecombineerde vaccinatie: een casusrapport. J Med Case Rep. 2018 Nov 30;12(1):356
- Cabrera-Maqueda JM, Hernández-Clares R, Baidez-Guerrero AE et al. Optische neuritis tijdens de zwangerschap na Tdap-vaccinatie: rapport van twee gevallen. Clin Neurol Neurochirurg. 2017 september;160:116-118.
- Ruhrman-Shahar N, Torres-Ruiz J, Rotman-Pikielny P, Levy Y Auto-immuunreactie na vaccinatie tegen tetanus - beschrijving van vier gevallen en literatuuroverzicht. Immunol Res. 2017 Feb;65(1):157-163.
- Shoenfeld Y, Aron-Maor A. Vaccinatie en auto-immuniteit - 'vaccinose': een gevaarlijke verbinding? J auto-immuun. 2000 Feb;14(1):1-10.
- Bijwerkingen van medicijnen Jaarlijks. Deel 12. (Elsevier, 988).
- Bijwerkingen van medicijnen Jaarlijks. Deel 13. (Elsevier, 1989).
- Adebahr, G. [Dood door shock bij eerste preventieve subcutane injectie van tetanusserum]. Dtsch. Z. Gesamte Gerichtl. Med.41, 405-8 (1952).
- Bijwerkingen van medicijnen jaarlijks. Deel 11. (Elsevier, 1987).
- Frank, K.-H. Todliche Imptkomplikationen (Lyell-Syndrom) voor Tetatoxoid. Dt.Gesundh.wes. 29, 1430-4 (1974).
- Relihan, M. Reacties op tetanustoxoïd. J. Jr. Med. Assoc. 62, 430-4 (1969).
- Levine, L., Ipsen, J. & McComb, J. Immunisatie voor volwassenen. Bereiding en evaluatie van gecombineerde vloeibare tetanus- en difterietoxoïden voor gebruik door volwassenen. Ben J. Hyg. 73, 20 (1961).
- Zafack, JG et al. Risico op herhaling van bijwerkingen na immunisatie: een systematische review. Kindergeneeskunde 140, (2017).
- Cody, CL, Baraff, LJ, Cherry, JD, Marcy, SM & Manclark, CR Aard en snelheid van bijwerkingen geassocieerd met DTP- en DT-immunisaties bij zuigelingen en kinderen. Kindergeneeskunde 68, 650-60 (1981).
- Institute of Medicine Committee om bijwerkingen van vaccins te beoordelen. Bijwerkingen van vaccins: bewijs en causaliteit. (Evaluatie van biologische mechanismen voor bijwerkingen: verhoogde vatbaarheid). Washington, DC: De National Academies Press. 1994. Hoofdstuk 5 Difterie en tetanustoxoïden blz. 67 - 117
- Institute of Medicine Committee om bijwerkingen van vaccins te beoordelen. Bijwerkingen van vaccins: bewijs en causaliteit. (Evaluatie van biologische mechanismen voor bijwerkingen: verhoogde vatbaarheid). Washington, DC: De National Academies Press. 2012
- Mogensen SW, Andersen A, Rodrigues A et al. De introductie van difterie-tetanus-kinkhoest en oraal poliovaccin bij jonge zuigelingen in een stedelijke Afrikaanse gemeenschap: een natuurlijk experiment. EBioGeneeskunde. 2017 mrt; 17: 192-198.
- Tsairis, P., Dyck, PJ & Mulder, DW Natuurlijke geschiedenis van neuropathie van de plexus brachialis. Rapport van 99 patiënten. Arch. Neuro/. 27, 09-17 (1972).
- Blumstein, GI & Kreithen, H. Perifere neuropathie na toediening van tetanustoxoïd. JAMA 198, I 030-1 (1966)
- Gersbach, P. & Waridel, D. [Verlamming na tetanuspreventie]. Zwitserland. Med Wochenschr. 106, 150-3 (1976).
- Baust, W., Meyer, D. & Wachsmuth, W. Perifere neuropathie na toediening van tetanustoxoïd. J.Neur/. 222, 131-33 (1979).
- Cutter, R. Betrokkenheid van de gehoorzenuw na tetanus-antitoxine: eerste gemelde casus. J Am Med Ass 106, I006-7 (I 936).
- Wirth, G. Omkeerbare ziekteverwekker na tetanus-injectie. Munch Med Wschr 101, 349-81 (1965).
- Harrer, G., Melnizky, V. & Wendt, H. Akkomodationssparese en Schlucklahmung nach Tetanus-Toxoid-Auffrlschungsimpfung. Wien Med Wochenschr 15, 296-7 (1971)
- Basek, M. Eenzijdig! verlamming van de stembanden na toediening van tetanus-antitoxine (TAT). Laryngoscoop 68, 805-807 (1958).
- Cunningham, AA Anafylaxie na injectie van tetanustoxoïde. Br. Med. J. 2, 522-3 (1940).
- Ridder. Plexuslahmung nach Schutzimpfung met Tetanusserum. Munch. med. Wsch. 81, 1035 (1934).
- Holliday, PL & Bauer, RB Polyradiculoneuritis secundair aan immunisatie met tetanus- en difterietoxoïden. Arch Neuro/40, 56-57 (1983).
- Ehrengut, W. Reaktionen der Wundstarrkrampfimpfung. Dtsch Med Wochenschr 95, 1799-1800 (1970).
- 1Woolling, KR & Rushton, JG Serumneuritis; verslag van twee gevallen en kort overzicht van het syndroom. Aarts Neuro/. Psychiatry 64, 568-73 (1950).
- Martin, GI & Weintraub, MI Brachiale neuritis en verlamming van de zevende zenuw: een zeldzaam gevaar van DPT-vaccinatie. Clin. Kinderarts. (fila). 12, 506-507 (1973).
- Pollard, JD & Selby, G. Terugkerende neuropathie als gevolg van tetanustoxoïde. Verslag van een zaak. J.Neur/. Sci.37, 113-125 (1978).
- Bijwerkingen van medicijnen annua/. Deel 09. (Elsevier, 1985).
- Harrfeldt, HP [Dood na actieve en passieve tetanusimmunisatie]. Monatsschr. Unfallheilkd. Versicherungsmed. 66, 36-7 (1963).
- Elsasser, G. Zur Entstehung, Localization und Verhiitung der Serumpolyneuritis. Nervenarzt 15, 280 (1942).
- Whittle, E. & Robertson, NR Transverse myelitis na difterie-, tetanus- en polio-immunisatie. Br. Med. J. 1, 1450 (1977).
- Bijwerkingen van medicijnen annua/. Deel 14. (Elsevier, 1990).
- Hopf, HC [Guillain-Barré-syndroom na toediening van tetanustoxoïd. Onderzoek en verslag van een zaak]. Aktuelle Neuro/. 7, 195-200 (1980).
- Palfty, GF & Merei, T. Geen titel. orv. Hetil. 102, 2321 (1961).
Dit artikel is samengevat en vertaald door National Vaccine Information Center.

