Kan het Hepatitis B-vaccin letsel en/of de dood veroorzaken?

BELANGRIJKE OPMERKING: Corvelva nodigt u uit om diepgaande informatie te krijgen door alle secties en links te lezen, evenals de productfolders en technische gegevensbladen van de fabrikant, en om met een of meer vertrouwde professionals te spreken voordat u besluit uzelf of uw kind te vaccineren. Deze informatie is alleen voor informatieve doeleinden en is niet bedoeld als medisch advies.
Het probleem van meerdere vaccins (klik om te openen)
Het probleem van meerdere vaccins

De huidige vaccinatiekalenders, vooral voor de pediatrische leeftijd, voorzien in de toediening van meerdere antigenen en vaccins in één enkele sessie, wat het comfort bevordert ten koste van de veiligheid. Om een specifieke toespraak te kunnen houden over de veiligheid van vaccins, moeten we noodzakelijkerwijs rekening houden met de complexiteit van het fenomeen en alle lezers adviseren om zich voldoende te informeren over alle aspecten van vaccinatie, voor- en nadelen.
Dr. Russell Blaylock, klinisch assistent-professor neurochirurgie aan het University of Mississippi Medical Center, heeft jarenlang "toxische synergie" bestudeerd en was in staat om te observeren dat wanneer twee zwak giftige pesticiden, waar geen van beide het syndroom van Parkinson kan veroorzaken bij proefdieren, met elkaar worden gecombineerd, kunnen de ziekte zelfs snel veroorzaken en vergelijkt dit fenomeen met dat van meerdere vaccins die tegelijkertijd worden toegediend: "Vaccinaties, als ze te talrijk en te dicht bij elkaar liggen, gedragen zich als een chronische ziekte".(A). Overige Twee onderzoeken hebben bevestigd dat plotselinge kindersterfte kan optreden na inenting van meerdere vaccins in een enkele toediening.(bc)
Een studie gepubliceerd in Human and Experimental Toxicology toonde aan dat landen die meer vaccins voorschrijven aan kinderen, een hogere kindersterfte hebben.(D) In de Verenigde Staten, waar kinderen 26 vaccins krijgen, sterven bijvoorbeeld meer dan 6 kinderen per 1000 levendgeborenen, terwijl in Zweden en Japan, waar 12 pediatrische vaccins worden toegediend, 3 sterfgevallen worden gemeld voor elke 1000 levendgeborenen. In de bovengenoemde studie wordt ook gekeken naar de link tussen vaccins en wiegendood.
Uit een Zwitserse studie gepubliceerd in 2005 in het European Journal of Pediatrics(E) we verkrijgen dat, met betrekking tot de effecten op te vroeg geboren baby's, de incidentie van recidiverende of verhoogde apneu en bradycardie na toediening van hexavalente vaccins 13% is. Datzelfde jaar publiceerde hetzelfde tijdschrift een Duitse studie die de plotselinge kindersterfte na hexavalent had onderzocht. De auteurs schrijven: «Deze resultaten, gebaseerd op spontane rapporten, bewijzen geen causaal verband tussen vaccinatie en wiegendood, maar vormen een signaal met betrekking tot een van de twee beschikbare hexavalenten; signaal dat moet leiden tot een intensivering van het toezicht op wiegendood na vaccinatie".(F)
In 2006 werd het gepubliceerd in het medische tijdschrift Vaccine(G) de brief van een team van onderzoekers van de Universiteit van München die melding maakten van «zes gevallen van plotselinge kindersterfte na hexavalente vaccinatie. Allen dood aangetroffen zonder uitleg 1-2 dagen na vaccinatie». Ze waren geclassificeerd als typische gevallen van wiegendood, maar de autoptische verificatie had neuropathologische en histologische afwijkingen aan het licht gebracht en alle kinderen vertoonden een significant hersenoedeem, waardoor ze een uitzondering vormden in vergelijking met de andere wiegendoodgevallen (Wiegendood). De onderzoekers schreven: “Voor de introductie van het hexavalente vaccin (in de jaren 1994-2000) hadden we het geval waargenomen van slechts één op de 198 kinderen met wiegendood die kort na de DTP-vaccinatie stierf. Maar tussen 2001 en 2004 hadden ze vijf van de 74 soortgelijke gevallen met wiegendood geïdentificeerd. Dat zou duiden op een dertienvoudige toename."
Ook in 2006 op Virchows Archief(H), schreef het team van het Instituut voor Pathologie van de Universiteit van Milaan: “Deskundigen van het Europees Agentschap voor de Evaluatie van Medische Producten hebben de mogelijkheid geanalyseerd dat er een verband bestaat tussen zeswaardige vaccins en sommige gevallen van overlijden. Onder de deelnemers bevonden zich pathologen met ervaring in vaccins en wiegendood die de autopsies uitvoerden, maar voor zover bekend werd er weinig aandacht besteed aan onderzoek van de hersenstam en het bloedhart op seriële secties en was er geen mogelijkheid om een triggerrol vast te stellen van het vaccin voor deze sterfgevallen. Hier rapporteren we het geval van een 3 maanden oud meisje dat plotseling stierf na hexavalente vaccinatie. Onderzoek van de hersenstam op seriële secties onthulde bilaterale arcuate nucleus hypoplasie. Het geleidingssysteem van het hart had aanhoudende foetale dispersie en degeneratie. Deze casus biedt een uniek inzicht in de mogelijke rol van het zeswaardige vaccin bij het veroorzaken van een dodelijk gevolg bij een kwetsbaar kind. Elk geval van plotseling en onverwacht overlijden dat zich kort na de geboorte of in de vroege kinderjaren voordoet, vooral na een vaccinatie, moet volgens de richtlijnen altijd een volledige autopsie ondergaan.
Referenties
- Blaylock R, "Vaccinaties: de verborgen gevaren", The Blaylock Wellness Report, mei 2004, pp.1-9
- Ottaviani G. et al., "Sudden infant death syndrome (SIDS) kort na hexavalente vaccinatie: een andere pathologie bij vermoedelijke wiegendood?", Virchows Archief, 2006, 448, blz. 100-104.
- Zinka B. et al., "Onverklaarde gevallen van plotselinge kindersterfte kort na zeswaardige vaccinatie", Vaccine, juli 2006, 24 (31-32), pp. 5779-5780.
- Miller NZ et al1. , "Kindersterfte daalde ten opzichte van het aantal routinematig toegediende vaccindoses: is er een biochemische of synergetische toxiciteit?", Hum. Exp. Toxicol., mei 2011.
- https://pubmed.ncbi.nlm.nih.gov/15843978/
- https://pubmed.ncbi.nlm.nih.gov/15602672/
- https://pubmed.ncbi.nlm.nih.gov/15908063/
- https://pubmed.ncbi.nlm.nih.gov/16231176/
Het aluminium probleem (klik om te openen)
Aluminium in vaccins: wat ouders moeten weten

1. Wat is aluminium?
Aluminium is een zilverwit licht metaal, kneedbaar en resistent. Deze eigenschappen maken het bruikbaar in tal van industrieën en producten, waaronder machines, bouw, magazijnen, kookgerei, keukengerei, textiel, kleurstoffen en cosmetica. Aluminium is ook het meest voorkomende metaal in de aardkorst en vrijwel al het aluminium in de omgeving wordt in de bodem aangetroffen. Aluminium wordt echter van nature niet in significante hoeveelheden aangetroffen in levende organismen (zoals planten en dieren) en heeft geen bekende biologische functie. In de afgelopen eeuw heeft het gebruik van aluminium in sommige producten geleid tot een verhoogde blootstelling van de mens. De belangrijkste bronnen van blootstelling zijn aluminiumbevattende voedingsmiddelen (bijv. bakpoeder, bewerkte voedingsmiddelen, babyvoeding, enz.), medische producten (bijv. anti-transpiranten, maagzuurremmers, enz.), allergie-injecties en vaccins.1-3
2. Waarom is aluminium aanwezig in vaccins?
Sommige vaccins gebruiken aluminiumverbindingen (aluminiumhydroxide en aluminiumfosfaat) als hulpstoffen, dit zijn ingrediënten die de immuunrespons op een antigeen (vreemde stof) versterken.4-5 De Amerikaanse Food and Drug Administration (FDA) zegt dat als sommige vaccins geen aluminium bevatten, de immuunrespons die ze veroorzaken zou kunnen afnemen.6
3. Welke vaccins bevatten aluminium?
De volgende vaccins bevatten aluminium en worden gegeven aan zuigelingen, kinderen en adolescenten (Fig. 1):
- Hepatitis B (HepB)
- zeswaardig
- Difterie, tetanus en kinkhoest (DTaP en Tdap)
- Haemophilus influenzae type b (PedvaxHIB)
- Pneumokokken (PCV)
- Hepatitis A (HepA)
- Humaan papillomavirus (HPV)
- Meningokokken B (MenB)
Figuur 1: Er worden tot 18 doses aluminiumbevattende vaccins gegeven vanaf de geboorte tot 22 jaar7-8
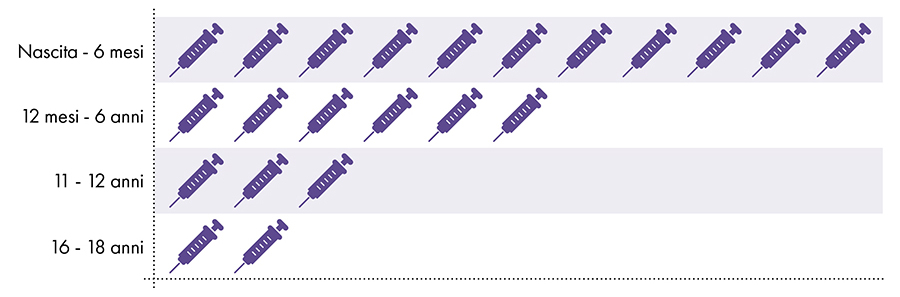
4. Is blootstelling aan aluminium veilig?
De FDA beschouwt aluminium sinds 1975 als algemeen erkend als veilig (GRAS).9 Vóór 1990 was er echter geen technologie om nauwkeurig kleine hoeveelheden aluminium te detecteren die aan proefpersonen werden toegediend in wetenschappelijke studies.10 Bijgevolg was de hoeveelheid aluminium die kon worden geabsorbeerd voordat de bijwerkingen optreden, niet bekend.
Sinds de jaren negentig is dankzij technologische vooruitgang waargenomen dat de kleine hoeveelheden aluminium die in het menselijk lichaam achterblijven een aantal cellulaire en metabolische processen in het zenuwstelsel en weefsels van andere delen van het lichaam verstoren.1-10-11 De grootste negatieve effecten van aluminium zijn waargenomen in het zenuwstelsel en variëren van verminderde motoriek tot encefalopathie (veranderde mentale toestand, persoonlijkheidsveranderingen, denkproblemen, geheugenverlies, toevallen, coma en meer).2-12
Het Amerikaanse ministerie van Volksgezondheid en Human Services (HHS) erkent aluminium als een bekend neurotoxine.2 Bovendien heeft de FDA gewaarschuwd voor de risico's van aluminiumtoxiciteit bij zuigelingen en kinderen.13
FEDERAAL REGISTER: Het dagblad van de regering van de Verenigde Staten"Zelfs voldragen zuigelingen met een normale nierfunctie lopen mogelijk risico vanwege de snelle groei en onvolgroeidheid van de hersenen en het skelet, evenals onvolgroeidheid van de bloed-hersenbarrière. Tot de leeftijd van 1 of 2 hebben zuigelingen een lagere glomerulaire filtratiesnelheid dan volwassenen, wat hun nierfunctie beïnvloedt. Het bureau vreest dat jonge kinderen en mensen met een onvolgroeide nierfunctie een verhoogd risico lopen op blootstelling aan aluminium. " |
5. Hoeveel oraal aluminium is niet veilig?
In 2008 gebruikte het Agency for Toxic Substances and Disease Registry (ATSDR), een afdeling van HHS, onderzoeken naar de neurotoxische effecten van aluminium om vast te stellen dat niet meer dan 1 milligram (1.000 microgram) aluminium per kilogram lichaamsgewicht per dag vermijd de negatieve effecten van aluminium.2
6. Hoeveel aluminium geïnjecteerd is niet veilig?
Om de hoeveelheid aluminium te bepalen die veilig kan worden geïnjecteerd, is het noodzakelijk om de orale aluminiumlimiet van de ATSDR om te rekenen. De ATSDR-limiet voor oraal aluminium (1.000 microgram aluminium per kilogram lichaamsgewicht per dag) is gebaseerd op 0,1% van het orale aluminium dat in de bloedbaan wordt opgenomen, aangezien het spijsverteringskanaal bijna al het orale aluminium blokkeert.2 Omgekeerd, intramusculair geïnjecteerd aluminium omzeilt het spijsverteringskanaal en 100% van het aluminium kan in de loop van de tijd in de bloedbaan worden opgenomen (d.w.z. het geabsorbeerde aandeel aluminium is 1.000 keer groter). Om rekening te houden met deze verschillende hoeveelheden absorptie, moet de orale aluminiumlimiet van de ATSDR worden gedeeld door 1000. Deze conversie leidt tot een ATSDR-afgeleide bloedaluminiumlimiet van 1 microgram aluminium (0,1% van 1.000 microgram) per kilogram lichaamsgewicht per dag. Om de neurotoxische effecten van aluminium te voorkomen, mag daarom dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan terechtkomen. Figuur 3 toont de ATSDR-afgeleide bloedaluminiumlimiet voor zuigelingen van verschillende leeftijden op basis van hun gewicht.
7. Hoeveel aluminium zit er in vaccins?
De hoeveelheid aluminium in vaccins varieert.16 In 1968 stelde de Amerikaanse federale overheid de limiet voor de hoeveelheid aluminium in vaccins op 850 microgram per dosis, gebaseerd op de hoeveelheid aluminium die nodig is om sommige vaccins effectief te maken.6-17 Bijgevolg varieert de hoeveelheid aluminium in aluminiumbevattende zuigelingenvaccins van 125 tot 850 microgram per dosis. Figuur 4 toont het aluminiumgehalte van één dosis van verschillende vaccins die aan kinderen worden gegeven.
8. Zijn er onderzoeken die de hoeveelheid aluminium in vaccins hebben vergeleken met de limiet die is afgeleid van de Agency for Toxic Substances and Disease Registry (ATSDR)?
In 2011 werd een studie gepubliceerd die tot doel had de hoeveelheid aluminium in vaccins te vergelijken met de door de ATSDR vastgestelde bloedstroomlimiet.18 Deze studie baseerde zijn berekeningen echter ten onrechte op 0,78% oraal aluminium dat in de bloedbaan werd opgenomen, in plaats van de 0,1% waarde die door de ATSDR in zijn berekeningen werd gebruikt.19-20 Als gevolg hiervan veronderstelde de studie van 2011 dat bijna 8 keer (0,78% / 0,1%) aluminium veilig in de bloedbaan kan komen, en dit heeft tot een onjuiste conclusie geleid.
9. Is blootstelling aan aluminium door vaccins veilig?
Vaccins worden intramusculair geïnjecteerd en de snelheid waarmee aluminium uit vaccins migreert van menselijke spieren naar de bloedbaan is onbekend. Dierstudies suggereren dat het een paar maanden tot meer dan een jaar kan duren voordat aluminium uit vaccins in de bloedbaan terechtkomt, vanwege meerdere variabelen.21-23 Aangezien de cumulatieve blootstelling aan aluminium uit vaccins bij kinderen jonger dan één jaar de door de ATSDR vastgestelde dagelijkse limiet met enkele honderden overschrijdt (Fig. 3 en 4), zou de limiet nog steeds worden overschreden als aluminium uit vaccins in de loop van de tijd in de bloedstroom zou komen van ongeveer een jaar. Bovendien hebben sommige onderzoeken aangetoond dat aluminium uit vaccins wordt geabsorbeerd door immuuncellen en delen van het lichaam bereikt die ver van de injectieplaats verwijderd zijn, inclusief de hersenen.24
De omvang van de bijwerkingen van aluminium in vaccins is niet bekend, aangezien er geen veiligheidsonderzoeken zijn uitgevoerd waarin een populatie die is gevaccineerd met aluminiumbevattende vaccins is vergeleken met een populatie die niet met dergelijke vaccins is gevaccineerd.
Aluminiumbeperking van de bloedstroom afgeleid van de ATSDR2-14-15
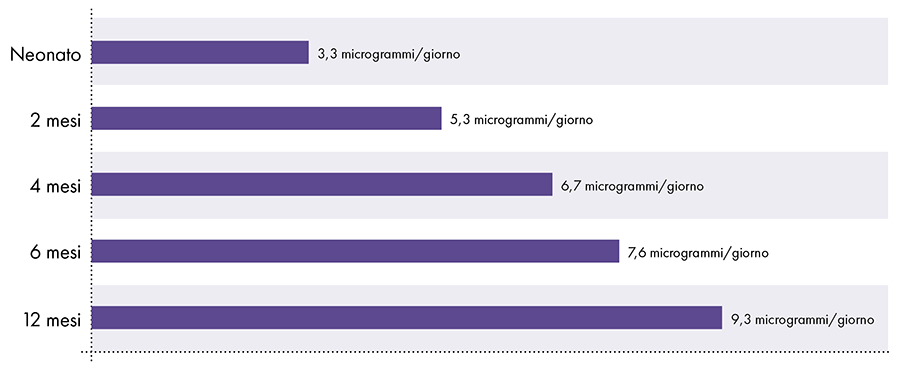 Afbeelding 3: Deze grafiek toont de aluminiumlimiet voor kinderen van verschillende leeftijden, zoals afgeleid van de Toxic Substances and Disease Registry, een afdeling van het Amerikaanse ministerie van Volksgezondheid en Human Services. De limiet geeft aan dat er dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan mag komen om de neurotoxische effecten van aluminium te voorkomen.
Afbeelding 3: Deze grafiek toont de aluminiumlimiet voor kinderen van verschillende leeftijden, zoals afgeleid van de Toxic Substances and Disease Registry, een afdeling van het Amerikaanse ministerie van Volksgezondheid en Human Services. De limiet geeft aan dat er dagelijks niet meer dan 1 microgram aluminium per kilogram lichaamsgewicht in de bloedbaan mag komen om de neurotoxische effecten van aluminium te voorkomen.
Hoeveelheid aluminium in vaccins
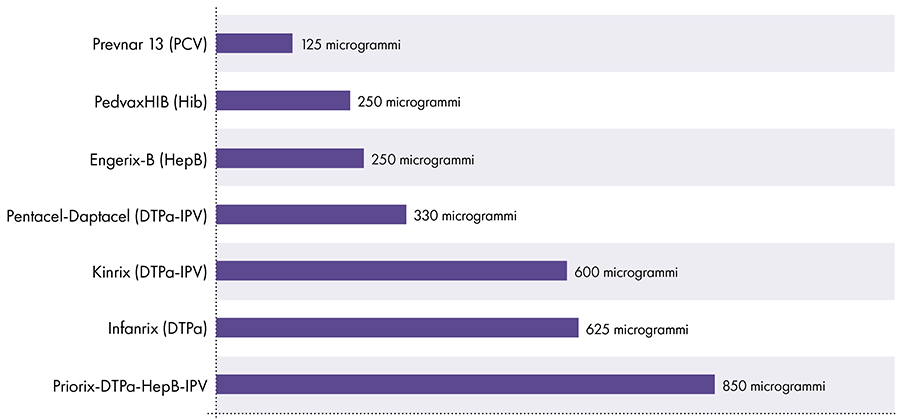
Referenties
- American Academy of Pediatrics, Comité voor voeding. Aluminiumtoxiciteit bij zuigelingen en kinderen. Kindergeneeskunde. 1996 maart; 97 (3): 413.
- Agentschap voor Toxic Substances and Disease Registry (ATSDR). Toxicologisch profiel voor aluminium. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services; 2008.3, 13-24, 145, 171-7, 208.
- Yokel RA. Aluminium in voedsel — de aard en bijdrage van levensmiddelenadditieven. In: El-Samragy Y, redacteur. Additief voor levensmiddelen. Rijeka (Kroatië): InTech; 2012. 203-28.
- Marrack P, McKee AS, Munks MW. Naar een begrip van de adjuvante werking van aluminium. Nat Rev Immunol. april 2009; 9 (4): 287.
- Volk VK, Bunney WE. Difterie-immunisatie met vloeibaar toxoïde en met aluin neergeslagen toxoïde. Am J Volksgezondheid Volksgezondheid. juli 1942; 32 (7): 690-9.
- Baylor NW, Egan W, Richman P. Aluminiumzouten in vaccins - Amerikaans perspectief. Vaccin. 2002 31 mei 20 Suppl 3: S18-22.
- Amerikaanse Food and Drug Administration. Silver Spring (MD): Amerikaanse Food and Drug Administration. Vaccins waarvoor een vergunning is verleend voor gebruik in de Verenigde Staten; [bijgewerkt 2018 februari 14; geciteerd 2018 februari 27. https://www.fda.gov/BiologicsBloodVaccines/Vaccines/ApprovedProducts/Ucm093833.htm.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Aanbevolen immunisatieschema voor kinderen en adolescenten van 18 jaar of jonger, Verenigde Staten, 2018. https://www.cdc.gov/vaccines/schedules/downloads/child/0-18yrs-child-combined-schedule.pdf.
- Amerikaanse Food and Drug Administration. Silver Spring (MD): Amerikaanse Food and Drug Administration. SCOGS (Select Committee on GRAS Substances); [geciteerd 2018 aug. 16]. https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS.
- Priester N.D. Het biologische gedrag en de biologische beschikbaarheid van aluminium bij de mens, met speciale aandacht voor onderzoeken waarbij aluminium-26 als tracer wordt gebruikt: beoordeling en studie-update. J Omgeving Monit. 2004;6:376,392.
- Poole RL, Pieroni KP, Gaskari S, Dixon TK, Park KT, Kerner JA. Aluminium in parenterale voedingsproducten voor kinderen: gemeten versus gelabelde inhoud. J Pediatr Pharmacol Ther. 2011;16 (2):92-7.
- Sedman A. Aluminiumtoxiciteit in de kindertijd. Pediatr Nephrol. 1992 juli;6 (4): 383-93.
- Amerikaanse Food and Drug Administration, ministerie van Volksgezondheid en Human Services. Regels en voorschriften. Fed-register. juni 2003; 68 (100): 34286.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. Nationaal centrum voor gezondheidsstatistieken: gegevenstabel voor grafieken van lengte-naar-leeftijd en gewicht-naar-leeftijd voor jongens; [geciteerd op 2019 april 2]. https://www.cdc.gov/growthcharts/who/boys_length_weight.htm.
- Centrum voor ziektecontrole en Preventie. Washington, DC: Amerikaanse ministerie van Volksgezondheid en Human Services. National Center for Health Statistics: gegevenstabel voor grafieken van lengte-naar-leeftijd en gewicht-naar-leeftijd van meisjes; [geciteerd op 2019 april 2]. https://www.cdc.gov/growthcharts/who/girls_length_weight.htm.
- Amerikaanse Food and Drug Administration, ministerie van Volksgezondheid en Human Services. Herziening van de eisen voor samenstellende materialen. Laatste regel. Fed-register. 2011 april 13; 76 (71): 20513-8.
- Bureau van de Federal Register, National Archives and Records Service, General Services Administration. Regels en voorschriften. Fed-register. 1968 jan; 33 (6): 369.
- Mitkus RJ, King DB, Hess MA, Forshee RA, Walderhaug MO. Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie. Vaccin. 2011 november 28; 29 (51): 9538-43.
- Miller S, artsen voor geïnformeerde toestemming. Erratum in 'Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie.' In: ResearchGate. Berlijn (Duitsland): ResearchGate GmbH; 2020 maart 6 [geciteerd 2020 maart 6]. https://www.researchgate.net/publication/51718934_Updated_Aluminum_pharmacokinetics_following_infant_exposures_through_diet_and_vaccines/comments.
- Artsen voor geïnformeerde toestemming. Newport Beach (CA): artsen voor geïnformeerde toestemming. Erratum in 'Bijgewerkte farmacokinetiek van aluminium na blootstelling van zuigelingen via dieet en vaccinatie'; [geciteerd 2020 maart 6]. https://physiciansforinformedconsent.org/mitkus-2011-erratum/.
- Flarend RE, Hem SL, Witte JL, Elmore D, Suckow MA, Rudy AC, Dandashli EA. In vivo absorptie van aluminiumbevattende vaccinadjuvantia met 26Al. Vaccin 1997 aug-sept; 15 (12-13): 1314-8.
- Verdier F, Burnett R, Michelet-Habchi C, Moretto P, Fievet-Groyne F, Sauzeat E. Aluminiumtest en evaluatie van de lokale reactie op verschillende tijdstippen na intramusculaire toediening van aluminiumbevattende vaccins bij de Cynomolgus-aap. Vaccin. 2005 februari 3; 23 (11): 1359-67.
- Weisser K, Göen T, Oduro JD, Wangorsch G, Hanschmann KO, Keller-Stanislawski B. Aluminium in plasma en weefsels na intramusculaire injectie van menselijke vaccins met adjuvans bij ratten. Boog toxicol. 2019 okt; 93 (10): 2787-96.
- Masson JD, Crépeaux G, Authier FJ, Exley C, Gherardi RK. Kritische analyse van referentieonderzoeken naar de toxicokinetiek van op aluminium gebaseerde hulpstoffen. J Inorg Biochem. 2018 april 181: 87-95.
Artikel vertaald door Artsen voor geïnformeerde toestemming
In 1981 gaf de Amerikaanse Food and Drug Administration (FDA) toestemming voor een uit plasma afkomstig hepatitis B-vaccin dat antigenen bevatte die afkomstig waren van geïnfecteerde personen. Dit vaccin werd later van de markt gehaald omdat het, zoals alle vaccins die uit menselijk bloed worden geproduceerd, ongewenste en potentieel gevaarlijke virussen kon overbrengen. In 1986 werd de eerste van een reeks genetisch gemodificeerde (recombinant-DNA) vaccins goedgekeurd.
Talrijke onderzoeken hebben de waarschijnlijkheid onderzocht dat degenen die het uit plasma afkomstige vaccin kregen, ook ongewenste virussen hadden kunnen ontvangen, vooral HIV, de voorloper van AIDS.(1-2) Bovendien werden klinische onderzoeken om de veiligheid van het huidige hepatitis B-vaccin aan te tonen slechts uitgevoerd bij 147 gezonde kinderen die slechts vijf dagen na toediening werden gevolgd.(3) Dit is niet een steekproef die groot genoeg is en ook niet lang genoeg om de werkelijke incidentie van bijwerkingen vast te stellen. De productiebedrijven hebben zelf toegegeven dat “het wijdverbreide gebruik van het vaccin zou kunnen leiden tot het optreden van bijwerkingen die niet in klinische onderzoeken zijn waargenomen”.(4)
Zelfs volwassen proefpersonen werden slechts vijf dagen na de vaccinatie gevolgd en desondanks werden systemische effecten zoals artralgie, myalgie, paresthesie, rug- en nekpijn, lymfadenopathie, hoofdpijn, koorts, malaise, koude rillingen en braken nog steeds gemeld. pijn, infecties van de bovenste luchtwegen, oorpijn en hypotensie.(5)
Ondanks de officiële technische gegevensbladen en andere documenten die zich verspreiden(6) het hepatitis B-vaccin, hebben de neiging ernstige bijwerkingen te minimaliseren of te ontkennen, talrijke onderzoeken gepubliceerd in medische en wetenschappelijke tijdschriften over de hele wereld en rapporten doorgestuurd naar VAERS(7) bevestigen verschillende pathologieën als gevolg van vaccinatie. Enkele van deze onderzoeken worden hieronder samengevat.
artritis
In 1990, kort na de introductie van het hepatitis B-vaccin, documenteerde het British Medical Journal een verband tussen het vaccin en polyartritis, een pijnlijke ontsteking van vijf of meer gewrichten.(8) In hetzelfde jaar publiceerde de Journal of Rheumatology een artikel over reactieve artritis na hepatitis B-vaccinatie.(9)
In 1994 publiceerde het British Journal of Rheumatology gegevens die reumatoïde artritis na het vaccin documenteerden(10) en de BMJ publiceerde nog drie rapporten die het verband tussen het vaccin en reactieve artritis bevestigden.(11-12) In 1995 werden twee onderzoeken gepubliceerd in het Scandinavische Journal of Rheumatology die gevallen van artritis na vaccinatie bevestigden(13-14) en datzelfde jaar documenteerde het Irish Medical Journal het verband met arthropathie.(15) In 1997 publiceerde het British Journal of Rheumatology twee andere onderzoeken waarin verschillende gevallen van inflammatoire polyartritis na het vaccin werden gedocumenteerd.(16-17) en in 1998 bevestigde de Journal of Rheumatology opnieuw reumatoïde artritis.(18) Ook dat jaar publiceerde het Franse tijdschrift Revue de Médecine Interne een onderzoek naar de ziekte van Still die op volwassen leeftijd begint – een zeldzame en pijnlijke vorm van artritis – na vaccinatie tegen hepatitis A en B.(19) In 1999 documenteerde Reumatologie reumatologische aandoeningen na het vaccin(20) en in 2000 publiceerde het American College of Rheumatology onderzoek in het peer-reviewed tijdschrift Arthritis & Rheumatology dat het syndroom van Sjögren – een zeldzame vorm van chronische artritis – documenteerde na vaccinatie tegen hepatitis B.(21)
Auto-immuunziekten en neurologische ziekten, waaronder multiple sclerose
In 1983 publiceerde de New England Journal of Medicine een studie die het begin aantoonde van polyneuropathie – gelijktijdige storing van talrijke zenuwen – na vaccinatie tegen hepatitis B.(22) In 1988 rapporteerde het American Journal of Epidemiology meerdere “neurologische bijwerkingen” na het vaccin, waaronder talrijke gevallen van het Guillain-Barré-syndroom, lumbale radiculopathie, brachiale plexusneuropathie, optische neuritis en transversale myelitis.(23) In hetzelfde jaar documenteerde het tijdschrift Archives of Internal Medicine myasthenia gravis - een ernstige chronische auto-immuun-neuromusculaire ziekte - opnieuw na vaccinatie tegen hepatitis B.(24)
In 1991 publiceerde The Lancet een rapport waarin de demyelinisatie van het centrale zenuwstelsel na het vaccin werd gedocumenteerd(25) en in 1992 publiceerde Nephron gegevens die vaccinatie koppelden aan systemische lupus erythematosus, een chronische auto-immuunziekte die meerdere organen aantast.(26) Eveneens in 1992 publiceerde het tijdschrift Clinical Infectious Diseases een onderzoek waarin het Evans-syndroom – een zeldzame auto-immuun- en bloedziekte met een hoog sterftecijfer – werd gekoppeld aan het vaccin.(27) en het Franse tijdschrift Thérapie publiceerde opnieuw een onderzoek naar "perifere gezichtsverlamming" na toediening van het medicijn.(28) Bovendien bracht Infectious Disease News een rapport uit waarin talrijke gevallen van neurologische schade werden vermeld die op multiple sclerose leken(29) en in 1993 verscheen er een artikel in de Journal of Hepatology over transversale myelitis – ontsteking van het ruggenmerg – na vaccinatie tegen hepatitis B.(30) Datzelfde jaar publiceerde de Franse krant La Nouvelle Presse Médicale gegevens die post-vaccinatie ‘acute myelitis’ bevestigden.(31) en Clinical Infectious Diseases documenteerden ‘klassieke multiple sclerose’.(32) In 1994 publiceerden Archives of Pediatrics and Adolescent Medicine gegevens die lupus aan het vaccin koppelden.(33) en het tijdschrift Acta Neurologica Scandinavica publiceerden een rapport over acute cerebellaire ataxie – ernstig verlies van evenwicht en motorische coördinatie – na de vaccinatie in kwestie.(34)
In 1995 werd demyelinisatie van het centrale zenuwstelsel gerapporteerd in de Journal of Neurology, Neurosurgery and Psychiatry(35) en in het American Journal of Neuroradiology myelitis. De auteurs van laatstgenoemde studie merkten op dat dit soort bijwerkingen mogelijk te weinig worden gerapporteerd omdat de symptomen laat komen.(36) In 1996 publiceerden zowel Nephron als het Franse tijdschrift Annales de Dermatologie et de Vénéréologie studies die de correlatie tussen lupus erythematosus en het hepatitis B-vaccin aantoonden.(37-38) In hetzelfde jaar publiceerde de Journal of Hepatology een rapport over het verband met leuko-encefalitis, een ontsteking van de witte hersenmassa.(39) In 1996 documenteerde de New England Journal of Medicine post-vaccinatie cryoglobulinemie, een zeldzame auto-immuunziekte die de bloedsomloop schaadt, bloedingen en andere problemen veroorzaakt.(40)
Door vaccins geïnduceerde auto-immuniteit werd gecertificeerd in het Journal of Autoimmunity(41) en in 1997 publiceerde het Indian Journal of Pediatrics een onderzoek waarin het Guillain-Barré-syndroom, een auto-immuunziekte die zenuwbeschadiging, spierzwakte en verlamming veroorzaakt, werd gekoppeld aan het vaccin.(42) In hetzelfde jaar documenteerde het Journal of Korean Medical Science acute myelitis(43) en ook het verband met "mentale zenuwneuropathie" kwam naar voren.(44)
Vervolgens verschenen in JAMA gegevens over 46 mensen – voornamelijk vrouwen – die hun haar waren kwijtgeraakt na vaccinatie tegen hepatitis B.(45)
In 1998 werden zowel lupus erythematosus als trombocytopenie gedocumenteerd bij gevaccineerde personen(46) en in 1999 meer alopecia in het American Journal of Gastroenterology.(47) In hetzelfde jaar documenteerde Auto-immuniteit een demyeliniserende polyneuropathie, terwijl Neurology gegevens publiceerde die multiple sclerose en encefalitis aan het vaccin koppelden.(48-49) Ook in 1999 schreef La Nouvelle Presse Médicale over post-vaccinatie cervicale myelitis(50) en in 2000 werd multiple sclerose besproken in Neurology.(51) Ook in 2000 schreef de Journal of the Medical Association of Thailand over het Guillain-Barré-syndroom na recombinant DNA-hepatitis B-vaccin(52) en in 2001 werd in de Klinische Infectieziekten leuko-encefalitis gedocumenteerd.(53) In 2004 publiceerde Neurology een onderzoek dat het verband aantoonde tussen het vaccin en een statistisch significant risico op multiple sclerose;(54) in 2006 documenteerde het Chinese Medical Journal ook multiple sclerose.(55) In 2008 publiceerde Neurology twee onderzoeken die een statistisch significante correlatie aantoonden tussen hepatitis B-vaccinatie bij kinderen en de ontwikkeling van multiple sclerose bij kinderen (demyelinisatie van het centrale zenuwstelsel), meer dan drie jaar later.(56-57)
Zintuiglijke beperking
Talrijke medische en wetenschappelijke publicaties hebben zicht- en gehoorstoornissen gedocumenteerd na vaccinatie tegen hepatitis B. In 1987 publiceerde The Lancet bijvoorbeeld een artikel over uveïtis – ontsteking van de binnenwand van het oog die vaak tot blindheid leidt – na het vaccin.(58) In 1993 verschenen opnieuw in The Lancet verdere gegevens die verlies van gezichtsvermogen en eosinofilie – een allergische bloedziekte – documenteerden, opnieuw na vaccinatie.(59) In 1994 documenteerde Optometry and Vision Science post-vaccinatie optische neuritis(50) en in 1995 werd epitheliopathie – een zeldzame oogaandoening die verslechtering van het gezichtsvermogen veroorzaakt – besproken in de Archives of Ophthalmology.(61) In 1996 publiceerde The Lancet een rapport waarin de “centrale retinale veneuze occlusie” na het vaccin werd gedocumenteerd,(62) terwijl in het American Journal of Ophthalmology melding werd gemaakt van het bilaterale witte-vlek-syndroom, dat verlies van het gezichtsvermogen in beide ogen veroorzaakt.(63) Ook in 1996 documenteerde La Nouvelle Presse Médicale neuropapillitis - ontsteking en verslechtering van de oogzenuw - na het vaccin(64) en een ander Frans tijdschrift, Annales d'Otolaryngologie et de Chirurgie Cervico-Faciale, maakte melding van gehoorverlies.(65) In 1997 publiceerde La Nouvelle Presse Médicale vervolgens twee verschillende onderzoeken waarin ernstige gevallen van centrale retinale veneuze occlusie na vaccinatie werden gedocumenteerd.(66-67) In hetzelfde jaar bevestigde Nefrologie Dialyse Transplantatie het begin van optische neuritis na het vaccin(68) en International Ophthalmology gecertificeerde “oogheelkundige complicaties” bij gevaccineerde proefpersonen.(69) Eveneens in 1997 merkten de Annals of the New York Academy of Sciences en het internationale tijdschrift Auris, Nasus, Larynx gehoorverlies na vaccinatie op,(70-71) terwijl in 1998 het Journal of French Ophthalmology gegevens over epitheliopathie publiceerde.(72) In 1999 bevestigde de BMJ optische neuritis na vaccinatie tegen hepatitis B(73) en Acta Ophthalmologica Scandinavica papilledema - zwelling van de optische schijf.(74) In 2001 bevestigde een Duits tijdschrift, Klinische Monatsblätter Für Augenheilkunde, ook optische neuritis na vaccinatie.(75)
Bloedziekten
In 1990, kort na de massale marktintroductie van het hepatitis B-vaccin, documenteerde de BMJ vasculitis, een ontsteking van de bloedvaten, na toediening van het medicijn.(76) In 1993 gaf het Engelse tijdschrift Thorax bevestiging(77) en The Lancet publiceerde een onderzoek naar eosinofilie, een allergische bloedziekte, opnieuw na vaccinatie.(78) In 1994 en 1995 documenteerde The Lancet ook trombocytopenie - een ernstige ziekte die overmatige bloedingen, blauwe plekken en stollingsproblemen veroorzaakt.(79-80) In 1998 werd het begin van trombocytopenie bevestigd bij talrijke recent gevaccineerde patiënten(81) Ook uit het Scandinavische Journal of Infectious Diseases zijn gegevens gepubliceerd die bevestigen dat deze ziekte een bijwerking van het vaccin is.(82) In 1999 bevestigde het European Journal of Pediatrics opnieuw trombocytopenie na zowel hepatitis B- als BMR-vaccins(83) en hetzelfde jaar publiceerde de Journal of Rheumatology twee belangrijke onderzoeken waarvan de eerste de correlatie tussen vaccins en vasculitis had aangetoond(84) en de tweede erythermalgie, vasculaire spasmen in de handen en voeten die pijn en een branderig gevoel veroorzaken.(85) In 2000 bestudeerde Clinical and Experimental Rheumatology gevallen van polyartritis nodosa(86) - een zeldzame, systemische, necrotiserende (celbeschadigende) vorm van vasculitis - en het British Journal of Hematology documenteerde ernstige pancytopenie - een gevaarlijke vermindering van het aantal rode bloedcellen.(87) In 2001 publiceerde de Journal of Rheumatology aanvullende gegevens die de mogelijkheid van vasculitis bevestigden na recombinant hepatitis B-vaccin(88) en het Italiaanse tijdschrift Haematologica bevestigde trombocytopenie als een bijwerking.(89)
Huidziektes
In 1989 documenteerde de New England Journal of Medicine erythema nodosum – pijnlijke ontsteking van de huid met zachte bultjes – na vaccinatie tegen hepatitis B.(90) In 1993 rapporteerde de Journal of Rheumatology gevallen van zowel erythema nodosum als Takayasu-artritis – een zeldzame vorm van vasculitis.(91) In hetzelfde jaar schreef het Zweedse tijdschrift Acta Dermato-Venereologica over lichen ruber planus na vaccinatie(92) - een jeukende uitslag op de huid die wordt gekenmerkt door dicht bij elkaar gelegen dikke, harde laesies die lijken op algen of schimmels die op rotsen groeien. In 1994 documenteerde het Archief voor Dermatologie ook lichen planus na vaccinatie(93) en kinderdermatologie hebben een verband aangetoond met erythema multiforme.(94) In 1997 bevestigde het Australasian Journal of Dermatology de “lichenoïde reactie” (lichen planus) na het vaccin(95) en het Journal of the American Academy of Dermatology schreef over anethodermie(96) - plaatselijke rimpels, verlies van elasticiteit en atrofie van de huid - na vaccinatie. In 1998 publiceerde het British Journal of Dermatology twee onderzoeken waarin huidziekten na vaccinatie werden gedocumenteerd: de ene betrof lichen planus(97) en de andere over urticaria en angio-oedeem,(98) allergische pathologieën gekenmerkt door brandende, stekende en pijnlijke zwelling. In 1999 werd lichen planus ook vermeld in het International Journal of Dermatology(99) en in 2000 werden gegevens die erythema multiforme na vaccinatie bevestigden gepubliceerd in Clinical and Experimental Dermatology.(100) In hetzelfde jaar schreef de Nepal Journal of Dermatology opnieuw over lichen planus na hepatitis B-vaccinatie(101) in 2001 verscheen de vermelding in het Journal of the American Academy of Dermatology(102) terwijl kinderdermatologie sprak van lichenoïde uitbarsting.(103)
Diabetes lever- en nierziekten
In 1994 documenteerde The Lancet leverdisfunctie na hepatitis B-vaccinatie(104) en in 1995 publiceerde Clinical Nephrology een onderzoek naar nefrotisch syndroom – nierbeschadiging – opnieuw na vaccinatie.(105) In 1996 publiceerde het New Zealand Medical Journal twee documenten die antihepatitis B in verband brachten met epidemieën van insuline-afhankelijke diabetes mellitus (IDDM). De auteurs ontdekten dat er in de drie jaar na een nieuw geïntroduceerde en zeer uitgebreide massale vaccinatiecampagne een toename van 60% in IDDM-gevallen was.(106-107) In 1997 schreef Intensive Care Medicine over leverontsteking en acute luchtwegaandoeningen na vaccinatie (108). In 2000 bevestigde kindernefrologie de mogelijkheid om na toediening van het vaccin aan een nefrotisch syndroom te lijden.(109) Andere publicaties documenteerden ook de bijwerkingen van dit vaccin.(110-111-112-113-114-115-116-117-118-119)
Frankrijk heeft antihepatitis B geschrapt van de kindervaccinatiekalender
In juli 1998 spanden ongeveer 15.000 Franse burgers die lid waren van vijftien verenigingen een rechtszaak aan tegen de Franse regering, omdat zij beweerden dat zij het publiek had misleid over de risico's en voordelen die verbonden waren aan het hepatitis B-vaccin. Honderden – misschien wel duizenden – mensen hadden aan auto-immuunziekten geleden en neurologische aandoeningen, waaronder multiple sclerose, na vaccinatie.(120) Als gevolg hiervan werd Frankrijk in oktober 1998 het eerste land dat de vereiste voor toelating van dit vaccin tot school afschafte.(121)
Het hepatitis B AIDS-vaccin
In 1978 injecteerde het New York Blood Center in Manhattan, New York, homoseksuele mannen met een experimenteel vaccin tegen hepatitis B, geproduceerd door Merck, voor de bereiding waarvan chimpansees werden gebruikt. Kort daarna kregen mannelijke homoseksuelen in San Francisco, Los Angeles, Denver, Chicago en St. Louis ook drie doses van het medicijn gedurende een periode van drie maanden.
In 1980 testte 20% van de homomannen die zich vrijwillig aanmeldden voor het Manhattan-experiment positief op HIV - de hoogste incidentie ter wereld, inclusief Afrika. In 1981 werd de AIDS-epidemie officieel. Hoewel er geen bewijs is dat het experimentele hepatitis B-vaccin bij deze homoseksuele vrijwilligers AIDS veroorzaakte, lijdt het geen twijfel dat de ziekte kort na de vaccinatie een piek bereikte.(122)
Hoe effectief is het hepatitis B-vaccin?
De effectiviteit van het hepatitis B-vaccin werd bepaald door het medicijn te injecteren bij proefpersonen bij wie vervolgens de in het bloed geproduceerde specifieke antilichamen werden gemeten. Deze antilichamen moeten aan bepaalde door deskundigen vastgestelde niveaus voldoen of deze overschrijden en waarvan wordt aangenomen dat ze bescherming bieden. Wetenschappers noemen het 'seroprotectie'. Volgens deze definitie wordt het vaccin als “zeer immunogeen” beschouwd wanneer de antilichaamniveaus meetbaar zijn in de korte periode na de laatste dosis van een cyclus van drie boosters.(123) Toch is volgens de verwerkende industrie niet bekend hoe lang het beschermende effect bij gezonde gevaccineerde mensen duurt. Uit vervolgstudies al vijf tot negen jaar later blijkt dat ongeveer de helft van alle gevaccineerde personen niet langer beschermende niveaus van antilichamen heeft.(124-125)
Uit een studie gepubliceerd in de New England Journal of Medicine bleek bijvoorbeeld dat na vijf jaar de antilichaamniveaus (waarvan wordt aangenomen dat ze verband houden met immuniteit) dramatisch waren gedaald of niet langer detecteerbaar waren bij 42% van de gevaccineerden. Bovendien waren 34 van de 773 proefpersonen (4,4%) besmet met het virus.(126-127) In een ander onderzoek had minder dan 40% van de gevaccineerden na vijf jaar beschermende antilichamen.(128)
Uit soortgelijk onderzoek bleek dat 48% van de gevaccineerde proefpersonen na slechts vier jaar een ontoereikend antilichaamniveau had.(129) Volgens de WHO zal tot "60% van de volwassenen binnen zes tot tien jaar alle meetbare antilichamen verliezen die door het hepatitis B-vaccin zijn geïnduceerd."(130) en de medische literatuur staat vol met gegevens die het falen van vaccinatie bevestigen.(131-132)
Referenties
- Jacobson IM et al., "Gebrek aan effect van het hepatitis B-vaccin op T-celfenotypes", NEJM, 1984, 311 (16), blz. 1030-1032.
- Institute of Medicine, Adverse Events Associated with Childhood Vaccines: Evidence Bearing on Causality, National Academy Press, Washington, DC, 1994.
- Merck & Co., Inc. Recombivax HB Hepatitis B-vaccin (recombinant), bijsluiter vanaf juni 2005.
- Ibid.
- Ibid.
- Tan LJ, “The hepatitis B vaccin”, American Medical Association, AMA die artsen helpt patiënten te helpen, www.arna-assn.org, 9 december 2004.
- Rapportagesysteem voor bijwerkingen van vaccins VAERS. Rockville, MD.
- Rogers ton SJ et al. , "Hepatitis B-vaccin geassocieerd met erythema nodosum en polyartritis", BMJ, 1990, 301, p. 345.
- Hachulla E. et al., "Reactieve artritis na hepatitis B-vaccinatie Journal of Rheumatology”, 1990, 17, pp. 1250-1251.
- Vautier G. et al., "Acute seropositieve reumatoïde artritis die optreedt na hepatitisvaccinatie", Br. J. Rheumatol., oktober 1994, 33 (10), p. 991.
- Hassan W. et al., "Reiter's syndroom en reactieve artritis bij gezondheidswerkers na vaccinatie", BMJ, 9 juli 1994, 309 (6967), p. 94.
- Birley HD et al., "Hepatitis B immunization and reactive artritis", BMJ, december 1994, 309 (6967), p. 1514.
- Gross et al., "Artritis na vaccinatie tegen hepatitis B. Rapport van drie gevallen", Scand. J. Rheumatol., 1995, 24 (1), blz. 50-52.
- Biasi D. et al., "Reumatologische manifestaties na hepatitis B-vaccinatie. Rapport van drie gevallen", Scand. J. Rheumatol., 1995, 24, blz. 50-52.
- Aherne P. et al., "Psoriatische artropathie", Irish Medical Journal, maart-april 1995, 88 (2), p. 72.
- Harrison BJ et al., "Patiënten die inflammatoire polyartritis (PH) ontwikkelen na immunisatie zijn klinisch niet te onderscheiden van andere patiënten met PH", Br. J. Rheum., maart 1997, 36 (3), pp. 366-369.
- Bracci M. et al., "Polyartritis geassocieerd met hepatitis B-vaccinatie", Br. J. Rheumatol., februari 1997, 36 (2), blz. 300-301.
- Pope JE et al., "De ontwikkeling van reumatoïde artritis na recombinante hepatitis B-vaccinatie", J. Rheum., september 1998, 25 (9), pp. 1687-1693.
- Grasland A et al., "De ziekte van Still bij volwassenen na vaccinatie tegen Hepatitis A en B?", Rev. Internal Med., februari 1998, 19 (2), pp. 134-136.
- Maillefert JF et al., "Reumatische aandoeningen ontwikkeld na vaccinatie tegen hepatitis B", Rheumatol. (Oxford), oktober 1999, 38 (10), blz. 978-983.
- Toussirot E. et al., "Het syndroom van Sjögren treedt op na vaccinatie tegen hepatitis B", Arthritis Rheuma, september 2000, 43 (9), pp. 2139-2140.
- Ribera ER et al., "Polyneuropathie geassocieerd met toediening van hepatitis B-vaccin", N. Engl. J. Med., 8 september 1983, 309 (10), blz. 614-615.
- Shaw FE Jr. et al., "Postmarketing surveillance voor neurologische bijwerkingen gemeld na hepatitis B-vaccinatie. Ervaring van de eerste drie jaar", Am. J. Epidemiol., februari 1988, 27 (s), pp. 337-352 .
- Biron P. et al., "Myasthenia gravis na algemene anesthesie en hepatitis B-vaccin", Arch.Intern. Med., december 1988, 148 (12), p. 2685.
- Herroelen L. et al. , "Demyelinisatie van het centrale zenuwstelsel na immunisatie met recombinant hepatitis B-vaccin", The Lancet, 9 november 1991, 338 (8776), pp. 1174-1175.
- Tudela P. et al., "Systemische lupus erythematosus en vaccinatie tegen hepatitis B", Nephron, 1992, 62 (2), p. 236.
- Martinez E. et al., "Evan's syndroom getriggerd door recombinant hepatitis B-vaccin", Clin. Infect. Dis., 1992, 15, p. 1051.
- Ganry O. et al., "Peripheral facial paralysis after vaccinatie against hepatitis B. Apropos of a case", Therapie, 0, 1992, pp. 47-437.
- Waisbren BA, "Andere kant van de medaille (letter)", Inf Dis. Nieuws, 1992, 5, p. 2.
- Trevisani F. et al., "Transverse myelitis na hepatitis B-vaccinatie",]. of Hepatology, september 1993, 19 (2), pp. 317-318.
- Mahassin F. et al. , "Acute myelitis na vaccinatie tegen hepatitis B", Presse Med., december 1993, 22 (40), pp. 1997-1998.
- Nadler JP, "Multiple sclerose en hepatitis B-vaccinatie", Clin. Infecteren. Dis., november 1993, 17 (5), blz. 928-929.
- Mamoux V. et al., "Lupus erthymatosus verspreiding en vaccinatie tegen het hepatitis B-virus", Arch. Pediatr., 1994, 1, pp. 307-309.
- Deisenhammer F. et al., "Acute cerebellaire ataxie na immunisatie met recombinant hepatitis B-vaccin", Acta Neurol. Scand., juni 1994, 89 (6), blz. 462-463.
- Kaplanski G. et al., "Demyelinisatie van het centrale zenuwstelsel na vaccinatie tegen hepatitis B en HLA-haplotype", J. Neurol. Neurochirurg. Psychiatrie, juni 1995, 58 (6), pp. 758-759.
- Tartaglino LM et al., "MR imaging in a case of post vaccinatie myelitis", Am. J. Neuroradiol., 1995, 16 (3), pp. 581-582.
- Guiserix J., "systemische lupus erythematosus na hepatitis B-vaccin", Nephron, 1996, 74 (2), p. 441.
- Grezard P. et al., "Cutane lupus erythematosus en buccale aftose na hepatitis B-vaccinatie bij een 6-jarig kind", Ann. Dermatol. Venereal., 1996, 123 (10), blz. 657-659.
- Manna R. et al., "Leukoencephalitis after recombinant hepatitis B vaccin", J. of Hepatology, juni 1996, 24 (6), pp. 764-765.
- Mathieu E. et al., "cryoglobulinemie na hepatitis B-vaccinatie", New England]. Med., augustus 1996, 335 (5), p.335.
- Cohen AD. et al., "Vaccine-geïnduceerde auto-immuniteit", J. Autoimmunity, december 1996, 9 (6), pp. 699-703.
- Kakar A. et al., "Guillain Barre-syndroom geassocieerd met hepatitis B-vaccinatie", Ind. J. Ped., september-oktober 1997, 64 (5), 710-712.
- Song HK et al., "Acute Myelitis na hepatitis B-vaccinatie", J. Korean Med.Sci., juni 1997, 12 (3), pp. 249-251.
- Maillefert JF et al., "Mentale zenuwneuropathie als gevolg van hepatitis B-vaccinatie", Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology and Endodontology, juni 1997, 83 (6), pp. 663-664.
- Wise RP et al., "Hair loss after routine immunizations", JAMA, 8 oktober 1997, 278 (14), pp. 1176-1178.
- Finielz P. et al, "Systemische lupus erythematosus en trombocytopenische purpura bij twee leden van dezelfde familie na het hepatitis B-vaccin", Nephrol. Wijzerplaat. Transplant., 1998, 13 (9), blz. 2420-2421.
- Flemner M. et al., "The kale waarheid", Am. J. Gastroenterol., april 1999, 94 (4), p. 1104.
- Creange A et al., "Lumbosacrale acute demyeliniserende polyneuropathie na hepatitis B-vaccinatie", Autoimmunity, 1999, 30, pp. 143-146.
- Tourbah A. et al., "Encephalitis after hepatitis B vaccinatie: recidiverende gedissemineerde encefalitis of MS?", Neurology, 22 juli 1999, 53 (2), pp. 396-401.
- Renard JL et al., "Acute transverse cervicale myelitis na hepatitis B-vaccinatie. Evolutie van anti-HBs-antilichamen", Presse Med., 3-10 juli 1999, 28 (24), pp. 1290-1292.
- Gran B. et al., "Martin R. Ontwikkeling van multiple sclerose na hepatitis B-vaccinatie", Neurol., 2000, 54 (suppl 3), A164.
- Sinsawaiwong S. et al., "Guillain-Barre-syndroom na recombinant hepatitis B-vaccin en literatuuronderzoek", J. Med. Assoc. Thai., september 2000, 83 (9), blz. 1124-1126.
- Konstantinou D. et al., ''Twee episodes van leuko-encefalitis geassocieerd met recombinante hepatitis B-vaccinatie bij één patiënt'', Clin.Inf.Dis., 15 november 2001, 33, blz. 1772-1773.
- Heman MA et al., "Recombinant hepatitis B-vaccin en het risico op multiple sclerose: een prospectieve studie", Neurology, 2004, 63, pp. 838-842.
- Terney D. et al., "Multiple sclerose na hepatitis B-vaccinatie bij een 16-jarige patiënt", Chinese Medical Journal, 2006, 119 (1), pp. 77-79.
- Yann M. et al., “Hepatitis B-vaccin en het risico op inflammatoire demyelinisatie van het CZS in de kindertijd”, Neurology, 8 oktober 2008 [online gepubliceerd].
- Ness JM et al. “Hepatitisvaccins en pediatrische multiple sclerose. Doet timing of type er toe?”, Neurology, 17 december 2008 (online gepubliceerd).
- Fried Met al., "Uveïtis na hepatitis B-vaccinatie", The Lancet, 12 september 1987, pp. 631-632.
- Brezin A. et al., "Visual loss and eosinophilia after recombinant hepatitis B vaccin", The Lancet, 28 augustus 1993, 342 (8870), pp. 563-564.
- Achiron LR et al., "Postinfectieuze hepatitis B optische neuritis", Optom. Weergave Sci., 1994, 71, blz. 53-56.
- Brezin AP et al., "Acute posterior multifocal placoid pigment epitheliopathy after hepatitis B vaccin", Arch. Ophthalmol., maart 1995, 113 (3), pp. 297-300.
- Devin F. et al., "Occlusion of central retinale vein after hepatitis B vaccinatie", The Lancet, juni 1996, 347 (9015), p. 1626.
- Baglivo E. et al., "Multiple evanescent white dot syndrome after hepatitis B vaccin", Am. J. Ophthalmol., september 1996, 122 (3), pp. 431-432.
- Berkman N. et al., "Bilateral neuro-papillitis after hepatitis B vaccinatie", Presse Med., 28 september 1996, 25 (28), p. 1301 (Frans).
- Bonfils P. et al., "Fluctuante perceptie van gehoorverlies na hepatitis B-vaccin", Ann. Otolaryngol. Chir. Cervicofac., 1996, 113 (6), blz. 359-361 (Frans).
- Granel B. et al., "Occlusie van de centrale retinale ader na vaccinatie tegen virale hepatitis B met recombinante vaccins. 4 gevallen", Presse Med., 1 februari 1997, 26 (2), pp. 62-65 [Frans].
- Berkman N., "Een geval van segmentale unilaterale occlusie van de centrale retinale ader na vaccinatie tegen hepatitis B", Presse Med., 26 april 1997, 26 (14), p. 670 [Frans].
- Albitar S. et al., "Bilaterale retrobulbaire optische neuritis met hepatitis B-vaccinatie", Nephrol. Wijzerplaat. Transplantatie, oktober 1997, 12 (10), blz. 2169-2170.
- Arya SC, "Oftalmische complicaties van vaccins tegen het hepatitis B-virus", Int. Ophth., 1997, 21 (3), pp. 177-178.
- Orlando MP et al., "Plotseling gehoorverlies als gevolg van hepatitis B-vaccinatie: een casusrapport", Annals of the New York Academy of Sciences, 29 december 1997, 830, pp.319-321.
- Biacabe B. et al., ‘A case report of fluctuant perceptief gehoorverlies na hepatitis B-vaccinatie’, Auris, Nasus, Larynx, oktober 1997, 24, (4), pp. 357-360.
- Bourges JL et al., “Multifocal placoid epitheliopathy and anti-hepatitis B vaccinatie”, J. Fr. Ophtalmol., november 1998, 21(9), pp. 696-700 [Frans].
- Stewart O. et al., “Gelijktijdige toediening van hepatitis B- en poliovaccins geassocieerd met bilaterale optische neuritis”, Br. J. Ophthalmol., oktober 1999, 83 (10), pp.1200-1201.
- Fledelius HC, “Eenzijdig papiloedeem na hepatitis B-vaccinatie bij een migrainepatiënt. Een casusrapport inclusief forensische aspecten", Acta Ophthalmol. Scand., december 1999, 77 (6), pp. 722-724.
- Voigt u. et al., “Neuritis van de oogzenuw na vaccinaties tegen hepatitis A, hepatitis B en gele koorts”, Klin. Monatsbl. Augenheilkd., oktober 2001, 218 (10), pp. 688-690 (Duits).
- Cockwell P. et al., "Vasculitis gerelateerd aan hepatitis B-vaccin", BMJ, 1 december 1990, 301 (6763) p.1281.
- Allen MB et al., "Pulmonale en cutane vasculitis na hep B-vaccinatie", Thorax, mei 1993, 48 (5), pp. 580-581.
- Nagafuchi S. et al., "Eosinofilie na intradermale hepatitis B-vaccinatie", The Lancet, 1993, 342, p. 998.
- Poullin P. et al., "Trombocytopenische purpura na recombinant hepatitis B-vaccin", The Lancet, november 1994, 344 (8932), p. 1293.
- Meyboom RH et al., "Trombocytopenie gerapporteerd in associatie met hepatitis B- en A-vaccins", The Lancet juni 1995, 345 (8965), p. 1638.
- Neau D. et al., "Immune trombocytopenische purpura na recombinant hepatitis B-vaccin: retrospectief onderzoek van zeven gevallen", Scan J. Infect Dis., 1998, 30 (2), pp. 115-118.
- Ronchi F. et al., "Trombocytopenische purpura als bijwerking op recombinant hepatitis B-vaccin", Arch. Dis. Child., maart 1998, 78 (3), blz. 273-274.
- Muller A. et al., "Trombocytopenische purpura: bijwerkingen op gecombineerde immunisatie (recombinant hepatitis B en bof-mazelen-rubella-vaccin) en na therapie met co-trimoxazol", Eur.]. Pediatr., december 1999, 158 suppi. 3, S209-10.
- Le Hello C. et al., “Vermoedelijke hepatitis B-vaccinatiegerelateerde vasculitis”, J. of Rheumatology, januari 1999, 26 (1), pp. 191-194.
- Rabaud C. et al., "Eerste geval van erythermalgie gerelateerd aan hepatitis B-vaccinatie", J. uit Rheum., januari 1999, 26 (1), pp. 233-234.
- De Keyser F. et al., “Immuun-gemedieerde pathologie na hepatitis B-vaccinatie” Twee gevallen van polyarteritis nodosa en één geval van pityriasis rosea-achtige medicijnuitbarsting”, Clin. Exp. Rheumatol., januari-februari 2000, 18 (1), pp. 81-85.
- Viallard JF et al., "Ernstige pancytopenie veroorzaakt door recombinant hepatitis B-vaccin", Br. J. Haematol., juli 2000, 110 (1), pp. 230-233.
- Zaas A. et al., uVasculitis van de grote slagader na recombinante hepatitis B-vaccinatie. 2 cases", J. Rheumatol., mei 2001, 28 (S), pp.1116-11120.
- Conesa V. et al., "Trombocytopenische Purpura na recombinant hepatitis B-vaccin. Een zeldzame associatie", Haematologica, maart 2001, 86 (3), E09 [Italiaans].
- Goolsby PL, “Erythema nodosum na Recombivax HB hepatitis B-vaccin”, N. Engl. J. Med., oktober 1989, 321, 1198-1199.
- Castresana-Isla CJ et al., "Erythema nodosum en Talkayasu's arteritis na immunisatie met uit plasma afkomstig hepatitis B-vaccin", J. Rheumatol., augustus 1993, 20(8), blz. 1417-1418.
- 109. Trevisian G. et al., "Lichen ruber planus na HBV-vaccinatie". Acta Dermato-Venereotogica, februari 1993, 73 (1), p. 73.
- Aubin F. et al., “Lichen planus na hepatitis B-vaccinatie”, Archives of Dermatology, oktober 1994; 130 (10), blz. 1329-1330.
- Di Lernia V. et al., "Bisighini G. Erythema multiforme na hepatitis B-vaccin", Ped. Derma., december 1994, 11 (4), blz. 363-364.
- Saywell CA. et al., "Kossard S. Lichenoid reaction to hepatitis B vaccinatie", Australasian J. Derm., augustus 1997, 38 (3), pp. 152-154.
- Daud MS et al., “Anetoderma na hepatitis B-immunisatie bij twee broers en zussen,”/. Amer. Acad. Dermatol., mei 1997, 36 (5 Pt 1), blz. 779-780.
- Ferrando MF et al., "Lichen planus na hepatitis B-vaccinatie”, Br. J. Dermatol., augustus 1998, 139 (2) p. 350.
- Barbaud A. et al., "Allergische mechanismen en urticaria/angio-oedeem na hepatitis B-immunisatie", Bt. J. Dermatot, november 1998, 139 (5), pp. 925-926.
- Schupp P. et al., "Lichen planus na vaccinatie tegen hepatitis B", Inter. J. uit Dermat., oktober 1999, 38 (10), blz. 799-800.
- Loche F. et al., "Erythema multiforme geassocieerd met hepatitis B-immunisatie", Cfin. Exp.Dermatol., maart 2000, 25 (2), blz. 167-168.
- Agrawal S. et al., "Lichen planus na HBV-vaccinatie bij een kind: een casusrapport uit Nepal", J. Dermatol., september 2000, 27 (9), pp. 618-620.
- Al-Khenaizan S., "Lichen planus die optreedt na hepatitis B-vaccinatie: een nieuw geval", J. Am. Acad. Dermatol., oktober 2001, 4S (4), blz. 614-615.
- Usman A. et al., “Lichenoïde uitbarsting na hepatitis B-vaccinatie: eerste Noord-Amerikaanse casusrapport”. Pediatr. Dermato J., maart-apr. 2001, 18 (2) pp. 123-126.
- Lilic D. et al., “Lever dysfunctie en DNA-antilichamen na hepatitis B-vaccinatie”, The Lancet, november 1994, 344 (8932), pp. 1292-1293.
- Macario F. et al., “Nefrotisch syndroom na recombinant hepatitis B-vaccin”, Clin. Nephrol., mei 1995, 43 (5), p. 349.
- Classen John Barthelow, "Childhood immunization and diabetes mellitus", New Zealand Med. J., 24 mei 1996, p. 195.
- Classen John Barthelow, ''De diabetesepidemie en het hepatitis B-vaccin'', New Z. Med. J., 24 mei 1996, p. 366.
- Ranieri VM et al., "Leverontsteking en acuut ademhalingsnoodsyndroom bij een patiënt die het hepatitis B-vaccin krijgt: een mogelijke relatie?", Intensive Care Medicine, januari 1997, 23 (1), pp. 119-121.
- Islek I. et al., “Nefrotisch syndroom na hepatitis B-vaccinatie”, Pediatr. Nephrol., januari 2000, 14, pp. 89-90.
- Snider GB et al., “Een mogelijke systemische reactie op het hepatitis B-vaccin”, JAMA. 1 maart 1985, 253 (9), blz. 1260-1261.
- AADRAC, "Australian Adverse Drug Reactions Advisory Committee: Reactions to hepatitis B vaccins", Australian Adverse Drug Reactions Bulletin, augustus 1990.
- Germanaud J. et al., "Een geval van ernstige cytolyse na vaccinatie tegen hepatitis B", Amer. J. Med., juni 1995, 98 (6), blz. 595-S96.
- Fisher BL, Ed., “Hepatitis B-vaccin: het onvertelde verhaal”, The Vaccine Reaction, National Vaccine Information Center, september 1998.
- Belkin Michael, “Door de overheid verplichte thalidomide voor baby’s”, WorldNetDaily, 25 januari 1999, worldnetdaily.com
- Howd A., “Ounce of Prevention, Pound of Misery”, Insight Magazine, 12 maart 1999,
- Bethell T., “Shots in the Dark". American Spectator. Mei 1999.
- Wallstin B., ‘Immune to Reason’, The Houston Press, 3 juni 1999, www.houstonpress.com
- Shaw FE, “Opschudding over een weinig bekend conserveermiddel, thimerosal, verdringt het Amerikaanse hepatitis B-vaccinbeleid”, Hepatitis Control Report, zomer 1999, deel 4, nr. 2. XNUMX.
- Spalding BJ: 'Wonder of moord? De controverse over het hepatitis B-vaccin", Biospace.com, 11 november 1999, www.biospace.com
- Wetenschap, 31 juli 1998.
- “Frankrijk schort het gebruik van het hepatitis B-vaccin op”. https://www.bmj.com/content/317/7165/1034.2
- Cantwell A., "The gay experiment that start AIDS in America”, Not Aids, 13 januari 2006, nu in http://rense.com/general68/gayex.htm
- Merck & Co.t Inc., Recombivax HB Hepatitis B-vaccin (recombinant), bijsluiter uit juni 2005; GlaxoSmithKline Biologicals, Engerix-B (hepatitis B-vaccin (recombinant), bijsluiter uit december 2005.
- Wainwright RB et al., "Duur van immunogeniciteit en werkzaamheid van hepatitis B-vaccin in een Yupik Eskimo-populatie, voorlopige resultaten van een 8-jarige studie", in “Virale hepatitis en leverziekte”, Hollinger FB et al. (red.) , Williams & Wilkins, 1990, blz. 762-766.
- Hadler SC et al., “Evaluatie van langdurige bescherming door het hepatitis B-vaccin gedurende 7 tot 9 jaar bij homoseksuele mannen.” in Virale hepatitis en leverziekte, Hollinger FB et al. (red..), Williams & Wilkinst 1990, blz. 766-768.
- Hadler SC et al., “Long-term immunogeniciteit en werkzaamheid van hepatitis B-vaccin bij homoseksuele mannen”, NEJM, 24 juli 1986, 315, pp. 209-214.
- Stevens CE et al., "Prospects for control of hepatitis B virus infectie: implicaties van vaccinatie bij kinderen en bescherming op lange termijn", Pediatrics, 1992, 90, pp. 170-173.
- Street AC et al., "Persistentie van antilichamen bij gezondheidswerkers die zijn gevaccineerd tegen hepatitis B", Infec. Controle Hosp. Epidem., 1990, 11, blz. 525-530.
- Pasko MT et al., "Persistentie van anti-HBs onder gezondheidszorgpersoneel geïmmuniseerd met het hepatitis B-vaccin", American Journal of Public Health, 1990, 80, pp. 590-593.
- Wereldgezondheidsorganisatie, ccHepatitis B-vaccins: immunogeniciteit opnieuw beoordeeld'', WHO Drug Infor., 1994, 8 (2).
- Ballinger, AB et al., "Ernstige acute hepatitis B-infectie na vaccinatie", The Lancet, 1994, 344, pp.1292-1293
- Goffin E. et al., "Acute hepatitis B-infectie na vaccinatie", The Lancet, 1995, 345, p. 263.
Vaccins: een gids voor een geïnformeerde keuze door Neil Z. Miller (auteur) en Claudia Benatti (vertaler)
Terra Nuova-edities, 2018

